Propiedades de los materiales metálicos:
Anuncio
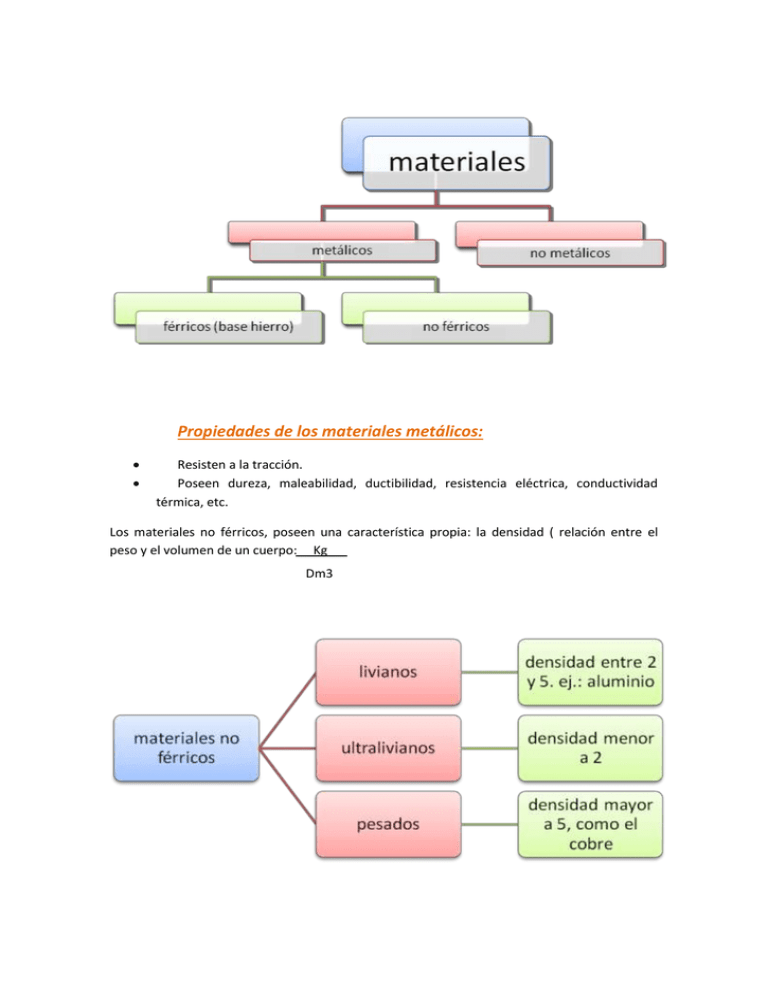
Propiedades de los materiales metálicos: Resisten a la tracción. Poseen dureza, maleabilidad, ductibilidad, resistencia eléctrica, conductividad térmica, etc. Los materiales no férricos, poseen una característica propia: la densidad ( relación entre el peso y el volumen de un cuerpo: Kg Dm3 ALUMINIO METALURGIA DEL ALUMINIO El aluminio es un material liviano, ya que su peso es 1/3, el del acero. Reemplaza al acero en muchas fabricaciones, así como al cobre en conductores eléctricos. Como calcular la resistencia del conductor: R= P . l S P: resistividad L: longitud del conductor S: sección del conductor R: resistencia Conductividad térmica: el aluminio es excelente conductor del calor para los utensilios domésticos, a nivel industrial reemplaza al acero y la fundición, en los blocks de motor, cabezales de cilindros, etc. Resistencia a la corrosión: en contacto con el aire, genera una capa de óxido que lo aísla de la corrosión. A nivel industrial, dicha capa se genera mediante un proceso electrónico. Otras características: Bajo punto de fusión. Apto para la fabricación de envases livianos, reciclables El proceso Bayer Objetivo: separar material que no sirve, de los óxidos de aluminio. Pasos: - Molienda previa. - Eliminación del agua. - secado en un horno rotativo. - molienda fina. El material se lleva a un proceso de digestión con soda cautica, a una presión de 240 ºC. Se obtiene una pasta, de aluminato de sodio e impurezas. El aluminato es tratado en un reactor, donde se obtiene hidróxido de aluminio, este es filtrado y llevado a un horno de descomposición, donde se separa el monóxido de sodio de la alúmina. PROCESO ELECTROLICO La alúmina se mezcla con criolita, un fundente que se encarga de bajar el punto de fusión. El producto obtenido es llevado a hornos de fusión, luego se pasa a tolvas y, finalmente, a celdas electrólicas, en la que se produce la reducción de óxidos y se obtiene aluminio metálico. (VER ECUACIÓN Y GRÁFICO) ELECTROQUÍMICA: Parte de la química que estudia las reacciones químicas que convierten la energía químicas en eléctricas y viceversa. ELECTROLITO: Sustancia que disuelta en agua o fundida, se disocia en 2 partículas cargadas eléctricamente, y son capaces de conducir corriente eléctrica. Aleaciones del aluminio: Cobre: mayor resistencia mecánica y dureza. Nombre comercial: DURALUMINIO. Silicio: mejora el moldeo, con el cobre, se obtiene muy buena terminación superficial. Magnesio: elevada resistencia a la corrosión, facilidad de mecanizado, y resistencia a las cargas de impacto. Ductilidad. Zinc: resistencia mecánica y ductilidad a temperatura ambiente. Níquel: resiste altas temperaturas. FUSIÓN DEL ALUMINIO La forma más utilizada, es en el horno de crisol de grafito. Para proteger al material de la oxidación, se coloca en la base escoria de cloruro de sodio. El crisol de grafito puede utilizarse unas 200 coladas. El inconveniente es que es mal conductor del calor Los crisoles de acero mejoran el rendimiento térmico pero se funden en el aluminio, aumentando el tamaño del grano, por lo que requieren un recubrimiento interno. GAS INDUCCIÓN HORNOS ELÉCTRICO ARCO CONTAMINACIONES DURANTE LA FUSIÓN * ABSORCIÓN DEL HIDRÓGENO: por las altas temperaturas o por el uso de chatarra sucia, lo que genera sopladuras en las piezas moldeadas. * ÓXIDO EN SUSPENSIÓN: debido al mal posicionamiento del quemador. Por lo que facilita la absorción de hidrógeno. * ESCORIA MUY GRUESA: debido a la mala limpieza del crisol, entre una colada y otra.











