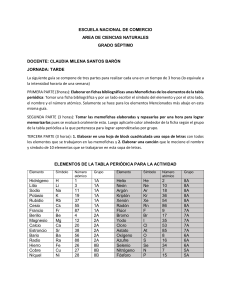
TablaPerioClasica
Anuncio

La tabla periódica (versión reducida). (Archivo EXCEL: “TablaPerioClasica.xls”) En esta actividad empezarás a familiarizarte con la información contenida en la tabla periódica de los elementos. Abre el archivo “TablaPerioClasica.xls” de Excel. Observarás en la pantalla los elementos organizados en siete periodos (filas) y ocho grupos (columnas). Por ejemplo, en el quinto periodo y el grupo IIA, encontramos el estroncio con símbolo _______________________. Notarás también que en la parte inferior de cada columna se describe el grupo con un nombre característico. El estroncio está en la familia de los metales ___________________________________________________ Escribe a continuación los nombres de los seis gases nobles que están en el grupo _______ ____________________ ___Neón____________ ____________________ _____________________ ____________________ ____________________ Sus correspondientes símbolos son: _____________________ __Ne_________________ _____________________ _____________________ ____________________ _____________________ En la tabla siguiente aparece una lista de elementos. Tienes que completar su nombre, su símbolo y el grupo en el que se encuentra según se requiera: Nombre: Símbolo: Grupo: Helio Li P Cloro Pb Radio O K Aluminio Iodo Competencia 1: En la tabla de la izquierda, un alumno escoge y escribe cinco símbolos de elementos sin que vea el otro. Tu compañero tiene que llenar el nombre y el grupo de ellos lo más rápidamente que pueda. Cuando termines, inviertan los papeles usando la tabla de la derecha (si es posible, tómese a cada uno el tiempo que tarda): Símbolo: Nombre: Grupo: Símbolo: Nombre: Grupo: En la parte superior de la pantalla notarás que está escrito “Opción (2-4):”. Esto quiere decir que en la celda de la derecha puedes poner un 2, un 3 o un 4 para cambiar la información en la tabla, de acuerdo con lo siguiente: Un Un Un 2 3 4 el “Nombre del elemento”. su “Número atómico”. su “Masa atómica”. te da te da te da Cambia este valor de la opción 2 a la 3 y a la 4 para que observes esto. Completa la tabla siguiente. Nombre: Símbolo: Número atómico: Masa atómica: Grupo: Be Argón Ga S Sodio Bi 6 137.34 9 14.007 Compara los números atómicos con las masas atómicas. ¿Cuál de ellos es siempre mayor? _______________________________________ Más o menos, ¿cuántas veces más grande? _________________________________ ¿Siempre? _______________________________ Competencia 2: Con la opción 3 para que el programa muestre los números atómicos, uno de ustedes escoge un elemento y le dice al compañero su número atómico. El compañero tiene que adivinar su masa atómica. Gana el que se encuentre más cerca al valor exacto dado en la opción 4. Repitan dos veces esto cada uno. Hagan sus operaciones en una hoja. Competencia 3: Coloca la opción 2 en la pantalla para que se vean los nombres de los elementos. Uno de ustedes escoge un elemento cualquiera, lo escribe en la tabla de la izquierda sin que lo vea su compañero. A tu compañero le dices solamente el grupo del elemento que elegiste y él tiene que adivinarlo, diciéndote el nombre, en el menor número de intentos. Cuando haya adivinado, inviertan los papeles, usando la tabla de la derecha (hagan esto dos veces cada uno): A l u m n o 1 Nombre del elemento: Número de intentos: A l u m n o 2 Nombre del elemento: Número de intentos: Repitan esto dos veces más cada uno, pero ahora con la opción 3 para que no puedan ver los nombres de los elementos. Sumen los intentos de cada uno para saber quién ganó. Con la opción 3, que te da el número atómico de cada elemento, escoge el grupo que tu quieras y escribe a continuación los símbolos con su número atómico de los cinco elementos de ese grupo que están del segundo al sexto periodos: Grupo escogido: Símbolo: # atómico: Diferencias: 8 En la tabla de arriba calcula las cuatro diferencias entre los cinco números atómicos. Por ejemplo, si los primeros dos números atómicos que escribiste fueron el 6 y el 14, su diferencia sería de 14-6 = 8. Sigue así restando los números atómicos de tu tabla de dos en dos. Recuerda que el número atómico representa la cantidad de electrones que tiene el átomo de cada elemento. ¿Qué significa que la primera diferencia encontrada fue de 8? _______________________________________________________________________ ¿Qué significa que la tercera diferencia que calculaste fue de 18? ____________________ _________________________________________________________________________ Al final de la clase compara tus resultados con otros equipos que escogieron grupos de elementos distintos y saquen juntos algunas conclusiones (nota que del grupo IIA al IIIA hay saltos en el número atómico). La tabla periódica completa. (Archivo EXCEL: “TablaPerio.xls”) En esta actividad explorarás la tabla periódica completa de los elementos. Abre el archivo “TablaPerio.xls” de Excel, donde encontrarás la tabla periódica completa. Abre también el archivo “TablaPerioClasica.xls”. Compara estas dos tablas y escribe abajo tus observaciones: Discute éstas con todo el grupo. De las columnas agregadas a la tabla completa (IIIB hasta la IIB) elige los 10 elementos que tu consideres más importantes de estos grupos y escríbelos abajo con sus nombre, símbolo, número atómico, masa atómica y grupo: Nombre: Símbolo: Número atómico: Masa atómica: Grupo: ¿Por qué lo elegiste? Discute tu lista y la de otros con todo el grupo.