El titanio es un elemento químico, de símbolo Ti y
Anuncio

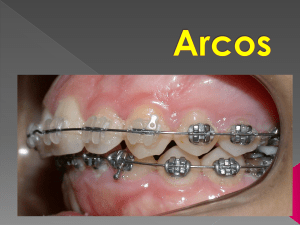
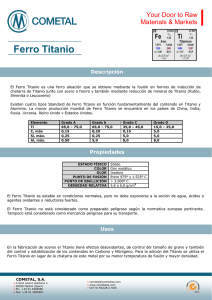
PROPIEDADES DEL TITANIO Brais Díaz Sánchez El titanio es un elemento químico, de símbolo Ti y número atómico 22. Se trata de un metal de transición de color gris plata. Comparado con el acero, metal con el que compite en aplicaciones técnicas, es mucho más ligero (4,5/7,8 g/cm3). Tiene alta resistencia a la corrosión y gran resistencia mecánica, pero es mucho más costoso que el acero, lo cual limita su uso industrial. Es un metal abundante en la naturaleza; se considera que es el cuarto metal estructural más abundante en la superficie terrestre y el noveno en la gama de metales industriales. No se encuentra en estado puro sino en forma de óxidos, en la escoria de ciertos minerales de hierro y en las cenizas de animales y plantas. Su utilización se ha generalizado con el desarrollo de la tecnología aeroespacial, donde es capaz de soportar las condiciones extremas de frío y calor que se dan en el espacio y en la industria química, por ser resistente al ataque de muchos ácidos; asimismo, este metal tiene propiedades biocompatibles, dado que los tejidos del organismo toleran su presencia, por lo que es factible la fabricación de muchas prótesis e implantes de este metal. Posee propiedades mecánicas parecidas al acero, tanto puro como en las aleaciones que forma, por tanto compite con el acero en muchas aplicaciones técnicas, especialmente con el acero inoxidable. Puede formar aleaciones con otros elementos, tales como hierro, aluminio, vanadio, molibdeno y otros, para producir componentes muy resistentes que son utilizados por la industria aeroespacial, aeronáutica, militar, petroquímica, agroindustrial, automovilística y médica. El titanio (llamado así por los Titanes, hijos de Urano y Gea en la mitología griega) fue descubierto en Inglaterra por William Gregor, en 1791, cuando estudiaba un metal de color gris-plata que había encontrado. Poco después, en 1795, el químico austríaco Martín Kalprotz, descubridor también del uranio, le dio el nombre de titanio.. El mineral más importante del que se extrae titanio es el rutilo (óxido de titanio), muy abundante en las arenas costeras. Por su parte el titanio debe ser sometido previamente a un proceso metalúrgico de refinado, para prevenir su eventual reacción con sustancias gaseosas, tales como el nitrógeno, el oxígeno y el hidrógeno. 1 Entre las propiedades del titanio podemos destacar las siguientes: 1. Características físicas -Es un metal de transición. -Ligero: su Densidad o peso específico es de 4507 kg/m3. -Tiene un punto de fusión de 1675ºC (1941 K). -La masa atómica del titanio es de 47,867 u -Es de color plateado grisáceo. -Paramagnético. No se imanta gracias a su estructura electrónica. -Abundante en la Naturaleza. -Reciclable. -Forma aleaciones con otros elementos para mejorar las prestaciones mecánicas. -Muy resistente a la corrosión y oxidación. -Refractario. -Poca conductividad. No es muy buen conductor del calor ni de la electricidad. 2. Características mecánicas -Mecanizado por arranque de viruta similar al acero inoxidable. -Permite fresado químico. -Maleable, permite la producción de láminas muy delgadas. -Dúctil, permite la fabricación de alambre delgado. -Duro. Escala de Mohs 6. -Muy resistente a la tracción. -Gran tenacidad. -Permite la fabricación de piezas por fundición y moldeo. -Material soldable. -Permite varias clases de tratamientos tanto termoquímicos como superficiales. -Puede mantener una alta memoria de su forma. 3. Características químicas -Se encuentra en forma de óxido, en la escoria de ciertos minerales y en cenizas de animales y plantas. -Presenta dimorfismo, a temperatura ambiente tiene estructura hexagonal compacta (hcp) llamada fase alfa. Por encima de 882 ºC presenta estructura física centrada en el cuerpo (bcc) se conoce como fase beta. -La resistencia a la corrosión que presenta es debida al fenómeno de pasivación que sufre (se forma TiO2 que lo recubre). -Sus iones no tienen existencia a pH básicos. Aplicaciones del titanio. Entre las muchas aplicaciones del titanio podemos destacar: Aplicaciones biomédicas, industria energética, Industria de procesos químicos, industria automovilística, industria militar, industria aeronáutica y espacial, construcción naval, joyería y bisutería, anillos, instrumentos deportivos, decoración, etc. 2 Bibliografía. - http://www.wikipedia.org/ - Ciencia de materiales. Editorial Donostiarra. José María Lasheras, Javier F. Carrasquilla. Año 1991. 3