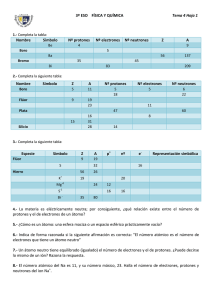
ESTRUCTURA ATOMICA 1. PARTICULA FUNDAMENTAL: Son los bloques constituyentes básicos de cualquier átomo. El átomo está formado principalmente por 3 partículas fundamentales: electrones, protones y neutrones. 2. ÁTOMO: Los átomos constan de núcleos muy pequeños y sumamente densos, rodeados por nubes de electrones a distancias relativamente grandes del núcleo. Todos los núcleos contienen protones; los núcleos de todos los átomos con excepción de la forma común del hidrogeno, también contienen neutrones. Los diámetros nucleares son de aproximadamente 10-4 Angstroms (10-5 nanómetros); los diámetros atómicos son de aproximadamente 1 Angstroms (1 Angstroms = 10-10 m). 3. NÚMERO ATOMICO: Según del físico británico Moseley, el número atómico de un átomo es igual al número de protones del núcleo; este, a su vez, es igual al número de electrones que giran a su alrededor. Es representado por la letra Z. En la tabla periódica los elementos están ordenados de acuerdo a su número atómico. Por ejemplo, el calcio tiene el número atómico 20. Z=20; por lo tanto tiene: 20 protones en el núcleo 20 electrones en la envoltura Ocupa el lugar 20 en la tabla periódica. 4. NÚMERO DE MASA E ISOTOPOS: La mayoría de los elementos están formados de átomos con masa distinta que se llaman isotopos. Los isotopos de un elemento dado contienen el mismo número de protones (o electrones) porque son átomos del mismo elemento. Su masa varía por que contienen distintos números de neutrones en el núcleo. Por ejemplo, existen 3 tipos distintos de átomos de hidrogeno que suelen llamarse hidrogeno, deuterio y tritio. Cada uno de ellos tiene un protón en el núcleo atómico. La 1 forma predominante de hidrogeno no tiene neutrones, pero el átomo de deuterio tiene un neutrón y el de tritio dos neutrones en el núcleo. Las 3 formas del hidrogeno tienen propiedades químicas muy similares. Nombre °N de abundancia electrones(en Símbolo atomica en °N de °N de atomos Símbolo núclido la naturaleza protones neutrones neutros) hidrogeno H 99,985% 1 0 1 deuterio D 0,015% 1 1 1 tritio T 0,00% 1 2 1 El número de masa (siempre un número entero) de un átomo es la suma del número de protones y neutrones del núcleo. 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑚𝑎𝑠𝑎 = 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑝𝑟𝑜𝑡𝑜𝑛𝑒𝑠 + 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑛𝑒𝑢𝑡𝑟𝑜𝑛𝑒𝑠 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑚𝑎𝑠𝑎 = 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑎𝑡𝑜𝑚𝑖𝑐𝑜 + 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑛𝑒𝑢𝑡𝑟𝑜𝑛𝑒𝑠 𝐴 = 𝑍 + °𝑁 La composición del núcleo se indica por el símbolo nuclido. 𝐴 𝑍𝐸 Dónde: E= Símbolo del elemento A= número de masa Z = número atómico 1 𝑚𝑜𝑙 = 6,022 ∗ 1023 𝑝𝑎𝑟𝑡𝑖𝑐𝑢𝑙𝑎𝑠 Átomos Moléculas El peso atómico de un elemento es el promedio en peso de las masas de los isotopos que lo constituyen (Números fraccionarios). 2 5. ESTRUCTURA ELECTRONICA. La envoltura atómica es el espacio que rodea al núcleo en donde se encuentran los electrones; estos giran a grandes velocidades alrededor del núcleo, observándose como una nube electrónica tridimensional. Según Niels Bohr, este espacio está formado por espacios diferenciados a los que denomino capas o niveles de energía. En estas los electrones se encuentran ordenados según la cantidad de energía que poseen; aquellas que están girando cerca al núcleo, son de menor energía; cuanto más se alejan del núcleo tienen más energía. Hay 7 capas de energía y en todo nivel de energía se hallan subniveles de energía u orbitales atómicos, estos son 4: Sharp (s), principal (p), difuso (d) y fundamental (f). Un orbital atómico es la región espacial en la que hay mayor probabilidad de encontrar un electrón. El ordenamiento electrónico que se va a describir para cada átomo se conoce como configuración electrónica, existe una regla de selección que nos permite ordenar los electrones de un átomo. Para encontrar el orden de ocupación de los electrones, debe seguirse la “regla se selección” hasta completar el número total de electrones del elemento. Figura 1 : regla de seleccion 3 Como ya se mencionó estos los electrones se encuentran ordenados según la cantidad de energía que poseen, donde se llenan primero los niveles de energía más bajos: 𝑒𝑛𝑒𝑟𝑔𝑖𝑎 = 𝑛 + 𝐿 n 1 2 2 3 3 3 4 + + + + + + + + L= 0 (s) = 0 (s) = 1 (p) = 0 (s) = 1 (p) = 2 (d) = 0 (s) = energia 1 2 3 3 4 5 4 6. NÚMEROS CUANTICOS. Estos números nos permiten describir el ordenamiento electrónico de cualquier átomo, lo que llamamos configuración electrónica. Estos números nos describen los niveles de energía de los electrones y la forma de los orbitales, que indica la distribución espacial del electrón. 1) Numero cuántico principal (n): describe el nivel de energía principal que el electrón ocupa. Puede ser cualquier número entero positivo. K L M N O P Q n= 1 2 3 4 5 6 7 Número de electrones por nivel = 2* n2 (sólo hasta el nivel 4) número de orbitales = n 1 2 3 4 5 6 7 n2 Número de electrones 2 8 18 32 (maximo) 32 18 8 4 2) Número cuántico secundario o azimutal (L): indica la forma de la región del espacio que ocupa el electrón dentro de cada nivel de energía definido por “n”, “L” puede tomar valores de 0 hasta (n-1). 𝑙 = 0,1,2 … (𝑛 − 1)𝑚𝑎𝑥 Nos indica el subnivel o un tipo específico de orbital atómico que el electrón puede ocupar. s p d f L= 0 1 2 3 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑜𝑟𝑏𝑖𝑡𝑎𝑙𝑒𝑠 = 2𝐿 + 1 L s p d f numero orbitales 1 3 5 7 de °N electrones 2 6 10 14 3) Numero cuántico magnético (m): Determina la oscilación magnética de la nube electrónica en relación al núcleo, cuando el átomo es sometido a un campo magnético. Dicha orientación esta referida a los tres ejes cartesianos: x, y, z. En cada subnivel, “m” puede tomar valores integrales desde –L hasta cero e incluyendo +L 𝑚 = −𝐿, 0, +𝐿 Por ejemplo, cuando “L=1” permisibles de “m” indica que en el subnivel “p” hay 3 valores 𝑚 = −1 , 0 , +1 Por lo tanto hay tres regiones distintas en el espacio llamados orbitales atómicos con un subnivel “p”: 𝑝𝑥 , 𝑝𝑦 , 𝑝𝑧 5 4) Numero cuántico de giro o spin (s): se refiere al giro del electrón y a la orientación del campo magnético que este produce para cada conjunto de “n”. 𝑠= + 1 1 Ó − 2 2 Los valores de “n, L, m “describen un orbital atómico determinado: cada orbital 1 atómico solo puede acomodar a 2 electrones, uno con un spin de + 2 y otro con 1 − 2. 7. PRINCIPIO DE EXCLUSION DE PAULI: indica que ningún par de electrones de cualquier átomo puede tener los 4 números cuánticos iguales. 8. REGLA DE HUND: los electrones deben ocupar todos los orbitales de un subnivel dado en forma individual antes de que se inicie el apareamiento. Estos electrones desapareados suelen tener giros paralelos. 6