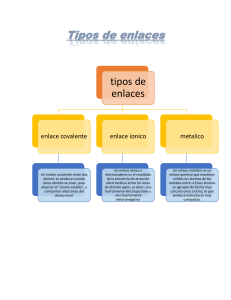
CIENCIA DE LOS MATERIALES Clase 1: Introducción a la ciencia de los materiales Contenido 1. 2. 3. 4. 5. 6. Ciencia e ingeniería de los materiales. Materiales. Ciencias de los materiales. Estructura de los materiales. Nivel atómico. Módulo de Young en materiales. Resultado de aprendizaje Interpreta las propiedades de los materiales según el tipo de enlace: metálico, iónico o covalente. Introducción a la ciencia de los materiales Contenidos del curso Evaluaciones • Unidad 1: Estructura de los materiales. En este curso se rendirán las siguientes evaluaciones: • Unidad 2: Diagrama de fases para dos y tres componentes. • • • 4 Talleres (30%): los cuales son guías de ejercicio a desarrollar. • 2 Pruebas solemnes (70%). Unidad 3: Propiedades de los materiales. Unidad 4: Técnicas de caracterización. Cada clase contiene un taller formativo. Introducción a la ciencia de los materiales Introducción Si se está evaluando qué material va a utilizar para una taza de café... ¿? Poliestireno ¿Qué propiedades en particular hará que ese material sea el adecuado? Cerámica Madera Metálico Introducción a la ciencia de los materiales Ciencia e ingeniería de los materiales Ingeniería de los materiales Ciencia e ingeniería de los materiales Ciencia de los materiales Elaboración propia a partir de Smith, 2006. • Conocimiento aplicado de los materiales. • Conocimiento resultante de la estructura, propiedades, elaboración y comportamiento de los materiales de ingeniería. • Conocimiento básico de los materiales. Introducción a la ciencia de los materiales Ciencia e ingeniería de los materiales Obtenida de Smith, 2006, p. 6. Introducción a la ciencia de los materiales Materiales Los materiales más estudiados y utilizados hoy son: 1. Metales y sus aleaciones. 2. Cerámicos. 3. Polímero. Introducción a la ciencia de los materiales Materiales 1. Metales y sus aleaciones Entre ellos se encuentra el acero, aluminio, magnesio, zinc, hierro colado, titanio y níquel. Características: • En su mayoría son cristalinos (estructura). • Resistentes, electroconductor, electromagnético. • Alta densidad. • Dúctil, maleable y duro. Obtenida de Wikipedia, 2020. Introducción a la ciencia de los materiales Materiales 2. Cerámicos Características: • Estructuras amorfas (vidrios) o cristalinas (cerámicos). • Muy duros. • Densidad menor a los metálicos. • Aislantes eléctricos, térmicos, dureza, fragilidad, resistencia a la compresión. Introducción a la ciencia de los materiales Materiales 3. Polímeros Los polímeros son muy utilizados en todo el mundo. Características: • Material orgánico. • Material de menor densidad que los anteriores. • Moléculas en su mayoría amorfas y largas cadenas (rompecabezas). • Tipos: termoplástico, termoestable y elastómero. • Ductilidad formalidad, aislante térmico, aislante eléctrico, dureza y resistencia mecánica. Obtenida de Los Adhesivos, 2020. Introducción a la ciencia de los materiales Ciencias de los materiales Al trabajar con los materiales se deben considerar las dimensiones de tiempoespacio diferentes a lo habitual. Mundo Nanocuántico Obtenida de ICAMS, 2020. Introducción a la ciencia de los materiales Ciencias de los materiales Al estudiar los materiales hay 3 partes importantes: Estructura: que va desde lo atómico hasta la inspección visual. Tiene relación con los enlaces, formación de cristales e imperfecciones. Estructura Obtenida de Smith, Hashemi, 2006. Método de procesamiento Lámina Procesamiento: se refiere a la implementación del material. Soldaduras, conformado, colado, etc. Propiedades: las cuales están separadas en física y mecánicas. Esto tiene relación en cuanto a resistencia, rigidez, ductilidad, color, conductividad térmica y eléctrica, magnetismo. Propiedades Introducción a la ciencia de los materiales Ciencias de los materiales Para realizar un estudio de los materiales es necesario comprender su estructura y cómo varían según la temperatura y presión, para observar su estructura y comportamiento en cada una de sus fases. Obtenida de Procesos industriales, 2020. Introducción a la ciencia de los materiales Estructura de los materiales La estructura se divide en varios subsistemas: Atómico Estudia cómo están formado los átomos: • Enlaces primario y secundario. • Cuántico. Cristalina Microestructura Estudia cómo están agrupados los átomos en redes y arreglos para formar un estado sólido. Enfoque desde el agrupamiento de cristales y zonas amorfas o irregulares, llamadas fases. Escala tiempo espacio Macroestructura Elementos vistos de forma directa por los ojos (continúo). 1 Introducción a la ciencia de los materiales Estructura de los materiales En cada nivel afecta a diferentes propiedades del material: Atómico Cristalina Microestructura Macroestructura Rigidez y cambio térmico. Fatiga, rigidez, resistencia, ductilidad. Ductilidad, resistencia, fatiga. Costo, durabilidad, eficiencia. Introducción a la ciencia de los materiales Nivel atómico • En este nivel se considera un modelo atómico propuesto por Bohr y mejorado por Schrödinger con los números cuánticos. • En especial, interesa el tipo de compuesto metal y no metal, junto con su estructura eléctrica. • Además, es importante la electronegatividad de la molécula. Obtenido de Wikipedia, 2020. Introducción a la ciencia de los materiales Nivel atómico Enlaces primarios y secundarios Para lograr formar un material es necesario unir átomos, lo cual se logra a través de enlaces químicos primarios, junto con los secundarios. Obtenida de Askeland, 1998. p. 28. 1. Enlace iónico. Obtenida de Askeland, 1998. p. 28. 2. Enlace covalente. Obtenida de Askeland, 1998. p. 24. 3. Enlace metálico. Obtenida de Askeland, 1998. p. 29. 4. Enlace de Van der Waals. Cada enlace tiene una particularidad respecto a los elementos que lo componen y la energía de unión de los átomos. Esto afecta a la propiedad de rigidez y los cambios térmicos. Introducción a la ciencia de los materiales Nivel atómico Enlaces primarios y secundarios 1. Enlace iónico • Un átomo entrega un electrón de valencia y queda cargado de forma positiva. Luego se unen por fuerzas de Coulomb. • Tienen un alto punto de fusión, son duros y frágiles producto de la alta energía de unión que tienen 3-8 eV/atom, conexión Coulomb. • Son aisladores térmicos y eléctricos (por su estabilidad eléctrica atómica). Obtenida de Askeland, 1998. p. 28. Introducción a la ciencia de los materiales Nivel atómico Enlaces primarios y secundarios 2. Enlace covalente Obtenida de Askeland, 1998. p. 28. • Dos átomos comparten los electrones de valencia para generar estabilidad entre ellos (lograr gas noble). • Enlace más fuerte de la naturaleza con el diamante (carbono), pero posee enlaces más débiles como es el caso de los polímeros. • Si es un enlace direccional, tienen mayor dureza y densidad que aquellos no direccionales (electronegatividad). • Su fragilidad depende del material. Introducción a la ciencia de los materiales Nivel atómico Enlaces primarios y secundarios 3. Enlace metálico Obtenida de Askeland, 1998. p. 24 • Son enlaces que se generan por la alta electronegatividad de los elementos. Sólo se da entre metales o metaloides. Entre los átomos se forma una "marea" de electrones. • Son de alta resistencia y ductilidad. • Excelentes conductores de electricidad y temperatura. • Propiedades magnéticas (hierro). • Alto rango de temperatura de fusión -39° a 3410°C. Introducción a la ciencia de los materiales Nivel atómico Enlaces primarios y secundarios 4. Enlace de Van der Waals • Es el enlace más débil, ya que se forma por electronegatividad inducida (polarización); dipolo dipolo, dipolo dipolo inducido, fuerzas de dispersión. • Una forma especial del enlace secundario es el puente de hidrógeno que explica por qué el hielo flota. • Se observa en polímeros, ya que las moléculas largas se enlazan de forma secundario con otra molécula igual. • Tiene bajos puntos de fusión, son blandos y tienen baja resistencia. Obtenida de Askeland, 1998. p. 29 Introducción a la ciencia de los materiales Nivel atómico Energía de unión entre átomos A mayor energía, se requiere mayor temperatura para lograr una frecuencia de movimiento de los átomos, lo que genera menor deformación y mayor rigidez. También se tienen materiales con mayor resistencia a los cambios producto de la temperatura (coeficiente cambio térmico). Enlace Energía de unión (Kcal/mol) Iónico 150 – 370 Covalente 125 – 300 Metálico 25 – 200 Van der Waals < 10 Obtenida de Askeland, 1998. p. 31 Introducción a la ciencia de los materiales Resumen de enlaces primarios y secundarios Enlace Sólidos típicos Energía unión [eV/atom] Temperatura de fusión [°C] Densidad [gr/cm3] Propiedades típicas NaCl MgO 3.2 10 801 2852 40 250 Aislador eléctrico. Alto módulo de elasticidad. Media conducción de la electricidad. Metálico Cu Mg 3.1 1.1 1083 650 120 44 Conductor eléctrico. Buen conductor térmico. Alto módulo de elasticidad. Generalmente dúctil. Covalente Si C 4 7.4 1410 3550 190 827 Buen módulo de elasticidad. Frágil. Excelente aislador térmico. Puente de Hidrógeno PVC (polímero) H2O (Hielo) 0.52 212 0 1.3 0.917 Bajo módulo de elasticidad. Algo dúctil. Baja conductividad térmica. Gran coeficiente expansión térmica. 8 Bajo módulo de elasticidad. Aislador eléctrico. Baja conductividad térmica. Gran coeficiente expansión térmica. Iónico Dipolo Inducido Argón Obtenida de Askeland, 1998. p. 31. 0.09 -189 Introducción a la ciencia de los materiales Módulo de Young en materiales Obtenida de Dyah Y en Quora, 2020. Introducción a la ciencia de los materiales Cierre • En la ciencia de los materiales, los materiales se dividen en cuatro categorías: metálicos, cerámicos, polímeros y compuestos (a veces se consideran los semiconductores). • En el estudio de los materiales se considera su estructura atómica del material, principalmente el tipo de enlace entre átomos. • El tipo de enlace afecta directamente a la propiedad mecánica del módulo de Young y el coeficiente de expansión térmica térmico. Introducción a la ciencia de los materiales Bibliografía Askeland, D. (1998). Ciencia e Ingeniería de los Materiales. Estados Unidos: International Thomson Editores. Smith, W., Hashemi, J. (2006). Fundamentos de la ciencia e ingeniería de los Materiales. México: Mc-GrawHill.