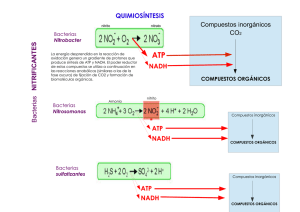
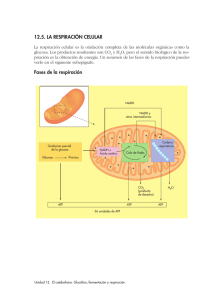
EL ATP FUENTE ENERGÉTICA Prof. FERNANDO PIFARRÉ Si aceptamos como símil la comparación que un deportista es como un coche de carreras, el músculo sería el motor y el combustible (la energía que consume) es el adenosín trifosfato (ATP). Por consiguiente es preciso conocer cuanto combustible necesita el deportista para realizar un esfuerzo determinado, a que velocidad se gasta el combustible, las reservas que dispone el músculo y como se recuperan dichas reservas. El ATP o Adenosin -5'- trifosfato o trifosfato de adenosina es la molécula utilizada por todos los organismos vivos para proporcionar energía por medio de sus reacciones químicas. Figura 1 Fórmula estructural del ATP Está compuesta por de adenosina y tres grupos fosfatos que se unen al carbono 5 de la pentosa. La molécula posee enlaces ricos en energía y la reacción de hidrólisis de la adenosina trifosfato (ATP), facilitada por la coenzima ATPasa, la convierte en adenosina difosfato (ADP) y fosfato. Se trata de una reacción exergónica o de liberación de energía en formas de calor, donde la variación de la energía liberada en condiciones de reposo es igual a 70 kJ/mol o 16.73 kcal/mol y puede descender durante un ejercicio intenso a 52.1 kJ/mol o 12.45 kcal/mol (Wilmore & Costill, 2004). ATP + H2O Figura 2 Hidrólisis del ATP ADP + Pi + energía Pi= fósforo inorgánico. La función del ATP en la contracción muscular. En un músculo esquelético cada célula o fibra muscular contiene muchas miofibrillas y en su longitud se hallan los sarcómeros que son las unidades funcionales. Figura 3 Figura 3 Músculo estriado, fibra, miofibrillas y sarcómero La Figura 4 muestra una representación esquemática del sarcómero estando el músculo relajado. Figura 4 representación esquemática del sarcómero Cada sarcómero está formado por muchos filamentos de dos clases de proteínas: la actina, que es el filamento más delgado y la miosina cuyo filamento es más grueso. Representación esquemática de los filamentos de actina y miosina (Figura 5). Figura 5 Las proteínas que forman el sarcómero Cuando una célula muscular es estimulada, se liberan iones de calcio ( Ca++) que se enlazan a la unidades de troponina desplazando la tropomiosina a lo largo de los filamentos de actina, liberando de esta forma las zonas donde se van a enlazar las cabezas esféricas de la miosina. Figura 6 Puntos de unión de la miosin con la actina En la miosina existen unas cabezas esféricas que se unen a los receptores de los filamento de actina para formar los "puentes cruzados". Figura 7 Movimiento del ATP hacia las cabezas esféricas de la miosina. Las moléculas de ATP se mueven hacia las cabezas esféricas y provocan que cada una suelte el filamento activo. El ATP libera energía formando ADP y un grupo de fosfato. La Figura 7 muestra la representación esquemática de la hidrólisis de la molécula de ATP. Figura 8 Hidrólisis del ATP en ADP más P liberando energía. Esta energía dispara a la cabeza esférica que se une al filamento activo, pero en una posición posterior. Ver Figura 9. Figura 9 Nueva posición de la cabeza esférica de la miosina. Tras la reacción química, la cabeza esférica regresa a su posición inicial arrastrando al filamento de actina. La repetición de los procesos mencionados en las figuras anteriores (de la 6 a la 9) hace que la actina se desplace sobre la miosina y se produzca la contracción muscular. Figura 10 Desplazamiento del filamento de actina. Habiéndose deslizado los filamentos de actina sobre la miosina. Esta acción se denomina Teoría de los filamentos deslizantes. Comparen esta Figura 11 con la número 4. Figura 11 Deslizamiento de los filamentos de actina sobre la miosina, provocando la contracción del músculo. Las reservas de ATP en la célula muscular son escasas y solo permiten la contracción muscular durante un tiempo muy corto. En teoría, la reserva de ATP se agotaría después de realizar un esfuerzo máximo durante ½ segundo (Chicharro & Vaquero, 2006). Por consiguiente, para poder proseguir con el ejercicio físico se tendrá que formar o reponer más cantidad de ATP a partir de otros compuestos. El primer mecanismo exergónico que libera energía para conseguir sintetizar ATP a partir del ADP es merced a la fosfocreatina (PCr) formada por creatina y fosforo y en su descomposición libera energía. Desde la década de 1990 el desarrollo tecnológico ha permitido la expansión de una metodología que permite obtener información de las reacciones químicas que ocurren en la célula, en este caso concreto en la fibra muscular. Esta técnica es la espectroscopía por resonancia magnética nuclear (RMN) que se caracteriza, en relación a otras metodologías que en principio proporcionan información parecida, como son las biopsias y las determinaciones sanguíneas, ya que tiene la capacidad de ofrecer información "en vivo", de una forma no invasiva y sin causar molestias o trastornos a la persona estudiada. El espectro del fósforo 31 del músculo esquelético de una persona, sea deportista o sedentario, presenta una serie de picos o resonancias que provienen de tres compuestos químicos: el ATP, la fosfocreatina y el fosfato inorgánico. El ATP contiene tres núcleos de fósforo que son químicamente diferentes, dando lugar a tres picos o resonancias (gamma, beta y alfa). La fosfocreatina (PCr) solamente tiene un núcleo de fósforo, por consiguiente produce una sola resonancia. Es el equivalente a un depósito de reserva, ya que la PCr regenera instantáneamente el carburante (ATP), que puede ser utilizado directamente por el músculo. En consecuencia se puede afirmar que la concentración de ATP no disminuirá de una manera apreciable durante el esfuerzo, mientras haya una reserva de PCr. El fosfato inorgánico se puede considerar como un producto resultante de la utilización del combustible (ATP) (Gonzalez de Suso et al., 1993) Figura 12 Un espectro del isótopo fósforo-31 obtenido en la zona analizada de un músculo estriado por espectroscopia de RMS. El área debajo de los picos es proporcional a la concentración relativa de estos metabolitos en el tejido estudiado. (González de Suso, Bernús, et al., 1993; Gutiérrez & Acero, 1988) El ADP + PCr (Cr + P+ energía) ATP + H2O ATP+ Cr. ADP + Pi + energía Figura 13 En la parte superior la hidrólisis de la Fosfocreatina que se junta con el ADP para formar ATP. En la parte inferior, hidrólisis del ATP Merced a la enzima creatin kinasa se provoca la hidrólisis de la PCr liberándose energía que facilita la unión del ADP con el fosfato de la creatina para producir más moléculas de ATP, que a su vez se descompone en ADP + Fosfato + energía y se vuelve a iniciar el ciclo energético. No obstante, tal como se expone Figura 12, los depósitos de Fosfocreatina son también limitados, siendo mayores en deportistas de velocidad respecto a los deportistas de fondo y a los sedentarios (Bernús et al., 1993). Figura 14 Diferencia de concentración de fosfocreatina (PCr) en un sujeto sedentario, un velocista y un fondista. 1 espectro del fosfato inorgánico, 2 Fosfodiésteres, 3 Fosfocreatina, 4, 5 y 6 los tres picos de ATP α, β, γ (Bernús et al., 1993). La concentración de la PCr puede llegar a disminuir un 90% cuando el esfuerzo del o la deportista se halla próximo/a al agotamiento, mientras que la concentración del ATP sólo disminuye un 10%. En consecuencia, la concentración de ATP no disminuirá mientras haya una reserva de PCr. Figura 15 Espectros de fosforo 31 en reposo y en diferentes tiempos de recuperación en el vasto medial del músculo recto femoral. La Figura 15 muestra diferentes tiempos de recuperación después de realizar un ejercicio de 10 segundos de duración a máxima velocidad. Como se puede observar después de acabar el ejercicio la PCr ha disminuido, mientras que el fosfato inorgánico ha aumentado. La recuperación del pH se produce en este sujeto a los 264 segundos, es decir: 4 minutos y 24 segundos de haberlo finalizado. El tiempo de recuperación puede variar de una persona a otra, aunque los valores que se obtienen no son muy dispares. A medida que un esfuerzo aumenta en el tiempo, el sujeto es incapaz de mantener la intensidad del mismo, ésta decae progresivamente dado que la cantidad de ATP que se puede aportar por unidad de tiempo de esfuerzo va disminuyendo. Si se estudia la disminución progresiva de la fosfocreatina en función del tiempo de esfuerzo en el recto medial del cuádriceps, se observa que a medida que éste aumenta se produce una disminución de fosfocreatina. La Tabla 1 muestra los datos medios y sus desviaciones estándar de seis deportistas de 22.2 años de media que se sometieron a 3 series de ejercicios de 10, 20 y 40 segundos de duración a la máxima frecuencia de contracción posible con una resistencia cercana al 50% de su máxima contracción voluntaria. Tiempo de esfuerzo Potencia en watios Frec. de contracción Fuerza en Newtons 10 seg. 20 seg. 40 seg. 300 ± 108 275 ± 85 230 ± 68 193 ± 25 188 ± 25 179 ± 23 759 ± 169 718 ± 133 635 ± 113 Máxima contracción voluntaria % 50 ± 12 48 ± 10 42 ± 7 pH reposo Disminución del %PCr 7.12 ± 0.04 7.12 ± 0.04 7.16 ± 0.04 48 ± 5 64 ± 4 69 ± 5 T.recuperar el pH inicial en seg. 270 ± 48 442 ± 50 812 ± 209 Tabla 1 Valores medios y desviaciones estándar de los datos mecánicos y el pH de reposo y el tiempo necesario para recuperar el pH inicial, junto con la disminución porcentual de la PCr. La recuperación del pH, que nos indicaría la recuperación de la PCr, va desde 4 minutos y 30 segundos para esfuerzos de 10 segundos de duración a 13 minutos y 32 segundos para los esfuerzos de 40 segundos de duración(González de Suso, Alonso, Bernús, Prat, & Arús, 1993). Para poder continuar un esfuerzo es necesario aportar energía (ATP) por otras vías, aunque este aporte sea más lento y por ello el esfuerzo bajará en intensidad, dado que el proceso de generar energía (ATP) es mas lento que el de la PCr. Via anaeróbico lactácida o via anaeróbico láctica. Si el esfuerzo es intenso, el oxígeno aportado por la sangre no es suficiente y la utilización de la glucosa y del glucógeno (polímero de la glucosa) para crear ATP, lo hace sin presencia del mismo, dando lugar a la via anaeróbica lactácida. Esta via o proceso de formación de energía que se pone en marcha sin presencia de oxígeno en la célula, en nuestro caso en la fibra muscular. Si se observa la Tabla 1 la disminución de la PCr a medida que aumenta el tiempo del esfuerzo, cada vez es más ostensible y por consiguiente aumenta el aporte de ATP por la via anaeróbica lactácida. El primer paso de la respiración celular es la denominada glucólisis o degradación de la glucosa hasta el ácido pirúvico, es decir, pasar de una molécula de 6 átomos de carbono (glucosa) a 2 moléculas de 3 átomos de carbono cada una (ácido pirúvico). Ello implica que se han de romper enlaces que unen los átomos de carbono y al romperse producen energía (ATP). La glucólisis ocurre en el citoplasma de la célula y tiene 10 pasos o procesos de degradación de la glucosa merced a las acción de diferentes enzimas . La procedencia de la glucosa para la célula muscular puede provenir del glucógeno almacenado y la que entra directamente que proviene de la circulación. Figura 16 La molécula de glucosa tiene 6 átomos de carbono, mientra que la del ácido pirúvico solo tiene 3 átomos de carbono. Dado que las reacciones que se producen en la glucólisis no requieren oxígeno, se dice que la glucólisis es anaeróbica Figura 18. La glucólisis hasta la producción de ácido láctico genera 2 moléculas de ATP que representa solo un 2.2% de la energía disponible, el 59% se pierde en forma de calor y el 38.8% se almacena como NADH que es un portador intermedio de energía. Por consiguiente la energía no se puede aportar con la inmediatez que se ha estudiado ni con las reservas de ATP, ni con las de PCr. Ello hace que al ser más lento dicho aporte de energía, se deba disminuir la intensidad del esfuerzo. Figura 17 Transformación del ácido pirúvico a ácido láctico. Actúa la enzima lactato deshidrogenasa para facilitar + la reacción y como coenzima el Nicotin Adenin dinucleótido reducido NADH+H cede electrones y se oxida a NAD+. Figura 18 Glucólisis. Carbono Oxigeno Hidrógeno Cuando el pirúvico se transforma en ácido láctico, la concentración de lactato en la sangre puede llegar a más de 20 mmol/litro de sangre, hecho que ocurre con esfuerzos extenuantes, aunque mecánicamente sean menos intensos que los observados con las reservas de ATP y PCr muscular, cuya duración no exceda de los 45 segundos. Figura 19 Variación porcentual teórica de la glucolisis anaeróbica y aeróbica en esfuerzos de diferente duración. Tal como se ha expuesto en la Tabla 1 un esfuerzo de 40 segundos de duración había disminuido la concentración de PCr en casi un 70%, aportando la mayor parte de la energía requerida, pero otra parte de la energía se debe aportar por la vía anaeróbica lactácida y una mínima parte por la vía aeróbica. El ácido láctico producido por los músculos no es un producto de desecho, ya que constituye un aporte energético valioso. Cuando el ejercicio disminuye de intensidad o bien cuando finalizamos el esfuerzo, tiene dos posibilidades de destino. La primera es que se convierta de nuevo en pirúvico y continúe, en presencia del oxígeno, el camino hacia la coenzima A y entre en el ciclo de Krebs o ciclo del ácido cítrico. El segundo camino es entrar en el torrente circulatorio, para que sea transportado al hígado y se vuelva a convertir en glucosa y glucógeno. La eliminación del lactato en sangre se produce de forma rápida, en menos de 15 minutos, dependiendo del sujeto. Durante la realización de una prueba de esfuerzo en laboratorio se puede medir la concentración de lactato en sangre en mmol/litro de sangre por micrométodos (con una sola gota de sangre). Siempre existe una pequeña concentración de lactato en sangre incluso 11 estando en reposo, que normalmente se halla por debajo de los 2 mmol/L dependiendo de cada sujeto. Se acepta por regla general que a 4mmol/L se halla el umbral anaeróbico y este dato es bastante coincidente con el Umbral anaeróbico ventilatorio (VT2) medido con un analizador de gases. Figura 20 Medición del lactato en sangre por micro métodos. Figura 21 Medición de la concentración de lactato en una prueba de esfuerzo progresiva y su relación con la frecuencia cardíaca del deportista. 12 El estudio analítico de cada uno de los sistemas para el aporte de energía puede inducir al error, que en función de la duración del esfuerzo, solo actúa uno u otro sistema, pero en realidad todos actúan al unísono pero en mayor o menor proporción, en función a la intensidad del mismo y al tiempo de duración. % Intensidad del esfuerzo 100 si s co li A DP+ PCr---- aer Via i ca ób a róbic is ae lipídico s i l có mo Glu tabolís e M ATP muscular n de ATP intra 50 D egradació 60 aeróbic Glu 80 70 an a 90 Tiempo 5s. 10s. 20s. 30s. 40s. 50s. 1min2min 3min 60min 90min 6 h. Figura 22 Integración de los diferentes sistemas energéticos para la obtención de ATP Via aeróbica. La fase I de la respiración celular, es decir la glucólisis, que convierte la molécula de glucosa en pirúvico, genera solo 2 moléculas de ATP, no obstante solo representan un 2.2% de la energía disponible. El resto se guarda como NADH (38.8%) y otra parte se pierde en forma de calor (59%). En presencia del oxígeno, el ácido pirúvico , continua su camino hacia la matriz mitocondrial uniéndose a la CoA (coenzima A) formando Acetil CoA y posteriormente sigue su transformación en el ciclo de Krebs, que es la segunda fase de la respiración celular. Cuando el pirúvico se une a la CoA el complejo suelta 2 electrones, un átomo de hidrógeno y dióxido de carbono (CO2) para formar un Acetil CoA. Los electrones y el Hidrógeno son captados por una molécula de NAD+ formando NADH que se trata de un portador de energía intermedio. En el ciclo de Krebs el Acetil CoA (Figura 23) se une a una molécula de ácido oxalacético y produce una molécula de ácido cítrico de 6 átomos de Carbono. A partir de este compuesto siguen un total de 10 pasos o transformaciones liberando en su conjunto en cada ciclo: 1 ATP, 3 moléculas de NADH, una molécula de FADH2 que es también un portador de energía intermedio que junto con el NADH llevan asociados electrones activados que se utilizarán para almacenar energía en forma de ATP. 13 Si se hace un resumen de la cantidad de energía producida hasta este momento partiendo de la molécula original de glucosa y repasando su transformación, se observa que: La glucólisis generó 2 moléculas de pirúvico y se formaron 2 ATP y 2 moléculas de NADH • Las 2 moléculas de pirúvico entraron en la decarboxilación oxidativa y se formaron 4 moléculas de NADH. • En el ciclo de Krebs participan 2 moléculas de Acetil CoA, el ciclo da dos vueltas proporcionando 2 ATP, 6 moléculas de NADH y 2 moléculas de FADH2. Por consiguiente, hasta este punto se han formado 4 moléculas de ATP, 10 moléculas de NADH y 2 moléculas de FADH2 • Figura 23 Ciclo de Krebs que se produce en la matriz mitocondrial 14 Mucha de la energía de la glucosa ha sido transferida a las molécula NADH y FADH2 entrando en la fase final denominada fosforilación oxidativa, que es donde los portadores de energía descargan sobre numerosas moléculas de ATP. La fosforilación oxidativa se produce en el interior de la mitocondria dentro de las crestas de membrana interna y siempre en presencia de oxígeno. Figura 24 Mitocondria, matriz mitocondrial y crestas de la membrana interna Dentro de las crestas de la membrana interna existen un sinfín de estructuras conocidas con el nombre de Cadena de Transporte de Electrones. Una cadena de transporte de electrones consta de cuatro complejos adyacentes que se hallan fijos dentro de la membrana interna. Figura 25 Los IV complejos de la fosforilación oxidativa La fosforilación oxidativa comienza cuando el NADH del ciclo de Krebs cede 2 electrones al primer complejo. A medida que los electrones (e-) pasan al complejo siguiente, los protones (H+) pasan de la matriz al espacio que hay entre las membranas. El NADH reducido pasa a ser NAD oxidado. Figura 26 Primer paso de la fosforilación oxidativa. 15 Los electrones (e-) pasan al segundo complejo hasta llegar al lado que da a la matriz. Al pasar al tercero complejo (Coenzima Q) un segundo par de protones (H+) serán captados de la matriz. Figura 27 Paso segundo de la fosforilación oxidativa El coenzima Q recorre toda la membrana y empuja a los protones (H+) al espacio que hay entre las membranas, mientras que los electrones pasan al IV complejo. Figura 28 Paso 3 de la fosforilación oxidativa Al final de la cadena, otros protones provenientes de la matriz pasan a través de la membrana al espacio entre membranas Figura 29 Paso 4 de la fosforilación oxidativa 16 Finalmente un átomo de oxigeno recoge dos electrones (e-) de la cadena y dos protones de la matriz (H+) para formar agua (H2O) Figura 30 Cada molécula de NADH libera 2 electrones, que moviéndose por la cadena bombean 6 protones de la matriz. El papel principal del oxígeno es recoger electrones (e-) al final de la cadena respiratoria y se une a dos protones (H+) de la matriz para formar agua. Otras moléculas portadoras intermedias de energía del ciclo de Krebs es FADH2 que entra en la cadena de transporte de electrones en la coenzima Q. Dos electrones son transportados por la cadena y 4 protones pasan al espacio entre membranas. Al final de la cadena, el oxígeno coge de nuevo los dos electrones y dos protones (H+) de la matriz para producir agua. Figura 31 El FADH2 Hasta este punto, la energía del NADH y el FADH2 se ha utilizado para bombear protones (H+) desde la matriz hasta el espacio entre membranas, dando como resultado una gran concentración de protones siendo ésta mayor en el espacio entre membranas que en la matriz. Ello crea dos tipos de desniveles en la membrana: un desnivel de concentración de protones y un desnivel electrostático. Estos desniveles tienen una energía potencial que será utilizada para sintetizar el ATP. 17 La evidencia sugiere que la energía potencial que cruza la membrana se utiliza cuando un par de protones pasan por unos canales especiales de la misma. De esta forma cada par de protones activa una enzima (ATPsintasa) en el lado del canal que da hacia la matriz. Figura 32 Flujo de protones hacia la matriz Finalmente esta enzima cataliza la reacción del ADP con un grupo fosfato para sintetizar el ATP. Figura 33 Formación de ATP En síntesis, a partir de NADH y FADH2. Cada NADH traslada 3 pares de protones al espacio entre membranas, que al volver a la matriz producen 3 moléculas de ATP. Cada FADH2 traslada 2 pares de protones al espacio inter membranas, que al volver a la matriz produce 2 moléculas de ATP. En resumen, partiendo de una sola molécula de glucosa: La glucólisis generó 2 ATP y 2 NADH que al llegar a la cadena de transporte de electrones produjeron 4 moléculas más de ATP. La decarboxilación oxidativa y el ciclo de Krebs produjeron 2 moléculas de ATP, 8 moléculas de NADH y 2 moléculas de FADH2. La 8 moléculas de NADH se convirtieron en 24 ATP y las 2 moléculas de FADH2 formaron 4 moléculas de ATP adicionales. Si se suma todas las moléculas de ATP en la respiración celular, representa que por una molécula de glucosa se producen en total 36 moléculas de ATP. 18 A falta de oxígeno, la cadena respiratoria en su punto de fosforilación oxidativa comienza a saturarse y deja de utilizarse el NADH no pudiendo reciclarse el NAD+ y deja de producirse ATP. (EMAbiolog, 2012a, 2012b, 2012c, 2012d, 2013)https://es.slideshare.net/trenmx/energa-parael-ejercicio?next_slideshow=1 Referencias bibliográficas Bernús, G., de Suso González, J., Alonso, J., Martin, P. A., Prat, J. A., & ArÚs, C. (1993). 31P-MRS of quadriceps reveals quantitative differences between sprinters and long-distance runners. Medicine and science in sports and exercise, 25(4), 479-484. Chicharro, J. L., & Vaquero, A. F. (2006). Fisiología del ejercicio. Madrid: Ed. Médica Panamericana. EMAbiolog. (2012a). Cadena Respiratoria. Mare Nostrum Ciencia y Tecnología Retrieved Noviembre, 2018, from https://www.youtube.com/watch?v=T1ndgXs8zkk EMAbiolog. (2012b). El ciclo de Krebs paso a paso. Mare Nostrum Ciencia y Tecnología Retrieved noviembre 2018, from https://www.youtube.com/watch?v=rumUBQPykHA EMAbiolog. (2012c). Glucólisis Segunda parte. Mare Nostrum Ciencia y Tecnología Retrieved Noviembre, 2018, from https://www.youtube.com/watch?v=PL_vvy28LtM EMAbiolog. (2012d). Glucólisis: Primera parte. Mare Nostrum Ciencia y Tecnología Retrieved Noviembre, 2018, from https://www.youtube.com/watch?v=Zj76gN0Qkjk EMAbiolog. (2013). Metabolismo y Nutrición. Mare Nostrum Ciencia y Tecnología Retrieved noviembre, 2018, from https://www.youtube.com/watch?v=F1Pzcy_kAXY González de Suso, J., Alonso, J., Bernús, G., Prat, J., & Arús, C. (1993). Estudi per 31P-MRS del pH muscular durant la recuperació nd'esforços d'intensitat elevada i curta durada. Paper presented at the International Meeting on Oxygen transport in health and disease, Barcelona. González de Suso, J., Bernús, G., Alonso, J., Pujol, P., Prat, J., & Arús, C. (1993). Biochemical changes in skeletal muscle after a marathon race, as assessed by Phosphorus-31 nuclear magnetic resonance spectroscopy. Med. Exerc. Med. Exerc. Nutr. Health, 2, 5054. Gonzalez de Suso, J. M., Bernús, G., Alonso, J., Alay, A., Capdevila, A., Gili, J., . . . Arús, C. (1993). Development and characterization of an ergometer to study the bioenergetics of the human quadriceps muscle by 31P NMR spectroscopy inside a standard MR scanner. Magnetic resonance in medicine, 29(4), 575-581. Gutiérrez, G., & Acero, A. (1988). Resonancia magnetica en el estudio del metabolismo celular. Archivos de bronconeumología, 24(4), 174-179. Wilmore, J. H., & Costill, D. L. (2004). Fisiología del esfuerzo y del deporte. Barcelona: Editorial Paidotribo. 19