Tema 1.1 Metales
Anuncio

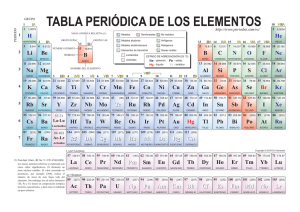
¿Qué son los metales? En el ámbito de la química, se conocen como metales o metálicos a aquellos elementos de la Tabla Periódica que se caracterizan por ser buenos conductores de la electricidad y del calor, poseer altas densidades y ser generalmente sólidos a temperatura ambiente (excepto el mercurio). Muchos además pueden reflejar la luz, lo cual les otorga su brillo característico. Los metales son los elementos más abundantes de la Tabla Periódica y de la corteza terrestre: de los 118 conocidos apenas 25 son no metálicos. Algunos de ellos suelen hallarse en estado de mayor o menor pureza en la naturaleza, mientras que la mayoría forman parte de minerales del subsuelo terrestre, de los cuales deben ser separados artificialmente. Los metales presentan enlaces característicos: enlaces metálicos (los que forman moléculas de un mismo elemento metálico entre sí) o enlaces iónicos (por préstamo de electrones). Las sales constituidas a partir de elementos metálicos forman iones electropositivos (cationes) en una disolución. Debe aclararse que incluso las aleaciones de un metal con otro (o con un no metal) continúan siendo materiales metálicos, como es el caso del acero y el bronce, aunque sean mezclas y no sustancias. Los metales han servido a la humanidad desde tiempos inmemoriales gracias a su carácter idóneo para formar herramientas, estatuas o estructuras de todo tipo, debido a sus particulares propiedades físicas: Maleabilidad. Al someterse a compresión, algunos metales pueden formar láminas delgadas de material homogéneo. Ductilidad. Al ser sometidos a fuerzas de tracción, algunos metales pueden formar alambres o hilos de material homogéneo. Tenacidad. Capacidad de resistirse a la fractura, cuando se les somete a fuerzas bruscas (golpes, caídas, etc.). Resistencia mecánica. Capacidad de soportar tracción, compresión, torsión y otras fuerzas sin ceder en su estructura física ni deformarse. Además, su brillo les hace idóneos para forjar joyas y elementos de ornato, y su buena conducción de la electricidad los hace indispensables en la transmisión de la corriente eléctrica en los sistemas modernos de energía eléctrica. Fuente: https://concepto.de/metales/#ixzz67ZwIVrnk Tipos de metales El magnesio (Mg) pertenece a los alcalinotérreos. Los elementos metálicos pueden ser de diversos tipos, según los cuales se agrupan en la Tabla Periódica. Cada grupo tiene propiedades compartidas: Metales alcalinos. Brillantes, blandos, muy reactivos a condiciones normales de presión y temperatura, por lo que nunca están puros en la naturaleza. Tienen bajas densidades y son buenos conductores del calor y la electricidad. En la Tabla Periódica ocupan el grupo I (1), excepto el hidrógeno. Metales alcalinotérreos. Situados en el grupo II (2) de la Tabla Periódica, su nombre proviene de las propiedades alcalinas de sus óxidos (llamados “tierras” antiguamente). Suelen ser más duros y menos reactivos que los alcalinos, son brillantes y buenos conductores del calor y la electricidad. Tienen baja densidad y color. Metales de transición. La mayoría de los metales pertenecen a esa categoría. Ocupan la región central de la tabla periódica y casi todos son duros, con elevados puntos de fusión y ebullición, y buena conducción de calor y electricidad. Lantánidos. También llamados lantanoides, son las llamadas “Tierras raras” de la tabla periódica, que con los actínidos forman los “elementos de transición interna”. Son elementos muy similares entre sí, y a pesar de su nombre, son muy abundantes en la superficie terrestre. Tienen comportamientos magnéticos y espectrales muy característicos. Actínidos. Junto a las Tierras raras forman los “elementos de transición interna”, y son muy similares entre sí. Presentan altos números atómicos y muchos de ellos son radiactivos en todos sus isótopos, siendo por ende sumamente escasos en la naturaleza. Transactínidos. También llamados “elementos superpesados”, son aquellos que superan en número atómico al más pesado de los actínidos, el lawrencio (103). Todos los isótopos de estos elementos tienen una vida media muy corta, son todos radiactivos y se han obtenido por síntesis en un laboratorio, por lo que poseen los nombres de los físicos responsables de su creación. Fuente: https://concepto.de/metales/#ixzz67ZwVT8Hg Ejemplos El litio (Li) es un metal alcalino. Alcalinos: Litio (Li), Sodio (Na), Potasio (K), Rubidio (Rb), Cesio (Cs), Francio (Fr). Alcalinotérreos: Berilio (Be), Magnesio (Mg), Calcio (Ca), Estroncio (Sr), Bario (Ba) y Radio (Ra). Metales de transición: Escandio (Sc), Titanio (Ti), Níquel (Ni), Cobre (Cu), Osmio (Os), Platino (Pt), Cadmio (Cd), Plata (Ag), Mercurio (Hg), y un largo etcétera. Tierras raras: Lantano (La), Cerio (Ce), Praseodimio (Pr), Neodimio (Nd), Prometio (Pm), Samario (Sm), Europio (Eu), Gadolinio (Gd), Terbio (Tb), Iterbio (Yb), etc. Actínidos: Actinio (Ac), Uranio (U), Plutonio (Pu), Americio (Am), Nobelio (No), Lawrencio (Lr), etc. Transactínidos: Rutherfordio (Rf), Bohrio (Bh), Hassio (Hs), Moscovio (Mc), Oganesón (Og), etc. Fuente: https://concepto.de/metales/#ixzz67ZwnndaN ¿Cuáles son los no metales? Los elementos esenciales para la vida orgánica son los no metálicos. Los elementos esenciales para la vida orgánica son los no metálicos, en su mayoría pertenecientes a los halógenos (7 electrones en su última capa de valencia), gases nobles (8 electrones en su última capa de valencia, excepto el helio), así como a otros grupos diversos. Se distinguen de los metálicos al no ser buenos conductores de calor y temperatura, no ser brillantes y formar enlaces covalentes. Fuente: https://concepto.de/metales/#ixzz67ZwtHF4U