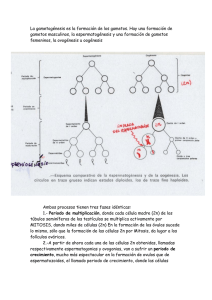
INNOVACIONES TECNOLÓGICAS Ovocito criopreservación: la búsqueda de nuevas estrategias de mejora Natalie A. Clark y Jason E. Swain 10.1007 / s10815-013-0028-8 Recibido: 11 Abril 2013 / Aceptado: 31 mayo 2013 / Publicado en línea: 19 Junio 2013 # Springer Science + Business Media Nueva York 2013 Resumen Palabras clave Ovocito. La vitrificación. Criopreservación. etapas meióticas. Propósito Para poner de relieve las técnicas destinadas a mejorar la crioconservación de Microfluídica. Composición. Membrana . Los tampones ovocitos emergente. métodos Revisión de la literatura disponible y relevante a través de búsquedas en PubMed y Medline. resultados la crioconservación de ovocitos es un procedimiento cada vez más común Introducción utilizado para la reproducción asistida y puede beneficiar a varias poblaciones de pacientes. Por lo tanto, la mejora de la eficiencia es de suma importancia en la criopreservación de ovocitos es un procedimiento cada vez más común utilizado realización de la gran promesa de este enfoque. Sin embargo, además de numerosos para la reproducción asistida y es muy prometedora para varias poblaciones de [email protected] J Assist Reprod Genet (2013) 30: 865 - 875 DOI estudios que buscan mejorar la eficacia de crioconservación de oocitos a través de pacientes. el almacenamiento de ovocitos permite preservación de la fertilidad examen de variables implicadas con la metodología de protocolo, como el tipo / para una variedad de individuos, incluidos los que sufren enfermedades o concentración de crioprotector (CPA), el tipo de dispositivo de almacenamiento, o de tratamientos que amenaza la fertilidad, los que desean retrasar la reproducción, enfriamiento / tasas de calentamiento, hay más nuevos enfoques para mejora. Estos así como aquellos que pueden ser incapaces de preservar la preimplantación de enfoques alternativos incluyen la utilización de diferentes las etapas de ovocitos, el embriones por razones sociales, médicas, éticas o legales. Por otra parte, la examen de la alteración de medios basales y composición del tampón, la optimización de criopreservación de ovocitos proporciona alternativas logísticas para la gestión protocolos de intercambio de CPA y la carga de dispositivo a través del uso de tecnología del ciclo, permite pruebas de enfermedades, y facilita servicios emergentes, automatizada, así como el examen / manipulación de la composición celular de los como los bancos de donación de óvulos. ovocitos para mejorar criotolerancia. Por último, la elucidación de los indicadores más precisos o interesantes de “ éxito ” es crucial para la mejora continua de la crioconservación de ovocitos. No es sorprendente que cantidades crecientes de la investigación se han centrado en mejorar la eficiencia de los ovocitos criopreservación. Sin embargo, Place Bldg 1 Ste B, Ann Arbor, MI 48108, EE.UU. e-mail: aspectos únicos del ovocito lo convierten en una celda muy difíciles de criopreservar. Conclusión criopreservación de ovocitos ha mejorado dramáticamente en los Por ejemplo, la relación de volumen-tosurface del ovocito es mayor que otras células, últimos años y está recibiendo su uso clínico generalizado. Nuevos enfoques lo que complica el proceso de deshidratación [ 5 , 73 , 74 , 100 ]. También, para mejorar aún más el éxito, así como la mejora de los métodos para evaluar características de la membrana y las diferencias de permeabilidad aparecen tomake este éxito ayudará en la mejora continua. el ovocito más sensibles al daño por frío [ 73 , 97 ]. Es bien sabido que la crioconservación de ovocitos induce la liberación prematura gránulo cortical causando endurecimiento zona que interfiere con la fertilización, lo que exige el uso Cápsula Nuevas estrategias para mejorar la crioconservación de ovocitos pueden permitir una de ICSI [ 20 , 35 , 38 , 40 , mayor eficacia y una mayor aplicación. NA Clark: JE Swain 64 - 66 , 69 , 92 ]. Además, debido a las altas tasas de ovocitos deriva aneuploidía humana, Departamento de OB / GYN, Universidad de Michigan, Ann Arbor, MI 48108, alteraciones en el ovocito huso meiótico en respuesta a las bajas temperaturas EE.UU. fromcryopreservation [ 36 , 56 , 86 ] Son preocupantes en relación con el impacto potencial JE Swain (*) Centro de Medicina Reproductiva de la Universidad de Michigan, 475 Market sobre la remodelación del cromosoma. Por lo tanto, mientras que los métodos exitosos de la criopreservación de embriones pueden ser un punto de partida válido en la exploración de métodos para la crioconservación de oocitos, estos únicos J Assist Reprod Genet (2013) 30: 865 - 875 866 cualidades de ovocitos deben tenerse en cuenta al adoptar o modificar la estos componentes de husillo despolimerizan, aunque se debe mencionar que el metodología para mejorar los resultados. aumento de temperatura lo permite aparente normal de re-polimerización [ 37 , 56 ]. Aunque a velocidad controlada o lenta tasa de congelación de ovocitos puede Es importante destacar que, como se mencionó, no todas las etapas de oocitos tener éxito [ 9 - 11 ], La vitrificación ha surgido como el enfoque preferido aparente que han formado distintamente / organizado husos meióticos y, curiosamente, no todas produce excepcionalmente altas tasas de supervivencia y nacidos vivos exitosas [ 19 las etapas de ovocitos parecen tener el mismo nivel de sensibilidad a los efectos , 82 ]. Numerosos artículos de revisión han resumido los principios detrás de la térmicos sobre el huso meiótico. Por ejemplo, se demostró que los ovocitos refrigeración de tipo lento y vitrificación de células, incluyendo ovocitos [ 9 , 44 , 58 , 74 telofase I de ratón mantenido la estabilidad más husillo cuando se enfría a 4 ° C , 81 , 82 ]. Estas revisiones tienden a cubrir ampliamente los enfoques tradicionales durante 10 min en comparación con los dos ovocitos MI y MII, como se indica por destinadas a optimizar estos dos enfoques de crioconservación, que incluyen microscopía de luz polarizada [ 36 ]. alteraciones en la temperatura de solución de equilibrado, el uso y la optimización de penetrar numerosos y no penetrante CPAs y sus combinaciones, así como la aplicación de diversos contenedores que pueden afectar el enfriamiento y tasas de Ciertamente, la estabilidad husillo previamente ha sido examinada como un calentamiento. Estos enfoques han dado como resultado tasas de supervivencia de método para mejorar la competencia de desarrollo después de la crioconservación. los ovocitos de ~ 90%, y los resultados reproductivos asistidos se aproximan a las Varios estudios han examinado el uso de compuestos farmacológicos, tales como de los ciclos de ovocitos frescos. Taxol, para manipular la estabilidad del huso meiótico en la esperanza de mejorar criotolerancia [ 31 , 62 , 63 , 79 ]. Sin embargo, el uso de compuestos farmacológicos no puede ser clínicamente factible. Independientemente, si una etapa meiótica específica de ovocitos Sin embargo, además de estos métodos de mejora ampliamente examinados, muestra mayor menos integridad / husillo, este pone la base básica y promueve la puede haber más novedosos enfoques que podrían mejorar aún más la eficiencia de cuestión de si una etapa de ovocito progresión meiótica puede ser más adecuado para crioconservación de ovocitos. Esta opinión se centra en estas técnicas emergentes y soportar las tensiones térmicas u otros insultos transmitidos por el proceso de presenta los datos preliminares para las metodologías que incluyen la alteración de la criopreservación [ 12 ] (Higo. 1 ). oocitos GV intactos carecen de un huso meiótico distinta, etapa de la fase meiótica del ovocito criopreservado, la alteración de medios de y el material genético está confinado dentro de la envoltura nuclear. Por lo tanto, la comunicación y la composición del tampón para aliviar el estrés pH, la optimización de criopreservación en esta etapa puede proporcionar un medio para mitigar los daños protocolos de intercambio de CPA y la carga de dispositivo a través del uso de causados por la crioconservación y para mejorar la supervivencia de los ovocitos. Sin tecnología automatizada, como así como el examen / manipulación de la composición embargo, los primeros estudios indicaron dificultad con la preservación de oocitos GV celular de los ovocitos para mejorar la selección de células y / o criotolerancia. intactos humanos, como se evidencia por las bajas tasas de éxito [ 89 , 90 ]. Las tasas de supervivencia actuales de GVoocytes vitrificados después de calentamiento están en el rango de 55 a 75% [ 2 , etapas de ovocitos para la criopreservación 18 ]. En al menos un estudio, la vitrificación de GVoocytes no tuvo ningún impacto aparente sobre la reanudación de la meiosis como estos ovocitos alcanzaron la Tradicionalmente, la metafase II (MII) ovocitos se seleccionan para la maduración nuclear completa hasta la metafase II postwarming y mantenido metilación crioconservación. Sin embargo, como se mencionó, sensibilidad a la normal de genes tales como H19DMR y KvDMR1 [ 2 ]. Como un beneficio adicional, temperatura del huso meiótico en esta etapa puede ser motivo de GVoocytes se pueden obtener de ciclos no estimulados o mínimamente estimuladas, preocupación en lo que se refiere a la fidelidad de la remodelación cromosoma que pueden proteger al paciente de condiciones perjudiciales asociados con la y ovocito derivado aneuploidía embrionario. Para revisar, el ovocito de reposo estimulación de la hormona, y es menos costoso. Por supuesto, eficiente vitro la en la profase de la meiosis I, también conocido como un ovocito intacta maduración de ovocitos en (IVM) también es un pre-requisito para la crioconservación vesícula germinal (GV-intacto), se reanuda la meiosis, se somete la disolución de oocitos GV-y lleva consigo preocupaciones de su propio. oocitos crioconservados de la membrana nuclear, a continuación, avanza a MI, anafase I, telofase I y maduran menos eficazmente que sus homólogos frescos [ 15 , 28 ]. Además, la presencia re-detenciones en MII hasta que se produce la fertilización. Durante este de células del cumulus es un factor a considerar, ya que su presencia mejora la tiempo, el huso meiótico se dispersa en primer lugar con un poste situado maduración de ovocitos, sin embargo, no pueden sobrevivir crioconservación de manera cerca de la periferia del ovocito. Como se reanuda la meiosis y se disuelve la eficiente en los protocolos optimizados para la supervivencia de ovocitos [ 87 ]. GV, las formas de husillo MI la estructura bipolar familiarizados ya que reúne Actualmente, sólo un hijo nacido vivo se ha reportado después de la criopreservación de en la placa de la metafase. GVoocytes humanos que fueron posteriormente maduraron in vitro antes de la ICSI [ 93 ]. Por lo tanto, en este momento, la eficiencia de la criopreservación GV intactos sigue siendo inferior a ovocitos MII Es importante destacar que, el huso meiótico es un conglomerado dinámica de la tubulina y proteínas asociadas que están en un estado constante de flujo como microtúbulos / proteínas despolimerizan y re-polimerizan. Disminuciones en la temperatura aparecerá para desplazar este equilibrio dinámico de modo que al menos una parte de Alternativamente, si la crioconservación de ovocitos telofase, debido a su aparente estabilidad husillo mejorada a baja 867 Reprod Genet (2013) 865 - 875 pueden hacer que sea30: atractivo para la criopreservación Jque Assist etapa tiene propiedades células y negativas características únicas dede las célulaspositivas en las diversas etapas. potencialmente mejorar supervivencia resultados debido Cada a las meióticas puede ofrecer la más opciones de/en tratamiento Figura 1 La criopreservación de ovocitos diferentesyetapas temperatura, puede permitir tasas de supervivencia superiores o los resultados en Medios de comunicación comparación con los ovocitos MII tradicionales sigue siendo desconocida. Curiosamente, se informó de que congelación lenta tasa de ovocitos dentro de 2 h de Gran parte de la atención en los medios de comunicación utilizados para la recuperación resultó en una mayor calidad de embriones, las tasas de embarazo e crioconservación se centra en el tipo, concentración y tiempo de exposición de implantación en comparación con los oocitos congelados después de 2 h [ 68 ]. Debido a crioprotectores (CPAs). CPAs funcionan como su nombre implica, la protección que los ovocitos se recuperan en un momento antes de la ovulación, su maduración contra el daño celular crio-inducida, incluyendo los daños mecánicos de la final se completa in vitro. ovocitos telofase hacen mostrar un cuerpo polar. Por lo tanto, formación de cristales de hielo. Existen varios CPAs, tanto impregnando y no es factible que una parte de estos ovocitos congelado <2 h después de la recuperación impregna, y han sido revisados en otras partes [ 88 ], Y un examen detallado de eran todavía en la telofase I etapa. Existe muy poca información en cuanto a cómo cada compuesto está más allá del alcance de esta revisión. Sin embargo, está metafase I o anafase I ovocitos tolerar la criopreservación. También hay que mencionar claro que no todos los contadores públicos funcionan igual de bien con el ovocito que la fertilización después de la descongelación de ovocitos criopreservados tendría delicada. Esto probablemente se debe a un equilibrio entre la CPA ' s permeabilidad que ser optimizado para asegurar el estado de maduración y fertilización adecuada [ 22 , en relación con el tamaño y la permeabilidad única de la membrana del ovocito, así 45 ]. Esto sería más fácil que la maduración de ovocitos criopreservados GV-intacta, ya como la CPA ' toxicidad s. Como resultado, algunos contadores públicos han que no es probable ser necesarios medios especializados IVM. recibido un uso más extendido de lo que los demás, y esto sin duda sigue siendo un área de mejora futura J Assist Reprod Genet (2013) 30: 865 - 875 868 El uso de nuevas macromoléculas y polímeros sintéticos también tienen beneficiosa para la vitrificación de oocitos, la protección de la función mitocondrial [ 98 ]. potencial para mejorar la crioconservación de ovocitos. Los estudios que examinan el uso de Ficoll [ dieciséis , 23 ], Fetuina [ 42 ] Y hialuronano [ 54 ] Tener toda promesa Además de los requisitos de sustrato de energía, lo que probablemente deben ser se muestra en la mejora de los resultados de criopreservación, incluyendo la de los optimizados basado en la fisiología de los ovocitos, en lugar de usar la formulación de medio ovocitos. El uso de estos compuestos y métodos novedosos para su carga celular, basal para diversas etapas de embriones de preimplantación, se debe considerar a otros como la microinyección, se han discutido en otra parte [ 88 ]. componentes de los medios de comunicación basal. Para que no olvidemos, los medios de comunicación de base también pueden afectar a los efectos tóxicos de los contadores públicos [ 49 Un aspecto menos bien estudiado de mejorar la crioconservación de ovocitos ]. Por ejemplo, la sustitución de colina de cloruro de sodio mejoró ovocito lenta velocidad de incluye la consideración del medio basal utilizado (Fig. 2 ). Por ejemplo, muchos enfriamiento [ 84 , 85 ]. Además, debido a la función de las oscilaciones de calcio en desarrollo de medios de comunicación utilizan un HEPES estándar o MOPS base de manipulación, los ovocitos y la función, incluyendo un papel si exocitosis de gránulos cortical, y el potencial que a menudo se formulan para varios embriones en la etapa e incluyen niveles de para la crioconservación para provocar o interferir con estas oscilaciones, el agotamiento de glucosa elevados. desprovistas de ovocitos no tienen las mismas necesidades calcio de los medios de comunicación de ovocitos de criopreservación puede ser beneficioso y metabólicas como embriones y los niveles de glucosa o de otros sustratos probable prudente [ 57 ]. El uso de un Ca + 2 medios de comunicación libres, se informó de que los ovocitos deben ajustarse. Otros requisitos de los ovocitos fisiológicas únicas, como de ratón vitrificados tenían menos endurecimiento zona y la mejora de la fertilización y el complemento de aminoácidos, también deben ser considerados. El ovocito tiene desarrollo embrionario. métodos únicos de la regulación del volumen celular [ 6 , 102 ], Y esto es una consideración crítica debido a los cambios de osmolalidad extremas experimentadas durante la exposición a y la eliminación de las soluciones utilizadas en la En una manera similar, otras alteraciones medios basales pueden ser importantes. criopreservación. Debido al papel de los aminoácidos como osmolitos, los Específicamente, medios basales contienen tampones zwitteriónicos para estabilizar el pH aminoácidos correctos también deben ser incluidos. Por ejemplo, la glicina es un y prevenir perturbaciones perjudiciales en la concentración de iones de hidrógeno que osmolito potencial y se han encontrado niveles elevados podrían comprometer la función de los ovocitos. Se sabe que el pH incorrecto puede afectar el desarrollo del embrión, el metabolismo y el desarrollo fetal [ 53 , 83 , 99 ]. Figura 2 El uso de crioprotectores específicos ovocitos, dirigidas a abordar características de formulación de medios, incluyendo sustrato y la composición de sal. Aunque el uso de un permeabilidad de la membrana de los ovocitos y otras propiedades fisiológicas únicas, es crítico en la solo sistema de medios y criopreservación basal para preimplantación de embriones de optimización de los resultados. Del mismo modo, la consideración de los requisitos de los ovocitos se varias etapas y oocitos puede ser conveniente, las condiciones deben ser optimizado basado debe dar la selección de la basal en la fisiología del ovocito 869 J Assist Reprod Genet (2013) 30: 865 - 875 También puede interrumpir la organización del citoesqueleto y las mitocondrias [ 70 , 83 ]. Es importante destacar que existen cuestiones prácticas con regímenes de exposición CPA impactos similares pueden ser evidentes en el ovocito también. Esta probabilidad se actuales que limitan la precisión y repetibilidad. La mayoría de los protocolos dan rangos amplios incrementa cuando se considera el hecho de que el ovocito maduro denudado, la etapa para la exposición de la célula. También, se requieren etapas de dilución manual discretos para más comúnmente criopreservados, carece de mecanismos robustos para regular el pH hacer a la exposición CPA factible. Sin embargo, mientras que logísticamente importante para el interno [ 29 , 30 ] Y es por tanto muy dependiente de la estabilidad del pH externo de los embriólogo, estos enfoques no pueden ideal de la célula. Por lo tanto, es evidente que en la medios de comunicación. Además, la vitrificación puede resultar en un lapso temporal actualidad, los laboratorios carecen de las herramientas necesarias para llevar a cabo el en los mecanismos de regulación unidas a la membrana destinadas a regular el pH intercambio de CPA precisamente en el nivel celular. interno dentro del embrión [ 53 ]. Por lo tanto, la vitrificación probable compromisos adicionales lo poca capacidad tiene el ovocito maduro denudada para regular su pH Aunque el concepto de intercambio de CPA de tres pasos está ampliamente interno. Por lo tanto, el mantenimiento de un pH externo estable y apropiada durante la aceptado para la vitrificación de ovocitos, el procedimiento exacto varía de un crioconservación de ovocitos es especialmente importante. laboratorio a contribuir a la variabilidad en las tasas de éxito de criopreservación. Más fundamentalmente, hay un problema que hay más combinaciones potenciales de CPAs y procedimientos de intercambio de CPA que podrían utilizarse que puede ser probado de manera eficiente y fiable para por ensayo y error experimentos solo. Debido a los diferentes medios y sus buffers responden de manera diferente al El enfoque de uso de dispositivos de bioingeniería especializados para diseñar proceso de congelación, algunas que conduce a grandes perturbaciones en pH [ 96 ], protocolos de intercambio de vitrificación de CPA, donde diluciones manuales no Esto podría ser problemático para los protocolos de tasa lenta, lo cual puede exponer a limitan la eficacia, podría ayudar a aliviar tanto el choque osmótico (efectos las células a las perturbaciones de pH con el tiempo. Por ejemplo, el uso de un medio mecánicos) y la toxicidad CPA (efectos químicos). A más gradual, en lugar de tamponado con fosfato parece ser ácida cuando se enfría, mientras tampones tales aumentos escalonados repentinos, en CPA se conoce la concentración para como HEPES o MOPS resultan en la alcalinización como lo demuestra el rojo aumentar la viabilidad [ 51 ]. Existe un límite práctico y capacidad, sin embargo, en colorimétrico pH indictor fenol [ 96 ]. Formulación de un medio tamponado independiente términos de howmany pasos de exposición y en qué momento el intercambio de CPA temperatura aunque combinación de tampones puede ser beneficiosa en la se puede realizar utilizando el estándar de oro actual: pipeteo manual. Además, la estabilización de pH durante el proceso de enfriamiento. De hecho, este enfoque se transferencia de ovocitos de solución a solución para cada paso implica pipeteado utilizó para la refrigeración de las células somáticas [ 80 ] Y enfoque similar puede ser útil rápido que puede introducir tensión mecánica [ 51 ]. para los ovocitos. Alternativamente, tampones específicos pueden transmitir otros efectos beneficiosos independientes de su capacidad de estabilización del pH. la supervivencia espermática y daño de la membrana se diferencialmente afectados por diferentes tampones [ 14 , 21 , 33 , 39 , Para hacer frente a estas limitaciones actuales con los enfoques manuales, dispositivos microfluídicos se han diseñado donde, en lugar thanmoving el ovocito de una solución de CPA a otra mediante pipeteado, el ovocito se mantiene estacionario con 96 ]. Lo mismo puede decirse respecto a los ovocitos. Por ejemplo, se informó de soluciones de CPA automatizados flujo e intercambio sobre la celda. Esto permite la que MOPS fue superior a HEPES en la vitrificación de embriones humanos, exposición celular continua y gradual, en lugar de paso discretos incrementos en las aunque la razón de esto no está clara y existió otras variables [ 24 ]. Además, TES concentraciones de CPA. Los informes preliminares indican controlados exposición CPA puede ser un tampón beneficioso para la crioconservación debido a la similitud con una plataforma de microfluidos reducida ovocito cambio de tamaño en comparación estructural con algunas crioprotectores [ 47 ]. con los enfoques tradicionales, que puede ser importante para la viabilidad celular [ 41 ] (Higo. 3a ). Enfoques similares han sido utilizados con embriones [ 61 ]. Por lo tanto, la selección de tampones específicos basados en la sensibilidad de oocitos, la exploración de nuevas combinaciones de amortiguamiento para mitigar los cambios de pH y dando como resultado el estrés ovocito, así como la inclusión de estos tampones en un medio Otra mejora potencial evidente a través de la exposición crioprotector automatizado basal formulado en las necesidades metabólicas de los ovocitos pueden ayudar aún más a es la estandarización de la carga de ovocitos cryodevice. De hecho, una limitación que ha refinar y mejorar metodologías de crioconservación de ovocitos actuales. dificultado rápida y amplia aceptación de los enfoques de vitrificación se ha centrado en cuestiones de facilidad de uso de los dispositivos de vitrificación. Hay numerosos dispositivos disponibles comercialmente y interno para contener ovocitos para el almacenamiento a baja temperatura de vitrificación siguientes [ 17 ]. Estos utilizan exposición CPA optimizada y la carga volúmenes muy pequeños de solución para permitir el rápido enfriamiento / vitrificación y evitar dañar los cristales de hielo formation.While recipientes tanto de apertura y cierre se Quizás tan importante como protección de la infancia, las condiciones de exposición CPA puede utilizar con éxito, la combinación de la baja volumen y necesidad rápido tiempo puede afectar la función celular y la supervivencia; con factores como la concentración y necesario para cargar los dispositivos para prevenir la toxicidad de CPA la exposición tiempo de exposición como variables cruciales [ 96 ]. Esto es especialmente cierto para los puede ser problemático, especialmente en comparación con 0,25 pajitas cc utilizados con enfoques de vitrificación, que utilizan altas concentraciones de crioprotectores. Se pensó que los enfoques de tasa lenta. Una novedosa plataforma de regulación exposición solución a la optimización de los procedimientos de intercambio de CPA podría ayudar a reducir el daño los ovocitos, que también integra una de los ovocitos sub-letal (Fig. 3 ). J Assist Reprod Genet (2013) 30: 865 - 875 870 Fig. 3 carga optimizada de crioprotectores (CPA) puede mejorar cryosurvival ovocito mediante la dispositivo teórico para automatizar y optimizar ovocito mezcla CPA y la carga por el flujo de medios mitigación de tensiones debidas a intercambio de medios rápida y resultante turnos de osmolalidad. una de comunicación en el ovocito. La incorporación de un dispositivo de soporte en la cámara de carga dispositivo Amicrofluidic se ha demostrado que ser capaz de cargar gradualmente CPA en ovocitos de CPA puede aliviar la variabilidad y reducir los errores de carga con dispositivo. Después de la ratón y evitar excursiones de volumen rápidos normalmente experimentar con métodos manuales exposición, el dispositivo de carga se puede retirar y se enfrió inmediatamente / vitrificado. Un actuales de movimiento ovocitos entre los medios de comunicación separado (0 mM PROH a PROH dispositivo de mezcla gradual similar puede ser útil durante la descongelación / calentamiento para 1,5 mM; adaptado de [ 41 ]). Además, este enfoque puede reducir el estrés debido al movimiento físico optimizar CPA descarga del ovocito. segundo Esquemática de una congelación dispositivo, podría simplemente pasar por alto el procedimiento actual paso a paso y En efecto, los intentos de modificación de la composición de la membrana plasmática del eliminar los errores con diluciones manuales y movimiento de las células a través de diversos oocito bovino mediante la alteración de la composición de ácido graso poliinsaturado con medios de comunicación y la carga de dispositivos complicados (Fig. 3b ). liposomas para resistir lesión Luego del enfriamiento a ~ 16 ° C o 0 ° C se han intentado y parecen mejorar la viabilidad tal como se determina por el aumento de formación de blastocistos [ 4 , 101 ]. Del mismo modo, la maduración de ovocitos bovinos con medio suplementado con composición de los ovocitos altos niveles de ácidos grasos no esterificados podría impactar negativamente criotolerancia, posiblemente a través de la membrana de composición de alteraciones, Mientras varios intentos de mejorar la crioconservación de ovocitos se han centrado en los aunque esto queda por demostrar [ 78 ]. A la inversa, el aumento del contenido de colesterol enfoques técnicos o metodología que implican regímenes de exposición, CPA / de las membranas de esperma o de ovocitos con ciclodextrano cargado colesterol también refrigeración tasas de calentamiento o recipientes para almacenar los ovocitos, la parece mejorar criotolerancia [ 43 , 76 ]. Estos factores probable transmiten sus efectos a composición celular inherente es una variable crucial tener en cuenta. Componentes de la través de alteraciones en la fluidez de la membrana y los cambios en la resistencia a los célula que controlan la fluidez de la membrana y / o regulan el cambio de agua / CPA factores estresantes mecánicos. tendrá un impacto en la dinámica del proceso de congelación / vitrificación e influir en las tensiones mecánicas experimentadas por la célula (Tabla 1 ). de membrana cambios de composición adicionales que pueden beneficiar a los ovocitos durante la criopreservación incluyen los que 871 J Assist Reprod Genet (2013) 30: 865 - 875 tabla 1 Ovocitos composición modificaciones y enfoques utilizados que pueden mejorar criotolerancia modificación de la composición la reducción de lípidos citoplasmática grasos de membrana composición de ácidos alteración Enfoque tipo de célula / Especies Referencia [ 7 , 67 ] Micromanipulación / eliminación mecánica Ovocito / Porcino ajuste de los medios de comunicación / manipulación farmacológica Embrión / Bovino Los liposomas Ovocitos, esperma / Bovino [ 4 , 19 , 101 ] la suplementación de medio de maduración manipulación contenido de colesterol de membrana carga ciclodextrano Ovocito / Bovino [ 43 , 76 ] contenido acuaporina membrana microinyección ARNc Ovocito / Ratón [ 97 ] regular la permeabilidad al agua. El aumento del ratón membrana del ovocito daño letal. Por ejemplo, aunque la intención de CPAs es para evitar daños acuaporina 3 de expresión a través de la inyección de ARNc pareció aumentar la durante el enfriamiento / congelación, algunos de estos compuestos pueden ellos permeabilidad al agua y ayudó a mejorar criotolerancia, medido por el mejor mismos resultan en daño celular. En oocitos, la evaluación de los daños de CPAs desarrollo del embrión después de la vitrificación / calentamiento [ 97 ]. y refrigeración ha tendido a concentrarse en modificaciones ultraestructurales del huso meiótico, citoesqueleto de actina, arreglo cromosómico y otra distribución contenido de lípidos citoplasmática es otro aspecto de composición de células orgánulo. Otros estudios han examinado los puntos finales funcionales por medio que influye criotolerancia celular. alto contenido de lípidos citoplasmática reduce la de la evaluación de la fecundación y el desarrollo embrionario. Por desgracia, los supervivencia de embriones bovinos y porcinos siguiente vitrificación y cultivo de efectos adversos pueden no ser tan evidente. están siendo identificados todavía embriones en presencia de compuestos que reducen el contenido de lípidos Los mecanismos exactos por los que surgen de la toxicidad de agentes citoplasmática mejora criotolerancia [ 1 , 71 ]. En teoría, la importancia del contenido de crioprotectores. Los ejemplos de daños inducidos por la exposición de células lípidos de criotolerancia también puede ser cierto para los ovocitos y los enfoques de impropio CPAs van desde la eliminación o la fusión de las membranas celulares a cultivo se pueden adaptar para manipular el contenido de lípidos de ovocitos para la actividad enzimática alterada, alterado estructura orgánulo y la función, 3 , 26 , 27 mejorar el éxito. En apoyo de esta teoría, la eliminación mecánica de lípidos ]. efectos perjudiciales de la exposición CPA en genotoxicidad, incluso sin la citoplasmática de ovocitos porcinos GV-intactas mejoró cryosurvival siguiente crioconservación, además, se han demostrado [ 8 ]. Incluso genotoxicidad sub-letal vitrificación [ 67 ]. tales como la fragmentación del ADN [ 60 ] Todavía puede causar resultados catastróficos [ 25 , 94 ] Si el contenido de lípidos citoplásmica es inversamente proporcional a cryosurvival, a continuación, el contenido de lípidos, o falta de ella, puede ser un factor importante en los criterios de selección de los ovocitos que mejor sobrevivirán criopreservación. Por desgracia, la cuantificación de lípidos se ha visto limitado por sus técnicas y todavía Por lo tanto, tan importante como nuevos métodos para mejorar la tiene que ser un ensayo común integrado en el entorno clínico. Los enfoques actuales crioconservación de ovocitos son, la determinación de nuevos métodos de evaluación para la cuantificación de lípidos de fluorescencia celular incluyen etiquetado [ 44 , 58 , 81 ], de estaciones viabilidad puede también ser útil en la mejora de los protocolos (Tabla 2 ). En capa fina y cromatografía de gases [ 31 , Estos incluyen los marcadores moleculares y bioquímicos que se pueden utilizar para evaluar la eficacia de los enfoques de crioconservación experimentales. Por otra parte, 37 , 62 , 63 ] Y microscopía electrónica [ 12 , 32 , 79 ]. Sin embargo, estas técnicas no si se quiere aplicar la evaluación de la viabilidad de selección de ovocitos después de destructivas no pueden ser utilizados para selecciones de ovocitos candidato para su la descongelación, a continuación, se requiere también el desarrollo de técnicas no eventual crioconservación. Por lo tanto, si los métodos de cuantificación de lípidos no invasivas. Hay muchos de las técnicas de evaluación nuevos postulados para evaluar invasiva pueden ser desarrollados e integrados en un entorno clínico, esto puede ser la eficacia de los enfoques de crioconservación, incluyendo cuantificación de calcio útil en la selección de candidatos para la crioconservación de ovocitos y la mejora de intracelular, la metabolómica, proteómica, imágenes celulares, la evaluación de la las estrategias para mejorar la gestión de los ciclos de los pacientes. De hecho, se unión y el análisis de la modificación epigenética hidrógeno. está explorando la cuantificación no invasiva de lípidos ovocito para facilitar esta tarea. Coherente anti-Raman Stokes microscopía (CARSM) se ha utilizado para cuantificar el contenido de lípidos de los oocitos a partir de especies con diferencia conocidos, incluyendo ratón, humana y de cerdo [ 46 ]. La cuantificación de calcio intracelular (Ca yo) es un método para examinar la viabilidad de punto final en el contexto de la crioconservación de ovocitos. California yo es responsable de iniciar la liberación de gránulos cortical después de la penetración del esperma, y por lo tanto su análisis pueden ser esenciales para el diagnóstico de trauma celular [ 48 ]. California yo oscilaciones se pueden cuantificar usando calciumindicators fluorescentes, tales Métodos de evaluación de la viabilidad como Indo-1, y los cambios resultantes se pueden cuantificar usando sistemas de detección basados en tubo CCD o fotomultiplicador. Aunque no es probable útil A pesar del éxito con la vitrificación de ovocitos, todavía hay mucho trabajo a realizar en cuanto a la supresión de sub-ovocito para propósitos de selección clínicos, este enfoque puede ser útil en experimental J Assist Reprod Genet (2013) 30: 865 - 875 872 Tabla 2 Métodos de evaluación de la viabilidad de los ovocitos. Existen varios métodos de evaluación útiles son métodos que permiten la evaluación no invasiva de la viabilidad de oocitos siguientes invasivas que pueden usarse para mejorar aún más protocolos de crioconservación y descongelación calentamiento / descongelación a una mejor ayuda en la selección de los ovocitos de alta calidad y los experimentales. Sin embargo, especialmente embriones resultantes para uso clínico subsiguiente Objetivo Evaluación Referencia la captación de piruvato la captación de piruvato Disminución se puede utilizar como un proxy para el estrés crio-inducida en el ovocito. Si analítica [ 52 ] métodos son lo suficientemente sensibles y los tiempos de giro alrededor apropiado, las células podrían ser cultivadas individualmente para ayudar en la selección de embriones para la transferencia que vinieron de oocitos de mayor calidad. aparición de LDH Lactato deshidrogenasa (LDH) aparición en los medios de comunicación que rodean el ovocito se puede utilizar para indirectamente [ 13 ] evaluar daño de la membrana crio-inducida. estabilidad huso meiótico / formación Polscope de imágenes permite una rápida visualización del huso meiótico de vida y de ovocitos MII no fijado [ 50 , 95 ] sin comprometer la viabilidad. Esos oocitos que muestran un huso meiótico intacta pueden ser más adecuados para su uso. protocolos de optimización. Hay varios informes de zona crioinducido endurecimiento [ 57 , 59 destinada a la producción de ovocitos con perfiles proteoma similares después de la ] Secundaria a Ca yo- inducida por la liberación de gránulos cortical, y el análisis de Ca yo ha crioconservación, más similares a las de los oocitos frescos, puede ser un medio puesto de manifiesto que la exposición a los crioprotectores impregnan convencionales, para mejorar diversos protocolos. tales como propanodiol, etilenglicol y DMSO, todo el resultado de forma independiente en Tal vez lo más prácticamente en este punto, los avances en la tecnología de un aumento de Ca yo, que a su vez tiene el potencial para iniciar la activación del ovocito, imagen permiten la evaluación morfológica del huso meiótico y el citoesqueleto sin culminando en zona de endurecimiento [ 34 ]. Por lo tanto, el uso de crioprotectores menos requerir la fijación de células. Con el advenimiento de un microscopio de luz nocivos y / o concentraciones para reducir al mínimo la liberación Calicium puede ser útil. polarizada, ahora es posible a la imagen del huso meiótico de los vivos y de los Sin embargo, la utilización de la inyección intracitoplasmática de espermatozoides (ICSI) ovocitos MII no fijado, sin comprometer la viabilidad [ 50 , 95 ]. Esto permite la puede pasar por alto algunos de estos efectos perjudiciales sobre la fertilización supervisión casi continua del huso durante la criopreservación y podría aclarar aún subsiguiente. más cambios celulares relacionados con la protección de la infancia o diferentes protocolos de criopreservación / calentamiento y quizás identificar las células que lo hará o tienen “ sobrevivió ” el proceso más eficaz. Curiosamente, existen varios otros Otro método que puede ser útil en los protocolos no sólo la optimización, sino enfoques de formación de imágenes no invasiva que se ha demostrado que ser también como una herramienta de selección, puede ser a través del examen de la compatible con la viabilidad del embrión y puede facilitar la evaluación de más nuevos metaboloma ovocito. En un estudio realizado por Lane & Gardner, se encontró que la criterios de valoración para evaluar ovocito viabilidad postwarming / descongelación. medición no invasiva de la captación de piruvato de oocitos vitrificados a ser menor que los oocitos frescos, sin embargo, mayores ovocitos de tasa lenta congeladas, lo que sugiere que la captación de piruvato se pueden utilizar como sustituto de la inducida por crio- la tensión en el ovocito [ 52 ]. Estudios similares han indicado que mediante la Finalmente, las modificaciones epigenéticas pueden ser utilizados para medición de la aparición de la lactato deshidrogenasa (LDH) en los medios de monitorear los cambios secundarios de la crioconservación. metilación del ADN y comunicación que rodea el oocito, es posible evaluar indirectamente-cryo inducida las histonas modificaciones son dos modificaciones epigenéticas que alteran el membrana daños [ 13 ]. Es importante destacar que, para ser clínicamente útiles, estos estado funcional de la cromatina y activan o reprimen la activación de genes. La enfoques tendrían que ser capaces de llevar a cabo con rapidez, y con la sensibilidad epigenética mechanismwhereby una copia de un gen se silencia, lo que lleva a la para detectar los niveles de ovocitos cultivados de forma individual si se utiliza un medio expresión parental-específico, se conoce como la impronta genómica. Un estudio de evaluación de la viabilidad / selección. realizado por Trapphoff et al. demostró que ultra-rápido de vitrificación de los folículos preantrales ratón seguido de largo plazo IVM a oocitos de la GV llevó a Snrpn LOM (1/50 hebras), pero no Igf2r LOM (0/15 hebras) o H19 GOM (0/58 Con los recientes desarrollos en la espectrometría de masas, ahora es posible hebras) en agrupado vitrificado ovocito [ 91 ]. En un segundo estudio, los ratones evaluar los patrones específicos de expresión de proteínas, o los proteomas, que produjeron siguiente conjunto de crioconservación ovario H19 normales mantenido reflejan diferentes estados biológicos [ 72 , 77 ]. Mediante el uso de superficie y proporciones de metilación Kcnq1ot1. Por desgracia, una limitación de este mejorada láser de desorción / ionización de espectrometría de masas en tiempo estudio es que un promedio de los niveles de metilación de tres tejidos de 5 a 36 offlight es posible determinar el proteoma de pequeños grupos de oocitos [ 55 ]. La ratones puede tener defectos de impronta oscurecidas en ratones individuales [ 75 ]. ventaja de este enfoque es que es posible obtener a través de chips de proteínas, un En los seres humanos, la vitrificación de GVoocytes seguido de corto plazo IVM amplio perfil de proteínas en gametos en diferentes condiciones, tales como las resultó en H19 GOM en piscinas de ovocitos MII (5/29 hebras), aunque esto no fue congelado con diferentes CPAs. Esto ha sido utilizado para mostrar alteraciones significativamente diferente de MIV-sólo ovocitos MII (3/34 hebras) [ 2 ]. Análisis de importantes con oocitos crioconservados con técnicas de congelación de tasa lenta 17 humana vitrificado-IVM en comparación con la vitrificación [ 34 ]. enfoques experimentales Así, por etapas 873 J Assist Reprod Genet (2013) 30: 865 - 875 ovocitos MII mostraron Kcnq1ot1 LOM (1/28 hebras), que de nuevo no fue significativamente diferente 20 IVM-sólo ovocitos MII (2/37 hebras) [ 2 ]. En general, estos estudios en su conjunto sugieren que la congelación no imparte un riesgo mayor que la IVM sola. Sin embargo, poca información se da con respecto al posible impacto de las medidas específicas del proceso de vitrificación en el estado epigenético de los ovocitos. Además, la aplicación práctica de este enfoque para la selección de ovocitos es probablemente limitado. Los estudios futuros utilizando mediciones de punto final Epigentics similares, que se centran en la optimización de los protocolos de criopreservación de ovocitos pueden resultar perspicaz. 4. Arav A, Pearl M, Zeron Y. ¿El perfil de lípidos de membrana a explicar transición de fase sensibilidad y lípidos de membrana de enfriamiento de los espermatozoides y oocitos? Cryo-Lett. 2000; 21: 179 - 86. 5. Arav A, Zeron Y, Leslie SB, et al. temperatura de transición de fase y la sensibilidad de enfriamiento de oocitos bovinos. Cryobiology. 1996; 33: 589 - 99. 6. Baltz JM, Tartia AP. regulación del volumen celular en ovocitos y embriones tempranos: la conexión de la fisiología de los medios de cultivo exitoso. Hum Reprod actualización. 2010; 16: 166 - 76. 7. Barceló-Fimbres M, Seidel GE. Efectos de la glucosa o fructosa y reguladores metabólicos en el desarrollo de embriones bovinos y la acumulación de lípidos in vitro. Mol Reprod Dev. 2007; 74: 1406 - 18. 8. Berthelot-Ricou A, Perrin J, Di Giorgio C, et al. Evaluación de 1,2-propanodiol (PrOH) genotoxicidad en ovocitos de ratón mediante un ensayo de cometa. Steril. 2011; 96: 1002 - 7. 9. Boldt J. actual da como resultado con la congelación lenta y vitrificación del ovocito humano. Reprod Biomed línea. 2011; 23: 314 - 22. Conclusión Es evidente que la crioconservación de ovocitos es una herramienta valiosa en el arsenal de ART y mejorar la eficiencia lleva recompensa sustancial. Aunque puede mentir potencial de mejora por la crioconservación de ovocitos en etapas meióticas anteriores, el enfoque que más se utiliza actualmente incluye ovocitos MII. Por lo tanto, lo más probable es mejor centrarse en los medios para mejorar la metodología para optimizar los resultados utilizando esta etapa meiótica. Esto puede incluir el uso de nuevos CPAs y macromoléculas, y ciertamente debe implicar el uso de medios basales formulados para las necesidades específicas de los ovocitos, tal vez incluso la modificación de su composición o membrana estructura para aumentar criotolerancia. Además, 10. Borini A, Bianchi V, Bonu MA, et al. evolución clínica basada en la evidencia de un enfriamiento lento de ovocitos. Reprod Biomed línea. 2007; 15: 175 - 81. 11. Borini A, Coticchio G. La eficacia y seguridad de la crioconservación de ovocitos humanos por enfriamiento lento. Semin ReprodMed. 2009; 27: 443 - 9. 12. Borini A, Gambardella A, Bonu MA, et al. Comparación de la FIV e ICSI cuando sólo unos pocos ovocitos están disponibles para la inseminación. Reprod Biomed línea. 2009; 19: 270 - 5. 13. Brinster RL. actividad de lactato deshidrogenasa en el embrión de ratón preimplanted. Biochim Biophys Acta. 1965; 110: 439 - 41. 14. Brown KI, Graham EF, Crabo BG. Efecto de algunos tampones de iones de hidrógeno en el almacenamiento y la congelación de los espermatozoides pavo. Poultry Sci. 1972; 51: 840 - 9. mediante el uso de tecnología emergente, el enfoque actual de mover manualmente los ovocitos a través de pasos discretos de CPAs y cargar sobre / en dispositivos de almacenamiento engorrosos puede ser evitado. Más bien, en el futuro previsible, seleccione ovocitos de la etapa meiótica correcta o con la composición celular / membrana adecuada para sobrevivir mejor las tensiones de 15. Cao Y, Xing Q, Zhang ZG, et al. Crioconservación de inmaduro y en-vitro madurado ovocitos humanos por vitrificación. Reprod Biomed línea. 2009; 19: 369 - 73. 16. Checura CM, Seidel GE. Efecto de macromoléculas en soluciones para la vitrificación de la crioconservación pueden ser elegidos para la crioconservación. Estos oocitos se pueden cargar oocitos bovinos maduros. Teriogenología. 2007; 67: 919 - en novedosas cámaras diseñadas para optimizar la exposición CPA y también sirven como 30. dispositivos de carga para simplificar los procedimientos y reducir la variabilidad. Ciertamente, la criopreservación de ovocitos tiene un lugar en rápida expansión en el arte y debe hacerse todo lo posible para facilitar su continua mejora. Estos oocitos se pueden cargar en novedosas cámaras 17. Chian RC, P Quinn (2010) Fertilidad criopreservación. 18. Chung HM, Hong SW, Lim JM, et al. En la formación de blastocisto vitro de ovocitos humanos obtenidos a partir de los ciclos no estimuladas y estimuladas después de la vitrificación en varias etapas de maduración. Steril. 2000; 73: 545 - 51. diseñadas para optimizar la exposición CPA y también sirven como dispositivos de carga para simplificar los procedimientos y reducir la variabilidad. Ciertamente, la criopreservación de ovocitos tiene un lugar en rápida expansión en el arte y debe hacerse todo lo posible para facilitar su continua mejora. Estos oocitos se pueden cargar en novedosas cámaras diseñadas para optimizar 19. Cobo A, Diaz C. La aplicación clínica de la vitrificación de oocitos: una revisión sistemática y meta-análisis de ensayos controlados aleatorios. Steril. 2011; 96: 277 - 85. 20. Coticchio G, Borini A, Distratis V, et al. El análisis cualitativo y morfométrico de la ultraestructura de ovocitos humanos la exposición CPA y también sirven como dispositivos de carga para simplificar los procedimientos y reducir la variabilidad. Ciertamente, la criopreservación de ovocitos tiene un lugar en rápida expansión en el arte y debe hacerse todo lo posible para facilitar su continua mejora. crioconservados por dos protocolos de enfriamiento lento alternativos. J Assist Reprod general 2010; 27: 131 - 40. 21. Crabo BG, Brown KI, GrahamEF. Efecto de algunos tampones en el almacenamiento y congelación de espermatozoides de cerdo. J Anim Sci. 1972; 35: 377 - 82. 22. Dib LA, de Araújo MCPM, Giorgenon RC, et al. ovocitos inyectados en telofase aparentemente madurado tengo peores resultados de la reproducción asistida. referencias Rev Bras Ginecol Obstetricia: Federação Rev Bras Sociedades Ginecol Obstetricia. 2012; 34: 203 - 8. 23. Dumoulin JC, Bergers-Janssen JM, Pieters MH, et al. Los efectos protectores 1. Abe H, Yamashita S, Satoh T, Hoshi H. La acumulación de gotitas de lípidos citoplásmicos en embriones de bovino y criotolerancia de embriones desarrollados en diferentes sistemas de cultivo utilizando medios de comunicación o que contiene suero libre de suero. Mol Reprod Dev. 2002; 61: 57 - 66. 2. Al-Khtib M, Perret A, Khoueiry R, et al. La vitrificación en la fase de vesícula de polímeros en la criopreservación de embriones pellucidae y zonae humano y de ratón. Steril. 1994; 62: 793 8. 24. El-Danasouri I, Selman H, Strehler E. Comparación de MOPS y HEPES tampones durante la vitrificación de embriones humanos. Hum Reprod. 2004; 14: i136. germinal no afecta al perfil de metilación de los centros de impronta H19 y Kcnq1ot1 en ovocitos humanos posteriormente madurados in vitro. Steril. 2011; 95: 1955 - 60. 3. Anchordoguy TJ, Rudolph AS, carpintero JF, Crowe JH. Modos de interacción de crioprotectores con fosfolípidos de la membrana durante la congelación. Cryobiology. 1987; 24: 324 - 31. 25. Eroglu A, Bailey SE, Toner M, Toth TL. crioconservación con éxito de los ovocitos de ratón mediante el uso de bajas concentraciones de trehalosa y dimetilsulfóxido. Biol Reprod. 2009; 80: 70 - 8. 26. Fahy GM. La vitrificación: un nuevo enfoque para la criopreservación de órganos. Prog Clin Biol Res. 1986; 224: 305 - 35. J Assist Reprod Genet (2013) 30: 865 - 875 874 27. Fahy GM, Lilley TH, Linsdell H, et al. toxicidad crioprotector y la reducción de la toxicidad del crioprotector: en busca de mecanismos moleculares. Cryobiology. 1990; 27: 247 - 68. 28. Fasano G, Demeestere I, Englert Y. In-vitro la maduración de ovocitos humanos: antes o después de la vitrificación? J Asistente general Repod 2012; 29: 507 - 47. RS Jeyendran, Graham EF. Una evaluación de compuestos crioprotectores en espermatozoides de bovinos. Cryobiology. 1980; 17: 458 - 64. 48. Jones A, Van Blerkom J, Davis P, Toledo AA. La criopreservación de ovocitos en metafase II humanos efectos potenciales de membrana mitocondrial: implicaciones para la competencia de desarrollo. Hum Reprod. 2004; 19: 1861 - 6. 12. 29. Fitzharris G, Baltz JM. células de la granulosa regulan intracelular pH del ovocito creciente murino a través de uniones de hendidura: el desarrollo de la homeostasis independiente durante el crecimiento de los ovocitos. Development (Cambridge, Inglaterra). 2006; 133 (4): 591 - 9. 30. fitzharris G, Siyanov V, Baltz JM. células de la granulosa regulan ovocito intracelular pH contra acidosis en los folículos preantrales por múltiples mecanismos. Development 49. Karran G, la formación Legge M. no enzimática de formaldehído en mezclas de congelación de ovocitos de ratón. Hum Reprod. 1996; 11: 2681 - 6. 50. Keefe D, Liu L, Wang W, Silva C. Imaging husos meióticos por microscopía de luz de polarización: principios y aplicaciones a FIV. Reprod Biomed línea. 2003; 7: 24 - 9. 51. Kuwayama M, Fujikawa S, Nagai T. Ultraestructura de blastocistos bovinos IVM-FIV (Cambridge, Inglaterra). 2007; 134: 4283 - vitrificados después del equilibrio en 1,2propanediol glicerol utilizando procedimientos 95. de 2 pasos y 16 pasos. Cryobiology. 1994; 31: 415 - 22. 31. Fu XW, Shi WQ, Zhang QJ, et al. Los efectos positivos de Taxol pretratamiento sobre la morfología, distribución y ultraestructura de las mitocondrias y los lípidos gotitas en la vitrificación de in vitro maduraron ovocitos porcinos. Anim Reprod Sci. 2009; 115: 158 - 68. 52. Carril M, Gardner DK. La vitrificación de oocitos de ratón utilizando un bucle de nylon. Mol Reprod Dev. 2001; 58: 342 - 7. 53. La calle M, Lyons EA, Bavister BD. La crioconservación reduce la capacidad de hámster 32. Fuchinoue K, Fukunaga N, Chiba S, et al. La congelación de ovocitos inmaduros humanos embriones de 2 células para regular el pH intracelular. Hum Reprod. 2000; 15: 389 - 94. utilizando cryoloops con Taxol en la solución de vitrificación. J Reprod Asistente general 2004; 21: 307 - 9. 33. Garcia MA, Graham EF. Desarrollo de un sistema tampón para la diálisis de espermatozoides de bovinos antes de la congelación. I. Efecto de ion híbrido de buffers. Teriogenología. 1989; 31: 1021 - 8. 34. Gardner DK, Sheehan CB, Rienzi L, et al. Análisis de la fisiología de los ovocitos para mejorar los procedimientos de criopreservación. Teriogenología. 2007; 67: 64 - 72. 54. Carril M, Maybach JM, Hooper K, et al. Cryo-supervivencia y el desarrollo de los blastocistos bovinos se han mejorado por la cultura con albúmina recombinante y hialuronano. Mol Reprod Dev. 2003; 64: 70 - 8. 55. Larman MG, Katz-Jaffe MG, Sheehan CB, Gardner DK. 1,2propanediol y el tipo de procedimiento de criopreservación afectan negativamente a la fisiología de los ovocitos de ratón. Hum Reprod. 2007; 22: 250 - 9. 56. Larman MG, Minasi MG, Rienzi L, Gardner DK. Mantenimiento del huso meiótico 35. Ghetler Y, Skutelsky E, Ben Nun I, et al. la crioconservación de ovocitos humanos y el destino de los gránulos corticales. Steril. 2006; 86: 210 - 6. 36. Gomes C, Merlini M, Konheim J, et al. Ovocitos diferencias meiótica-stagespecific en la despolimerización del huso en respuesta a cambios de temperatura durante la vitrificación en ovocitos humanos y de ratón. Reprod Biomed línea. 2007; 15: 692 - 700. 57. Larman MG, Sheehan CB, Gardner DK. vitrificación libre de calcio reduce la zona pelúcida endurecimiento-crioprotector inducida y aumenta las tasas de fertilización en ovocitos de ratón. Reproducción. 2006; 131: 53 - 61. monitorizados con microscopía de campo polarizado y inmunocitoquímica. Steril. 2012; 97: 714 - 9. 37. Gomes CM, Silva CA, Acevedo N, et al. Influencia de la vitrificación en metafase II dinámica ovocito husillo de ratón y la alineación de la cromatina. Steril. 2008; 90: 1396 - 404. 38. Gook DA, Osborn SM, WI Johnston. Crioconservación de ratón y ovocitos humanos utilizando 1,2-propanodiol y la configuración del huso meiótico. Hum Reprod. 1993; 8: 1101 - 9. 39. Graham EF, Crabo BG, Brown KI. Efecto de algunos tampones ión zwitterión en la congelación y almacenamiento de los espermatozoides. I. Bull J Dairy Sci. 1972; 55: 372 - 8. 58. Leibo SP, piscina TB. Las principales variables de la criopreservación: soluciones, temperaturas y cambios de la tasa. Steril. 2011; 96: 269 - 76. 59. Matson PL, Graefling J, SM basura, et al. La crioconservación de ovocitos y embriones: el uso de un modelo de ratón para investigar los efectos sobre la dureza zona y formular estrategias de tratamiento en un programa de fertilización in vitro. Hum Reprod. 1997; 12: 1550 - 3. 60. Hombres H, Monson RL, Parrish JJ, Rutledge JJ. La degeneración de oocitos crioconservados bovina a través de la apoptosis durante el cultivo posterior. Cryobiology. 2003; 47: 73 - 81. 40. Gualtieri R, Iaccarino M, Mollo V, et al. El enfriamiento lento de ovocitos humanos: lesiones ultraestructurales y el estado apoptótico. Steril. 2009; 91: 1023 - 34. 61. MengQ, WUX, Manojo TD, et al. La enucleación de oocitos demecolcina tratadas con la especie bovina en medio libre de citocalasina: investigación mecanismo y mejora práctica. Reprogram Cell. 2011; 13: 411 - 8. 41. Heo YS, Lee HJ, Hassell BA, et al. carga controlada de crioprotectores (CPAs) a 62. Morató R, Izquierdo D, Albarracín JL, et al. Efectos de pre-tratamiento en ovocitos bovinos in ovocito con perfiles de CPA lineales y complejos en una plataforma de microfluidos. vitro-madurado con el citoesqueleto de la estabilización de taxol agente antes de la Chip de laboratorio. 2011; 11: 3530 - vitrificación. Mol Reprod Dev. 2008; 75: 191 - 7. 42. Horvath G, Seidel Jr. GE. El uso de fetuina antes y durante la vitrificación de ovocitos bovinos. Reprod Domest Anim. 2008; 43: 333 - 8. 201. 63. Morató R, Mogas T, Maddox-Hyttel P. Ultraestructura de ovocitos bovinos expuestos a Taxol antes de OPS vitrificación. Mol Reprod Dev. 2008; 75: 1318 - 26. 43. Horvath G, Seidel GE. La vitrificación de oocitos bovinos después del tratamiento con el colesterol-cargado metil-beta-ciclodextrina. Teriogenología. 2006; 66: 1026 - 33. 64. Nottola SA, Coticchio G, De Santis L, et al. Ultraestructura de ovocitos maduros humanos después de la crioconservación enfriamiento lento con etilenglicol. Reprod 44. Hu W, Marchesi D, J Qiao, Feng HL. Efecto de la congelación lenta frente a la vitrificación en el ovocito: un modelo animal. Steril. 2012; 98: 752 - 760.e3. 45. Hyun CS, Cha JH, Hijo WY, et al. Optimal temporización ICSI después de la primera extrusión cuerpo polar en in vitro madurado ovocitos humanos. Hum Reprod. 2007; 22: 1991 - 5. Biomed línea. 2008; 17: 368 - 77. 65. Nottola SA, Coticchio G, Sciajno R, et al. marcadores ultraestructurales de la calidad en ovocitos maduros humanos vitrificados utilizando Cryoleaf y cryoloop. Reprod Biomed línea. 2009; 19 Suppl 03:17 - 27. 66. Nottola SA, Macchiarelli G, Coticchio G, et al. Ultraestructura de ovocitos maduros humanos después de la crioconservación enfriamiento lento utilizando diferentes concentraciones de 46. Jasensky J, Boughton A, Khmaladze A, et al. Título / Autor Año Células vivas análisis de lípidos intra-ovocito y cuantificación de las imágenes hiperespectrales sacarosa. Hum Reprod. 2007; 22: 1123 - 33. 67. Parque KE, Kwon IK, Han MS, Niwa K. Efectos de la eliminación parcial de lípido citoplásmico por múltiplex coherente anti-Stockes dispersión Raman microscopía (CARS-M). en la supervivencia de vesícula germinal oocitos de cerdo etapa vitrificados. J Repro Dev. Steril. 2012; 98: S79. 2005; 51: 151 - 60. 875 J Assist Reprod Genet (2013) 30: 865 - 875 68. Parmegiani L, Bertocci F, Garello C, et al. Eficiencia de ovocitos humanos congelación sobrecalentamiento: un estudio mediante microscopía de luz polarizada. Cigoto. 2004; 12: 241 - 9. lenta: resultados de cinco centros de reproducción asistida. Repro Biomed línea. 2009; 18: 352 - 9. 69. Porcu E, Fabbri R, Seracchioli R, et al. Nacimiento de una mujer sana después de la inyección intracitoplasmática de espermatozoides de ovocitos humanos criopreservados. Steril. 1997; 68: 87. Suo L, Zhou GB, Meng QG, et al. OPS vitrificación de ovocitos inmaduros ratón antes o después de la meiosis: el efecto sobre las células del cumulus mantenimiento y el desarrollo posterior. Cigoto. 2009; 17: 71 - 7. 724 - 6. 70. Regula CS, Pfeiffer JR, Berlín RD. ensamblaje de los microtúbulos y desmontaje a pH alcalino. J Cell Biol. 1981; 89: 45 - 53. 71. Rizos D, Gutiérrez-Adán A, Pérez-Garnelo S, et al. el cultivo de embriones bovinos en presencia o ausencia de suero: implicaciones para el desarrollo de blastocisto, criotolerancia, y la expresión del ARN mensajero. Biol Reprod. 2003; 68: 236 - 43. 72. Röcken C, Ebert MPA, Roessner A. Proteómica en la patología, la investigación y la práctica. Pathol Res Pract. 2004; 200: 69 - 82. 88. Swain JE, Smith GD. Crioprotectores. En: Cihian RC, P Quinn, editores. criopreservación de la fertilidad. Cambrige: Cambridge University Press; 2010. p. 24 - 39. 89. Toth TL, Baka SG, Veeck LL, et al. Fertilización y en el desarrollo in vitro de ovocitos criopreservados profase I humanos. Steril. 1994; 61: 891 - 4. 90. Toth TL, Lanzendorf SE, Sandow BA, et al. La criopreservación de ovocitos Profase I humano recogido de los folículos estimulados. Steril. 1994; 61: 1077 - 82. 73. Ruffing NA, Steponkus PL, Pitt RE, Parques JE. behaavior osmométrico, conductividad hidráulica, y la incidencia de la formación de hielo intracelular en ovocitos bovinos en diferentes etapas de desarrollo. Cryobiology. 1993; 30: 562 - 80. 91. Trapphoff T, El Hajj N, Zechner U, et al. la integridad del ADN, el patrón de crecimiento, la formación del huso, constitución cromosómica y la impresión patrones de ovocitos de ratón a partir de folículos pre-antrales vitrificados. Hum Reprod. 2010; 25: 3025 - 42. 74. Saragusty J, Arav A. progreso actual en ovocitos y embriones criopreservación por congelación lenta y vitrificación. Reproducción. 2011; 141: 1 - 19. 92. Tucker M, Wright G, Morton P, et al. La experiencia preliminar con la crioconservación de ovocitos humanos utilizando 1,2-propanodiol y sacarosa. Hum Reprod. 1996; 11: 75. Sauvat F, Capito C, Sarnacki S, et al. ovario criopreservados inmadura restaura la pubertad y la fertilidad en ratones sin alteración de las marcas epigenéticas. Más uno. 2008; 3: e1972. 76. Seidel GE. La modificación de ovocitos y embriones para mejorar su criopreservación. Teriogenología. 2006; 65: 228 - 35. 77. Shau H, Chandler GS, Whitelegge JP, et al. perfiles proteómicos de biomarcadores de cáncer. Breve Func Genómica Proteómica. 2003; 2: 147 - 58. 78. Shehab-El-Deen MA, Leroy JLMR, Maes D, Van Soom A. criotolerancia de blastocistos bovinos se ve afectada por la maduración de ovocitos en medios que contienen palmítico o ácido esteárico. Reprod Domest Anim. 2009; 44: 140 - 2. 1513 - 5. 93. Tucker MJ, Wright G, Morton PC, Massey JB. Nacimiento después de la crioconservación de oocitos inmaduros con la posterior maduración in vitro. Steril. 1998; 70: 578 - 9. 94. Vincent C, Cheek TR, Johnson MH. progresión del ciclo celular de ovocitos de ratón por partenogénesis activadas para interfase depende del nivel de calcio interno. Sci J Cell. 1992; 103: 389 96. 95. Wang WH, Meng L, Hackett RJ, et al. La observación de husillo y su relación con la fertilización después de la inyección intracitoplasmática de espermatozoides en vivir ovocitos humanos. Steril. 2001; 75: 348 - 53. 79. Shi WQ, Zhu SE, Zhang D, et al. Mejora el desarrollo de Taxol pretratamiento después de la vitrificación de ovocitos madurados in vitro porcinos. Reproducción. 2006; 131: 795 - 804. 80. Sieracki NA, Hwang HJ, Lee MK, et al. (2008) A pH independiente de la temperatura 96. Will MA, Clark NA, Swain JE. tampones de pH biológicos en la FIV: ayuda o un obstáculo para el éxito. J Assist Reprod general 2011; 28: 711 - 24. 97. Yamaji Y, Seki S, Matsukawa K, et al. la capacidad de desarrollo de los ovocitos de ratón vitrificados que expresan canales de agua. J Reprod Dev. 2011; 57: 403 - 8. (TIP) tampón para aplicaciones biomédicas biofísicas a bajas temperaturas. Chem Commun 823 - 825. 81. Smith GD, Motta EE, Serafini P. Base teórica y experimental de la vitrificación de ovocitos. Reprod Biomed línea. 2011; 23: 298 - 306. 82. Smith GD, Serafini PC, Fioravanti J, et al. comparación prospectivo aleatorizado de la crioconservación de ovocitos humanos con congelación-tasa lenta o vitrificación. Steril. 2010; 94: 2088 - 95. 83. Squirrell JM, La calle M, Bavister BD. La alteración de pH intracelular interrumpe el desarrollo y la organización celular en embriones de preimplantación de hámster. Biol Reprod. 2001; 64: 1845 - 54. 84. Stachecki JJ, Cohen J, efectos Willadsen S. perjudiciales de sodio durante la crioconservación de ovocitos de ratón. Biol Reprod. 1998; 59: 395 - 400. 98. Zander-Fox D, Cashman KS, el carril M. La presencia de glicina 1 mM en soluciones de vitrificación protege ovocito homeostasis mitocondrial y mejora el desarrollo de blastocisto. J Assist Reprod Gen. 2013; 30: 107 - dieciséis. 99. Zander-Fox DL, Mitchell M, Thompson JG, el carril M. Las alteraciones en el ratón embrión intracelular pH por DMO durante la implantación cultura impair y el crecimiento fetal. Reprod Biomed línea. 2010; 21: 219 - 29. 100. Zeron Y, Pearl M, Borochov A, Arav A. cinéticos y temporales factores influyen en el daño por frío de vesícula germinal y ovocitos bovinos maduros. Cryobiology. 1999; 38: 35 - 42. 101. Zeron Y, Tomczak M, Crowe J, Arav A. El efecto de los liposomas en las transiciones de fase de membrana termotrópicos de espermatozoides de bovinos y ovocitos: implicaciones para la 85. Stachecki JJ, Cohen J, Willadsen SM. La crioconservación de oocitos de ratón reducción de la sensibilidad de enfriamiento. Cryobiology. 2002; 45: 143 - 52. fertilizados: el efecto de la sustitución de sodio con colina en el medio de congelación. Cryobiology. 1998; 37: 346 - 54. 86. Sun XF, Zhang WH, Chen XJ, et al. la dinámica del cabezal en ovocitos de ratón viviendo durante la maduración meiótica, el envejecimiento, la refrigeración y 102. Zhou C, Baltz JM. JAK2 media la respuesta aguda a la disminución del volumen celular en embriones de preimplantación ratón mediante la activación de NHE1. J Cell Physiol. 2013; 228: 428 - 38.