Tesis - Universidad de Colima
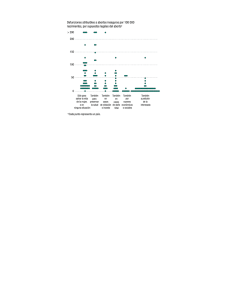
Anuncio

UNIVERSIDAD DE COLIMA Maestría en Ciencias Médicas IMPACTO DEL PERFIL BIOFÍSICO FETAL SOBRE LA MORBILIDAD Y MORTALIDAD PERINATAL EN EMBARAZOS DE ALTO RIESGO Tesis que para obtener el grado de Maestro en Ciencias Médicas presenta: Silvia Lorena Moctezuma Hernández Asesores: Dr. Carlos Enrique Tene Pérez Dr. Carlos A. Villanueva Díaz Colima, Col., Marzo del 2000 CARTA DE TERMINACIÓN FIRMADA POR LOS ASESORES Por medio de la presente hacemos constar que el presente trabajo cumple con los requisitos establecidos para ser presentado en examen a fin de que su autora pueda obtener el grado de Maestría en Ciencias Médicas. _________________________________ Dr. Carlos Enrique Tene Pérez Investigador Asociado A Endocrinólogo IMSS Colima ______________________________________ Dr. Carlos A. Villanueva Díaz Biólogo de la Reproducción Subdirector de Investigación Clínica Instituto Nacional de Perinatología COASESORES _________________________________ Dra. Rebeca Millán Guerrero Maestra en Ciencias Médicas Jefe Unidad de Investigación Médica en Epidemiología Clínica IMSS Colima _________________________________ Dr. Ricardo García Cavazos Jefe del Departamento de Genética Perinatal Instituto Nacional de Perinatología Doy gracias a: A mis Tutores A todos esos niños que nacieron en el trascurso de esta investigación y a sus madres que confiaron la vida de sus hijos apoyando a la ciencia A mis padres A mis hermanos: Ana Lilia y José en especial al amor de mi vida ÍNDICE TABLA DE CUADROS Y FIGURAS......................................................................... 1 SUMMARY………………………………………………………………………...… 2 RESUMEN……………………………………………………………………………. 3 ANTECEDENTES Embarazo de alto riesgo, morbilidad y mortalidad perinatal............................ 4 Importancia de la mortalidad perinatal como problema de salud pública........ 6 Técnicas de vigilancia fetal…………………………………………………... 8 Perfil biofísico………………………………………...................................... 9 PLANTEAMIENTO DEL PROBLEMA…………………………………………... 21 OBJETIVOS Objetivo general……………………………………………………………… 21 Objetivos específicos………………………………………………………… 21 MATERIAL Y MÉTODOS Tipo de estudio………………………………………………......................... 22 Procedimiento………………………………………………………………... 22 Criterios de selección Inclusión….……………………………………………………..….. 26 No inclusión………………………………………………………… 26 Eliminación………………………………………………………..... 26 Análisis estadístico…………………………………………………………... 27 RESULTADOS a) Perfil biofísico fetal……………………………………………………….. 28 b) Mortalidad perinatal………………………………………………………. 31 c) Morbilidad perinatal………………………………………………………. 34 DISCUSIÓN……………………………………………………….............................. 37 CONCLUSIONES……………………………………………………………………. 41 ANEXOS Anexo 1 Forma MF-7……………………………………………………… 42 Anexo 2 Carta de consentimiento informado……………………………… 44 Anexo 3 Hoja de recolección de datos…………………………………....... 45 REFERENCIAS BIBLIOGRÁFICAS……………………………………………… 47 TABLA DE CUADROS Y FIGURAS Cuadro 1. Tasas de mortalidad en la Delegación Regional Colima del Instituto Mexicano del Seguro Social………………………………. 7 Cuadro 2. Técnica e interpretación de la valoración del perfil biofísico fetal… 14 Figura 1. Prueba sin estrés (PSS) reactiva…………………………………… 12 Figura 2. Prueba sin estrés (PSS) no reactiva………………………………... 12 Figura 3. Perfil biofísico fetal………………………………………………... 15 Fotografía 1. Cardiotocógrafo……………………………………………………. 10 Fotografía 2. Realizando una prueba sin estrés (PSS)……………………………. 11 Fotografía 3. Valoración fetal a través de ultrasonografía……………………….. 13 Fotografía 4. Medición de líquido amniótico…………………………………….. 18 Fotografía 5. Morbilidad perinatal……………………………………………….. 19 Fotografía 6. Recién nacido en cuneros………………………………………….. 35 Tabla I. Características clínico epidemiológicas en los embarazos de alto riesgo en el grupo del perfil biofísico fetal y el grupo de control histórico…………………………………………………………….. Tabla II. 29 Indicaciones del perfil biofísico fetal en casos de embarazo de alto riesgo……………………………………………………………….. 30 Tabla III. Causas de mortalidad perinatal en el grupo de control externo (histórico)…………………………………………………………... 31 Tabla IV. Morbilidad y mortalidad perinatal en embarazos de alto riesgo…... 33 Tabla V. Resultados del último perfil biofísico fetal en 63 pacientes durante su embarazo de alto riesgo de acuerdo a su morbilidad perinatal….. Tabla VI. 34 Calificación de la valoración Apgar y de la obtenida en la forma MF-7 en embarazos de alto riesgo………………………………….. 36 SUMMARY OBJECTIVE: To determine if difference exists in both perinatal morbidity and mortality when is performed Biophysical Profile Scoring (BPS) in high-risk pregnancies. STUDY DESIGN: This trial with historic controls included patients and expedients of cases with high-risk pregnancies. We performed weekly BPS from 34 week to the birth, comparing them with historical controls without BPS. Statistical analysis. Averages, proportions, X², Fisher and t student. RESULTS: We analyzed 127 patients, (63 group study / 64 historical controls). There weren’t significant differences in: maternal age, gestational, and newborn’s age and weight. In study group there wasn’t deaths perinatals, but in historical control there were six cases (9.3%) (p = 0.028). Perinatal morbidity was similar with 6 (9.5%) and 8 (12.5%) cases respectively (p = 0.3). CONCLUSIONS: Perinatal mortality in pregnancies of high risk was smaller when was performed BPS. Key words Mortality and morbidity perinatal, biophysical profile scoring, pregnancy of high risk. 2 RESUMEN OBJETIVO: Determinar si existe diferencia en la mortalidad y morbilidad perinatal cuando se realiza perfil biofísico fetal (PBF) en embarazos de alto riesgo. DISEÑO: Ensayo clínico con controles históricos que incluyó pacientes y expedientes de casos con embarazos de alto riesgo. Realizamos PBF semanalmente de la semana 34 al nacimiento, comparándolos con los controles históricos sin PBF. Análisis estadístico. Promedios, proporciones, X², Fisher y t student. RESULTADOS: Analizamos 127 pacientes, (63 del grupo de estudio / 64 controles históricos). No hubo diferencias significativas en: edad materna, edad gestacional, edad del recién nacido y peso. En el grupo de estudio no hubo muertes perinatales, mientras que en el control histórico hubo seis casos (9.3%) (p = 0.028). La morbilidad perinatal fue similar 6 (9.5%) y 8 (12.5%) respectivamente (p = 0.3). CONCLUSIONES: La mortalidad perinatal en embarazos de alto riesgo fue menor en los casos en que se realizó perfil biofísico fetal. Palabras clave Mortalidad y morbilidad perinatal, perfil biofísico fetal, embarazo de alto riesgo. 3 Antecedentes ANTECEDENTES Embarazo de alto riesgo, morbilidad y mortalidad perinatal. La práctica médica gineco-obstétrica debe de tener en cuenta la presencia de dos pacientes: La madre y el feto1 . Este cuidado debe de ser todavía mayor cuando se trata de vigilar embarazos de alto riesgo. El embarazo de alto riesgo, es la gestación con probabilidad elevada de morbilidad y mortalidad perinatal y /o materna. El embarazo de alto riesgo fetal puede ocasionar: 1) Muerte fetal o muerte neonatal. 2) Morbilidad neonatal grave o leve sin secuela posterior. 3) Morbilidad neonatal grave o leve que dejará como secuela: a) Impedimento físico. b) Impedimento social. c) Impedimento intelectual. El embarazo de alto riesgo materno puede ocasionar: 1) Muerte materna inmediata o tardía. 2) Morbilidad materna grave o leve sin secuela posterior. 3) Morbilidad materna grave o leve que dejará como secuela: a) Impedimento físico. b) Impedimento social. c) Impedimento intelectual. El embarazo de alto riesgo generalmente desencadena disfunción feto-placentaria cuya expresión clínica es el sufrimiento fetal crónico (SFC). 4 Antecedentes No hay consenso para definir con exactitud a quién se le considera con embarazo de alto riesgo ya que cada hospital y/o departamento tiene su propia forma de evaluar este estado clínico. Para la Delegación Colima del Instituto Mexicano del Seguro Social (IMSS) se considera que tiene embarazo de alto riesgo la paciente con un puntaje mayor de cuatro, de una serie de parámetros que se encuentran contemplados en la forma MF 7 la cual evalúa la atención médica prenatal y riesgo reproductivo (anexo 1). En general todas las evaluaciones que se han propuesto en el transcurso del tiempo1-5 y las que se utilizan actualmente, han incorporado entre los factores de alto riesgo los antecedentes obstétricos y las complicaciones médicas maternas, otorgándoles distinto valor numérico de acuerdo a su importancia y repercusión sobre la gestación. Desafortunadamente, los factores de riesgo evaluados por los diferentes autores no son los mismos y su calificación varía de un sistema a otro. La ventaja de usar este sistema de puntuación de alto riesgo es permitir al médico general identificar a la paciente que requiere ser valorada por un especialista en medicina maternofetal. La desventaja es el limitado valor que tiene para establecer un pronóstico, debido a la baja sensibilidad de los indicadores de alto riesgo y a que la evolución del embarazo se ve influenciada por la intervención médica al identificar la situación de alto riesgo33 . La mortalidad perinatal es un indicador que permite evaluar la calidad del servicio que se presta en un centro hospitalario y también permite valorar el control prenatal de las pacientes6 . Bobadilla y colaboradores, señalan que la mortalidad perinatal es un indicador de la eficiencia reproductiva de la mujer en edad fértil y de la cobertura y calidad de la atención materno infantil7 . Las causas más importantes de muerte fetal incluyen retardo en el crecimiento, infección, desprendimiento de placenta e infartos placentarios. La prematurez es la causa principal de mortalidad neonatal. Las causas de muerte son el síndrome de dificultad respiratoria, las hemorragias en el sistema nervioso central y las infecciones8 . Se define como muerte perinatal a la defunción del feto de más de 20 semanas de embarazo hasta los 28 días de nacido. La mortalidad perinatal se divide a su vez en: 5 Antecedentes Mortalidad perinatal tipo I. Comprende el período desde las 28 semanas de embarazo hasta los 7 días de nacimiento. Mortalidad perinatal tipo II: Comprende el período desde las 20 semanas de embarazo hasta los 28 días del nacimiento9,19,47. Importancia de la mortalidad perinatal como problema de salud pública. Manning en 198110 , en un estudio clínico de 1184 pacientes consecutivas con embarazo de alto riesgo, documentó una mortalidad perinatal de 11.7 por 1000. Para 1985 11 , con 12,620 pacientes, documentó una mortalidad perinatal de 7.35 por 1000. En 198712 , la serie se amplió a 19,212 pacientes y la tasa de mortalidad perinatal permaneció en menos de 7 casos por 1000. Baskett13 evidenció una mortalidad perinatal de 7.6 por 1000 en 5,034 embarazos. Todas estas tasas de mortalidad perinatal ocurrieron en embarazos de alto riesgo en quienes se les realizó perfil biofísico fetal. Estudios hechos en Cuba, Estados Unidos e Inglaterra indican que las regiones con altas tasas de mortalidad perinatal tienen un nivel socioeconómico más bajo que el resto del país y los servicios médicos perinatales son menos accesibles y de menor calidad en estas regiones51 . En México se desconocen los datos reales, ya que las estadísticas no son confiables a consecuencia del subregistro de defunciones fetales tardías de más de 28 semanas de gestación y de neonatales tempranas cuya suma constituye el numerador de la tasa de mortalidad perinatal. Este subregistro se relaciona con el desarrollo socioeconómico de los estados, así los estados pobres donde se esperarían las tasas más altas, presentan las tasas más bajas y niveles de subregistro alto7 . Las tasas más altas de mortalidad perinatal se registran dentro del IMSS en la delegación 2 del Distrito Federal Noreste, Quintana Roo, Colima y Delegación 4 del Distrito Federal Suroeste14 . 6 Antecedentes En 1996 la tasa nacional de mortalidad perinatal 1, considerada esta como la ocurrida desde las 28 semanas de gestación a 7 días después del nacimiento, fue de 14.7 por 1000 en la población derechohabiente usuaria del Instituto Mexicano del Seguro Social (IMSS). En el estado de Colima ésta tasa fue de 15.3 por 1000 para el mismo año. Ambos indicadores constituyen el doble de las tasas reportadas a nivel internacional15 . En el cuadro siguiente observamos las tasas de mortalidad documentadas desde el año 1996 a 1999 en la delegación regional Colima en el IMSS. Cuadro mortalidad en en la laDelegación DelegaciónRegional RegionalColima Colimadel del Cuadro Tasas de de mortalidad mortalidad en la Delegación Regional Colima del Cuadro 1. 1. Tasas Instituto Instituto Mexicano del Seguro Social Instituto Mexicano Mexicano del del Seguro Seguro Social Social Año Año 1996 1996 1997 1997 1997 1998 1998 1998 1999 1999 1999 Total Total de nacimientos Total de de nacimientos nacimientos 5359 5359 5261 5261 5261 4704 4704 4704 4684 4684 4684 Total Total de recién vivos Total de de recién recién nacidos nacidos vivos vivos 5307 5307 5226 5226 5226 4691 4691 4691 4674 4674 4674 Tasa Tasa de mortalidad perinatal Tasa de de mortalidad mortalidad perinatal perinatal III 15.34 15.34 10.70 10.70 10.70 15.65 15.65 15.65 8.73 8.73 8.73 Tasa Tasa de mortalidad hebdomadal Tasa de de mortalidad mortalidad hebdomadal hebdomadal 7.85 7.85 5.22 5.22 5.22 7.89 7.89 7.89 4.06 4.06 4.06 Tasa Tasa de mortalidad fetal tardía Tasa de de mortalidad mortalidad fetal fetal tardía tardía 7.49 7.49 5.73 5.73 5.73 7.83 7.83 7.83 4.68 4.68 4.68 FUENTE: FUENTE: División División de de informática, informática, coordinación coordinación de de salud salud comunitaria comunitaria 15,16. Certificados Certificados de de defunción defunción yy de de muerte muerte fetal, fetal, 15,16. 7 Antecedentes Las defunciones perinatales registradas en el Hospital General de Zona y Medicina Familiar número l (HGZ/MF No. 1) del IMSS en Colima, de enero a junio de 1997 fue de 8 casos. Para 1998 en el mismo periodo (enero-junio) fue de 12 casos, lo que nos refleja un incremento de un 50% en las defunciones perinatales16 Durante el período de tiempo comprendido de diciembre de 1998 a junio de 1999 se presentaron 8 muertes perinatales desde la semana 21 a la 41 de gestación, en un total de 1637 nacimientos registrados en el HGZ/MF No. 1 del IMSS en la ciudad de Colima. Técnicas de vigilancia fetal En los últimos 20 años, los progresos en la atención perinatal han contribuido a la disminución en la mortalidad antes y después del parto; los progresos incluyen mejorías en los aspectos técnicos de la atención intensiva de neonatos, y mejores técnicas de vigilancia fetal17 . Desde el punto de vista histórico, los primeros intentos para identificar marcadores de enfermedad fetal se basaron en el análisis bioquímico de líquidos biológicos de la madre. Se midieron diferentes compuestos como hormonas peptídicas (lactógeno humano), enzimas (fosfatasa alcalina placentaria y la oxitocinasa); esteroides placentario (progesterona, estriol, estrona y estrógeno total) y proteínas específicas (alfafetoproteína). Con el paso del tiempo y la experiencia clínica, estos estudios fueron abandonados, cuando menos como marcadores de asfixia fetal y sustituidos por índices biofísicos fetales más directos y específicos17 . Desde la introducción del monitoreo electrónico de la frecuencia cardiaca fetal, la prueba sin estrés (PSS) y la prueba de estrés por contracción (PTO), se han convertido en los métodos más utilizados para la detección ante parto de asfixia fetal. La desventaja de estos métodos es que la única información que obtienen para valorar la salud del feto es la 8 Antecedentes frecuencia cardiaca fetal. Ambas pruebas son útiles para detectar al feto saludable (no asfixiado) en el momento del estudio pero son de valor limitado para detectar al feto no saludable (asfixiado)18 . La PSS permite analizar los cambios de la frecuencia cardiaca fetal relacionados con los movimientos espontáneos del feto (condiciones basales o sin estímulo). La PTO estudia los cambios de la frecuencia cardiaca fetal con las contracciones uterinas inducidas con oxitocina19 . Actualmente la forma más aceptada de realizar detección de riesgo fetal es mediante el perfil biofísico fetal. Este incluye además de la realización de la PSS, otros parámetros11-22 . Perfil biofísico Para evitar las tasas altas de falsos positivos, varios investigadores incorporaron algunas variables con el fin de mejorar la exactitud diagnóstica de asfixia fetal ante parto. Manning20 fue el primero en comunicar el uso de cinco variables biológicas fetales a las cuales les asignó un puntaje de 0 si era anormal o 2 si era normal. La evaluación de cada una de ellas se define en el cuadro 1. En la primera investigación realizada por Manning20 en la que propone el perfil biofísico fetal no se menciona la edad gestacional al nacimiento. En un articulo subsecuente21 la edad gestacional promedio al nacimiento fue de 3l.3 semanas con un rango de 26 a 43 semanas. Las variables biológicas evaluadas durante el perfil biofísico fetal son las siguientes: Movimientos respiratorios Movimientos corporales Tono fetal Volumen de líquido amniótico Reactividad de la frecuencia cardiaca fetal20 . 9 Antecedentes El procedimiento utilizado para obtener el perfil biofísico fetal es el siguiente: Primero se toma un registro cardiotocográfico. La cardiotocografía ante parto es un método que permite evaluar el estado de salud-enfermedad fetal mediante el registro y observación de las características de la frecuencia cardiaca fetal, en condiciones basales y con estímulo19 . Fotografía 1. Cardiotocógrafo La prueba sin estrés (PSS) permite analizar los cambios de la frecuencia cardiaca fetal relacionados con los movimientos espontáneos del feto (condiciones basales o sin estímulo). La paciente a quien se realiza una prueba sin estrés debe cumplir los siguientes requisitos: • Ingesta reciente de alimentos (máximo 3 horas) • No ingerir medicamentos, especialmente depresores del sistema nervioso central. 10 Antecedentes • Control externo de la frecuencia cardiaca fetal con transductor ultrasónico y registro en papel a velocidad de centímetro / minuto • Posición semisentada, en decúbito lateral. • Control de tensión arterial (TA), pulso, y temperatura al inicio y al final de la prueba Fotografía 2. Realizando una prueba sin estrés (PSS) El registro se efectúa durante 10 minutos en condiciones basales. Se considera prueba sin estrés reactiva (bienestar fetal) cuando se presentan dos o más ascensos de la frecuencia cardiaca fetal asociados a los movimientos fetales, al menos de 15 latidos de amplitud y 15 segundos de duración, en 10 minutos consecutivos de registro. Si el registro no es reactivo se moviliza el feto en forma manual y se observa el trazo de la frecuencia cardiaca fetal l0 minutos después19 . 11 Antecedentes Ascensos de la frecuencia cardiaca fetal Movimientos fetales FIGURA 1. Prueba sin estrés (PSS) reactiva Sin ascensos de la frecuencia cardiaca fetal Movimientos fetales FIGURA 2. Prueba sin estrés (PSS) no reactiva 12 Antecedentes Una vez realizado el registro cardiotocográfico fetal. Se efectúa una evaluación fetal con ultrasonido dinámico de los movimientos respiratorios del feto, movimientos corporales manifiestos, tono fetal y volumen de líquido amniótico. El tiempo estimado para este estudio es de 30 minutos. Cada una de las cinco variables tendrá una calificación de dos puntos de ser normal y cero de ser anormal. Fotografía 3. Valoración fetal a través de ultrasonografía 13 Antecedentes Cuadro Cuadro2.2. Técnica Técnicaeeinterpretación interpretaciónde dela lavaloración valoracióndel delperfil perfilbiofísico biofísico fetal fetal Variablebiofísica biofísica Variable Puntuación Puntuación normal normal (puntuación==2) 2) (puntuación Puntuación Puntuación anormal anormal (puntuación==0) 0) (puntuación Movimientosrespiratorios respiratorios Movimientos del feto (MFR) del feto (MFR) Cuandomenos menosun unepisodio episodiode de Cuando MFRque quedure durecomo comomínimo mínimo MFR 30 segundos en un lapso de30 30 30 segundos en un lapso de minutosde deobservación. observación. minutos Ausenciade deMFR MFRooningún ningún Ausencia episodioque quedure duremás másde de30 30 episodio segundos durante 30 minutos. segundos durante 30 minutos. Movimientoscorporales corporales Movimientos Comomínimo mínimotres tres Como movimientoscorporales corporalesen en movimientos extremidades perfectamente extremidades perfectamente delimitadosen enun unlapso lapsode de30 30 delimitados minutos(los (losepisodios episodiosde de minutos movimientos continuos activos movimientos continuos activos considerancomo comouno unosolo) solo) seseconsideran Tonofetal fetal Tono Frecuenciacardiaca cardiacafetal fetal Frecuencia reactiva (FCF) reactiva (FCF) Volumencualitativo cualitativode de Volumen liquidoamniótico amniótico liquido Comomínimo mínimoun unepisodio episodiode de Como extensión activa con vuelta a extensión activa con vuelta a lala flexiónde delas lasextremidades extremidadesooelel flexión troncofetal. fetal. tronco Se considera como tononormal normal Se considera como tono abriryycerrar cerrarlalamano. mano. abrir Cuandomenos menosdos dosepisodios episodios Cuando de aceleración de FCF superior de aceleración de FCF superior 15latidos latidospor porminuto minutoyyque que aa15 duren como mínimo 15 duren como mínimo 15 segundos, queseseacompañen acompañende de segundos, que movimiento fetal en un lapso movimiento fetal en un lapso de33minutos. minutos. de Comomínimo mínimoun undepósito depósitode de Como liquidoamniótico amnióticoque quemida mida22 liquido cm cuando menos en dos cm cuando menos en dos planosperpendiculares perpendiculares planos 14 Dosepisodios episodiosoomenos menosde de Dos movimientos corporales de movimientos corporales de extremidadesen en30 30minutos. minutos. extremidades Extensiónlenta lentacon conretorno retornoaa Extensión la flexión parcial la flexión parcial oo movimientode deuna una movimiento extremidad en extensión extremidad en extensión completa completa Menosde dedos dosepisodios episodiosde de Menos aceleraciónde delalaFCF FCFoo aceleración aceleración con menos de15 15 aceleración con menos de latidos/ /minuto minutodurante durante30 30 latidos minutos. minutos. Noexisten existendepósitos depósitosde de No líquidoamniótico amnióticooosese líquido advierte un depósitomenor menorde de advierte un depósito cmen endos dosplanos planos 22cm perpendiculares perpendiculares Antecedentes Figura 3. Perfil biofísico fetal Vintzileos hizo modificaciones a la técnica propuesta por Manning en la cual agregó la valoración placentaria a los puntos considerados anteriormente. La desventaja de esta propuesta es que requiere de mayor tiempo para su realización22 . Ambos métodos de evaluación inician con la realización de una prueba sin estrés y después evaluación ecográfica de las variables restantes durante un tiempo de 30 minutos. Estos métodos son una combinación de los marcadores agudos, los cuales son: la reactividad 15 Antecedentes de la frecuencia cardiaca fetal, movimientos respiratorios, movimientos corporales y tono fetal; así como los marcadores crónicos que son: volumen de líquido amniótico y la clasificación placentaria18 . El perfil biofísico fetal propuesto por Manning ha sido criticado por otorgar un valor de cero a dos puntos a cada uno de sus marcadores sin tomar en cuenta que cada uno de estos tiene distinta importancia en la valoración de la situación fetal pues son marcadores de actividades biofísicas desencadenadas y controladas por diferentes centros del sistema nervioso central22 , con sensibilidad diferente a la hipoxia. Cada uno de estos marcadores agudos aparece a diferente edad gestacional18,26. Las actividades biofísicas que aparecen primero durante la vida fetal son las últimas en desaparecer durante la asfixia fetal23-5 . El tono y los movimientos fetales aparecen entre las 7 y las 9 semanas de gestación y requieren de la actividad de la corteza cerebral. Los movimientos respiratorios fetales se inician en la semana 20 a 21 y dependen de los centros de la superficie ventral del cuarto ventrículo18 . La reactividad de la frecuencia cardiaca fetal aparece entre la semana 28 y 30 y depende probablemente de la funcionalidad del hipotálamo posterior y del núcleo del bulbo superior26 . El líquido amniótico tiene un papel importante en el crecimiento y desarrollo fetal ya que rodea al feto proporcionando un colchón contra los límites constrictivos del útero grávido, que da al feto espacio para moverse y crecer protegido de traumatismos externos27 . El líquido amniótico también ayuda a mantener la temperatura corporal fetal y participa en la homeostasis hidroelectrolítica28 . Las alteraciones en la cantidad del líquido amniótico son un signo indirecto de trastorno subyacente como hipoxia fetal, defecto de tubo neural u obstrucción gastrointestinal. Por lo tanto, la evaluación ecográfica del líquido amniótico ayuda a diagnosticar compromiso fetal y anomalías estructurales que permiten orientar en la toma de decisiones respecto al embarazo 27 . Durante el primer trimestre la principal fuente del líquido amniótico es la membrana amniótica, la cual presenta transporte activo de electrolitos 16 Antecedentes y otros solutos por el amnios con la consiguiente difusión pasiva del agua en respuesta a los cambios de presión osmótica29 . Para la segunda mitad del primer trimestre y la primera mitad del segundo trimestre aparecen otras vías de producción y consumo de líquido amniótico. Éstas vías de producción son el movimiento del líquido a través del corion frondoso28-30 y la piel fetal, la cual permite intercambio directo hasta que sobreviene la queratinización entre las 24 y 26 semanas de gestación, la diuresis del feto y la deglución, que comienzan entre las 8 y 11 semanas de gestación, las cuales constituyen la principal vía tanto de producción como de consumo de líquido amniótico a partir de la mitad del segundo trimestre del embarazo 29-30 . En el sistema respiratorio fetal el líquido puede ser absorbido o excretado a través de los capilares alveolares y la traquea28 . Para evaluar por medio del ultrasonido el volumen del líquido amniótico, se han propuesto varios métodos entre los que se encuentran: la evaluación subjetiva, la determinación del bolsillo aislado más profundo verticalmente, el índice de líquido amniótico de los cuatro cuadrantes, la determinación planimétrica del volumen intrauterino total y diversas fórmulas matemáticas para el cálculo del volumen. En el perfil biofísico fetal se utiliza la determinación del bolsillo aislado más profundo verticalmente31-32 . 17 Antecedentes Líquido amniótico Fotografía 4. Medición de líquido amniótico El perfil biofísico fetal propuesto por Manning no tiene contraindicaciones y no supone riesgos para la madre ni para el feto33 . La frecuencia de falsos negativos para el PBF es de 0.7% lo cual es significativamente mejor que la prueba sin estrés (PSS) y similar a la prueba de estrés por contracción (PTO). La frecuencia de falsos positivos es de aproximadamente un 30% mejor que la prueba sin estrés o la prueba de estrés por contracción17 . El valor predictivo negativo es similar al de la PSS (prueba sin estrés 98% y perfil biofísico fetal 98.5%) mejor para la prueba sin estrés no reactiva34 . 18 Antecedentes Baskett en 198435 y Manning 199036 estudiaron la relación entre el perfil biofísico Vfetal y la morbilidad neonatal. Los valores de la prueba obtenida por el perfil biofísico fetal guardan una relación lineal inversamente proporcional con la morbilidad perinatal. No así con la mortalidad perinatal la cual guarda una relación exponencial inversamente proporcional36 . Fotografía 5. Morbilidad perinatal La relación entre el perfil biofísico fetal y la mortalidad perinatal refleja la falla de la respuesta compensatoria de adaptación fetal37 . Cuando se realiza un perfil biofísico fetal se toma en cuenta que el diagnóstico de hipoxia, como el de acidosis fetal, debe de ser establecido por exclusión; ya que la ausencia 19 Antecedentes de la actividad biofísica del feto no puede ser atribuida siempre a dichos diagnósticos, por lo que primeramente se deben descartar otros factores como son: ingesta de medicamentos depresores del sistema nervioso central tales como sedantes (barbitúricos, benzodiacepinas), fármacos utilizados por la gestante como analgésicos (morfina, meperidina), anestésicos (halotano) los cuales reducen o inhiben la actividad biofísica del feto38 y la periodicidad normal de las actividades biofísicas fetales que han sido demostradas y que se presentan en períodos cortos (cada 20 a 40 minutos)39-40 . La relación que existe entre el resultado del último perfil biofísico fetal y la parálisis cerebral es inversamente proporcional, exponencial y muy significante41 por lo que se considera que el último resultado del perfil biofísico fetal es un predictor de parálisis cerebral. La última aportación hecha por Manning a la comunidad científica documenta que la asfixia antenatal es una causa de parálisis cerebral importante y que es potencialmente evitable42 . El realizar este estudio es importante en nuestro centro hospitalario debido a que no se conoce el método de evaluación; si bien es reconocido a nivel internacional que es la mejor forma de evaluar riesgo fetal en embarazos de alto riesgo, el llevarlo a cabo y demostrar estadísticamente su utilidad llevará a modificar protocolos de manejo e implementar su aplicación con la consiguiente mejoría en la calidad de atención. 20 Planteamiento del problema y objetivos PLANTEAMIENTO DEL PROBLEMA ¿Existe diferencia en la mortalidad y morbilidad perinatal cuando se realiza perfil biofísico fetal en el embarazo de alto riesgo? OBJETIVOS Objetivo general Determinar si existe diferencia en la mortalidad y morbilidad perinatal cuando se realiza perfil biofísico fetal en el embarazo de alto riesgo. Objetivos específicos 1. Determinar si existe diferencia en la mortalidad perinatal cuando se realiza perfil biofísico fetal en el embarazo de alto riesgo. 2. Determinar si existe diferencia en la morbilidad perinatal cuando se realiza perfil biofísico fetal en el embarazo de alto riesgo. 21 Material y métodos MATERIAL Y MÉTODOS Tipo de estudio Ensayo clínico con control externo (histórico)52 Procedimiento De diciembre de 1998 a junio de 1999 se realizó un ensayo clínico con control externo (histórico) en el Departamento de Ginecología y Obstetricia del Hospital General de Zona y Medicina Familiar número 1 del Instituto Mexicano del Seguro Social de la ciudad de Colima, Col. Se incluyeron 63 pacientes referidas en forma consecutiva con embarazo de 34 semanas o más por fecha de última menstruación segura y confiable (considerando como menstruación segura y confiable a toda paciente que refirió ser eumenorreica, no tener el antecedente de utilización de ningún método de planificación familiar cuando menos tres meses a la fecha de su ingreso al estudio y no estar lactando). Todas las pacientes fueron consideradas con embarazo de alto riesgo según el puntaje obtenido en un formato institucional (forma MF-7) el cual se aplica a las mujeres embarazadas que acuden a consulta de control prenatal. Este formato sirve para evaluar la atención médica prenatal y el riesgo reproductivo otorgando una calificación de 4 puntos o más a los embarazos que cumplen una serie de características que los hacen ser considerados como de alto riesgo (anexo 1). Se excluyó del estudio a toda mujer con embarazo de alto riesgo que presentó ruptura de membranas y/o antecedente de isoinmunización materno-fetal, uso de medicamentos depresores o sedantes del sistema nervioso central y trauma abdominal materno. El control prenatal de las pacientes se realizó en el servicio de Ginecología y Obstetricia por su médico tratante. A cada paciente se le explicó la naturaleza y riesgos derivados de la realización del perfil biofísico fetal para obtener su consentimiento informado (anexo 2). El PBF se realizó cada semana, como parte de su protocolo de evaluación antenatal 22 Material y métodos a partir de su ingreso al estudio y hasta el término de la gestación. Cuando se trató de embarazadas con diagnóstico adicional de diabetes y/o embarazo prolongado, se efectuó el perfil biofísico fetal dos veces por semana. Para detectar riesgo fetal se evaluaron las cinco variables del perfil biofísico fetal que incluyen: a) reactividad de la frecuencia cardiaca fetal, b) movimientos corporales, c) movimientos respiratorios, d) tono fetal y e) volumen de líquido amniótico. Cada variable se calificó con dos o cero puntos según fuera normal o anormal respectivamente20 . La reactividad de la frecuencia cardiaca fetal se evaluó con un cardiotocógrafo (Sonicaid team Oxford. USA Florida) mediante la prueba sin estrés (PSS). Esta prueba se consideró como normal cuando se presentaron al menos dos episodios de aceleración de la frecuencia cardiaca fetal mayores de 15 latidos por minuto, los cuales debían durar al menos 15 segundos, acompañados de movimientos fetales en un lapso mínimo de l0 minutos. Todas las pacientes habían ingerido alimentos recientemente (ayuno no mayor de 3 horas) y no estaban bajo tratamiento con depresores del sistema nervioso central. El estudio se realizó con la paciente en posición en decúbito lateral y semisentada. A cada una de ellas se les determinó la tensión arterial, pulso y temperatura antes y después de cada prueba. Las otras cuatro variables se evaluaron mediante la observación, durante al menos 30 minutos con un equipo de ultrasonido de tiempo real modo B (Toshiba corporation Japan. Model SAL-32B). Los movimientos corporales se consideraron como normales cuando se presentaron al menos tres movimientos corporales, considerándose los episodios de movimientos continuos activos como uno solo. Los movimientos respiratorios fetales se consideraron normales cuando se presentó al menos un episodio de movimiento respiratorio que hubiera durado al menos 30 segundos. El tono fetal se consideró como normal cuando se presentó al menos un episodio de extensión activa con vuelta a la flexión de las extremidades o el tronco fetal, o cuando se presentaron movimientos de cierre y apertura de la mano. El volumen de líquido amniótico fue considerado normal cuando se encontró como mínimo un depósito de líquido amniótico que midió 2 centímetros cuando menos en dos planos perpendiculares. 23 Material y métodos La morbilidad perinatal fue definida como la presencia –a juicio del pediatra y/o ginecólogo- de una o más de las variables perinatales descritas a continuación y que hubieran sido consignadas en el expediente clínico: a) Apgar a los cinco minutos menor de 7 b)..Admisión del recién nacido a cuneros por razones no relacionadas a problemas médicos maternos durante el puerperio inmediato, con una estancia por lo menos de 24 horas (decisión tomada por el pediatra). Se consideraron casos de mortalidad perinatal a las defunciones de fetos de más de 34 semanas de embarazo por fecha de última regla hasta los 28 días de nacimiento, que hubieran constado en el expediente clínico, y que no pudieron ser atribuidas a causas de índole externo como traumatismos, desastres naturales o accidentes. Estos casos debieron haber ocurrido durante el período de tiempo comprendido de diciembre de 1997 a junio de 1998 para el grupo control histórico y de diciembre de 1998 a junio de 1999 para el grupo sometido al PBF. Las variables dependientes morbilidad y mortalidad perinatales fueron consideradas como cualitativas, nominales y dicotómicas en términos de presencia o ausencia de la característica. Como control externo (histórico) se recolectaron, en forma aleatoria, 64 expedientes a partir de todos los embarazos considerados como de alto riesgo según la evaluación asentada en la forma MF 7 que fueron atendidos en el período transcurrido de diciembre de 1997 a junio de 1998 y a los cuales no se les realizó PBF. Los criterios de inclusión y exclusión para el grupo control externo fueron los mismos que los considerados para el grupo sometido a PBF. De cada expediente se obtuvo información para establecer si hubo morbilidad o mortalidad perinatal de acuerdo a los mismos criterios establecidos para el grupo en que se realizó la intervención. En el Hospital General de Zona y Medicina Familiar número 1 del Instituto Mexicano del Seguro Social en Colima, se considera como embarazo prolongado a toda 24 Material y métodos aquella gestación que dura más de 41 semanas calculadas de acuerdo a la fecha de última menstruación segura y confiable proporcionada por la paciente. 25 Material y métodos Criterios de selección Inclusión • Toda mujer con embarazo de alto riesgo de 34 semanas por FUR segura y confiable. • Que firme carta de consentimiento informado (anexo 2). No inclusión • Ruptura prematura de membranas. • Isoinmunización materno-fetal. • Medicamentos depresores o sedantes del sistema nervioso central en la madre. • Trauma abdominal materno. Eliminación • Cambio de residencia que impida su control en el Hospital General de Zona 1. • Muerte de la embarazada. 26 Material y métodos Análisis estadístico Las diferencias entre ambos grupos con respecto a edad materna, peso del recién nacido, edad gestacional por fecha de última menstruación y del recién nacido por Capurro se evaluaron mediante t de Student Se describió la calificación de la forma MF-7 y del Apgar mediante frecuencias y proporciones. Para comparar la mortalidad entre el grupo sometido a perfil biofísico fetal y el control externo se utilizó la prueba exacta de Fisher. Las diferencias de morbilidad perinatal entre los grupos se analizaron mediante la prueba de Ji Cuadrada. 27 Resultados RESULTADOS a) Perfil biofísico fetal Se evaluaron 63 mujeres con embarazo de alto riesgo (mediana 2 y recorrido intercuartílico de 1 a 4 pruebas; rango 1 a 10 estudios por paciente), realizando en total 162 estudios. No se encontraron diferencias significativas entre el grupo sometido al perfil biofísico fetal (n = 63) y el grupo control histórico (n = 64) con respecto a edad materna (28±6 vs. 29±6 años, p = 0.45), edad gestacional por fecha de última menstruación (39±3 vs. 39±2 semanas, p = 0.35), edad del recién nacido evaluado mediante Capurro (39±1 vs. 39±2 semanas, p = 0.99) y peso del recién nacido (3350±512 vs. 3358±581 gramos, p = 0.99) tabla I. 28 Resultados Tabla alto Tabla I.I. Características Característicasclínico clínicoepidemiológicas epidemiológicasenenlos losembarazos embarazosdede riesgo en el en grupo del perfil biofísico y el grupo de control histórico alto riesgo el grupo del perfil biofísico y el grupo de control histórico PERFIL BIOFÍSICO FETAL Si (n = 63) No (n = 64) Valor de p* Edad materna 28±6 29±6 0.45 Edad gestacional por 39±3 39±2 0.35 39±1 39±2 0.99 FUM Edad al (Capurro) nacer Peso del recién nacido 3350±512 3358±581 * *t de t de Stude Student 29 0.99 Resultados Las indicaciones más frecuentes para realizar perfil biofísico fetal fueron embarazo prolongado (16 casos), hipertensión inducida por el embarazo (10 casos), edad materna avanzada (5 casos) y antecedente de hijo macrosómico (5 casos). El resto de las indicaciones se muestran en la tabla II. Tabla II. Indicaciones del perfil biofísico fetal en casos de embarazo de alto Tabla II. Indicaciones del perfil biofísico fetal en casos de embarazo de alto riesgo riesgo Indicaciones Indicación del Perfil Biofísico Fetal No.Frecuencia de pacientes Embarazo Embarazo prolongado prolongado Hipertensión Hipertensión Inducida inducida por por el el embarazo embarazo Edad materna avanzada Edad materna avanzada Antecedente Antecedente de de hijo hijo macrosómico macrosómico Sospecha de oligohidramnios Sospecha de oligohidramnios Madre Madre Rh Rh negativo negativono noisoinmunizada isoinmunizada Sospecha Sospecha de de RCIU RCIU ** Disminución Disminución de de movimientos movimientos fetales fetales Diabetes Diabetes Muerte previa Muerteperinatal perinatal previa Enfermedad tiroidea materna Enfermedad tiroidea materna Muerte fetal in-útero previa Muerte fetal in yútero Polihidramnios NICprevia III† Polihidramnios y NIC III† Toxicomanía ‡ Toxicomanía ‡ Hijo previo con alteración estructural y muerte perinatal Hijo previo y muerte perinatal Sangrado delcon 3er.alteración trimestreestructural § Sangrado del tercer trimestre § Antecedente de esterilidad primaria Antecedente de esterilidad primaria Paraplejia Paraplejia Total Total Retardo de de crecimiento crecimiento intrauterino intrauterino ** Retardo †Neoplasia Intraepitelial Intraepitelial de de Cervix Cervix †Neoplasia Cocaína ‡‡ Cocaína § Inserción baja de placenta 30 16 16 10 10 55 55 44 44 33 33 22 22 22 11 11 11 11 11 11 11 63 63 Resultados El embarazo prolongado constituyó el 25% (n = 16) del total de la población de alto riesgo en el grupo de estudio. La edad gestacional al realizar el primer perfil biofísico fetal fue de 38.4 ± 3 semanas (rango 34 a 42.4 semanas). b) Mortalidad perinatal Las causas de muerte perinatal en el grupo control externo (histórico) reportadas en el certificado de defunción, se enuncian en la tabla III. Tabla III. Causas de mortalidad perinatal en el grupo de control Tabla III. Número Sexo de caso externo (histórico)* Causas mortalidad perinatal en el grupo de control Peso Edad Vía de Causa de la muerte* nacimiento externo (histórico)* (g) gestacional (semanas) Número Edad de caso Óbito gestacional (semanas) F 2925 Óbito Muerte 1 neonatal 39 2 Muerte neonata 3 l 4 2 3 4 5 6 39 39 Vaginal M 4000 42 F 3450 40 F 41.5 2250 40 5 Vía de nacimiento M 36.5 M Causa de la muerte* Peso Sexo (g) Vaginal Interrupción de la circulación materno-fetal Interrupción de la circulación 2925 F materno-fetal Abdominal Asfixia neonatal severa Vaginal Acidosis mixta severa 37 Abdominal Vaginal Enfermedad hemorrágica del recién Asfixia neonatal severa 4000 M Nacido Vaginal 39 Vaginal 2550 37 Abdominal Acidosis mixta severa 3450 F Abdominal Coagulación intravascular diseminada Enfermedad hemorrágica del 2250 F recién nacido Vaginal Síndrome de aspiración de meconio Coagulación Intravascular 3500 M Diseminada 3500 *Información obtenida del certificado de defunción 31 Resultados Las muertes perinatales incluyeron 1 óbito y 5 muertes neonatales. De las cinco muertes neonatales, cuatro ocurrieron antes de las 72 horas de vida extrauterina. La asfixia intrauterina fue la causa más frecuente de muerte neonatal en cuatro de los seis casos de mortalidad perinatal. No se documentaron anomalías congénitas mayores incompatibles con la vida, únicamente en el caso número 4 de la tabla III se reportaron alteraciones estructurales Vcompatibles con trisomía 21 ( hipotonía, puente nasal amplio y deprimido, pliegues epicánticos, braquidactilia, clinodactilia, separación amplia entre ortejos 1 y 2 y radiografía con imagen de doble burbuja sugestiva la cual sugería probable atresia duodenal ). En ninguno de los casos de las muertes perinatales, se realizó necropsia. Durante el período de tiempo comprendido de diciembre de 1998 a Junio de 1999 se presentaron 8 muertes perinatales desde la semana 21 a la 41 de gestación, en un total de 1637 nacimientos registrados en el Hospital General de Zona y Medicina Familiar No.1 del Instituto Mexicano del Seguro Social en la ciudad de Colima. Ninguno de estos casos fue enviado como embarazo de alto riesgo para realizar el perfil biofísico fetal. No se presentaron casos de mortalidad perinatal en el grupo al que se le realizó perfil biofísico fetal (n = 63) a diferencia del grupo control externo (histórico) (n = 64) en el cual se presentaron seis muertes perinatales (tabla IV). 32 Resultados Tabla IV. Morbilidad Morbilidady ymortalidad mortalidad perinatal en embarazos de riesgo alto Tabla IV. perinatal en embarazos de alto riesgo PBF Control Valor de p Valor de p (nPBF = 63) % (nn = 63) (n = 64) Control n(n =% 64) Mortalidad n0 (0) % 6n (9.3)% Mortalidad Morbilidad 06 (9.5) (0) (9.3) 86 (12.5) 0.028* 0.3 † Morbilidad 6 (9.5) 8 (12.5) 0.3 † * Prueba exacta de Fisher † Ji Cuadrada 33 0.028* Resultados c) Morbilidad perinatal El 79% de las pacientes en el grupo con la intervención obtuvieron una calificación mayor de 8 en el último PBF realizado antes del nacimiento, lo cual fue acorde con el buen resultado perinatal obtenido (tabla V). Tabla V. Tabla V. Resultados del último perfil biofísico fetal y morbilidad Resultados último perfil biofísico de fetal enriesgo 63 pacientes perinatal endel pacientes con embarazo alto durante su embarazo de alto riesgo de acuerdo a su morbilidad perinatal Morbilidad perinatal Puntaje Puntaje PBF PBF 6 86 108 10 Total Casos Pacientes (n = 63) (n) (%) (n) (%) 13 13 32 32 18 18 63 21 2151 5128 28 (100) Admisión a cuneros* Admisión a cuneros (n =5) (%) (n)(n) (%) 2 2 2 2 1 1 5 15 15 6 65 5 (7.9) *Al menos 24 horas durante sus primeras horas de vida extrauterina PBF = Perfil biofísico fetal 34 Apgar<<88 Apgar (n =6) (n) (%) (n) (%) 2 22 22 2 6 15 615 116 11 (9.5) Resultados Fotografía 6. Recién nacido en cuneros La morbilidad perinatal fue similar entre el grupo al que se realizó perfil biofísico fetal y el grupo control externo (histórico) (n = 6, 9.5% vs. n = 8, 12.5%; p = 0.3) respectivamente (tabla IV). Se describe la calificación del formato MF-7 (que evalúa riesgo reproductivo) y de la valoración Apgar mediante frecuencias y proporciones en la tabla VI. Note la similitud de los valores en la puntuación Apgar tanto en el grupo de estudio como en el grupo de control histórico. El alto riesgo en ambos grupos fue determinado por la evaluación realizada en el formato MF7. 35 Resultados Tabla VI. Calificación de la valoración Apgar y de la alto riesgo. Tabla VI. Calificación de la valoración Apgar y de la obtenida en la forma MF-7 en embarazos de alto riesgo. PBF Puntaje (n=63) PBF n (%) Puntaje (n = 63) n (%) Apgar Apgaralalminuto minuto 55(8) <8 <8 (8) ≥ ≥8 8 5858(92) (92) Apgar a los 5 minutos Apgar a los 5 minutos <8 00 (0) <8 (0) ≥ ≥8 8 6363(100) (100) MF-7 MF-7 3333(52) <8 (52) <8puntos puntos ≥ ≥8 8puntos 30 (48) puntos 30 (48) 36 Control (n=64) Control n(n = (%) 64) n (%) 66(9) (9) 5858(91) (91) 11(2) (2) 6363(98.4) (98.4) 4242(66) (66) 2222(34) (34) Discusión DISCUSIÓN El embarazo prolongado siempre ha sido un tema polémico tanto para su diagnóstico como su manejo. El consenso general es que embarazos que se prolongan más de 42 semanas presentan un aumento significativo en la mortalidad y morbilidad perinatales43-5 . Boyd y cols.46 documentaron una incidencia de embarazos prolongados de 7.5% cuando la edad gestacional se diagnosticó considerando la fecha de última menstruación. En el presente estudio, el embarazo prolongado representó el 25% de los embarazos de alto riesgo (EAR) con base en la fecha de última menstruación segura y confiable. El embarazo prolongado fue también la indicación más frecuente para solicitar un perfil biofísico. Es probable que el resultado obtenido haya sido debido principalmente, a que dicho diagnóstico se otorga, en el Hospital General de Zona y Medicina Familiar No.1 del Instituto Mexicano del Seguro Social en Colima, Col., a toda paciente con gestación mayor de 41 semanas y no a toda aquella gestación que rebasa las 42 semanas o los 294 días a partir del primer día del último período menstrual47 . Siendo esta entidad la mas frecuentemente observada en nuestro medio, cabe señalar que la vigilancia prenatal con el estudio propuesto ha impactado satisfactoriamente en el resultado perinatal. Esta situación va de acuerdo con estudios internacionales los cuales documentan que el método más útil para valorar el estado fetal en embarazos prolongados es la determinación del perfil biofísico fetal48-50 . Por lo que identificar el embarazo prolongado como principal entidad dentro de los EAR que requieren una vigilancia y seguimiento estrecho, nos ayuda a conocer cual es el punto crítico donde debemos poner nuestra atención y ser la pauta para estudios e investigaciones futuras que arrojen resultados a mediano y corto plazo esencialmente a nivel operativo pero que repercutirán finalmente en uno de los principales indicadores de la salud y la mortalidad perinatal. El no encontrar diferencias significativas en cuanto a la edad materna, edad gestacional por fecha de última menstruación (FUM), edad del recién nacido según Capurro y peso del recién nacido entre los dos grupos, nos permite comprobar que las mujeres con 37 Discusión embarazo de alto riesgo (EAR) tuvieron características clínico-epidemiológicas similares a pesar de haber sido atendidas en nuestro hospital con diferencia de un año. Esto significa que la población beneficiaria de los servicios de salud en el Instituto Mexicano del Seguro Social en nuestra entidad es homogénea. Baskett en 198435 y Manning 199036 encontraron disminución de la morbilidad fetal cuando se realizó el perfil biofísico fetal (PBF), nosotros no encontramos diferencia significativa en la morbilidad fetal por el hecho de realizar perfil biofísico fetal, resultado que pudo ser debido al tamaño de la muestra. La edad gestacional promedio al nacimiento en uno de los estudios de Manning et al.21 fue de 31.3 semanas comparado con las 39.1 semanas en promedio que nosotros encontramos, y siendo que la prematurez es una de las principales causas tanto de morbilidad como de mortalidad perinatal, en nuestro estudio no tuvimos ningún caso de prematurez basándonos en la valoración del recién nacido realizada por el pediatra con el método de Capurro, lo que repercute en no encontrar diferencias en la morbilidad. Otra de las probables causas que influyó para que no se presentara una diferencia significativa en la morbilidad fueron los criterios de selección utilizados para el presente estudio, los cuales restringieron el ingreso a mujeres con embarazos menores de 34 semanas. Esto disminuyó la posibilidad de incluir en el estudio a casos de prematurez que constituyen unas de las principales causas tanto de mortalidad como de morbilidad perinatal. Sin embargo, este criterio fue considerado con base en la factibilidad ya que en el Hospital General de Zona y Medicina Familiar No.1 del Instituto Mexicano del Seguro Social en Colima no se cuenta con unidad de cuidados intensivos neonatales (UCIN) y además existe un lineamiento interno para el servicio de Ginecología y Obstetricia, donde se estipula que odo embarazo menor de 34 semanas de gestación debe ser enviado a un tercer nivel por no contar con la infraestructura adecuada para dar la mejor atención a este tipo de pacientes. por otro lado, la determinación de gasometría en sangre del cordón umbilical no fue factible realizarla. La asfixia intrauterina fue la causa más frecuente de muerte perinatal condicionando la presencia de un óbito fetal y tres de las cinco muertes neonatales dentro de las primeras 72 horas de vida extrauterina. El diagnóstico de muerte fue realizado por clínica. 38 Discusión Los diagnósticos tanto de muerte intrauterina (óbito fetal) como de muerte neonatal (hasta los 28 días de vida extrauterina) fueron realizados únicamente por examen físico al momento del desenlace y por ello no podemos descartar la presencia de alguna alteración estructural no macroscópica tanto en el feto como en el recién nacido y en la placenta que pudieran haber influido en el desenlace fatal. La calificación mayor de 8, (n = 50, 79%) antes del nacimiento obtenida en el último PBF realizado en cada paciente, estuvo asociada a resultado perinatal favorable. El hecho de no encontrarnos con calificaciones menores de 6 puntos en los estudios realizados en el grupo de estudio, fue resultado de una vigilancia más estrecha por un equipo multidisciplinario que permitió tomar y modificar decisiones ante variaciones en el comportamiento biofísico fetal reportados durante la evaluación del perfil biofísico fetal que sugieren situaciones de peligro fetal. Esto se pone de manifiesto con la ausencia de muertes perinatales en el grupo de estudio siendo que es la población donde se esperaría encontrar la tasa de mortalidad elevada. Los resultados en la presente investigación demuestran la utilidad del perfil biofísico fetal que además ha facilitado el poder implementar estrategias en beneficio de la salud materno-fetal. Aunque el apoyo tecnológico complementa la evaluación de la paciente permitiéndonos efectuar la toma decisiones, la evaluación individual de cada caso es el punto clave ya que la clínica juega un papel primordial e insustituible para el manejo en forma integral y multidisciplinario de toda paciente que se encuentra ante una situación de riesgo fetal. El perfil biofísico fetal permite evaluar el bienestar fetal, no confiere gran dificultad técnica, no tiene contraindicaciones y no supone riesgos para la madre ni para el feto33 . Algunas investigaciones23-5 han documentado que las actividades biofísicas que aparecen primero durante la vida fetal son las últimas en desaparecer durante la asfixia fetal (concepto de hipoxia gradual). Este concepto, sugiere diferentes grados de sensibilidad a la acidosis y a la hipoxia, por lo que se debe de tomar en cuenta al interpretar los resultados sobre la evaluación biofísica del feto38 . Por lo que cada criterio evaluado en el perfil biofísico posee un valor predictivo diferente con respecto a la hipoxia fetal21 . Este problema detectado 39 Discusión en la interpretación de los datos obtenidos al efectuar el perfil biofísico fetal se redujo con la introducción de un cambio en la calificación de normal cuando la puntuación fue de 8 o superior pero debiendo incluir la existencia de un volumen normal de líquido amniótico36 . Bien indicado el perfil biofísico fetal, puede ser útil para definir el momento en que el feto puede estar en una situación crítica y así poder intervenir a tiempo. De acuerdo a reportes internacionales la aplicación de este método a población obstétrica de alto riesgo ha logrado reducir la mortalidad perinatal11-22 . Por lo tanto el perfil biofísico fetal debería de ser utilizado como método de evaluación fetal antenatal en embarazos de alto riesgo. Con el presente trabajo no se puede concluir en forma definitiva si la realización del perfil biofísico fetal modifica la morbilidad perinatal. Por lo que Se requieren estudios con mayor tamaño muestral para investigar este aspecto. Con los resultados obtenidos, en nuestro estudio se confirma la necesidad en adicionar, al protocolo de manejo antenatal de los embarazos de alto riesgo, la realización de evaluaciones con perfil biofísico fetal que, aunque puedan implicar a corto plazo un incremento en los costos por tiempo y recursos humanos requeridos, a largo plazo evitará el costo que implica la rehabilitación y limitación del daño de los casos de morbilidad y mortalidad perinatales. Por todos es conocido que dentro de la mortalidad perinatal existen factores que pueden influir en el macro ambiente, micro ambiente, y ambiente materno, que en algunos casos los factores podrán ser modificados, en otros se podrá prevenir, también es cierto que en algún caso las acciones quedarán limitadas, pero cuando sea posible intervenir modificando o detectando situaciones de riesgo tenemos la obligación de actuar, por lo que si existe este recurso debe ser utilizado en cualquier centro hospitalario donde se cuente principalmente con un cardiotocógrafo, y un equipo de ultrasonido, así como el personal médico capacitado. 40 Conclusión CONCLUSIONES En el presente estudio la mortalidad perinatal en embarazos de alto riesgo fue menor en los casos en que se realizó perfil biofísico fetal. No se puede concluir en forma definitiva si la realización del perfil biofísico fetal modifica la morbilidad perinatal; a pesar de que no encontramos diferencia significativa en la morbilidad fetal por el hecho de realizar perfil biofísico fetal, este resultado pudo ser debido al tamaño de la muestra. La realización de perfil biofísico fetal en embarazos de alto riesgo se encuentra asociada a menor mortalidad perinatal aunque probablemente no a menor morbilidad 41 Anexos Anexo 1 Forma MF-7 (Evalúa la atención médica prenatal y riesgo reproductivo) 42 Anexos 43 Anexos ANEXO 2 CARTA DE CONSENTIMIENTO INFORMADO TITULO DEL ESTUDIO DE INVESTIGACION Impacto del perfil biofísico fetal sobre la morbilidad y mortalidad perinatal en embarazos de alto riesgo INVESTIGADOR Dra. Silvia Lorena Moctezuma Hernández. Instituto Mexicano del Seguro Social y Centro Universitario de Investigaciones Biomédicas de la Universidad de Colima. PROCEDIMIENTOS Si consiento en participar sucederá lo siguiente: Responderé a preguntas sobre mi historia médica. Me someterán a una exploración física obstétrica. Me realizarán registro cardiotocográfico fetal (Prueba sin estrés) y estudio ultrasonográfico. Estos no son dolorosos y no son peligrosos. Evaluación que podrá ser semanalmente y en algunas ocasiones nuevo estudio a las 24 hrs. Acudiré puntualmente a todas mis citas, siendo la última al mes de la resolución del embarazo, donde concluirá mi seguimiento. BENEFICIOS Tendré una vigilancia prenatal semanal por medio de registro cardiotocográfico y estudios ultrasonográficos. No existe ningún riesgo con la realización de estos métodos de vigilancia antenatal para mi hijo. CONFIDENCIALIDAD Los resultados de todas las pruebas del estudio me serán informados y la información obtenida será considerada confidencial. DERECHO DE REHUSAR O ABANDONAR Mi participación en el estudio es enteramente voluntaria y soy libre de rehusar a tomar parte o abandonar en cualquier momento, sin afectar o poner en peligro mi atención médica futura. CONSENTIMIENTO Consiento en participar en este estudio. He recibido una copia de este impreso y he tenido la oportunidad de leerlo. Firma:___________________ Testigo:__________________ Fecha__________________ 44 Anexos Anexo 3 Hoja de Recolección de Datos Caso No:________ Control No:________ Expediente:__________ Nombre:_________________________________________________Telefono:___________ Calificación MF7:_________ AGO: Edad:______ G____ P ____ A ____ C ____ No. Gesta Fecha Edad Gest Embarazos Previos Eut/Dist Sexo .Peso Cesarea Estado actual Vivo Muerto Muerte perinatal Tipo I Tipo II Fecha de ingreso al estudio:_____ Dx:______________________________________________________________________ Edad gestacional por FUM:____________ por USG:______________ USG ler. Nivel fecha:_______Resultado:_________________________________________ Perfil biofísico fetal Fecha Movimientos Movimiento respiratorios s corporales fetales Tono fetal Prueba sin estrés 45 Liquido amniótico Total Edad Gestacional Manejo Anexos Fecha de nacimiento:_________ Condición al nacimiento: Vivo:_____ Muerto:____ Vía de nacimiento: abdominal:____ vaginal:____ eutócico:____ distócico:____ Observaciones:_____________________________________________________________ Sufrimiento fetal documentado: Si:____ RPM: Si:____tiempo de evolución:____hrs. No:____ No:____ Circular de cordón: Si:____ Prematurez: Si:____ No:____ No:____ Sexo R/N: F:____ Peso:_______ Apgar: 1':____ 5':____ Silverman:______ M:____ Admisión a cuneros por lo menos 24 hrs: Si:____ No:____ Muerte Perinatal: Tipo I:____ Tipo II:____ Estudio Histopatológico:_____________________________________________________ _________________________________________________________________________ 46 Referencias Bibliográficas REFERENCIAS BIBLIOGRÁFICAS 1. Gleicher N y Elkayam U. Principios de Medicina Interna en el embarazo. En: Gleicher N: Medicina Clínica en Obstetricia, 1era ed. Panamericana 1992:25-29. 2. Goodwin JW, Dunne JT, Thomas BW. Antepartum identificatión of the fetus at risk. Can Med Assoc J 1969;101:458-465. 3. Aubry RH, Pennington JC. Identification and evaluation of high-risk pregnancy: The perinatal concept. Clin Obstet Gynecol 1973;16:3-27. 4. Hobel CJ. Hyvarinen MA, Okada DM, et al. Prenatal and intrapartum high-risk screening: I. Prediction of the high-risk neonate. Am J Obstet Gynecol 1973;117:1-9. 5. Coopland AT, Peddle LJ, Baskett TF et al. A simplified antepartum high-risk pregnancy screening form: Statistical analysis of 5459 cases. Can Med Assoc J 1977;116:999-1001. 6. De la Garza Q et al: Muerte Perinatal. Ginec Obst Mex 1995; 63: 186-9. 7. Bobadilla JL, Cerón S, Suárez P. Evaluación de la calidad de los datos de mortalidad perinatal. Registros vitales en México. Salud Pública de México 1988; 30 (1): 101-3. 8. Elrad Haim. Registros y estadísticas médicas durante el embarazo. En: Gleicher N: Medicina Clínica en Obstetricia, 1era ed. Panamericana 1992: 44-57. 9. Instituto Mexicano del Seguro Social. Manual de Normas y Procedimientos en Obstetricia. Norel Compañía Impresora,SA. 1986:11-21. 10. Manning FA, Baskett TF, Morrison I, Lange IR. Fetal biophysical profile scoring: A prospective study in 1,184 high-risk patients. Am J Obstet Gynecol 1981;140:289-93. 11. Manning FA, Morrison I Lange IR, et al. Fetal Assessment based biophysical profile scoring: Experience in 12,620 referred high-risk pregnancies. I Perinatal mortality by frecuency and etiology. Am J Obstet Gynecol 1985:343-50. 12. Manning FA, Morrison I, Harman CR, et al. Fetal assessment based on fetal biophysical profile scoring: Experience in 19,221 referref high-risk pregnancies. II An analysis of false negative fetal death. Am J Obstet Gynecol 1987;156:880-84. 47 Referencias Bibliográficas 13. Baskett TF, Allen AC, Gray JH, et al. Fetal Biophysical profile scoring and prenatal death. Obstet Gynecol 1987;70:357-60 14. Atlas epidemiológico del IMSS. 1985-1990 1era. Edición 1993. 15. Boletín Estadístico Anual de Mortalidad. Coordinación General de Comunicación Social/Publicaciones Instituto Mexicano del Seguro Social 1997. 16. Registros del sistema único de información del HGZ/MF No. 1 de la Delegación Regional Colima 17. Manning MD, Frank A. Valoración dinámica fetal por ultrasonido: Cuantificación del perfil biofísico fetal. Clínicas Obstétricas y Ginecológicas de Norteamérica 1996;2:27-43. 18. Vintzileos AM, Campbell WA, Rodis JF. Evaluación fetal anteparto mediante ecografía: Perfil biofísico fetal. En: Callen. Ecografía en Obstetricia y Ginecología 3era. Ed. Panamericana 1996;531-48. 19. Normas y Procedimientos de Obstetricia y Ginecología 1997. INPer. Marqueting y Publicidad de México. 20. Manning FA, Platt LD, Sipos L. Antepartum fetal evaluation: Development of a fetal biophysical profile score. Am J Obstet Gynecol 1980;136:787-95. 21. Manning FA, Morrison I, Marman CR. The abnormal fetal biophysical profile score V. Predictive accuracy according to score composition. Am J Obstet Gynecol 1990;162(4):918-27. 22. Vintzileos AM, Campbell WA, Ingardia CJ, et al. The fetal biophysical profile and its predictive value. Obstet Gynecol 1983;62:271-78. 23. Vintzileos AM, Gaffney SE, Salinger LM, et al. The relationship between fetal biophysical profile and Cord pH in patients undergoing cesarean section before the onset of labor. Obstet Gynecol. 1987;70:196. 24. Vintzileos AM, Fleming AD, Scorza WE, et al. Relationship between biophysical activities and umbilical cord blood gases. Am J Obstet Gynecol 1991;165:707-713. 48 Referencias Bibliográficas 25. Ribbert LSM, Snijders RJM; Nicolaides KH, et al. Relationship of fetal biophysical profile and blood gas values al cordocentesis in several growth- retarded fetus. Am J Obstet Gynecol 1990;163:569. 26. Thacker SB, Berkelman RL. Assessing the diagnostic accurancy and efficacy of selected antepartum fetal surveillance techniques. Obstet Gynecol Surv 1986;41:121141. 27. Doubilet PM, Benson CB. Evaluación ecográfica del líquido amniótico, En: Callen. Ecografía en Obstetricia y Ginecología 3era. Ed. Panamericana 1996;517-530. 28. Graham D, Sanders RC. Amniotic fluid. Semin Roentgenol 1982;17:210. 29. Sedes AE. Current concepts of amniotic fluid dynamics. Am J Obstet Gynecol 1980;138:575. 30. Wallenburg HCS. The amniotic fluid:I. Water and electrolyte homeostasis. J Perinat Med 1977;5:193. 31. Chamberlain PF, Manning FA,, Morrison I et al. Ultrasound evaluation of amniotic fluid volume: I The relationship of marginal and decreased fluid volumes to perinatal outcome. Am J Obstet Gynecol 1984;150:245. 32. Chamberlain PF, Manning FA, Morrison I et al. Ultrasound evaluation of amniotic fluid volume: II The relationship of increased fluid volume to perinatal outcome. Am J Obstet Gynecol 1984;150:250. 33. Arias F. Identificación y control preparto de la paciente de alto riesgo. En: Arias. Guía práctica para el embarazo y el parto de alto riesgo, 2da. Ed. Mosby 1994;3-21. 34. Manning FA, Lange IR. Morrison I et al. Fetal biophysical profile score and the nonstress test: A comparative trial. Obstet Gynecol 1984;64:326-31. 35. Baskett TF, Gray JH, Prewett SJ, et al. Antepartum fetal assessment using a fetal biophysical profile score. Am J Obstet Gynecol 1984;148:630-3. 36. Manning FA, Baskett TF, Morrison I, et al. Fetal Assessment based on fetal biophysical profile scoring. IV An analysis of perinatal morbidity and mortality. Am J Obstet Gynecol. 1990;162:703-9. 49 Referencias Bibliográficas 37. Manning FA. Fetal Biophysical Assessment by ultrasound. En: Creasy RK. Maternal fetal medicine 3rd ed. Saunders Company 1994:342-8. 38. Vintzileos AM, Campbell WA, Nochimson DJ, et al. The use and misuse of the fetal biophysical profile. Am J Obstet Gynecol 1987;156:527-33. 39. Patrick J, Challis J. Measurement of human fetal breathing movements in healthy pregnancies using a real-time scanner. Semin Perinatol 1980;4:275. 40. Patrick JE. Featherson W, Vick H, et al. Human fetal breathing and gross body movements at weeks 34 to 35 of gestation. Am J Obstet Gynecol 1978;130:693. 41. Manning FA, Bondagji N, Harman CR, Casiro O, Menticoglou S, Morrison I. Fetal assessment based on the fetal biophysical profile score: relationship of last BPS result to subsequent cerebral palsy. J Gynecol Obstet Biol Reprod (Paris) 1997;26(7):720-9. 42. Manning FA, Bondaji N, Harman CR, Casiro O, Menticoglou S, Morrison I, Berck DJ. Fetal assessment based on fetal biophysical profile scoring. VIII. The incidence of cerebral palsy in tested and untested perinates. Am J Obstet Gynecol 1998 Apr;178(4):696-706. 43. Clifford SA. postmaturity with placental dysfunction. J Pediatr 1954;44:1. 44. Zwerdling MA. Factors pertaining to prolonged pregnancy and its outcome. Pediatrics 1967;42:202. 45. Field TM, Dabiri C Hallock A, et al. Developmental effects of prolonged pregnancy and the postmaturrity syndrome. J Pediatr 1977;90:836. 46. Boyd ME, Usher RH, McLean FH, et al. Obstetric consequences of postmaturity. Am J Obstet Gynecol 1988;158:334. 47. Normas y Procedimientos de Obstetricia y Ginecología l998 Instituto Nacional de Perinatología. Embarazo con Amenorrea Prolongada 1998;55-6. 48. Hann L, McArdle C, Sach B. Sonographic biophysical profile in the postdate pregnancy. J Ultrasound Med 1987;6(4):191-5. 50 Referencias Bibliográficas 49. Jiménez Solís G, Izquierdo Puente JC, Barraza Espinoza RM, Sánchez Tenorio E, García Alonso A. Biophysical profile in prolonged pregnancy. Another alternative to fetal monitoring. Ginecol Obstet Mex 1990;58:284-8. 50. Bresadola M, Lo Mastro F, Arena V, Bellaveglia L, Di Gennaro D. Prognostic value of biophysical profile score in post-date pregnancy. Clin Exp Obstet Gynecol 1995;22(4):330-8. 51. Rodríguez Ye, Velásquez TM y Roís HJ. Mortalidad perinatal en las unidades de atención médica del IMSS en el Centro Médico Nacional de Torreón. Ginecol Obstet Mex 1998;66:297-300. 52. Dawson-Saunders B y Trapp RG. Study Design in Medical Research. En DawsonSaunders B y Trapp RG: Basic and Clinicals 1990: 6-19. 51 Biostatistics. 1ª ed. Appleton & Lange.