Actualización toxoplasmosis - Hospital Universitario Virgen de las
Anuncio

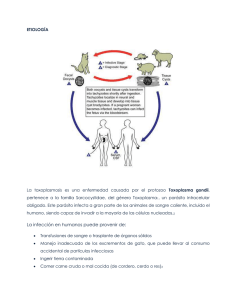
Clases de Residentes 2015 Actualización Toxoplasmosis Servicio de Obstetricia y Ginecología Hospital Universitario Virgen de las Nieves Granada ACTUALIZACIÓN TOXOPLASMOSIS. Cristina Félix Santamaría. 16 de marzo de 2015 EPIDEMIOLOGÍA Se trata de una zoonosis producida por Toxoplasma gondii, parásito protozario perteneciente a la especie Apicomplexa. Es de distribución universal, aunque la prevalencia varía de unos países a otros. Los valores de la prevalencia oscilan entre el 25-80% de la población según la región; siendo más frecuente en zonas rurales y climas templados y húmedos. El gato doméstico es su reservorio más importante, dado que se trata del huésped definitivo, donde tiene lugar el ciclo sexual del parásito. El Toxoplasma gondii puede presentar diferentes morfologías: - Taquizoítos o trofozoitos: formas de reproducción rápida que producen la fase aguda de la enfermedad. - Bradizoítos: formas de reproducción lenta que aparecen en las infecciones crónicas y son responsables de las reactivaciones. - Ooquistes inmaduros excretados en las heces de los gatos que maduran en el ambiente a los 3-4 días, sobreviviendo durante meses. La transmisión al hombre puede producirse por: - Ingestión de carne cruda o poco cocinada de los huéspedes intermediarios con quistes o taquizoitos. Forma más frecuente. Dra Félix / Dr Manzanares -1- Clases de Residentes 2015 - Actualización Toxoplasmosis Ingestión de ooquistes en las heces de gatos mediante contacto con el animal o su medio, trabajos de jardinería o ingestión de productos contaminados. - Transmisión vertical: paso de taquizoitos a través de la placenta, con un cierto retraso desde la infección materna a la infección fetal. - A través de transplantes, transfusiones… que contengan taquizoitos o bradizoitos. No hay evidencia de que exista transmisión mediante la lactancia, ni mediante contacto humano directo. Una vez ingerido el parásito el período de incubación varía entre 5 y 23 días. CLÍNICA Generalmente, en el adulto inmunocompetente se trata de una infección asintomática (90%). mononucleósico con Aunque astenia, a veces, fiebre, puede cefalea, producir mialgia un y síndrome adenopatías generalizadas; que es autolimitado. Y algunos casos (2%), cursan con coriorretinitis. En pacientes inmunodeprimidos el cuadro es más grave, pudiendo aparecer afectación multiorgánica y reactivaciones de infección pasada. La toxoplamosis congénita es debida a la transmisión vertical del parásito por vía transplacentaria, que puede ocurrir principalmente durante la primoinfección materna. De forma excepcional, puede producirse infección fetal si se adquiere la infección en los 3 meses previos a la concepción, por reactivación en caso de inmunosupresión o infección por un nuevo genotipo de Toxoplasma gondii. El riesgo de transmisión aumenta de forma importante a medida que avanza la gestación: - 15% en el 1º trimestre - 25-30% en 2º trimestre - 60% en 3º trimestre Dra Félix / Dr Manzanares -2- Clases de Residentes 2015 Actualización Toxoplasmosis Mientras que el grado de afectación fetal tiene una evolución inversa: - <16 s : 60% (grave afectación) - 17-23 s : 25 % - >24 s: 15% (formas leves o subclínicas) Algunos autores consideran que el momento más crítico está entra las semanas 10-26, momento en que la placenta tiene un tamaño suficiente como para infectarse al mismo tiempo que el feto es aún demasiado inmaduro. La toxoplasmosis congénita puede causar abortos, prematuridad, muertes fetales, formas sintomáticas e incluso formas subclínicas al nacimiento. - Neonatos sintomáticos al nacimiento: suponen el 15% de los fetos infectados, debido habitualmente a infecciones adquiridas antes de las 24 semanas. El pronóstico es malo, ya que muchos mueren o quedan con secuelas graves. La manifestación más frecuente es la coriorretinitis, pero también pueden presentar hepatomegalia, ictericia, esplenomegalia, púrpura, anemia, nefrosis compleja, convulsiones, parálisis de extremidades, hidrocefalia, microcefalia, atrofia óptica, cataratas, microftalmía, estrabismo, sordera, calcificaciones intracraneales, retraso psicomotor, fiebre, linfadenopatías, exantema, miocarditis, neumonitis… La clásica tétrada de Sabin incluye: hidrocefalia, calcificaciones intracraneales, coriorretinitis y convulsiones, pero es muy poco frecuente. - Neonatos asintomáticos al nacimiento: el 85% de los neonatos con infección congénita; sin embargo, una proporción importante de éstos (20-80%) puede presentar secuelas neurológicas o afectación ocular a largo plazo, sobretodo coriorretinitis. La incidencia de la toxoplasmosis gestacional y congénita varía mucho de unas regiones a otras. En los países con la incidencia más alta, nacen entre 3 y 6 de Dra Félix / Dr Manzanares -3- Clases de Residentes 2015 Actualización Toxoplasmosis cada 1000 niños anualmente con toxoplasmosis. Mientras que en Europa, se estima una incidencia entre 1-10 de cada 10.000 nacidos. En España existe poca información al respecto, pero se calcula que: - La seroprevalencia de toxoplasmosis en mujeres embarazadas en los últimos años está entre el 11 y el 28%. - La incidencia de toxoplasmosis gestacional se estima alrededor de alrededor de 2 casos por mil gestantes. - La incidencia de toxoplasmosis congénita debería situarse en torno al 0,1 – 0,3 por mil, según cálculos puramente teóricos. - Al igual que en otros países, se ha detectado un descenso de la prevalencia en los últimos años. DIAGNÓSTICO Diagnóstico serológico - IgG. Aparece entre la 1º- 2º semana postinfección y persiste positiva durante toda la vida. Su detección sólo indica exposición al parásito. La IgG se transmite por vía transplacentaria al RN. - IgM. Se hace positiva en la 1º semana postinfección y desaparece posteriormente de manera muy variable en cada caso (permaneciendo positiva en ocasiones durante varios años). Por lo tanto, la presencia de IgM en la gestante sólo sirve de orientación sobre la posibilidad de una infección reciente. En cambio, su presencia en el RN sí es diagnóstica de infección congénita, ya que no atraviesa la barrera placentaria. No obstante, se han descrito falsos positivos y falsos negativos (25-30%), debido a inmadurez del sistema inmunitario. - IgA. Presenta una dinámica similar a la IgM, por lo que no se usa habitualmente. Dra Félix / Dr Manzanares -4- Clases de Residentes 2015 Actualización Toxoplasmosis - IgE. No suele ser útil para el diagnóstico. - IgG-avidez. Se basa en el incremento de la fuerza de enlace entre la IgG específica y el antígeno a lo largo del tiempo. Un índice de alta avidez (> 30%) indica una infección en la que han transcurrido al menos 3-4 meses, mientras que una baja avidez (< 20%) señala una infección reciente, inferior a 3 meses. Reacción en cadena de la polimerasa (PCR) Para el diagnóstico prenatal la muestra de elección es el líquido amniótico, la cual se debe tomar 4 semanas después de la fecha estimada de infección y siempre a partir de las 18 semanas de gestación. La PCR en el líquido amniótico presenta una sensibilidad entre el 65 y 92% y una especificidad y VPP próxima al 100%. Un resultado positivo indica infección congénita, pero un resultado negativo no puede descartarla. No obstante, la sensibilidad de la PCR en el líquido amniótico parece superior a la que se obtiene en sangre, orina o LCR del recién nacido, por lo que debe ofrecerse siempre ante la sospecha de infección materna en cualquier trimestre. Parece ser que la PCR en sangre de cordón presenta una baja sensibilidad (16%), aunque su positividad permite el tratamiento temprano. Para el diagnóstico postnatal se puede realizar una PCR en sangre, orina y LCR, como complemento del estudio serológico del recién nacido con sospecha de infección. Esta técnica presenta buena especificidad; sin embargo, la sensibilidad es más baja, por lo que un resultado negativo no excluye la infección y en estos casos siempre se debe realizar un seguimiento serológico. Dra Félix / Dr Manzanares -5- Clases de Residentes 2015 Actualización Toxoplasmosis También existe la posibilidad de realizar un estudio con PCR de la placenta, pero lo cual se desaconseja. A veces la placenta puede estar infectada sin comprometer al recién nacido. Aislamiento del parásito Se realiza mediante inoculación intraperitoneal en animales (ratón) o en cultivos celulares. Puede usarse de forma complementaria a la determinación de la PCR en líquido amniótico para evitar los falsos negativos. También es posible la visualización microscópica del parásito en muestras de tejidos infectados, pero es una técnica poco rentable. Diagnóstico de la infección en la embarazada: toxoplamosis gestacional La toxoplasmosis es una infección habitualmente asintomática en la mujer embarazada inmunocompetente. Por ello, la mayoría de las infecciones maternas se diagnostican a partir del cribado serológico gestacional. El cribado para toxoplasmosis se realiza mediante la determinación de IgG en sangre materna en el primer trimestre de gestación. - Si la IgG es –: se realizan recomendaciones de profilaxis primaria y se hacen determinaciones seriadas de IgG cada 3 meses, para valorar una seroconversión asintomática. - Si la IgG es +: se debe estudiar la IgM (directamente por parte del laboratorio) - IgM negativa: se descarta infección aguda y se considera a la mujer inmunizada, no realizándose más determinaciones. - IgM positiva: es posible que se trate de una infección reciente y para comprobarlo se debe estudiar la avidez de la IgG y repetir la IgM. o Avidez alta: infección hace más de 3 meses o Avidez baja: posible infección en los últimos 3 meses. Dra Félix / Dr Manzanares -6- Clases de Residentes 2015 Actualización Toxoplasmosis Otra opción, si no se dispone de medios para determinar la avidez de la IgG, es comprobar los niveles de IgG pasadas 3-4 semanas. Un aumento por 3 o más veces indicaría infección aguda; sin embargo tiene la desventaja de retraso en el diagnóstico. Por tanto, el diagnóstico de infección materna aguda durante el embarazo sería: - Diagnóstico definitivo: seroconversión materna (IgG se hace positivo durante las determinaciones posteriores) o aumentan los niveles de IgG por 3. - Diagnóstico probable: IgG e IgM +, con avidez baja de IgG Para facilitar el diagnóstico, lo ideal sería conocer el estado inmune frente a toxoplasma antes de la gestación. Y sólo en el caso de las no inmune sería necesario un seguimiento posterior a lo largo del embarazo Diagnóstico de la infección en el feto: toxoplamosis congénita Ante la sospecha o la evidencia de una infección materna en cualquier trimestre, debe realizarse el diagnóstico de infección fetal mediante una amplificación del DNA del toxoplasma en líquido amniótico (PCR). Diagnóstico de afectación fetal Hay que remarcar que la detección del parásito en el líquido amniótico confirma la transmisión de la infección, pero no es sinónimo de afectación fetal. Por ello está indicado realizar un seguimiento ecográfico mensual, para detectar las posibles anomalías ecográficas compatibles con afectación fetal, a todas las pacientes con infección materna durante el embarazo; independientemente del resultado de la PCR en líquido amniótico. De esta manera, también se cubren los posibles falsos negativos de la PCR. Dra Félix / Dr Manzanares -7- Clases de Residentes 2015 Actualización Toxoplasmosis La ventriculomegalia y las calcificaciones intracraneales son las anomalías ecográficas más frecuentes. Otras lesiones menos frecuentes son: ascitis, microcefalia, hidropesía, hepatoesplenomegalia, calcificaciones intrahepáticas y engrosamiento placentario. Sin embargo, hasta el 70% de los fetos con afectación fetal presentan una ecografía normal y ninguno de estos hallazgos es patognomónico. Se ha visto que existe una buena correlación entre la gravedad de las lesiones ecográficas y el pronóstico neonatal. Las calcificaciones intracraneales aisladas no se correlacionan necesariamente con un mal pronóstico neurológico, pero parecen incrementar el riesgo de coriorretinitis. La ecografía tiene una capacidad diagnóstica elevada para la detección de anomalías, excepto las oculares; aunque estos marcadores ecográficos pueden aparecer de forma tardía. Por ello, la ausencia de anomalías ecográficas al final de la gestación es tranquilizadora sobre la posibilidad de infección neurológica grave al nacimiento. La mayoría de los protocolos y la opinión de los expertos recomiendan ofrecer la interrupción de la gestación únicamente cuando aparecen anomalías ecográficas. No obstante, en los casos de infección fetal antes de las 14 semanas, confirmada en líquido amniótico a partir de las 18 semanas, aún en ausencia de anomalías ecográficas, la paciente debe ser informada sobre los riesgos fetales y puede decidir la posibilidad de una interrupción legal de la gestación. Esta información se debería dar de forma preferente en un centro de referencia con experiencia. Además, para facilitar la opción de un seguimiento dirigido, la paciente debe ser informada de que en casos de afectación fetal grave existe la posibilidad de una interrupción legal tardía, ya sea en nuestro país o en otros países de la Unión Europea. Dra Félix / Dr Manzanares -8- Clases de Residentes 2015 Actualización Toxoplasmosis Diagnóstico neonatal Para llegar al diagnóstico de toxoplasmosis congénita, debe estudiarse a todos los niños con historia de toxoplasmosis gestacional o con síntomas propios de la enfermedad al nacimiento. Dado que la mayoría de los recién nacidos son asintomáticos al nacimiento y no presentan alteraciones ecográficas prenatales, el cribado gestacional representa la única manera de diagnosticar a todos los niños con toxoplasmosis congénita. Las pruebas a realizar son: - Hemograma y bioquímica completa con función hepática. - Fondo de ojo. - Ecografía cerebral transfontanelar o RM cerebral. - Estudio citoquímico del LCR. - Estudio microbiológico: o Obligado: IgM e IgG en la primera semana de vida. o Recomendado: PCR en sangre, LCR y orina. Para considerar que el recién nacido está infectado se debe valorar la historia gestacional, la clínica y los resultados de los estudios. Recién nacido con toxoplasmosis congénita: - Sintomático con IgM/IgA +, con historia de toxoplasmosis gestacional o PCR + - Asintomático con historia de toxoplasmosis gestacional y IgM/IgA + o PCR + Precisan tratamiento con seguimiento de los niveles de IgG. Recién nacido con toxoplasmosis congénita dudosa: - Sintomático sin datos en la gestación con IgM/IgA y PCR negativos. Descartando otras infecciones. Precisan tratamiento con seguimiento de IgG. Dra Félix / Dr Manzanares -9- Clases de Residentes 2015 - Actualización Toxoplasmosis Asintomático, con antecedentes de infección gestacional, pero pruebas negativas o Infección gestacional 1º trimestre: no precisa seguimiento o 2º trimestre: seguimiento de IgG sin tratamiento o 3º trimestre. seguimiento de IgG con tratamiento Inicialmente la IgG en el neonato carece de valor diagnóstico, ya que aparece por transferencia materna; sólo su estabilización o aumento en los meses posteriores confirma la infección. Dado que la IgG materna puede permanecer hasta 12 meses, todos estos niños precisan un seguimiento de al menos un año. El tratamiento puede disminuir o incluso negativizar transitoriamente la síntesis de anticuerpos, por lo que en pacientes tratados que han negativizado la IgG se recomienda repetirla al mes y a los 3 meses tras su suspensión antes de considerarlos no infectados. Si se positiviza la IgG de nuevo, se recomienda reiniciar el tratamiento hasta completar los 12 meses. TRATAMIENTO Tratamiento prenatal • Infección aguda materna Se debe pautar lo antes posible, sin esperar al resultado de la PCR de líquido amniótico, Espiramicina 1 g cada 8 horas (Rovamycine® 2 comp /8h) por vía oral preferentemente en ayunas. Se trata de un macrólido que no puede cruzar la placenta, por lo que sólo pretende disminuir el riesgo de transmisión fetal. La eficacia de tratamiento depende del momento de inicio, ya que parece ser que la transmisión vertical es menor cuando se inicia el tratamiento en las 3 semanas siguientes a la seroconversión. Dra Félix / Dr Manzanares - 10 - Clases de Residentes 2015 Actualización Toxoplasmosis Se recomienda que el tratamiento con espiramicina se mantenga hasta el final de la gestación, aún cuando el estudio del líquido amniótico sea negativo; por la posibilidad de falsos negativos de la PCR o que el Toxoplasma pueda permanecer en la placenta hasta el final del embarazo a pesar del tratamiento. No obstante, recomendaciones recientes sugieren que en casos con resultado negativo en el líquido amniótico y una vez completadas por lo menos 4 semanas de tratamiento, se puede valorar suspender la espiramicina. Lo cual podría estar especialmente indicado en gestantes con diagnóstico de infección probable. • Infección fetal confirmada Existen 2 regímenes posibles de tratamiento: - Administrar 3 semanas seguidas pirimetamina (50 mg/día vía oralDaraprim® 2 comp/24 h) junto con sulfadiazina (4 g/día por vía oral Sulfadiazina Reig Llofre® 2 comp/8h en ayunas) alternando con 3 semanas de espiramicina (1 g/8 h por vía oral) hasta el parto. - Administrar de forma continua pirimetamina y sulfadiazina hasta el parto. A cualquiera de estas 2 pautas debe añadirse ácido folínico en dosis de 10-15 mg/día para evitar la supresión medular, dado que la pirimetamina es un antagonista del fólico. Además se deben realizar hemogramas frecuentes, ya que si se objetivan alteraciones puede cambiarse a una pauta a días alternos. Este tratamiento pretende disminuir las secuelas en los fetos infectados. Aunque no hay estudios que demuestren una disminución de las lesiones intracraneales ni de la coriorretinitis posnatal a pesar del inicio precoz del tratamiento, sí se ha demostrado una reducción de las secuelas neurológicas graves y de la muerte posnatal. Sin embargo, la pirimetamina ha demostrado ser teratógeno en animales, por lo que no debe administrarse antes de las 18 semanas de gestación. Mientras que la sulfadiazina puede causar fallo renal agudo reversible. Por tanto, debido a la potencial toxicidad de estos fármacos, su uso durante el embarazo debería Dra Félix / Dr Manzanares - 11 - Clases de Residentes 2015 Actualización Toxoplasmosis restringirse únicamente a aquellas gestantes con confirmación de infección fetal en el líquido amniótico. En la actualidad, no existe una fuerte evidencia sobre la eficacia de estos tratamientos; dado que faltan estudios prospectivos randomizados. Si bien es cierto que no hay estudios que lo desaconsejen. Y además existen diversos estudios de casos y controles junto con estudios observacionales multicéntricos que defienden que el tratamiento reduce las secuelas en los recién nacidos, sin poder demostrar una clara disminución de la transmisión materno fetal. Por todo esto, parece indicado iniciar el tratamiento; sabiendo que puede reducir el riesgo y la gravedad de las secuelas, pero sin eliminar el riesgo por completo. Tratamiento neonatal Aunque no existen estudios controlados que confirmen la eficacia y las pautas del tratamiento, si hay estudios de cohortes que sugieren que los niños tratados durante 12-24 meses tienen menos secuelas y menor riesgo de coriorretinitis. Por lo que se recomienda el tratamiento en los neonatos con toxoplamosis confirmada. El tratamiento de elección es la combinación de pirimetamina, sulfadiazina y ácido folínico durante 1 año. En caso de coriorretinitis activa del niño mayor se debe añadir prednisona. Mientras que en las lesiones retinianas periféricas sin signos inflamatorios diagnosticadas durante un examen casual de fondo de ojo se recomienda dar una pauta de tratamiento habitual sin corticoides durante 3 o 4 meses para evitar recidivas Durante el tratamiento se aconseja un seguimiento clínico muy estrecho, ajustando frecuentemente las dosis al peso corporal y realizando controles Dra Félix / Dr Manzanares - 12 - Clases de Residentes 2015 Actualización Toxoplasmosis analíticos seriados para detectar precozmente efectos secundarios de la medicación, especialmente la neutropenia. Este tratamiento consigue disminuir el riesgo y la severidad de las secuelas pero no las elimina; por lo que deben tener un seguimiento multidisciplinar hasta la edad adulta, prestando especial atención a la exploración oftalmológica y neurológica PREVENCIÓN PRIMARIA Mientras que el cribado de la toxoplasmosis ha sido muy debatido, no se ha puesto en duda la eficacia de las medidas de prevención primaria, que son fuertemente recomendadas. De esta manera se deben dar consejos profilácticos a toda mujer embarazada que presente una serología IgG negativa o desconocida en la primera visita del embarazo. Su objetivo es evitar la primoinfección durante el embarazo. - Consumir únicamente carne cocinada a más de 60-66 ◦C o carne congelada a -20ºC durante un período de tiempo no inferior a 24 horas. (el parásito se inactiva en estas condiciones). - No consumir embutido ni carnes curadas, si no ha sido congelado previamente. Pueden contener el parásito, especialmente si son caseros. - Pelar o lavar las frutas y las verduras que se coman crudas. - Usar guantes o lavarse las manos después de haber tocado carne cruda o verduras. - Evitar durante la manipulación de carne cruda el contacto de las manos con la mucosa de la boca y ojos. - Mantener perfectamente limpios los utensilios y superficies que se utilicen para preparar carne. - No consumir leche ni productos lácteos que no estén pasteurizados. - Evitar el contacto con gatos desconocidos. Si se posee gato, evitar la limpieza de sus heces, limpiar su caja diariamente para evitar que los ooquistes maduren, no alimentarlo con carne cruda, mantenerlo alejado de Dra Félix / Dr Manzanares - 13 - Clases de Residentes 2015 Actualización Toxoplasmosis la calle, manipular el animal con guantes y desinfección de sus utensilios con agua hirviendo. - Si se realizan labores de jardinería o similares, protegerse las manos con guantes. - No deben utilizarse como donantes de sangre u órganos para transplantes las personas que tienen títulos elevados de anticuerpos de antitoxoplásmicos. Toxoplasmosis y jamón serrano Actualmente, hay muchas embarazadas que reciben información contradictoria sobre si pueden comer o no jamón serrano durante la gestación. Como profesionales sanitarios, tenemos que mantenernos actualizados y ser capaces de dar una información veraz basada en la evidencia científica. A día de hoy, en las recomendaciones dietéticas durante la gestación, se sigue desaconsejando el consumo de embutidos y carnes curadas, siempre que no hayan sido previamente congelados durante al menos 24 horas. Sin embargo, estos rumores sobre la posibilidad de comer jamón en el embarazo, no están del todo infundados. En 2012, el Centro Tecnológico Andaluz del Sector Cárnico (TEICA) dio a conocer la existencia de su estudio sobre toxoplasma en el jamón curado y su posible consumo por las mujeres embarazadas. Los resultados preliminares parecían indicar que el tiempo de curación y el contenido de sal del jamón pueden hacer inviable al Toxoplasma. Ante las buenas previsiones, presentó un acuerdo con la SEGO para elaborar en un futuro un protocolo unificado sobre toxoplasma en las mujeres embarazadas. En 2013, en la página web del “Parto es nuestro” apareció la sensacional noticia de que las señoras embarazadas podían comer jamón serrano al no tratarse de carne cruda. Por ello recibieron múltiples críticas, dado que esta afirmación iba en contra de las recomendaciones oficiales y no se basaba en Dra Félix / Dr Manzanares - 14 - Clases de Residentes 2015 Actualización Toxoplasmosis estudios con suficiente evidencia científica. Finalmente se retractaron, mostrando una posición más moderada. PREVENCIÓN SECUNDARIA: SCREENING TOXOPLASMOSIS Pese a la controversia existente en los últimos años respecto al cribado universal de la toxoplasmosis durante la gestación, muchos países lo han aplicado hasta el momento. Sin embargo, la falta de consenso ha dado lugar a una gran variabilidad a la hora de aplicar el screening en los diferentes territorios, incluso dentro del mismo país. Por ello es necesario definir un protocolo de actuación homogéneo basado en la evidencia científica y valorar la necesidad real de cribado universal. Parece ser que el cribado prenatal de la toxoplasmosis no cumple con las expectativas; por lo que en las últimas recomendaciones, se ha desestimado su uso. En el Documento de Consenso de la SEGO del 2002, ya explicaban que no cumplía con todos los criterios de la OMS para su aplicación: 1. El proceso a diagnosticar tiene que constituir un problema sanitario: No cabe duda que la toxoplasmosis congénita puede llegar a ser una enfermedad muy grave, sin embargo se desconoce su prevalencia en España. 2. Debe conocerse correctamente la historia natural de la enfermedad: Se ignora la evolución a largo plazo de la enfermedad congénita subclínica, que es la forma que presentan la mayoría de los casos. 3. Debe existir un estadio precoz detectable: Existe, pero se ignora con qué periodicidad deben de realizarse las pruebas de cribado para detectarlo a tiempo. Dra Félix / Dr Manzanares - 15 - Clases de Residentes 2015 Actualización Toxoplasmosis 4. Tiene que existir una prueba de cribado eficaz de la enfermedad, aceptable para la población: Las pruebas son aceptables, pero la interpretación del resultado puede ser compleja. Además se ignora su sensibilidad y especificidad real. 5. Debe contarse con pruebas diagnósticas y tratamientos eficaces: Aunque sí contamos con una prueba diagnóstica como la PCR de líquido amniótico, no existe una fuerte evidencia científica de la eficacia de los tratamientos existentes. 6. El beneficio obtenido debe superar a los posibles daños que conlleve el cribado: Se ignoran los beneficios y los daños en España. 7. El programa de cribado ha de ser coste-efectivo: Se desconoce, ya que puede ser difícil de calcular. Posteriormente, la SEGO en sus Documentos de Consenso y Guías de Práctica Clínica comunica que el cribado prenatal de la toxoplasmosis congénita no se recomienda ante la falta de cumplimiento de los criterios propuestos por la OMS. (grado de evidencia IV-C) También, explican el manejo frente a la toxoplasmosis en la consulta prenatal; recomendando la promoción de medidas higiénicas y dietéticas durante el embarazo, sin recomendarse el cribado serológico. (grado de evidencia IV-C). En la guía NICE del 2008, también informan que el screening no debería ser ofrecido porque sus riesgos pueden ser mayores a sus potenciales beneficios. Ofreciendo a la embarazada únicamente medidas de prevención primaria. En el año 2014, se publicó la Guía del Ministerio de Sanidad donde se hace un repaso a la bibliografía más reciente. Destacan que la toxoplasmosis congénita sólo puede ser evitada mediante el consejo preconcepcional y el tratamiento precoz de la infección. Además hacen referencia a la disminución de la tasa de infección congénita de Francia desde la introducción del cribado; también Dra Félix / Dr Manzanares - 16 - Clases de Residentes 2015 Actualización Toxoplasmosis señalan un estudio económico de Estados Unidos donde el cribado universal podría ahorrar billones de dólares al año. Sin embargo concluyen que, por la baja prevalencia de la toxoplasmosis, la escasa eficacia de los tratamientos disponibles, la yatrogenia terapeútica y diagnóstica junto con la muy baja calidad de la evidencia, el grado de recomendación del cribado era débil. Recientemente, la Junta de Andalucía ha publicado la guía de práctica clínica “Embarazo, parto y puerperio” donde el cribado prenatal del toxoplasma no aparece entre las serologías a solicitar en la embarazada. Recomendando únicamente medidas higiénico-dietéticas. PREVENCIÓN TERCIARIA Actualmente, ante la controversia con el cribado prenatal de la toxoplasmosis, se está investigando la posibilidad de hacer un cribado postnatal sistemático. De tal manera que en la sangre seca de talón, junto con las pruebas metabólicas de los recién nacidos, se determine la IgM, IgG y la PCR para toxoplasma. Como inconvenientes, parece presentar baja sensibilidad comparado con otras técnicas y se desconoce si el retraso en el tratamiento puede afectar negativamente. Como ventajas, presenta mayor sencillez y una relación costebeneficio más adecuada. Nueva Inglaterra, Dinamarca o Polonia fueron los primeros en desarrollar esta posibilidad. Y hoy en día, es uno de los campos en investigación por parte de la SEGO. BIBLIOGRAFÍA 1. Baquero-Artigao F, del Castillo Martín F, et al. Guía de la Sociedad Española de Infectología Pediátrica para el diagnóstico y tratamiento de la toxoplasmosis congénita. An Pediatr (Barc). 2013; 79 (2): 116.e1116e16. Dra Félix / Dr Manzanares - 17 - Clases de Residentes 2015 Actualización Toxoplasmosis 2. Hospital Universitari Clinic. Barcelona. Protocolo: Infecciones TORCH y por parvovirus B19 en la gestación. Guías clínicas Medicina MaternoFetal. Disponible en: http://www.medicinafetalbarcelona.org/clinica/protocolos_es.html 3. Asociación Española de Pediatría. Protocolo: Infecciones congénitas. Hospital Universitari Clínic. Barcelona. 2008: 177-179. 4. Hospital Virgen de las Nieves. Granada. Protocolo: Toxoplasmosis congénita. Protocolos Obstetricia HVN. 5. Shahnaz Akhtar Chaudhry, Nanette Gad, Gideon Koren. Toxoplasmosis and pregnancy. Motherisk Update. Canadian Family Physician - Le Médecin de famille canadien. 2014; 60: 334-336. 6. McAuley James B. Congenital Toxoplasmosis. Journal of the Pediatric Infectious Diseases Society. 2014; 3.1: S30–S35. 7. Díaz-Plaza MI. Infección en el embarazo. En: Cañete Palomo ML. Urgencias en Ginecología y Obstetricia. 1ºed. Albacete. FISCAM; 2003; 301-303. 8. Red Nacional de Vigilancia Epidemiológica. Protocolo de Vigilancia y Alerta de Toxoplasmosis Congénita. 2013; 1-8. 9. Sociedad Española de Obstetricia y Ginecología. Toxoplasmosis. Documentos de Consenso de la SEGO. 2002; 154-172 10. Sociedad Española de Obstetricia y Ginecología. Fundamentos de Obstetricia. 2007; 68, 567- 572 11. Sociedad Española de Obstetricia y Ginecología. Diagnóstico Prenatal. Documentos de Consenso SEGO. 2009; 152. 12. Sociedad Española de Obstetricia y Ginecología. Consulta Ginecología. Consulta Preconcepcional. Medicina Perinatal. 2010; 1-9. 13. Sociedad Española de Obstetricia y Preconcepcional. Documentos de Consenso SEGO. 2011; 243-244. 14. NICE. National Institute for Health and Care Excellence. Antenatal Care. NICE Guidelines. 2008; 1.8.11.1- 1.8.11.2 Disponible en: http://www.nice.org.uk/guidance/cg62/chapter/guidance 15. Ministerio de Sanidad, Servicios Sociales e Igualdad. Guía de práctica clínica de atención en el embarazo y puerperio. Guías de práctica clínica en el SNS. 2014; 102-107. Disponible en: Dra Félix / Dr Manzanares - 18 - Clases de Residentes 2015 Actualización Toxoplasmosis http://www.msssi.gob.es/organizacion/sns/planCalidadSNS/0Guiaatemb arazo.htm 16. Junta de Andalucía. Consejería de Igualdad, Salud y Políticas Sociales. Embarazo, Parto y Puerperio. 2014; 21- 22. 17. TEICA. Centro Tecnológico del Cárnico. Huelva: diciembre 2012 (fecha de consulta 7-3-2015). Disponible en: http://www.teica.es/index.php/widgetkit/66-el-centro-tecnologico-andaluzdel-sector-carnico-y-la-sociedad-espanola-de-ginecologia-y-obstetriciasego-elaboraran-un-protocolo-unificado-sobre-toxoplasma-para-lasmujeres-embarazadas 18. El Parto es Nuestro. España: Patricia López Izquierdo; abril 2013 (fecha de consulta 7-3-2015). Disponible en: http://www.elpartoesnuestro.es/blog/2013/04/10/las-embarazadas-losgatos-y-el-jamon 19. El Parto es Nuestro. España: junio 2013 (fecha de consulta 7-3-2015). Disponible en: http://www.elpartoesnuestro.es/blog/2013/06/27/jamonen-el-embarazo-punto-y-seguido 20. La Razón. Madrid: Beatriz Muñoz; junio 2013 (fecha de consulta 7-32015). Disponible en: http://www.larazon.es/jamon-la-curacion-destruyela-toxoplasmosis-EL2519723#.Ttt1QDAiRRGBpIV 21. SEGO. Grupos de trabajo SEGO. Madrid: Nieves González; (fecha de consulta 7-3-2015). Disponible en: http://www.sego.es/organizacion/grupos?g=toxoplasmosis#content Dra Félix / Dr Manzanares - 19 -