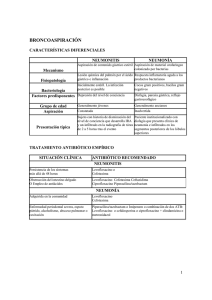
FICHA TÉCNICA LEVOFLOXACINO STADA 5 mg/ml SOLUCION
Anuncio

FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Levofloxacino STADA 5 mg/ml solución para perfusión frasco EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene 5 mg de levofloxacino (como hemidrato) Cada frasco de 100 ml contiene 500 mg de levofloxacino. Excipientes: 1 ml contiene 9 mg de cloruro de sodio Cada frasco de 100 ml contiene 900 mg de cloruro de sodio Ácido clorhídrico* Hidróxido sódico* *: Se añade ácido clorhídrico 1 N (ó hidróxido sódico 1 N) para ajustar el pH 3. FORMA FARMACÉUTICA Solución para perfusión. Levofloxacino STADA 5 mg/ml es una solución amarillo-verdosa. 4. DATOS CLÍNICOS 4.1. Indicaciones terapéuticas Levofloxacino STADA solución para perfusión está indicado, en adultos, para los cuales la terapia intravenosa se considera adecuada, para el tratamiento de las siguientes infecciones cuando son debidas a microorganismos sensibles al levofloxacino: Neumonía adquirida en la comunidad. Infecciones complicadas del tracto urinario incluyendo pielonefritis. Prostatitis bacteriana crónica. Infecciones de piel y tejidos blandos. Antes de recetar Levofloxacino STADA, deben tomarse en consideración las recomendaciones nacionales y/o locales sobre el uso adecuado de fluorquinolonas. 4.2. Posología y forma de administración Levofloxacino STADA solución para perfusión se administra mediante perfusión intravenosa lenta una o dos veces al día. La dosis depende del tipo y de la gravedad de la infección y de la sensibilidad del probable agente patógeno causal. Generalmente, y según el estado del paciente, se puede pasar del tratamiento intravenoso inicial a la vía oral después de pocos días. Duración del tratamiento La duración del tratamiento varía según la evolución de la enfermedad. Al igual que con otros antibióticos, la administración de Levofloxacino STADA solución para perfusión deberá continuarse durante un mínimo de 48 a 72 horas después de que el paciente permanezca sin fiebre o se haya demostrado la erradicación bacteriana. Forma de administración Levofloxacino STADA solución para perfusión sólo está indicado para perfusión intravenosa lenta; se administra una o dos veces al día. El tiempo de perfusión deberá ser como mínimo de 60 minutos (ver CORREO ELECTRÓNICO [email protected] Se atenderán exclusivamente incidencias informáticas sobre la aplicación CIMA (http://www.aemps.gob.es/cima) C/ CAMPEZO, 1 – EDIFICIO 8 28022 MADRID sección 4.4.). Dependiendo del estado del paciente, es posible pasar de una administración intravenosa inicial a la vía oral a la misma dosis después de algunos días. En cuanto a incompatibilidades, ver la sección 6.2, y en cuanto a la compatibilidad con otras soluciones de perfusión ver la sección 6.6. Las dosis recomendadas para Levofloxacino STADA son las siguientes: Dosis en los pacientes con la función renal normal (aclaramiento de creatinina > 50 ml/min) Indicación Neumonía adquirida en la comunidad Infecciones complicadas del tracto urinario incluyendo pielonefritis Prostatitis bacteriana crónica Infecciones de piel y tejidos blandos 1: Pauta posológica diaria (según gravedad) 500 mg una o dos veces al día 250 mg1 una vez al día 500 mg una vez al día 500 mg dos veces al día Debe tomarse en consideración el incremento de dosis en caso de infección grave. Dosis en pacientes con alteración de la función renal (aclaramiento de creatinina ≤ 50 ml/min) Aclaramiento de creatinina 50-20 ml/min 19-10 ml/min < 10 ml/min (incluyendo hemodiálisis y DPCA)1 1: Pauta posológica 250 mg/24 h 500 mg/24 h 500 mg/12 h Dosis inicial: 250 mg Dosis inicial: 500 mg Dosis inicial: 250 mg Después: 125 mg/24 h Después: 125 mg/48 h Después: 250 mg/24 h Después: 125 mg/24 h Después: 250 mg/12 h Después: 125 mg/12 h Después: 125 mg/48 h Después: 125 mg/24 h Después: 125 mg/24 h No se precisan dosis adicionales tras hemodiálisis o diálisis peritoneal continua ambulatoria (DPCA). Dosis en pacientes con alteración de la función hepática No es necesario ajustar la dosis, ya que el levofloxacino no se metaboliza principalmente en el hígado y se elimina fundamentalmente por vía renal. Dosis en ancianos No es necesario ajustar la dosis en ancianos, salvo en caso de alteración de la función renal. 4.3. Contraindicaciones Levofloxacino STADA solución para perfusión no deberá administrarse: A pacientes con hipersensibilidad a levofloxacino o cualquier otra quinolona. A pacientes con epilepsia. A pacientes con antecedentes de trastornos tendinosos relacionados con la administración de fluoroquinolonas. A niños o adolescentes en fase de crecimiento. Durante el embarazo. A las mujeres en periodo de lactancia. 4.4. Advertencias y precauciones especiales de empleo Levofloxacino STADA puede que no sea el tratamiento más adecuado en los casos más graves de la neumonía pneumocócica. MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Las infecciones nosocomiales debidas a P. aeruginosa pueden precisar tratamiento combinado. Tiempo de perfusión Debe respetarse el tiempo de perfusión recomendado de cómo mínimo 60 minutos. Es conocido para ofloxacino que durante la perfusión puede desarrollarse un descenso temporal de la presión sanguínea. En casos raros, puede producirse un colapso circulatorio como consecuencia de una caída profunda de la presión sanguínea. Si existe una caída remarcable en presión sanguínea durante la perfusión con levofloxacino (l-isómero de ofloxacino), la perfusión debe detenerse inmediatamente. Tendinitis y rotura de los tendones Raramente puede aparecer tendinitis, esto afecta generalmente al tendón de Aquiles, pudiendo llegar a producirse rotura del tendón. El riesgo de tendinitis y de rotura del tendón es mayor en pacientes ancianos y en pacientes que estén en tratamiento con corticosteroides. Debido a esto, estos pacientes deberán ser estrechamente monitorizados si se les prescribe Levofloxacino STADA. Se debe advertir a todos los pacientes que en caso de sentir dolor en los tendones deberán consultar inmediatamente con su médico. En caso de sospecha de tendinitis, deberá suspenderse inmediatamente el tratamiento con Levofloxacino STADA e iniciarse el tratamiento apropiado en el tendón afectado (p. ej., inmovilización). Enfermedad asociada a Clostridium difficile La aparición de diarrea durante o tras el tratamiento con Levofloxacino STADA solución para perfusión, en especial si es grave, persistente y/o sanguinolenta, podría ser síntoma de enfermedad asociada a Clostridium difficile, cuya forma más grave es la colitis pseudomembranosa. En caso de sospecha de colitis pseudomembranosa, deberá suspenderse inmediatamente la administración de Levofloxacino STADA solución para perfusión y los pacientes deberán tratarse inmediatamente con medidas de soporte y/o tratamiento específico (p. ej., vancomicina oral). En esta situación clínica se encuentran contraindicados los productos que inhiben el peristaltismo. Pacientes con predisposición a la presentación de convulsiones Levofloxacino STADA solución para perfusión está contraindicado en pacientes con antecedentes de epilepsia y, al igual que con otras quinolonas, deberá utilizarse con extrema precaución en los pacientes predispuestos a presentar convulsiones, como pacientes con lesiones del sistema nervioso central preexistentes, en tratamiento concomitante con fenbufen y fármacos antiinflamatorios no esteroideos similares o con fármacos que disminuyen el umbral convulsivo, como la teofilina (ver sección 4.5.). Pacientes con deficiencia en la G-6-fosfato deshidrogenada Los pacientes con defectos latentes o manifiestos en la actividad de la glucosa-6-fosfato deshidrogenada pueden tener una mayor tendencia a presentar reacciones hemolíticas cuando son tratados con agentes antibacterianos quinolónicos, y, por lo tanto, levofloxacino debe ser usado con precaución en estos pacientes. Pacientes con alteración renal La dosis de Levofloxacino STADA deberá ajustarse en pacientes con alteración renal, dado que levofloxacino se elimina fundamentalmente por vía renal. Prevención de la fotosensibilización Aunque la fotosensibilización es muy rara con levofloxacino, se recomienda que los pacientes no se expongan innecesariamente a la luz solar potente o a los rayos UV artificiales (p. ej., lámparas solares, solarium), a fin de prevenir la fotosensibilización. Pacientes tratados con antagonistas de la Vitamina K MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios El uso de Levofloxacino STADA en combinación con antagonistas de la vitamina K (p. ej., warfarina) puede dar lugar a un incremento en las pruebas de la coagulación (PT/INR) y/o hemorragia, motivo por el que en estos pacientes se debe controlar las pruebas de la coagulación (ver sección 4.5). Advertencias sobre excipientes Levofloxacino STADA 5 mg/ml solución para perfusión frasco contiene 354 mg (15,4 mmol) de sodio por frasco, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio. 4.5. Interacción con otros medicamentos y otras formas de interacción Teofilina, fenbufen o fármacos antiinflamatorios no esteroideos similares En un ensayo clínico no se hallaron interacciones farmacocinéticas entre levofloxacino y teofilina. Sin embargo, puede producirse una marcada disminución del umbral convulsivo en la administración concomitante de quinolonas con teofilina, fármacos antiinflamatorios no esteroideos, u otros agentes que disminuyen dicho umbral. Las concentraciones de levofloxacino fueron aproximadamente un 13% más elevadas en presencia de fenbufen que cuando se administró sólo levofloxacino. Probenecid y cimetidina Probenecid y cimetidina tienen un efecto estadísticamente significativo en la eliminación de levofloxacino. El aclaramiento renal de levofloxacino se vio reducido por cimetidina (24%) y probenecid (34%). Esto se debe a que ambas sustancias pueden bloquear la secreción tubular renal de levofloxacino. De todas maneras, en las dosis utilizadas en el estudio, las diferencias estadísticamente significativas observadas en la farmacocinética probablemente no tienen relevancia clínica. Se debe tener precaución al administrar levofloxacino conjuntamente con fármacos que afectan la secreción tubular renal como probenecid y cimetidina, especialmente en pacientes con alteración de la función renal. Ciclosporina La vida media de ciclosporina se incrementó en un 33%, cuando se administró conjuntamente con levofloxacino. Antagonistas de la vitamina K Se han notificado incrementos en las pruebas de la coagulación (PT/INR) y/o de la hemorragia que pueden ser graves, en pacientes tratados con levofloxacino en combinación con un antagonista de la vitamina K (p. ej., warfarina). Por lo tanto las pruebas de la coagulación deberían controlarse en aquellos pacientes que estén en tratamiento con antagonistas de la vitamina K. Otra información relevante Se han llevado a cabo estudios de farmacología clínica para investigar las posibles interacciones farmacocinéticas entre levofloxacino y otros fármacos prescritos habitualmente. La farmacocinética de levofloxacino no se altera de forma clínicamente relevante cuando se administra el producto junto con los siguientes fármacos: carbonato cálcico, digoxina, glibenclamida, ranitidina y warfarina. 4.6. Embarazo y lactancia Embarazo Los estudios de reproducción en animales no pusieron de manifiesto datos significativos de toxicidad. De todas maneras, dada la ausencia de datos en humanos, Levofloxacino STADA no deberá utilizarse en mujeres embarazadas, debido al riesgo experimental de lesión por fluoroquinolonas de los cartílagos que soportan peso de los organismos en crecimiento. Lactancia MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Dada la ausencia de datos en humanos, Levofloxacino STADA no deberá utilizarse en mujeres en periodo de lactancia, debido al riesgo experimental de lesión por fluoroquinolonas sobre los cartílagos que soportan el peso de los organismos en crecimiento. 4.7. Efectos sobre la capacidad para conducir y utilizar máquinas Algunas reacciones adversas (p. ej., mareo/vértigo, somnolencia, alteraciones visuales) pueden afectar a la capacidad de los pacientes para concentrarse y reaccionar y, por tanto, constituir un riesgo en aquellas situaciones en las que estas capacidades sean especialmente importantes (p. ej., al conducir un vehículo o utilizar maquinaria). 4.8. Reacciones adversas La información que se presenta a continuación se basa en los datos de estudios clínicos en más de 5.000 pacientes y en la amplia experiencia post-comercialización. Se ha utilizado la siguiente escala de frecuencia: Muy frecuentes ( 1/10); frecuentes ( 1/100, < 1/10); poco frecuentes ( 1/1.000, < 1/100); raras ( 1/10.000, < 1/1.000); muy raras (< 1/10.000), y casos aislados. Reacciones de hipersensibilidad: Poco frecuentes: prurito, rash. Raras: urticaria, broncospasmo/disnea. Muy raras: angioedema, hipotensión, shock de tipo anafiláctico; fotosensibilización. Casos aislados: erupciones bullosas graves, como síndrome de Steven Johnson, necrolisis epidérmica tóxica (síndrome de Lyell) y eritema exudativo multiforme. Las reacciones muco-cutáneas, anafilácticas/anafilactoides en ocasiones pueden producirse incluso tras la primera dosis. Trastornos gastrointestinales y metabólicos: Frecuentes: náuseas, diarrea. Poco frecuentes: anorexia, vómitos, dolor abdominal, dispepsia. Raras: diarrea sanguinolenta, que, en casos muy raros, puede ser indicativa de enterocolitis, incluida colitis pseudomembranosa. Muy raras: hipoglucemia, particularmente en pacientes diabéticos. Trastornos neurológicos: Poco frecuentes: cefalea, mareos/vértigo, somnolencia, insomnio. Raras: parestesias, temblor, confusión, convulsiones. Muy raras: hipoestesias, trastornos visuales y auditivos, trastornos del gusto y del olfato. Trastornos psiquiátricos: Raras: ansiedad, depresión, reacciones psicóticas, agitación Muy raras: alucinaciones, reacciones psicóticas con comportamiento autolesivo, incluyendo ideas suicidas o intentos de suicidio (ver sección 4.4) Trastornos cardiovasculares: Raras: taquicardia, hipotensión. Muy raras: shock (de tipo anafiláctico). Casos aislados: prolongación del intervalo QT (ver sección 4.9.). Trastornos músculo esqueléticos: Raras: artralgias, mialgias, trastornos tendinosos incluida tendinitis (p. ej., del tendón de Aquiles) (ver sección 4.4.). MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Muy raras: ruptura tendinosa (p. ej., del tendón de Aquiles); esta reacción adversa puede producirse dentro de las 48 horas del comienzo del tratamiento y puede ser bilateral (ver sección 4.4.). Debilidad muscular, que puede ser especialmente importante en pacientes con miastenia grave. Casos aislados: rabdomiolisis. Trastornos hepáticos y renales: Frecuentes: elevación de enzimas hepáticas (p. ej., ALT/AST). Poco frecuentes: aumento de la bilirrubina, elevación de creatinina sérica. Muy raras: reacciones hepáticas, como hepatitis; insuficiencia renal aguda (p. ej. debido a nefritis intersticial). Alteraciones de la sangre: Poco frecuentes: eosinofilia, leucopenia. Raras: neutropenia, trombocitopenia. Muy raras: agranulocitosis. Casos aislados: anemia hemolítica, pancitopenia. Otros: Frecuentes: dolor, enrojecimiento del punto de perfusión y flebitis. Poco frecuentes: astenia, crecimiento fúngico y proliferación de otros microorganismos resistentes. Muy raras: neumonitis alérgica, fiebre. Otras reacciones adversas que han sido asociadas con la administración de fluoroquinolonas incluyen: Síntomas extrapiramidales y otros trastornos de la coordinación muscular. Vasculitis por hipersensibilidad. Ataques de porfiria en pacientes con porfiria. 4.9. Sobredosis De acuerdo con los estudios de toxicidad animal o con los estudios de farmacología clínica llevados a cabo con dosis supra-terapéuticas, los signos más importantes que cabe esperar tras una sobredosis aguda de Levofloxacino STADA son síntomas del sistema nervioso central, tales como confusión, mareo, alteración de la consciencia y crisis convulsivas, así como aumentos del intervalo QT. En caso de que se produjera una sobredosificación, deberá instituirse tratamiento sintomático. Debe llevarse a cabo monitorización ECG, por la posibilidad de prolongación del intervalo QT. La hemodiálisis, incluyendo diálisis peritoneal y DPCA no son efectivas para eliminar el levofloxacino. No existe un antídoto específico. 5. PROPIEDADES FARMACOLÓGICAS 5.1. Propiedades farmacodinámicas Levofloxacino es un agente antibacteriano sintético de la familia de las fluoroquinolonas Código ATC: J01MA Levofloxacino es el enantiómero S (-) de la sustancia racemica ofloxacino. Mecanismo de acción Como agente antibacteriano fluoroquinolónico, levofloxacino actúa sobre el complejo ADN-ADN girasa y sobre la topoisomerasa IV. Puntos de corte de la sensibilidad MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Los Estándares de Laboratorio Clínico del Comité Nacional de EEUU (ELCCN) preliminares recomendaron unos puntos de corte de CMI para levofloxacino, separando los organismos sensibles de los de sensibilidad intermedia y estos últimos de los resistentes: Sensibles ≤ 2 mg/l. Resistentes ≥ 8 mg/l. Espectro antibacteriano La prevalencia de resistencias para las especies determinadas puede variar geográficamente y con el tiempo, y es preferible la información local sobre resistencias, particularmente en el tratamiento de infecciones graves. Por lo tanto, la información presentada proporciona sólo una orientación aproximada de la probabilidad de que los microorganismos sean sensibles o no a levofloxacino. A continuación se detallan sólo los microorganismos relevantes en las indicaciones clínicas. Espectro antibacteriano in vitro – Categoría con el intervalo europeo de resistencia dentro del cual se sabe que varía Sensibles Microorganismos Aerobios Gram-positivos: Enterococcus faecalis1 10-35% Staphylococcus aureus 1 meti-S 0-30% Staphylococcus coagulasa negativo meti-S y meti-R Staphylococcus saprophyticus Microorganismos aerobios Gram-negativos: 40% Acinetobacter baumannii 1 Citrobacter freundii 1 7% Eikenella corrodens 30% Enterobacter aerogenes Enterobacter agglomerans Enterobacter cloacae 1 7% Escherichia coli 1 0-20%2 1 Haemophilus influenzae ampi-S/R Haemophilus para-influenzae 1 Klebsiella oxytoca Microorganismos anaerobios: Bacteroides fragilis Clostridium perfringens Otros microorganismos: Chlamydia pneumoniae 1 Chlamydia psittaci Chlamydia trachomatis Sensibilidad intermedia Microorganismos aerobios Gram-positivos: Microorganismos anaerobios: Bacteroides ovatus Bacteroides thetaiotamicron Resistentes Streptococci, group C and G Streptococcus agalactiae Streptococcus pneumoniae 1 peniI/S/R Streptococcus pyogenes 1 Klebsiella pneumoniae 1 Moraxella catarrhalis 1 + / Morganella morganii 1 Pasteurella multocida Proteus mirabilis 1 Proteus vulgaris Providencia rettgeri Providencia stuartii Pseudomonas aeruginosa 1 Serratia marcescens 1 <5-10% 5% 0-15% 35% 10-50% 7% Peptostreptococcus Legionella pneumophila 1 Mycoplasma pneumoniae 1 Mycoplasma hominis Ureaplasma urealyticum Microorganismos aerobios Gram-negativos: Burkholderia cepacia Bacteroides vulgatus Clostridium difficile MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Microorganismos aerobios Gram-positivos: Staphylococcus aureus meti-R 1 2 Staphylococcus coagulase negative metiR La eficacia clínica se ha demostrado en ensayos clínicos (20% en España y Portugal) Otra información El principal mecanismo de resistencia es debido a una mutación de gyr-A. Existe una resistencia cruzada in vitro entre levofloxacino y otras fluoroquinolonas. Recientemente en 1997 se ha documentado resistencia adquirida a levofloxacino: S. pneumoniae: Francia ≤ 1%. H. influenzae: rara Debido al mecanismo de acción, generalmente no hay resistencia cruzada entre levofloxacino y otras familias de agentes antibacterianos. Las infecciones nosocomiales debidas a Pseudomonas aeruginosa pueden requerir tratamiento combinado. 5.2. Propiedades farmacocinéticas Absorción Levofloxacino se absorbe rápida y casi completamente tras su administración oral, alcanzándose la concentración plasmática máxima en el plazo de 1 hora. La biodisponibilidad absoluta es de aproximadamente el 100%. Levofloxacino sigue una farmacocinética lineal en el rango de 50 a 600 mg. Los alimentos afectan poco a la absorción de levofloxacino. Distribución Aproximadamente el 30-40% de levofloxacino está unido a proteínas séricas. El tratamiento repetido con 500 mg una vez al día mostró una acumulación insignificante del fármaco. Tras dosis de 500 mg dos veces al día se produce una acumulación modesta pero predecible de levofloxacino. El estado de equilibrio se alcanza en el plazo de 3 días. Penetración en tejidos y líquidos orgánicos: Penetración en mucosa bronquial, fluido del revestimiento epitelial (FRE) Las concentraciones máximas de levofloxacino en la mucosa bronquial y el fluido del revestimiento epitelial tras la administración oral de 500 mg fueron 8,3 microgramos/g y 10,8 microgramos/ml respectivamente. Estas concentraciones se alcanzaron aproximadamente una hora después de la administración. Penetración en tejido pulmonar Las concentraciones máximas de levofloxacino en el tejido pulmonar tras la administración oral de 500 mg fueron aproximadamente 11,3 microgramos/g y se alcanzaron 4 y 6 horas después de la administración. La concentración en los pulmones fue consistentemente superior a la plasmática. Penetración en el líquido de vesículas cutáneas Tras 3 días de tratamiento con 500 mg una o dos veces al día, las concentraciones máximas de levofloxacino en el líquido de vesículas cutáneas fueron, aproximadamente, de 4,0 y 6,7 microgramos/ml y se alcanzaron a las 2-4 horas de la administración. MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Penetración en el líquido cefalorraquídeo Levofloxacino presenta una penetración baja en el líquido cefalorraquideo. Penetración en el tejido prostático Tras la administración oral de 500 mg de levofloxacino una vez al día durante 3 días, las concentraciones medias en tejido prostático fueron 8,7 microgramos/g, 8,2 microgramos/g y 2,0 microgramos/g a las 2 horas, 6 horas y 24 horas, respectivamente; la relación entre concentración media próstata/plasma fue 1,84. Concentración en orina Tras la administración de una dosis oral única de 150 mg, 300 mg o 500 mg de levofloxacino, la concentración media en orina alcanzó 44 mg/l, 91 mg/l y 200 mg/l, respectivamente a las 8-12 horas de la administración. Metabolismo Levofloxacino se metaboliza muy poco, siendo sus metabolitos el desmetil-levofloxacino y el N-óxido de levofloxacino. Estos metabolitos suponen menos del 5% de la dosis eliminada por orina. Levofloxacino es estereoquímicamente estable y no sufre inversión quiral. Eliminación Levofloxacino se elimina del plasma de manera relativamente lenta (t1/2: 6-8 h), tras la administración oral e intravenosa. Su eliminación tiene lugar fundamentalmente por vía renal (>85% de la dosis administrada). No existen diferencias importantes en la farmacocinética del levofloxacino ya sea su administración intravenosa u oral, lo que sugiere que las vías oral e intravenosa son intercambiables. Pacientes con insuficiencia renal La insuficiencia renal influye sobre la farmacocinética de levofloxacino. Con la disminución de la función renal, disminuyen la eliminación y aclaramiento renales, y aumentan las semividas de eliminación, según la siguiente tabla: Clcr (ml/min) ClR (ml/min) t1/2 (h) < 20 13 35 20-40 26 27 50-80 57 9 Pacientes ancianos No existen diferencias significativas en la cinética de levofloxacino entre los sujetos jóvenes y ancianos, excepto las asociadas a las diferencias en el aclaramiento de creatinina. Diferencias por sexo El análisis separado de hombres y mujeres muestra que existen diferencias mínimas o insignificantes en la farmacocinética de levofloxacino entre los dos sexos no hay evidencia de que estas diferencias entre sexos sean de relevancia clínica. 5.3. Datos preclínicos sobre seguridad Toxicidad aguda Los valores medios de la dosis letal 50 (DL50) obtenidos en ratones y ratas tras la administración intravenosa de levofloxacino se situaron en el rango de los 250-400 mg/kg, en perros la DL50 era aproximadamente 200 mg/kg. Uno de los dos animales que recibieron esta dosis murió. MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Toxicidad tras administración repetida Se han realizado estudios de un mes de duración administrando levofloxacino por vía intravenosa en ratas (20, 60, 180 mg/kg/día) y monos (10, 25, 63 mg/kg/día) así como también un estudio de tres meses en ratas (10, 30, 90 mg/kg/día). Los “Niveles Sin Observación de Efectos Adversos” (NSOEA) en rata tuvieron unos valores de 20 y 30 mg/kg/día en los estudios de 1 mes y 3 meses, respectivamente. Se observaron depósitos de cristales en orina en ambos estudios a dosis de 20 mg/kg/día y superiores. Las dosis altas (180 mg/kg/día durante 1 mes o 30 mg/kg/día y superiores durante 3 meses) disminuyeron ligeramente el consumo de alimentos y el aumento de peso corporal. El examen hematológico mostró reducción de eritrocitos y aumento de leucocitos y reticulocitos al final del estudio de 1 mes, pero no del estudio de 3 meses. El NSOEA en el estudio en mono fue de 63 mg/kg/día con sólo una pequeña reducción en el consumo de alimentos y agua a esta dosis. Toxicidad sobre la reproducción Levofloxacino no afectó a la fertilidad o la capacidad reproductora en ratas a dosis de hasta 360 mg/kg/día por vía oral o de hasta 100 mg/kg/día por vía intravenosa. Levofloxacino no fue teratogénico en ratas a dosis de hasta 810 mg/kg/día por vía oral o a dosis de hasta 160 mg/kg/día por vía intravenosa. No se observó teratogenia en conejos tratados a dosis de hasta 50 mg/kg/día por vía oral o dosis de hasta 25 mg/kg/día por vía intravenosa. Levofloxacino careció de efectos sobre la fertilidad y su único efecto sobre el feto fue un retraso de su maduración como resultado de la toxicidad del producto sobre las madres. Genotoxicidad Levofloxacino no indujo mutaciones genéticas en células bacterianas o de mamífero, pero indujo aberraciones cromosómicas in vitro en células pulmonares de hámster chino a concentraciones iguales o superiores a 100 microgramos/ml, en ausencia de activación metabólica. Los ensayos in vivo (tests del micronúcleo, de intercambio de cromátides hermanas, de síntesis de ADN no programada, y letal dominante) no mostraron ningún tipo de potencial genotóxico. Potencial fototóxico Estudios en ratón tras administración oral e intravenosa mostraron que levofloxacino tiene actividad fototóxica sólo a dosis muy elevadas. Levofloxacino no mostró ningún potencial genotóxico en un ensayo de fotomutagenicidad y redujo el desarrollo de tumores en un estudio de fotocarcinogénesis. Potencial carcinogénico En un estudio de dos años de duración en la rata en el que se coadministraron diferentes dosis de levofloxacino (0, 10, 30 y 100 mg/kg/día) con los alimentos, no se observaron signos de potencial carcinogénico. Toxicidad articular Al igual que con otras fluoroquinolonas, levofloxacino mostró efectos sobre los cartílagos (desarrollo de vesículas y cavidades) en la rata y el perro. Estos hallazgos fueron más marcados en los animales jóvenes. 6. DATOS FARMACÉUTICOS 6.1. Lista de excipientes Cloruro de sodio, Ácido clorhídrico ó hidróxido sódico (para ajuste del pH) MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios Agua para inyección. 6.2. Incompatibilidades Levofloxacino STADA 5 mg/ml solución para perfusión frasco no debe mezclarse con heparina o soluciones alcalinas (p. ej., bicarbonato sódico). 6.3. Periodo de validez Periodo de validez en su acondicionamiento comercial: 2 años. Periodo de validez tras su extracción del acondicionamiento exterior: 3 días (bajo condiciones de luz interior). Periodo de validez tras la perforación del tapón de goma: ver sección 6.6. 6.4. Precauciones especiales de conservación Mantenga este medicamento dentro de su estuche exterior para protegerlo de la luz. 6.5. Naturaleza y contenido del envase Levofloxacino STADA 5 mg/ml solución para perfusión frasco se presenta en envases de 1 y 20 (Envase Clínico) frascos infusores de vidrio transparente tipo II con tapón de bromobutilo, de 100 ml, conteniendo 5 mg/ml de levofloxacino. 6.6 Precauciones especiales de eliminación y otras manipulaciones Levofloxacino STADA 5 mg/ml solución para perfusión frasco debe utilizarse inmediatamente (en el plazo de 3 horas) tras la perforación de su tapón de goma, a fin de impedir una eventual contaminación bacteriana. Durante la perfusión no se precisa protección frente a la luz. Mezcla con otras soluciones para perfusión: Levofloxacino STADA 5 mg/ml solución para perfusión frasco es compatible con las siguientes soluciones para perfusión: Solución de cloruro sódico al 0,9%, USP. Glucosa al 5%, USP. Glucosa al 2,5% en solución de Ringer. Soluciones de combinación para nutrición parenteral (aminoácidos, hidratos de carbono, electrolitos). Para las incompatibilidades, ver sección 6.2. Revise el frasco antes de usarlo. Sólo debe usarse si la solución es transparente, de color amarillo verdoso. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con las normativas locales. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Laboratorio STADA, S.L. Frederic Mompou, 5 08960 Sant Just Desvern (Barcelona) 8. NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN 69206 MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios 9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN Noviembre de 2007 10. FECHA DE LA REVISIÓN DEL TEXTO MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD Agencia española de medicamentos y productos sanitarios