09 Guía y TP 09 Lípidos
Anuncio

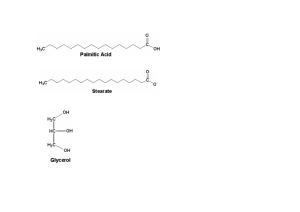
Trabajo Práctico N° 9 LIPIDOS Este grupo de sustancias naturales desde le punto de vista de su estructura química , es muy heterogéneo (esteres , amidas, alcoholes cíclicos superiores, libres o esterificados, vitaminas liposolubles de estructura terpénica o de estructura esteroidea); las sustancias que lo constituyen, tienen en común su alta solubilidad en solventes orgánicos y su escasa o nula solubilidad en agua. De esta manera pueden ser extraídos a partir de los materiales naturales en que se encuentran (tejidos vegetales o animales), por medio de solventes orgánicos, por ejemplo eter, cloroformo, eter de petróleo, etc. LIPIDOS HIDROLIZABLES SIMPLES: Son esteres de ácidos grasos superiores con distintos alcoholes. Son Lipidos neutros Los Acidos grasos esterificados pueden ser: Saturados No Saturados o Insaturados Otros (ramificados, hidroxilados, con enlace triple, cíclicos) El pKa es de 4,5 ; entonces a pH fisiológico se encuentran en forma anionica. Los ácidos grasos saturados son monocarboxilicos de cadena lineal, generalmente de numero par de atomos de carbono, mayor que 10. 12 át. de C: CH3-(CH2)10-COOH 14 át. de C: CH3-(CH2)12-COOH 16 át. de C: CH3-(CH2)14-COOH 18 át. de C: CH3-(CH2)16-COOH 20 át. de C: CH3-(CH2)18-COOH Ac. Laúrico o ácido dodecanoico Ac. Mirístico o ác. tetradecanoico (presente en el aceite de coco) Ac. Palmítico o ác. hexacanoico (presente en casi todas las grasas) Ac. Esteárico o ác. octadecanoico (presente en el sebo vacuno) Ac. Araquidico o ác. icosanoico Es excepción el: Acido Butirico de 4 át. de C; presente en la manteca Los ácidos grasos insaturados tienen uno (monoinsaturados) o mas dobles enlaces(poliinsaturados). Para indicar , en sus nombres, la ubicación del doble enlace, se recurre a la letra griega delta (∆) 16 át. de C: CH3-(CH2)5-CH=CH-(CH2)7-COOH: Ac. Palmitoleico o Ac. cis ∆9hexadecenoico 18 át. de C: CH3-(CH2)7-CH=CH-(CH2)7-COOH: Ac. Oleico o Ac. ∆ 9 octadecenoico 18 át. de C: CH3-(CH2)4-CH=CH-CH2-CH=CH (CH2)7-COOH: Ac. Linoleico o Ac. ∆ 9,12 octadecadienoico Ac. Linolenico o Ac. ∆ 9,12,15 octadecatrienoico 18 át. de C: CH3-CH2-(CH=CH-CH2)3-(CH2)6-COOH: Ac Araquidonico o Ac ∆ 5,8,11,14 eicosatetranoico 20 át. de C: CH3-(CH2)4-(CH=CH-CH2)4-(CH2)2-COOH: o 16:1 o 18:1 o 18:2 o 18:3 o 20:4 La configuración de los ácidos grasos insaturados (naturales) es cis. En general al aumentar el numero de carbonos en la cadena carbonada, aumenta el punto de fusión. Los ácidos grasos insaturados tienen punto de fusión bastante mas bajos que los saturados (Ej.:ác Estearico – PF:70C- es sólido a ToAmb. y el ac. Linoleico –PF:13C- es liquido a To Amb.) En general al aumentar el numero de dobles enlaces cadena carbonada, disminuye el punto de fusión. Estas ultimas dos propiedades se deben a que la presencia de dobles enlaces cis, impide la rotación de los enlaces, y produce como una vuelta ,esta evita la formación de un empaquetamiento apretado, bien ordenado, de los cristales y por consiguiente O C C C C disminuyen las interacciones (de tipo débil) C α C γ C C C entre las cadenas hidrocarbonadas β O C Nuestro organismo necesita algunos ácidos C insaturados; los ácidos grasos esenciales –AGE-(esencial ω Ac. Linolénico nos indica que se trata de nutrientes que nuestro cuerpo no C C CH3 C puede sintetizar y por ende deben procurarse a través de los C C C alimentos). AGE como el ácido linoleico están presentes en el aceite de oliva, de maíz, de girasol, el pan integral y las legumbres. Mientras que el ácido linolénico está en las hortalizas, el pescado y al aceite de linaza. El C adyacente al carbono carboxilico (C-2 en IUPAC) se designa como α, y a los otros se le asignan letras griegas en oden alfabetico: β,γ,δ,etc. Al C mas alejado del carbono carboxilico, se le asigna la letra ω cualquiera sea la longitud de la cadena. Así, los ácidos grasos poliinsaturados de cadena larga , omega 3 y omega 6 significan que las insaturaciones comienzan 3 (ó 6) carbonos después del ultimo carbono ().Los precursores de la serie ω3 y de la serie ω6 son el ácido α-linolénico (18:3ω3) y el ácido linoleico (18:2ω6), respectivamente. Es esencial el ácido docosahexanoico (22:6ω3, DHA) , ácido eicosapentanoico (20:5ω3, EPA) y el ácido araquidónico (20:4ω6, AA). Estos dos últimos son necesarios para la síntesis de los Eicosanoides (lípidos de 20 C, no hidrolizables). 1 Gliceridos Son esteres , formados entre glicerol (glicerina) y ácidos grasos. Según se hallen esterificados los tres, dos o uno de los hidroxilos del glicerol: se habla de trigliceridos, digliceridos o monogliceridos respectivamente. α CH2-OH Los atomos de la molecula de glicerol se designan: β CH-OH α CH2-OH O Asi O CH2O C R CH OH CH2OH CH O CH2O O C CH2OH CH2OH α-monoglicérido β-monoglicérido CH OH R CH2O C R O C R α,α '-diglicérido CH O O C R O O C R CH2 OH CH2 α,β-diglicérido Triglicerido: Si R’= R’’= R’’’, se trata de un homoglicerido, y se nombra, por ejemplo (si el ácido fuere el palmitico) tripalmitato de glicerilo o palmitina. CH 2 O C R' Si algun acido fuera diferente a los otros dos, o si fueran los tres distintos, se nombra como un heteroglicerido; por ejemplo:estearato oleato palmitato de CH O C R'' glicerilo. O Otros homotrigliceridos: butirina, estearina, oleína. CH 2 O C R''' Cuando en el triglicerido predominan los ácidos grasos saturados, la sustancia es O solida a 20oC y recibe el nombre de grasa. Cuando en el triglicerido predominan los ácidos grasos insaturados, la sustancia es liquida a dicha temperatura y constituye un aceite. Las grasas y los aceites naturales son, casi invariablemente, mezclas de composición variable de trigliceridos; contienen además pequeñas cantidades de ácidos grasos libres y una fracción llamada insaponificable, constituida por hidrocarburos y alcoholes superiores, esteroles, etc. Los trigliceridos, son la forma natural de almacenar los ácidos grasos, los cuales son moléculas combustibles muy importantes durante el metabolismo.(su oxidación produce mas energía -Calorías- que los carbohidratos o las proteínas). O O Ceras Son esteres de ácidos grasas superiores, con monoalcoholes alifáticos superiores. Los ácidos grasos que suelen constituirlas son: C15H31-COOH ác. palmítico C17H35-COOH ác. esteárico C23H47-COOH ác. lignocérico C25H51-COOH ác. cerótico C29H59-COOH ác. melístico Los alcoholes superiores mas importantes, que constituyen las ceras al estado libre, son: C16H33-OH alcohol cetílico (1-hexadecanol) C26H53-OH alcohol cerílico (1-hexaicosanol) C30H61-OH alcohol mirícico (1-triacontanol) Las ceras son sólidas a 37oC y funden a temperaturas menores que 100oC. Son solubles en solventes orgánicos e insolubles en agua. No se enrancian ( no contienen insaturaciones susceptibles a oxidación, como si ocurre en los ácidos grasos) Ceras animales: Blanco de Ballena o espermaceti : principalmente palmitato de cetilo. Cera de Abejas: principalmente palmitato de miricilo Ceras vegetales: Cera de Carnauba: principalmente ceroato de miricilo. Forman recubrimientos en hojas y frutos de vegetales superiores, evitando la deshidratación y protegiéndolos del agua. También forman recubrimientos a prueba de agua en pieles, plumas y exoesqueleto de animales O palmitato de miricilo: CH3-(CH2)14-C-O-(CH2)29-CH3 2 C palmitato de micirilo O LÍPIDOS HIDROLIZABLES COMPUESTOS: + NH3 Son Lípidos Polares Fosfogligéridos o Glicerofosfatidos Pueden ser nitrogenados o no nitrogenados. Todos contienen, como una O porción de su estructura, el éster fosfórico O P O de glicerol (fosfato de glicerilo o glicerolO 3-fosfato) H2C H C CH2 Cuando el glicerol 3-fosfato se esterifica con acidos grasos, forma un acido OH OH fostatidico (según el acido graso con el que Glicerol 3-fosfato este esterificado). Los fosfogliceridos se forman cuando el fosfato del ácido fosfatídico se esterifica a otro alcohol; según el alcohol que se une da origen a las distintas familias de glicerofosfolipidos. Las mas comunes son fosfatidiletanolaminas o cefalinas (se unen con una etanolamina); fosfatidilserinas (se unen con una serina) y las fosfatidilcolinas o lecitinas (se unen con una colina). Son compuestos que poseen una cabeza polar ( hidrofílica) y una cola hidrocarbonada no polar (hidrofóbica), estas sustancias se llaman anfipáticas y forman bicapas lipídicas, los cuales son componentes de las membranas biológicas. Los lípidos mas abundantes en las membranas son los fosfoglicéridos. CH2 etanolamina CH2 - O O O- P O- O O HC O O H2 C CH2 O un fosfatido (del ac. fosfatidico) O O O H2 C P HC O O CH2 O O una fosfatidiletanolamina (o una cefalina) Esfingolipidos Tambien se unen a acidos grasos pero el CH3 alcohol esqueleto es la esfingosina (un + CH3 N CH3 aminodiol insaturado de 18 C) CH colina CH2 OH NH Una ceramida, consiste en un 2 CH acido graso unido al grupo amino del CCH2OH CH2 2 mediante union amida. galactosa OH O Las tres familias principales de O OH esfingolipidos son: O P O O Esfingolmielinas : contienen un grupo OH O fosfato, por lo tanto se clasifican entre esfingosina H2C HC C H 2 H2 C HC CH2 los fosfolípidos. CH Son diesteres fosforicos, un ester NH NH CH fosforico al C-1 de la ceramida y otro CH CH O O ester fosfórico a la colina. Se hallan en las membranas plasmáticas animales y ceramida ceramida vegetales. En animales son componente principal de las vainas de mielina que rodean las neuronas Cerebrosidos y Gangliosidos: contienen residuos carbohidratos , entonces se clasifican como Glucolipidos Los cerebrosidos tienen residuo monosacarido unido con enlace β-glucosidico al C-1 de la ceramida. Tambien son abundantes en tejido nervioso y forman parte Una esfingomielina Un cerebrosido de las vainas de mielina. Los gangliosidos son mas complejos , tienen unido un oligosacarido (union de varios monosacaridos) que contiene un amino azucar acido.Son anionicos debido al grupo carboxilo del amino azucar. Tambien forman parte de membranas plasmaticas , quedando el oligosacarido por afuera de las membranas. H2C HC CH2 Esto sirve como marcador superficial de la celula Ej. los antigenos de un grupo sanguineo que determinan si el tipo de sangre es A, B, AB u O , son los distintos azucares terminales del oligosacarido del gangliosido. 3 LIPIDOS NO HIDROLIZABLES Esteroides Es un grupo de sustancias de esqueleto policiclico derivadas estructuralmente del ciclopentano perhidrofenentreno. ciclo pentano C27H16O colesterol perhidroEntre los esteroides mas HO fenantreno importantes encontramos alcoholes (esteroles) y cetonas (algunas hormonas). Los esteroles son alcoholes secundarios naturales donde el un ester de colesterol hidroxilo puede estar libre o combinado (Ej con un acido O graso). El esterol de mayor importancia es el colesterol, que OH se halla solo en células animales, El colesterol por si solo es componente de membranas biológicas (aporta fluidez) y es precursor de las hormonas esteroideas (glucocorticoides, mineralocorticoides y hormonas sexuales) y las sales biliares. Otros esteroles son el ergosterol (en levadura de cerveza y cornezuelo de centeno) y estigmasterol (en soja); etc. Los esteroides, biosinteticamente, derivan tambien de unidades de isopreno (5C), el anillo característico se va formando con bloques de 5C, para formar compuestos intermediarios de 10, 15 y finalmente 30C (escualeno). O Testosterona (una hormona sexual) Terpenoides: HO Los terpenos son, en un sentido restringido, los hidrocarburos de origen natural constituidos por una o mas unidades de isopreno, C5H10, con esqueletos cíclicos o acíclicos. Asi tenemos monoterpenos (10C), sesquiterpenos (15C), diterpenos(20C), isopreno triterpenos(30C),tetraterpenos(40C). Muchos de estos compuestos imparten los olores (aceites esenciales) y los colores (pigmentos) de las plantas. Los pigmentos vegetales citados a la izquierda pertenecen al grupo de los carotenoides, tetraterpenos de color amarillo a rojo, liposolubles. Usualmente se presentan varios en el mismo material Limoneno Licopeno (γ,γ caroteno) vegetal. El licopeno (C40H56) es el pigmento rojo del fruto maduro del tomate, también presente en sandia. El β-caroteno es un β-caroteno pigmento de color naranja que se α-pineno O halla en zanahorias y zapallo. En los vegetales se ha identificado una gran variedad de terpenos los cuales son reconocidos por sus olores y sabores Vitamina K (fitoquinona) característicos (aceites esenciales) los monoterpenos mentol O CH3 O citral, geraniol, pineno, alcanfor y carvona son ejemplos de estos. Vitamina E (α-tocoferol) También se incluyen las vitaminas liposolubles (A, D, E y K). escualeno En animales , el escualeno constituye el aceite de hígado de peces, llegando a (forma plegada) un 80%, en algunas especies de tiburón. Algunos Cofactores o Coenzimas tienen estructuras terpenoides.(sus dobles enlaces conjugados los convierten en excelentes transportadores de electrones, por lo que participan en los procesos oxidativos de la mitocondria: Coenzima Q y ubiquinona.) 4 escualeno (forma lineal) PROPIEDADES QUÍMICAS Hidrólisis: dado que los lípidos hidrolizables son esteres, estas reacción puede llevarse a cabo tanto en medio ácido, como en medio alcalino. La hidrólisis puede también ser enzimática ( la enzima especifica se llama Lipasa) CH2 O O CH O CH2 triglicerido CH2 CH CH2 O O O O C C O C O O C C O C O R R' + H 3 + H2 O Medio ácido R" CH2 OH CH OH CH2 OH + HO R" + 3 NaOH ácidos grasos Medio alcalino triglicerido +- R' C O + R" R + C R' + O +Na O C R" Sales de los O ácidos grasos CH CH2 OH glicerol + O C OH + Na O +Na O OH CH2 H2 O R C HO O HO glicerol R R' O C JABON Las sales de los ácidos grasos se llaman jabones y la hidrólisis alcalina que los forma , se llama “Saponificacion”. Los jabones de Na+ , K+, NH4+ son solubles en H2O; los de Mg++, Ca++ y metales pesados son insolubles en H2O. Indice de Saponificación: Es el numero de mg de KOH necesarios para saponificar completamente 1 gramo de grasa -o aceite-. Da una idea del tamaño o largo de cadena promedio de los ácidos grasos que componen la grasa, a menor largo de cadena (mas chicos), mayor el KOH requerido. Indice de acidez: Es análogo al índice de saponificación, pero en frio; cantidad de KOH necesarios para neutralizar los ácidos libres presentes; lo que está relacionado con la rancidez. La presencia de ácidos grasos libres, acidificaran el medio lo que llevara a un consumo de KOH en la valoración, una vez neutralizado, la gota en exceso de alcali virara el indicador fenoftaleina desde incoloro (medio acido y neutro) hacia el purpura (medio basico). Indice de Iodo (numero de Iodo): Es la cantidad de Iodo (expresada en gramos), que reacciona con 100 g de grasa -o aceite-. Esta definición es formal, ya que el reactivo no es el I2 sino el monocloruro de yodo (ICl) o monobromuro de yodo. Este parámetro da una idea del numero de >=< (insaturaciones) en la muestra. En la actualidad, la determinación de los ácidos grasos se efectúa por medio de métodos cromatográficos, por ej. : cromatografia en cape fina (cualitativo) o cromatografia gaseosa (cuantitativo). Hidrogenación: la reacciones de los triacilgliceroles no solo implican al enlace ester, ya que los dobles enlaces de los ácidos grasos insaturados pueden adicionar halógenos (como en índice de I2), oxigeno (ocasiona la rancidez) o Hidrogeno (Hidrogenación). Este es un proceso muy usado en la industria en la preparación de margarina, que implica una hidrogenación parcial de un aceite vegetal liquido (en gral. maíz o soja), donde algunos dobles enlaces se transforman en simples y el aceite se transforma en un sólido firme, de consistencia comparable a la de la manteca El proceso se realiza de la siguiente forma: se hace burbujear hidrógeno gaseoso a presión en el seno del aceite, se usa como catalizador de la reacción Ni. Se debe regular el grado de hidrogenación para mantener cierto número de enlaces insaturados, de lo contrario el producto se vuelve duro y quebradizo. Si la hidrogenación continúa por un tiempo prolongado, se forman glicerol y alcoholes de cadena larga (que se emplean para la fabricación de detergentes sintéticos). 5 I- Parte Experimental 1- Presencia de ácidos grasos libres: En 2 tubos de ensayo coloque 5 ml de agua destilada. En uno de ellos agregue 15-20 gotas de aceite vegetal, y 2 gotas de fenolftaleína; en el otro, solamente 2 gotas de solución de fenolftaleina. Agregue a cada tubo una gota de solución de NaOH al 0,05%. Agite. Si en algún tubo no aparece coloración debida al indicador, agregue gota por gota mas NaOH, hasta obtener coloración estable. Registre sus observaciones. Interprételas. 2- Saponificación de una grasa: En un tubo de ensayo coloque 0,5-1 g de grasa, y fúndala para que se recolecte en el fondo del tubo. Agregue una lenteja de NaOH (no lo toque, es cáustico) y 10 gotas de etanol; marque la altura de etanol en el tubo y caliente suavemente a ebullición durante algunos minutos (aprox. 10 minutos); reponga el etanol que pierda por evaporación. Agregue al contenido del tubo, agua hasta aproximadamente 1/3 del tubo. Agite. Interprete su observación. 3- Liberación de ácidos grasos a partir de jabón: A una pequeña cantidad de un jabón, agregue 1 ml de solución al 20% de H2SO4. Caliente suavemente durante 30 segundos. Deje enfriar en reposo, y observe. Interprete con una ecuación. 4- Separación de ácidos grasos volátiles (a partir de manteca): En un balón Engler pequeño coloque 5 g. de manteca. Agregue 10 ml de etanol y 10 ml de solución de NaOH al 40%. Caliente suavemente. Con precaución, durante 10 minutos. Agregue 20 ml de agua destilada al balón y acidifique con H2SO4 al 20%, compruebe la acidez con un trocito de papel tornasol (¿De qué color?), y destile, calentando suavemente. Recolecte el destilado en un vaso de precipitación que contenga unos ml de agua destilada. Tome la reacción ácido-base al destilado. Interprete con ecuaciones. Dibuje el aparato utilizado. 5- Diferenciación entre aceites animales o vegetales y aceites minerales: i- En un tubo de ensayo coloque 1 ml de aceite vegetal o animal; agregue una lenteja de NaOH y caliente suavemente durante pocos minutos. Observe. Deje enfriar, y verifique si el aspecto del sistema cambia. Repita el ensayo sobre 1 ml de aceite mineral (derivado del petróleo). Interprete sus observaciones ii- Sobre un papel de filtro deje caer en un extremo aceite mineral y en el otro extremo extremo un aceite vegetal. Flamee el papel de filtro sobre una tela metálica (cuidando de no excederse en el calentamiento). Registre sus observaciones. Interprételas. 6 II-Cuestionario Temario: Lípidos hidrolizables: Simples y compuestos. Nomenclatura. Acidos grasos. Grasas, aceites, ceras, jabones (saponificación). Fosfoglicéridos. Esfingolípidos. Glicolípidos. Lípidos no hidrolizables: Terpenos y esteroides. Nomenclatura. Aceites esenciales. Bibliografía:.-H. Hart; D. J. Hart, L. E. Craine, “Quimica orgánica”, McGraw-Hill Interamericana, 5ta ed. 1995, México - Guía de Trabajos Prácticos - Clases teóricas. 1) a)¿Qué son los ácidos grasos? Dé ejemplos de ácidos grasos saturados y no saturados. b)¿Qué son y cómo se clasifican los lípidos? 2) Defina un glicérido desde el punto de vista de su estructura. Mediante ejemplos indique como se nombran. 3) Indique mediante ecuaciones la obtención de jabones. 4) Exprese la diferencia entre una grasa, un aceite vegetal y un aceite mineral: a) en sus propiedades físicas; b) en su constitución; c) en sus propiedades químicas. 5) a)¿Qué son los fosfolípidos? ¿Qué función cumplen en la célula? Escriba la estructura molecular del ácido fosfórico, de un ester monoalquílico y de un dialquil éster del mismo. b) Escriba la estructura de un ácido fosfatídico. c)¿Cómo define un fosfoglicérido? Dé un ejemplo. 6) En muchos fosfolípidos, además del glicerol, aparecen otros alcoholes, como por ej. la etanolamina y la colina. Escriba la estructura de estos dos alcoholes y la de una fosfatidiletanolamina y una fosfatidilcolina. 7) a) Indique si en los fosfolípidos de las preguntas 5 y 6, existe un ión dipolar. En caso afirmativo recuádrelo. b) Indique donde se produce la ruptura de la molécula durante la hidrólisis ácida, y escriba los productos que se obtendrían en cada caso. 8) Además de las grasas, aceites y los fosfolípidos, también se conocen las ceras y los glicolípidos. ¿En qué se diferencian estructuralmente? Dé un ejemplo de cada clase. ¿Qué función cumplen los glicolípidos en la organización celular? 9) Explique que son los terpenos y los esteroides. De algunos ejemplos de cada clase. 10) El geraniol constituye aproximadamente el 70% de los aceites esenciales del geranio. OH a) Nombre este compuesto de acuerdo a la nomenclatura IUPAC, respetando la configuración indicada. Reconozca las unidades de isopreno en su estructura. b) Indique por lo menos dos reacciones químicas que le permitan caracterizarlo funcionalmente. 11) El limoneno es el principal componente del aceite esencial presente en la cáscara del limón. a) Represente la estructura espacial del mismo sabiendo que su nombre IUPAC es 1-metil4-(metiletenil)-1-ciclohexeno. b) Puede esta sustancia presentar actividad óptica? Justifique. c) Cual será el producto de su reacción con HBr? 7 12) Complete las siquientes reacciones: O O a) + + OH H O (Mentol) NaHSO3 + b) (Alcanfor) O O OH c) + H3C C Cl (Vitamina A1) O C d) + H (Citral) 8 NH-NH2 O Quimica Orgánica Lipidos -- Ejercicios Adicionales 1) a) El ácido linoleico (ácido ∆9,12 octadecadienoico) es conocido como Vitamina F, por estimular el crecimiento y el desarrollo cutáneo y está presente en grasas animales. Representar las reacciones de un mol del mismo frente a: i) Hidróxido de sodio. ii) Cloro. iii) Etanol (y un ácido como catalizador). iv) 1 mol de Glicerol. ¿ Cuántos productos pueden formarse en este caso? b) Predecir si dicho ácido será mas o menos ácido que el ácido propanoico. 2) Se llama ácido linolénico al ácido ∆9,12,15 octadecatrienoico. a) Determinar cuántos gramos de NaOH reaccionarán con 50 gramos de ácido linolénico. b) Representar su reacción frente al iodo. c) Determinar cuántos gramos de iodo reaccionarán con 120 gramos de ácido linolénico. d) ¿Cuál será el indice de iodo del triglicérido simple formado por este ácido y el glicerol? 3) Determinar el índice de saponificación de un monoglicérido, un diglicérido y el triglicérido formados a partir del ácido mirístico (ácido tetradecanoico) exclusivamente. 4) Dados los siguintes triglicéridos y sus índices de saponificación, determinar sus pesos moleculares: i) Triglicérido A; Indice de saponificación = 263,3. ii) Triglicérido B; Indice de saponificación = 188,8. 5) Representar la hidrólisis alcalina de: a) Una cera. b) Una cefalina. c) Una esfingomielina. d) Un cerebrósido. O 6) Dados los siguientes terpenos: O H citronelal geranial OH O pulegona H mentol 9 terpinoleno a) Indicar cuáles de ellos reaccionan con fenilhidrazina. Representar las reacciones en los casos en que éstas ocurran. b) Indicar cuáles dan positivo el ensayo de Tollens. Representar las reacciones en los casos en que éstas ocurran. c) Indicar cuáles de ellos reccionan con 2 moles de bromo por cada mol de terpeno. Representar las reacciones en los casos en que éstas ocurran. d) Cuál de ellos dará negativo todos los ensayos anteriores. e) ¿Qué tipo de terpenos son todos ellos? f) ¿Qué tipo de isómeros son la pulegona y el geranial? g) El geranial y el citronelal ¿són isómeros? h) Indicar si el citronelal y el geranial presentan isomería geométrica. i) Representar la formación del hemiacetal entre el citronelal y el mentol. 7) Completar las siguientes reacciones: a) mirceno Pt + H2 (Presente en las hojas de laurel) O + NH2OH b) HO androsterona (Hormona) c) + HCl α-terpineno (Presente en el aceite esencial del cilantro) COOH + CH3OH d) ácido araquidónico 10 H+