INTRODUCCIÓN El avance de la tecnología presenta nuevas
Anuncio
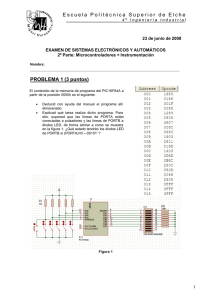
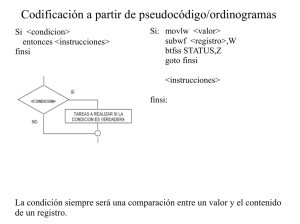
INTRODUCCIÓN El avance de la tecnología presenta nuevas posibilidades de respuesta a muchas de las necesidades de la sociedad, generando así un gran impacto en la vida diaria. Desde los inicios de la investigación del sistema circulatorio utilizando catéteres efectuada Claude Bernard en el siglo IXX, hasta las novedosas técnicas de cirugía robótica, los conocimientos en el campo de la bioingeniería han tenido grandes progresos; uno de los más destacados, es el desarrollo de sistemas de estimulación cardiaca artificial para el control y tratamiento de los bloqueos cardiacos, y arritmias en general Hoy en día, son cada vez más las personas que padecen enfermedades relacionadas con el sistema circulatorio, muchas veces mal diagnosticadas y sin seguir el tratamiento adecuado para superarlas, También los costos y la complejidad del tratamiento de las mismas se ha incrementado. El empleo de la Ingeniería Mecatrónica, específicamente en cardiología humana, busca responder las necesidades antes mencionadas, y servir como una guía de los parámetros determinantes identificados para el diseño de sistemas de implantación de dispositivos tipo Nano puente AV aplicables a futuras implementaciones. 11 1. PLANTEAMIENTO DEL PROBLEMA 1.1 ANTECEDENTES La implementación del catéter en la medicina ha tenido una evolución progresiva desde sus inicios y continúa desarrollándose para tareas de mayor complejidad, A continuación se resume esta evolución y como se va relacionando con este proyecto. • • • • • • • • En 1844, Claude Bernard insertó por primer vez un termómetro de mercurio en la arteria carótida de un caballo y avanzó a través de la válvula aórtica dentro del ventrículo izquierdo para medir la temperatura de la sangre. Él adaptó este procedimiento durante cuarenta años para lograr medir las presiones dentro del corazón de una gran variedad de animales. En 1912, Frizt Bleichroeder, E. Unger y W. Loeb publican descripciones de cateterismos de vasos sanguíneos sin contar con la ayuda de los rayos X. En 1929 Werner Forssmann experimentó en un cadáver humano y demostró lo sencillo que podía guiarse un catéter de una vena del brazo a la aurícula derecha, también se le atribuye la caracterización del corazón derecho humano utilizando técnicas de radiografía. En los inicios de 1940, Andre Cournand, Hilmert Ranges y Dickinson Richards, utilizando las técnicas de caracterización lograron identificar funcionamientos y enfermedades en corazones humanos. Werner Forssmann gana el premio Nobel de medicina en 1956. Hacia 1947, H. A. Zimmerman ya había desarrollado una completa técnica intravascular para la caracterización del corazón izquierdo y junto con sus colaboradores lograron caracterizar por completo el corazón. En 1953, Seldinger desarrollo la técnica de caracterización del corazón derecho e izquierdo por medio de cateterismo percutáneo, técnica que aún hoy es de gran uso..1 En 1956 Cournand, Richards y Forssmann compartieron el premio Nobel en Fisiología y medicina.2 Ryan TJ. The coronary angiogram and its seminal contribution to cardiovascular medicine over five decades. Circulation. 2002; 106: 752–756. 1 2 Geddes LA, Geddes LE. The Catheter Introducers. Chicago, Ill: Mobium Press; 1993: 38–39. 12 • • • En 1958 Mason Sones desarrollo la primera angiografía selectiva utilizando amplificación de imágenes y amplificación óptica con cinetoscópio de alta velocidad.3 En 1974, Andreas Gruentzig invento y llevo a cabo la primera angioplastia con un globo para bloqueo de arterias en Zúrich-Suiza. En el primer semestre de 1974, se hizo una investigación en el laboratorio K cirugía experimental del Hospital San Juan de Dios de Bogotá conjuntamente con la Universidad de los Andes con el fin de elaborar el trabajo para el proyecto de grado sobre el tema "medición de impedancia en el corazón". Se buscó determinar las formas de voltaje y corriente y magnitudes, así como la impedancia en la cara anterior del corazón. Se realizaron mediciones in vivo en 14 corazones de perros utilizando registros unipolares; para efecto de las medidas se dividió el corazón en 12 regiones y se registró la actividad eléctrica en 70 puntos sobre esas regiones; se estudiaron las tres capas del corazón: epicardio, miocardio y endocardio. Se encontraron formas de voltaje en espiga o polifásicas en epicardio y endocardio, siendo las amplitudes comparables en estas dos capas; la amplitud aumenta en el miocardio y las señales de voltaje y sus valores están en el rango de microamperios. No se hallaron valores en el dominio de frecuencia por carencia de un sistema de almacenamiento de datos conveniente a un proceso ulterior en computador digital.4 Década de los 80: • La Primera respuesta de estimulación utilizando un sensor hemodinámico: El sensor hemodinámico capta la Impedancia Intracardiaca usando los electrodos del marcapaso convencional para grabar y no requiere ningún hardware especial. Pueden usarse dos o más electrodos. Se inyectan los pulsos de umbral alterno de bajo nivel.5 3 FYE WB. American Cardiology. The History of a Specialty and Its College. Baltimore, Md: The Johns Hopkins University Press; 1996. 4 REYNOLDS Pombo Jorge, 30 Años de Estimulación Cardiaca en Colombia, Ed. Andes, Bogotá, 1988 5 CHIRIFE, Physiological principles of a new method for rate responsive pacing using the pre-ejection interval, PACE 1988;1545-1554p 13 • El catéter Indujo la Ablación Nodo AV Unión un Hombre: Se realizó en marzo, 1981 en el Hospital de Moffitt y descarga de alta energía alta DC excita a la región del Nodo de AV por medio de un desfibrilador normal.6 Década de los 90: • En los primeros días de los marcapasos, un problema mayor era la corta vida de la batería, con generadores del pulso que duraban sólo de 12 a 13 meses. Una interesante fuente de poder fue la de un generador de radio isotopo (RP) propuesta por Dr. Victor Parsonnet.7 • La Relación Entre la Incidencia y Número del Total de Muertes Súbitas entre la Población: La aproximación de la incidencia (el por ciento por año) y el número total de eventos por año para la población adulta global con respecto a los Estados Unidos mostró el aumento más alto. La población adulta global tiene una incidencia de muerte súbita estimada de 0.1-0.2% por año, ascendiendo a más de 300,000 muertes súbitas por año.8 • La Heterogeneidad eléctrica en el Corazón: El tejido ventricular comprende por lo menos tres tipos de la célula eectrofisiológicamente distintos: las epicardiales, endocardiales y células M. Porque las células de M despliegan un potencial de acción más largo, la dispersión del transmural de repolarización existe bajo las condiciones de la línea de fondo y es principalmente responsable de la ola de T en los electrocardiogramas.9 Año 2000 - Actualidad: • La fijación de marcapasos en lugares distintos a los utilizados y sus posibles beneficios: Varios estudios han hecho pensar en los beneficios potenciales del la estimulación cardíaca permanente en lugares diferentes, como el septum del interatrial y el ostium del seno coronario, En efecto, es en lo absoluto factible la 6 SCHEINMAN MM,Morady F,Hess DS,Gonzalez R. Catheter-induced ablation of the atriovetricular junction to control refractory supraventricular arrhythmias, JAMA 1982, 851-855p. 7 PARSONNET V. Bernstein AD, Perry GY.The nuclear pacemaker: Is renewed interest warranted. Am J Cardiol 1990, 837-842p. 8 MYERBURG. Kessler KM, Castellanos A: Sudden cardiac death: Structure, function and time-dependence of risk, 1992. 9 ANTZELEVITCH C, Yan GX, Shimizu W, Burashbikov A, Electrical heterogeneity, the ECG, and cardiacarrhythmias, Philadelphia, W.B. Saunders Co., 1999. 14 colocación exitosa en la mayoría (78-93%) de pacientes.10 • El Monitoreo ICD remoto: El poder monitorear por una vía telefónica ha sido un componente indispensable en los marcapasos hace más de tres décadas, pero sólo recientemente el monitoreo remoto ha aumentado de manera exponencial gracias a la mayor cobertura posible debido a los avances en las tecnologías de telecomunicaciones. 11 10 MANOLIS, Simeonidou E, Sousani E, Chiladakis J. Alternate sites of permanent cardiac pacing: A randomized study of novel technology, Hellenic J Cardiology 2004, 145-149p. 11 SCHOENFELD, Compton SJ, Mead RH, Weiss DN, Sherfesee L, Englund J, Mongeon LR Remote monitoring of implantable cardioverter defibrillators: a prospective analysis, PACE, 2004. 15 1.2 DESCRIPCIÓN Y FORMULACION DEL PROBLEMA En el procedimiento actual se debe considerar que las técnicas empleadas para la implantación de marcapasos convencionales son aun invasivas; Actualmente una implantación endocárdica toma entre 1-2 horas aproximadamente, utiliza dos fijaciones con un electrodo en forma de espiral o con una horquilla; el procedimiento quirúrgico usualmente practicado es el siguiente: • Inyección de anestésico. • Incisión en la piel debajo de la clavícula para crear el lugar de fijación del marcapaso “Bolsillo”. • Inserción del cable de los electrodos por la vena subclavia. • Ubicación por medio de rayos x para guiar el cable a las cavidades endocárdicas. • Unión del generador de pulsos el marcapaso al cable. • Programación y puesta en funcionamiento del marcapaso. El riesgo a contraer infecciones y otras complicaciones relacionadas con este tipo de procedimientos quirúrgicos está siempre presente, Así como de hemorragias y formación de coágulos; Además, se debe considerar los costos y los tiempos de las salas de operación. Al analizar esta situación se plantea la interrogante de ¿Qué características técnicas y funcionales debe tener el diseño de un sistema de cateterismo para la implantación de un dispositivo tipo Nano puente Aurículo Ventricular? 16 1.3 JUSTIFICACION El grupo de investigación Seguimiento del Corazón Vía Satélite (SCVS) propone el diseño de un dispositivo electrónico intracavitario, para hacer puente en la interrupción eléctrica Aurículo-Ventricular del área afectada. Para tal fin, se requiere investigar y diseñar un prototipo de catéter capaz de localizar el nodo aurículo ventricular, servir de canal de transporte entre el exterior y el interior del tejido cardiaco. El Nano puente ha sido, en principio, proyectado para eliminar los bloqueos Aurículo-Ventriculares. En la actualidad los bloqueos son manejados con el marcapasos convencional, con este dispositivos los pacientes deben dirigirse hasta el hospital para el respectivo control médico, en consecuencia, el Nano puente A-V por tener el sistema de telemetría el médico-cardiólogo no necesita tener en frente al paciente, ya que éste puede tener un seguimiento médico remoto Esta investigación es un módulo que hace parte de un proyecto macro, el cual es llamado “Nano puente A-V”. Este será un dispositivo que contribuirá a la sociedad al mejorar la forma como se tratan actualmente este tipo de cardiopatías ya que por su simplicidad y fabricación en masa se reducen los costos de producción, por lo tanto a él pueden acceder personas de diversos recursos económicos, además, el tiempo de implantación se reduce a una cirugía ambulatoria. El presente proyecto de investigación representa un aporte para el diseño de sistemas la implantación de nuevos dispositivos de estimulación cardiaca, porque suministra criterios de selección en cuanto a los tipos materiales apropiados, parámetros para el diseño de catéteres y sugiere el diseño de un instrumento para realizar mediciones de la impedancia del nodo AV; Además contribuirá a futuros desarrollos que se encaminen a la integración entre la ingeniería Mecatrónica y la Cardiología. 17 1.4 OBJETIVOS DE LA INVESTIGACIÓN 1.4.1 Objetivo General Diseñar un sistema de cateterismo capaz de acceder al tejido especializado del endocardio llamado nodo AV; realizando la medición de una de sus propiedades electrofisiologías la cual es muy importante para la posterior implantación manual de un dispositivo tipo “Nano puente AV” con la ayuda del mismo catéter. 1.4.2 Objetivos Específicos Diseñar un catéter con los materiales y dimensiones adecuados para servir como canal de transporte e implantación de un dispositivo tipo Nano puente AV de Forma Distal. Implementar el diseño uso de dispositivo portátil, liviano y fácil de utilizar que permita la medición de la resistencia eléctrica del tejido especializado llamado Nodo AV y visualizarla mediante el diseño de un software específico. Definir los criterios de diseño para los sistemas de cateterismo encaminados a implantar dispositivos tipo Nano puente AV, así como los del diseño de electrodos en sistemas de medición de impedancia endocárdica. Complementar al modulo del Grupo SCVS llamado “Pruebas Sobre Tejidos Vivos” encargado de realizar cultivos de células endocárdicas para experimentación de dispositivos de estimulación cardiaca artificial. 18 1.5 ALCANCES Y LIMITACIONES El diseño contempla un instrumento electrónico portátil de medición que permitirá una fácil implantación de dispositivos tipo nano puente AV, por medio de una cirugía ambulatoria, convirtiéndola en una intervención mínimamente invasiva; Reduciendo los tiempos de recuperación, los costos de toda la operación y el riesgo de infecciones. Las limitaciones de este tipo de proyectos están principalmente relacionadas con la escala a manejar, para el caso del Nano puente, las escalas utilizadas en algunos de sus componentes son manométricas, las tolerancias en la fabricación de los catéteres son del orden de las decimas de milímetro; También los procesos de manufactura de este tipo de dispositivos deben cumplir con las normas internacionales UNE 111600, ISO 10555, 10993. El acceso a bibliografía especializada es limitado y por último los costos en los materiales por ejemplo en las aleaciones de titanio comúnmente utilizadas en la fabricación de electrodos, son un impedimento adicional. 19 2. MARCO DE REFERENCIA 2.1 MARCO TEÓRICO CONCEPTUAL La instrumentación electrónica es aplicada en los circuitos requeridos para realizar la localización del nodo A-V por medio de la medición de la resistencia eléctrica del corazón, la ciencia de los materiales se utiliza para determinar la selección de los mejores materiales dependiendo de la aplicación futura de los mismos y de las normas internacionales para aplicaciones de este tipo, microcontroladores para la construcción del medidor y la interfaz con el usuario o sea, el médico especialista 2.1.1 Cateterismos. La palabra Catéter se deriva del griego καθετήρ que Significa sonda, usualmente estos dispositivos se introducen en diferentes tejidos del cuerpo para explorar, inyectar fármacos, y realizar mediciones; A continuación, se explicaran que son los cateterismos y como se aplican en cardiología (Ver Figura 1). Figura 1. Cateterismo Cardiaco. Fuente: Cateterización Cardiaca, Dirección URL:http://www.nlm.nih.gov/medlineplus/spanish/ency/esp_imagepages/1080.htm Ultima actualización 10/16/2006. Cateterización Cardiaca: La cateterización cardiaca es utilizada para estudiar las 20 diversas funciones del corazón. A través de diferentes técnicas, las arterias coronarias se pueden ver al inyectar un medio de contraste o se pueden destapar con una angioplastia de balón. Con ella, también es posible medir la concentración de oxígeno entre las válvulas y las paredes del corazón, así como las presiones dentro de cada cavidad cardiaca y a través de las válvulas. Esta técnica puede realizarse hasta en niños pequeños y en recién nacidos (Ver Figura 2). Figura 2. Catéter Venoso Central: Fuente: Catéter Venoso Central Dirección URL:http://www.nlm.nih.gov/medlineplus/spanish/ency/esp_imagepages/1080.htm Ultima actualización 10/16/2006. Es una sonda plástica larga y suave (generalmente hecha de silicona) que se coloca a través de una pequeña incisión en el cuello, el tórax o la ingle, dentro de una vena grande en el tórax con el fin de permitir la administración de líquidos y medicamentos por vía intravenosa, durante un período de tiempo prolongado.12 12 O. M. HIJAZI, J.J. Cheyney, P. C. Guzzetta, Jr, L.O. Toro-Figueroa. Venous Acces and Catheters. En Levin essentials of Pediatric Intensive Care. Second edition. Ed Churhill Livingstone,1997, 1189-1215 p. 21 2.1.2 Técnica de Seldinger. Inicialmente empleada como una técnica de canalización percutánea de vías venosas centrales (yugular interna, femoral y subclavia). El procedimiento fue descrito por Seldinger en la década de los 50. Actualmente las indicaciones del empleo de esta técnica se ha extendido a procedimientos no vasculares (colocación de drenajes pleurales, pericárdicos etc). Se realiza la localización de la vena mediante una aguja fina. Una vez obtenido el flujo de sangre se introduce una guía metálica flexible con punta blanda a través de la aguja (o del catéter de punción venosa periférica) y se progresa un catéter apoyándose en la guía sujetando ésta de manera firme para que no se deslice al territorio venoso. Cuando el catéter ha progresado lo suficiente (dependerá del acceso, edad y tamaño del paciente) retiraremos la guía sin arrastrar el catéter que queda situado en posición intravascular. Se debe realizar una técnica de imagen (generalmente radiografía de tórax, ecocardiografía) para comprobar su situación. De esta misma manera se localiza la zona adecuada para colocar los drenajes pleurales, pericárdicos entro otros, y tras pinchar con aguja se introduce la guía y el catéter de drenaje comprobando su correcta ubicación. EQUIPO Y MATERIAL Debe realizarse con la máxima asepsia, ya que conectamos el exterior con el espacio intravascular, con el riesgo de infección que ello conlleva. Se utilizará gorro, bata, guantes, mascarilla, campo estéril... siempre que la situación lo permita. Así también se procederá a desinfectar la piel del niño con derivados yodados y esperaremos uno o dos minuto antes de actuar. Preparación del campo estéril y del material que a utilizar: • Gasas y paños estériles. • Solución antiséptica. • Agujas y jeringas. • Suero salino heparinizado. • Bisturí, seda. • Aguja introductora, guía metálica flexible, dilatador. • Catéter biocompatible (de distintos materiales, cada vez menos trombogénicos, de superficie más lisa y recubiertos de heparina), de una a tres luces, de distinto diámetro grosor de 4 a 7 French y de distinta longitud, elegido según la vía y el niño, que se purga con el suero heparinizado. • Sistema de perfusión. Es necesaria la monitorización del paciente mientras se realiza esta técnica: • electrocardiograma, 22 • • frecuencia respiratoria saturación transcutánea de oxígeno. En los niños se considera imprescindible es la sedación y analgesia del paciente (midazolam o propofol con fentanilo ó ketolar y midazolam en pacientes no intubados) además de ser en ocasiones aconsejable la anestesia local, siempre que no sea una urgencia vital. DESCRIPCIÓN DE LA TÉCNICA: • Medir la distancia desde la zona de punción hasta la entrada de la aurícula derecha. Desinfectar la piel y tras purgar el catéter con suero heparinizado, sedoanalgesiar al paciente y comenzar la punción venosa con aguja o cánula sobre aguja y jeringa con suero heparinizado, siempre aspirando hasta que refluye sangre. Entonces se desliza la cánula sobre la aguja o se mantiene firme ésta donde refluye con fluidez y se introduce la guía blanda y flexible hasta la distancia que hemos medido o hasta que el registro del electrocardiograma detecta alguna extrasístole (retirar unos centímetros la guía). • Retirar la aguja o cánula y dejamos la guía. • Realizar una incisión en la piel • Con el bisturí. Introducir el dilatador a través de la guía avanzándolo y rotándolo tan sólo unos centímetros (piel y tejido subcutáneo) hasta que hayamos llegado al vaso para evitar lesionarlo. • Retirar el dilatador y dejar la guía sobre la que nuevamente deslizamos, ahora el catéter que no introduciremos por completo bajo la piel hasta no tener un extremo de la guía en nuestras manos (a través del cabo del catéter). • Retirar la guía, comprobar que refluyen todas las luces del catéter. • Se realiza radiografía de control y tras comprobar la correcta situación del catéter se fija a piel con unos puntos de sutura. 13 COMPLICACIONES: LIGADAS A LA PUNCIÓN (complicaciones al canalizar): • Extrasístoles o arritmias desencadenadas al introducir la guía, generalmente se resuelven espontáneamente al retirar ésta. • Sangrado o hematoma, se resuelve al comprimir sobre la zona (en vena femoral y yugular; no en subclavia ) • Neumotórax: especialmente en yugular y en subclavia. 13 DELGADO, Técnicas de Canalización Percutánea de Vías Venosas Centrales, Editorial Norma, Madrid, 1994: 1096-1098 p. 23 • • • Embolia gaseosa: es un riesgo inherente a toda punción (mayor riesgo en yugular y subclavia). Para intentar evitarlo se debe purgar bien todo el catéter y realizar la punción en posición declive (Trendelenburg). Lesiones nerviosas: por punción directa del nervio o por compresión de un hematoma. En particular el caso de la yugular interna pueden tener lugar lesiones del plexo braquial, del ganglio estrellado, del nervio frénico (parálisis diafragmática) y del nervio recurrente (parálisis unilateral de cuerdas vocales). Punción arterial: más frecuente en la yugular (7% si el abordaje es posterior) y en subclavia (1,5%). En este último caso es más complicado ya que no se puede realizar una compresión externa. LIGADAS AL CATÉTER (o a su utilización) Infección: Es la complicación más frecuente y está en relación con el tiempo de uso (aumenta sobre todo a partir de la primera semana) y la manipulación. Incidencia del 20 al 60% y llega a producir bacteriemia en el 10%. La incidencia de sepsis es variable y oscila entre 0% y 25%. Hay que distinguir entre colonización e infección 8 en función del número de colonias). La infección puede ser local, sistémica o ambas. Es más frecuente en los catéteres de la vía femoral que en yugular y subclavia. Se realiza tratamiento empírico con antibióticos hasta conocer los resultados de los cultivos. En ocasiones hay que retirar el catéter y otras veces, si la zona de punción y la entrada no están infectadas puede realizarse un intercambio de catéter a través de una guía.14 Trombosis: También es una complicación muy frecuente en ocasiones infraestimada. Existen factores que aumentan el riesgo de trombosis: • Dos o más veno-punciones para canalizar la vía • El tipo de líquido infundido (más frecuente con la nutrición parenteral). • Estados de hipercoagulabilidad. Existe una clara asociación entre septicemia y trombosis aunque se desconoce qué es primero. Se puede prevenir utilizando catéteres impregnados de heparina. Y puede tratarse 14 JC De Carlos Vicente, V. López Corominas, En J. López- Herce, Canalización Venosa Central y Manual de Cuidados Intensivos Pediátricos. Editorial Publ-Med. 1ª Edición 2001, 704-709 p. 24 con trombolíticos y/o heparina.15 Obstrucción: Puede ser total (imposibilidad de extraer e infundir) o parcial (imposibilidad de extraer) se produce por acumulación de fibrina. El tratamiento consiste en la administración de urokinasa 5000U/ml en el volumen de purgado del catéter (0,30,5-1 ml) y dejar actuar durante 30-60 minutos. Otras: Migración del catéter Rotura del catéter Mediastino ancho 2.1.3 Bloqueo AV. Cuando la perturbación en el tránsito de la onda de excitación ocurre desde las aurículas hasta los ventrículos, hablamos de bloqueo A-V, el nano puente está dirigido a los pacientes con esta cardiopatía. El estado actual de los conocimientos fisioeléctricos del sistema de excitación– conducción, se ha enriquecido con la técnica hisiográfica que nos permite conocer la electrogenia del espacio PR ó PQ y la localización exacta del sitio donde radica la lesión que origina el bloqueo, cuestión fundamental para establecer el pronóstico y tratamiento adecuados. Este ha mostrado 3 fenómenos eléctricos perfectamente definidos: • Un primer fenómeno corresponde al instante en que se comienza la despolarización en el nódulo de Keith – Flack. • El segundo fenómeno corresponde al momento en que se inicia la excitación en el haz de His. • El tercer fenómeno expresa la progresión del estímulo excitador en el sistema interventricular. Cada uno de estos tres instantes, se caracteriza por la presencia de descargas en forma de curso rápido, que delimitan dos espacios, los A-H(desde el inicio de la excitación miocárdica en el centro primario hasta su llegada al haz de His) y H-V (tránsito de la excitación desde el haz de His hasta la red de Purkinje). Para A-H los límites fluctúan entre 60 y 145 milisegundos, para H-V, la longitud normal se encuentra entre 30 y 60 mS (Ver Figura 3). 15 CENTENO Castillo, F Barranco Ruiz. Canalización Vascular en Principios de Urgencias, Emergencias y Cuidados críticos, 2001. 25 Figura 3. Valor del Hisiograma en los Bloqueos A-V Fuente: Revista Cubana de Cardiología, 2001, 56-60 p. El punto A corresponde al inicio de la onda de excitación en el nódulo de Keith – Flack. El punto H señala la llegada de la onda de excitación al haz de His y ambos puntos de referencia A y H constituyen el espacio A-H que mide normalmente entre 60 y 145ms. Después de su llegada al haz de His, la onda de excitación discurre por ambas ramas, los dos fascículos de la rama izquierda y la red de Purkinje, constituyendo una sucesión de puntos a los que se denomina genéricamente con la letra V. Entre los puntos H y V queda constituido el espacio H-V, cuyos valores fluctúan entre 30 y 60 ms. Ambos espacios coinciden con lo que en el electrocardiograma de superficie es el espacio P-R ó P-Q. Bloqueo AV de primer grado: En dicho bloqueo, el intervalo A-H del hisiograma se alarga. Bloqueo AV de segundo grado. Modalidad Morbitz I: En esta modalidad se alarga el intervalo A-H en forma progresiva. El intervalo H-V permanece normal, a menos que la lesión radique en regiones distales del haz de His, en cuyo caso, los complejos ventriculares se ensanchan y el intervalo H-V se alarga. Bloqueo AV de segundo grado. Modalidad Morbitz II: El intervalo H-V se alarga. 26 Bloqueo AV de tercer grado: El hisiograma nos muestra una ruptura de la correlación normal de los intervalos A-H y H-V con respecto a los complejos ventriculares ya que los complejos QRS no guardan una relación numérica fija con las ondas P.16 Para la resistencia, pueden esperarse valores de aproximadamente 500±100Ω En este caso la resolución adoptada fue de 25Ohm.17 2.1.4 Amplificadores de Instrumentación. Los amplificadores constituyen un componente muy importante en los sistemas de bioinstrumentación por lo cual sus características deben ajustarse a las condiciones impuestas por la señal a amplificar y al entorno físico de aplicación. Para realizar el diseño del Sistema Básico fueron analizados varios esquemas de amplificadores de instrumentación existentes en la literatura como el LM747, el INA128, el OPA2277, y finalmente el AD620. Cuando se elije un amplificador de instrumentación, se requiere guardar ciertas precauciones para conseguir que sus características no se vean afectadas por elementos externo, para solucionar esto se utiliza amplificadores de instrumentación con una alta impedancia de entrada y un alto rechazo al modo común (CMRR). Estos amplificadores de instrumentación amplifican la diferencia entre las dos señales que provienen de los electrodos, aumentando la sensibilidad del circuito. Es preciso señalar la interferencia capacitiva debida al equipo de medida, que se produce por la fuente de alimentación del equipo al cual llegan las señales. Otra fuente de ruido es la denominada interferencia inductiva, que es causada por la red eléctrica, la cual produce campos magnéticos que varían con el tiempo, los que a su vez inducen voltajes en la red formada por los electrodos del paciente.18 16 REVISTA CUBANA DE CARDIOLOGÍA, El Bloqueo AV Cardiaco, Página: 27 2001, 56-60 p. 17 SUN, W Cameron, S Heymsfield, H Lukaski, D Schoeller, K Friedl, R Kuczmarsyi, K Flegal, C Johnson, V Hubbard. Development of Bioelectrical Impedance Analysis Prediction Equations for Body Composition with the use of a Multicomponent model for use in Epidemiologic Surveys. American Society for Clinical Nutrition, 2003. OXFORD University, Signal Processing & Neural Networks Group, Dept. of Engineering Science, 2001. 18 27 2.1.5 Materiales. La selección de los materiales se determina mediante el análisis de las propiedades de los mismos, también es importe mencionar que las normas internacionales de la FDA y la USP dan ciertos parámetros a seguir en el momento de seleccionar el material para fabricar cualquier equipo en medicina. Siliconas: Son elastómeros fabricados a partir de compuestos de silicio que son de amplio uso en aplicaciones médicas por cumplir con las siguientes características: Biocompatibilidad: los materiales de silicona tienen una compatibilidad superior con el tejido humano y fluidos del cuerpo, y además una reacción del tejido sumamente baja cuando se realizan implantaciones comparado con otros elastómeros. Material Incoloro e insípido, las siliconas no permiten el crecimiento de bacterias y no manchan o se corroen con facilidad. La Resistencia de temperatura: las siliconas puede resistir un rango amplio de temperaturas, permaneciendo estable a través de las variaciones de temperatura de -175°F a 482° F., La Resistencia química: Es resistencia al agua y muchos otros químicos y solventes a cambiar la composición química. Las Propiedades mecánicas; Compuestos de silicona tiene una resistencia al esfuerzo tensor de alrededor 1500 psi, la capacidad de alargamiento es muy buena ( 1250%) así como la flexibilidad. Las Propiedades eléctricas: las siliconas exceden muchos materiales en sus propiedades aislantes así como su versatilidad para las aplicaciones eléctricas. ACRILO NITRILO BUTADIENO ESTIRENO (ABS): Esta modificación del polímero del estireno es la de mayor significado en las aplicaciones técnicas; La abreviatura ABS debe ser empleada para las modificaciones del butadieno. La flexibilidad que ofrece el uso del sistema de tres monómeros (A,B y S) permite definir y crear a medida el perfil de propiedades del producto. El acrilonitrilo aporta: 28 - Resistencia química - Resistencia al envejecimiento - Dureza - Rigidez - Brillo El butadieno aporta - Ductilidad a bajas temperaturas - Flexibilidad - Resistencia de la masa fundida El estireno aporta - Fluidez (fácil transformación) - Brillo (lustre) - Dureza - Rigidez Variando la proporción de los tres componentes, es posible sacar el máximo provecho a algunas propiedades, conservando al mismo tiempo un comportamiento excelente durante la transformación.19 19 ICIPC. Introducción a los Materiales Plásticos, Medellín, Julio 1996. 29 Tabla 1. Propiedades Cuantitativas Propiedades Resistencia al impacto, prueba D2546 Izod Resistencia a la D638 tensión elongación D638 Módulo de D638 tensión Dureza Grados de ABS Alto Impacto Bajo Resistente impacto medio Impacto al calor Mecánicas a 23°C Método ASTM D785 Peso específico D792 Coeficiente de D696 expansión térmica Distorsión por D648 calor Unidad J/m 375-640 215-375 105-215 105-320 Kg. / mm2 3,3 – 4,2 4,2-4,9 4,2-5,3 4,2-5,3 % 15-70 5-30 5-20 10-50 173-214 214-255 214-265 214-265 HRC 88-90 95-105 105-110 105-110 (Rockwell) 1,02-1,04 1,04-1,05 1,05-1,07 1,04-1,06 Térmicas X 105 cm / 9,5 –11,0 7,0-8,8 cm* °C 7,0-8,2 6,5-9,3 °C a 18,4 93-99 Kg /cm2 96-104 102-112 96-102 Fuente: Propiedades Cuantitativas del http://www.textoscientificos.com/polimeros/abs, 10/06/2008. ABS, Dirección URL: Última actualización 2.1.6 Diseños electrónicos. El puente de Wheatstone tiene dos aplicaciones fundamentales la medición de resistencias de alta precisión y como sensor dependiente de un desbalance de potencial, por ejemplo en una LDR. La precisión de un puente de resistencias depende solo de la temperatura y la sensibilidad del galvanómetro. Figura 4. Circuito Puente. 30 Fuente: Autor. Analizando por Nodos: I1 = V/ (R1 + R3) => VAC= I1 x R3 = V x R3 / (R1+ R3) I2 = V/ (R2 + R3) => VBC= I2 x R4 = V x R4 / (R2+ R4) Suponiendo que el circuito puente está equilibrado VAB = 0 R3 / (R1+ R3) = R4 / (R2+ R4) Operando R3 x (R2+ R4) = R4 x (R1+ R3) R3 x R2+ R3 x R4 = R4 x R1+ R4 x R3 R3 x R2+ R3 x R4 = R4 x R1+ R4 x R3 Operando los términos iguales: R3 x R2= R4 x R1 Ó también R1 / R2 = R3 / R4 Tres de las resistencias R1, R2 y R3 son patrones de alta estabilidad y baja tolerancia, La cuarta es la resistencia incógnita, a determinar su valor Rx, Conectando un galvanómetro entre los puntos A y B indica si hay paso de corriente a través de él. 31 Ajustando los valores R1, R2 y R3 hasta que el galvanómetro indique que no hay paso de corriente, queda claro que el potencial en el punto A es igual al potencial en el punto B. VAB = 0 y se cumplirá lo ya demostrado antes, que R1 / R2 = R3 / R4 La resistencia incógnita que en vez de R4= Rx se calcula utilizando: Rx =R3 x R2 / R1 32 2.2 MARCO LEGAL O NORMATIVO Para el diseño y modelamiento CAD-CAE del sistema de cateterismo e implantación se estableció el uso del sistema métrico internacional y de medición ISO, también se consultaron las siguientes normas: • UNE 111600:1992 catéteres intravasculares periféricos, sobre aguja introductora, estériles para un solo uso • UNE-EN ISO 10555-1/A1:2000 catéteres intravasculares estériles desechables. parte 1: requisitos generales. (ISO 10555-1:1996/A1:1999). • UNE-EN ISO 10555-2:1997 Catéteres intravasculares estériles, desechables parte 2: catéteres angiográficos. (ISO 10555-2:1996). • ISO 10993 es la encargada de evaluar el grado de biocompatibilidad. 33 3. METODOLOGIA 3.1 ENFOQUE DE LA INVESTIGACION El diseño de este dispositivo tiene un enfoque empírico-analítico el cual estudia cada uno de los posibles componentes basándose en las herramientas de modelado y simulación CAD-CAE, así como en la bibliografía de los temas relacionados Se enfoco el diseño de un instrumento portátil en forma de una pistola anatómica, para facilitar la manipulación en una sala de cirugía, Junto con un catéter de exploración y transporte. Debido a la naturaleza de las variables, se debe diseñar una etapa previa de acondicionamiento de la señal; La interpretación de los datos visualizados por el sistema es fundamental para la correcta ubicación del bloqueo del Nodo AV. Las tareas realizadas corresponden a las siguientes actividades: Revisión del estado del arte acerca del desarrollo de innovaciones en el área de la estimulación cardiaca y exploración por medio de cateterismos. Selección de los materiales adecuados con propiedades biocompatibles, con la ayuda de simulaciones y con base en la bibliografía disponible. Caracterización del comportamiento del sensor de impedancia para futuros desarrollos. Selección del tipo de microcontrolador adecuado para este diseño así como de acondicionador de señal requerido. Análisis de las características del software del controlador para obtener lecturas confiables de la impedancia endocárdica. 34 3.2 LÍNEA DE INVESTIGACIÓN LÍNEA DE INVESTIGACIÓN DE USB La línea de investigación se incluye dentro de tecnologías actuales y sociedad. SUB-LÍNEA DE FACULTAD La sub-línea de facultad se incluye dentro es instrumentación y control de procesos. 35 3.3 TÉCNICAS DE RECOLECCIÓN DE INFORMACIÓN Las señales de interés son básicamente los voltajes que son detectados en los electrodos dispuestos en la punta del catéter, estas señales son captadas mediante un instrumento electrónico de medición calibrado con una señal de referencia que me simula las características del Nodo AV, Luego es interpretada por el puerto de conversión análogo-digital microcontrolador , el microcontrolador detecta los cambios entre la referencia y la señal captada por los electrodos del catéter y esta diferencia a su vez es visualizada por el usuario mediante una pantalla LCD. 36 3.4 HIPÓTESIS Se propone una posible solución confiable a las necesidades propuestas en la implantación de marcapasos tipo Nano puente AV de mediciones de la impedancia del tejido endocardico, se espera que el diseño de este sistema contribuya a la sociedad ya que por su simplicidad de manejo, y fabricación en masa se reducen los costos de producción de forma comprobable, por lo tanto a este tipo de intervenciones pueden acceder personas de diversos recursos económicos, además, el tiempo de implantación es mínimo y la cirugía es ambulatoria. 37 3.5 VARIABLES 3.5.1 Variables Independientes. El voltaje de alimentación del circuito electrónico es una batería de 5V que se maneja mediante un interruptor de encendido y apagado. 3.5.2 Variables dependientes. Las principales variables que entran en el circuito de mediciones para ser interpretadas por el microcontrolador son: El voltaje DC de referencia: Se calibra manualmente por medio de un potenciómetro de precisión, el valor de esta resistencia es proporcional a este voltaje y este debe estar cercano a los ±500Ω porque este es el valor de impedancia del nodo AV. El voltaje de los electrodos: este voltaje es análogo y se convierte a señal digital proporcional a la cantidad de corriente que pasa entre los dos anillos del electrodo, el microcontrolador interpreta esto como la impedancia del tejido comprendido entre los anillos y lo visualiza en la pantalla LCD junto con el voltaje de referencia. 38 4. DESARROLLO INGENIERIL 4.1 PLANTEAMENTO GENERAL Se propone el diseño y construcción a escala nanométrica de un dispositivo electrónico implantable "Nano puente Aurículo-ventricular artificial cardiaco" que sustituiría el área interrumpida por lesión del nodo Aurículo-ventricular en pacientes con cardiopatías de este tipo. El tamaño físico final esperado del dispositivo ha sido estimado entre 4 y 5 milímetros aproximadamente, y con un funcionamiento básico que se diferencia del de los marcapasos artificiales cardiacos tradicionales, no solo en el tamaño sino en la serie de eventos mediante los cuales se logra la estimulación eléctrica artificial guardando mayor similitud con el sistema electrofisiológico natural (Ver Figura 5). Figura 5. Vasos Sanguíneos relacionados en el procedimiento Fuente: El Corazón, Microsoft Encarta ® 2008, Microsoft Corporation. El camino del catéter es a través de la vena cava superior, ya que es un acceso al nodo AV y porque tiene un diámetro interno grande en comparación con los vasos vecinos. Para localizar el tejido especializado del nodo AV, se procede a hacer mediciones de las propiedades electrofisiologías, más específicamente de la resistencia eléctrica, para esto el electrodo de la punta del catéter aplica un potencial a través del grupo de células en contacto, dependiendo del valor de voltaje que logra pasar de una punta a la otra, se asigna un valor en ohmios el programa de medición, 39 este es comparado con una referencia que esta previamente calibrada, de esta manera se logra detectar el lugar exacto del nodo AV, lo cual es fundamental para la implantación del marcapasos.20 Una vez localizado el nodo AV, el mismo catéter se convierte un canal de transporte entre el exterior y la superficie del nodo AV, de esta manera hacernos pasar por el interior del catéter el dispositivo y se ubica de manea manual sobre el tejido especializado. El especialista con la ayuda de una perilla, realiza los movimientos necesarios para fijar el dispositivo (Ver Figura 6). Figura 6. Medición de la resistencia eléctrica. Cátodo Ánodo Endocardio Tejido especializado: Nodo AV 4.1.1 Descripción del Nano puente. La diferencia del Nano puente A-V con el marcapasos tradicional está en que el Nano puente no genera pulsos eléctricos artificiales en su funcionamiento normal, sino que censa, retarda, conduce, amplifica y re-inyecta los pulsos (creando un puente artificial) fisiológicos naturales del corazón entre la Aurícula y el Ventrículo (ver figura 7). Figura 7. Posible apariencia externa del Nano puente. A. Tamaño y diseño básico En lo referente al tamaño y diseño básico de este dispositivo, se espera que el tamaño físico final del Nano puente A-V sea de 5 milímetros de largo por 3 20 PUURTINEN Merja. “Bioamplifier Work”. Tampere University of Technology, Ragnar Granit Institute, Medical Electronics Laboratory, 2003 40 milímetros de ancho aproximadamente, sin incluir los electrodos receptores y transmisores. Una capa de material flexible encapsula todo el sistema; en el interior se alojan la fuente de poder y los circuitos electrónicos que amplifican el pulso electrofisiológico; los sistemas de control internos, como también la conexión al sistema de transmisión y de control externos no invasivos (ver Figura 8). Figura 8. Posible apariencia interna del Nano puente. B. Sistema de control Para el control del Nano puente se establece comunicación bidireccional: la recepción de información en forma de electrocardiográfica, impedancia, resistencia para el funcionamiento de los electrodos y la transmisión de los parámetros para la programación del sistema como son: frecuencia, voltaje, selección de parámetros de baja y alta frecuencia, ancho de pulso, sensitividad de recepción de los pulsos naturales y control del sistema de estimulación para taquiarritmias. C. Fuente de poder La fuente piezoeléctrica de poder está formada por una disposición de cristales naturales seleccionados por alto rendimiento de producción de corriente eléctrica, tallados en forma ovalada cónica para obtener la mayor densidad de los cristales dentro del espacio físico diseñado. Por tratarse de circuitos que no requieren baterías, sino que dependen de un sistema piezoeléctrico u otro alterno, la longevidad puede considerarse teóricamente indefinida. El consumo eléctrico de los nano componentes del puente será muy bajo se utilizaran muy probablemente tecnología CMOs. 41 4.1.2 Diagrama de funcionamiento general INICIO Preparación del paciente, previo a la intervención Calibración del sistema, Unir el nano puente al collarín del cable guía Verificar la correcta ubicación angular y lineal del nano puente con respecto a la perilla Inicio procedimiento quirúrgico utilizando la técnica de Seldinger Encender el sistema electrónico e iniciar los movimientos de exploración observando Cada uno de los datos mostrados En la pantalla LCD Al ubicar el nodo AV, realizar los movimientos de implantación del dispositivo y proceder con la extracción del catéter Iniciar verificación del correcto funcionamiento del nano puente, Suturar FIN 42 4.2 DESARROLLO ELECTRÓNICO Características del microcontrolador. Para comparar un microcontrolador con otro, es necesario saber cuál será la aplicación que se le dará al microcontrolador, la relación costo-beneficio, las características funcionales y la facilidad de manejo; en este caso es necesario leer el valor de impedancia representado por un voltaje análogo proveniente de un circuito puente, es necesario el manejo de conversores analógicos-digitales y visualización de LCD. Microcontroladores Freescale MC68HC08. El uso microcontroladores Freescale MC68HC08 (originalmente Motorola HC08) se impone. Estos microcontroladores fueron introducidos al mercado para competir con los microcontroladores de Microchip. A pesar que actualmente la popularidad y disponibilidad de herramientas de software para estos microcontroladores es menor que la de los microcontroladores PIC, esta familia de dispositivos tiene ciertos atractivos, como un menor costo frente al PIC16F873, convertidores A/D en casi todas sus versiones, señales PWM, oscilador interno, y la disponibilidad gratuita del popular entorno de desarrollo CodeWarrior, pero el manejo de LCD no es tan sencillo com el de los microcontroladores PIC porque manejan una lógica distinta. Microcontroladores PIC de Microchip. Los microcontroladores PIC de Microchip Technology Inc. combinan una gran calidad unida a un bajo coste y un excelente rendimiento. Un gran número de estos microcontroladores se usan en una gran cantidad de aplicaciones tan comunes como periféricos del ordenador, datos de entrada automoción de datos, sistemas de seguridad y aplicaciones en el sector de telecomunicaciones Las características más representativas de los PIC son las siguientes: • • • • • • • Arquitectura del procesador tipo Harvard. Técnica de segmentación o pipe-line en la ejecución de las instrucciones. El formato de todas las instrucciones tiene la misma longitud. Procesador RISC (Computador de Juego de Instrucciones Reducido). Todas las instrucciones son ortogonales. Arquitectura basada en “banco de registros”. Diversidad de modelos de microcontroladores con prestaciones y recursos diferentes. 43 • Herramientas de soporte potentes y económicas.21 • En el modelo de arquitectura Harvard la UCP se conecta de forma independiente y con buses distintos con la memoria de instrucciones y con la de datos, permitiendo acceder simultáneamente a las dos memorias. 4.2.1 Características del microcontrolador PIC 16F873. Este microcontrolador es bastante es bastante práctico y fácil de usar porque ya tiene incorporados un conversor análogo A/D de 10 bits multicanal además de Puerto Serie multifuncional (Ver Figura 9). Figura 9. Descripcion Pines PIC 16F873. Fuente: MANUAL DE MICROCONTROLADOR PIC16F873, F.I.M.E.E En la siguiente tabla podemos observar más claramente la descripción de cada uno de los pines del microcontrolador 16F873 (Ver Tabla 2) 21 UNIVERSIDAD DE JAEN, Adquisición de Magnitudes Físicas Mediante Microcontrolador, Granada, España, Julio de 2000, 44 Tabla 2. Descripcion Pines PIC 16F873 Pin Tipo Descripción OSC1/CLKIN E Entrada de oscilador de cristal OSC2/CLKOUT S Salida de oscilador de cristal MCLR/VPP/THV E/V Reset o entrada de voltaje de programación RA0/AN0 RA1/AN1 3 3 RA2/AN2/VREF E/S E/S E/S RA3/AN3/VREF+ E/S RA4/T0CKI E/S RA5/SS/AN4 E/S RB0/INT E/S PUERTO A es un puerto bidireccional de E/S RA0 También puede ser entrada analógica 0 RA1 También puede ser entrada analógica 1 RA2 También puede ser entrada analógica 2 o referencia analógica de voltaje negativo RA3 También puede ser entrada analógica 3 o referencia analógica de voltaje positivo RA4 Puede ser también la entrada de reloj del módulo Temporizador 0 RA5 También puede ser entrada analógica 4 o esclavo en la selección de puertos serial síncrono PUERTO B es un puerto bidireccional de E/S RB0 También puede ser pin de interrupción externa RB1, RB2 RB3/ PGM E/S E/S RB3 Puede ser programación RB4, RB5 RB6/PGC RB7/PGD E/S E/S E/S Reloj de programación serial Dato serial de programación 45 entrada de bajo voltaje de RC0/T1OSO/T1CKI E/S RC1/T1OSI/CCP2 E/S RC2/CCP1 E/S RC3/SCK/SCL E/S RC4 E/S RC5 RC6/TX/CK RC7/RX/DT VSS VDD E/S E/S E/S G V PUERTOC es un puerto bidireccional de E/S RC0 Puede ser la salida del oscilador Timer1 o entrada de reloj de Timer1 ST RC1 Puede ser la entrada del oscilador Timer1 o entrada de Captura2/salida de Captura2/PWM2 RC2 entrada Captura1/salida Comparador1/salida PWM1 RC3 puede ser entrada reloj de reloj de síncrona serial RC4 puede ser entrada de dato SPI (en modo SPI) RC5 puede ser salida de dato SPI (en modo SPI) RC6 Puede ser pin transmisión USART RC7 Puede ser pin de recepción USART Referencia de tierra Fuente positiva Fuente: MANUAL DE MICROCONTROLADOR PIC 16F873, F.I.M.E.E 4.2.2 Diagrama de bloques funcionamiento electrónico. La siguiente figura explica mediante bloques el funcionamiento básico del equipo (Ver Figura 10). Breve descripción de las etapas Acondicionamiento de la señal: Esta etapa es la encargada de: elevar el nivel de tensión generada de la excitación del tejido, mediante los electrodos del catéter que a su vez están conectados a un puente de Wheastone para comparar los valores de resistencia eléctrica, esta salida se linealiza y se pasa a un amplificador de instrumentación AD620 AN, Módulo de control principal: implementado a partir de un microcontrolador PIC16F873 de Microchip. Tiene la función de controlar las conversiones análogas a digitales y realizar los cálculos de comparación y rutinas de visualización; Su programación se llevó a cabo en lenguaje assembler 46 Figura 10. Diagrama en bloques del sistema Sensor (Electrodos) Acondicionamiento Señal Microcontrolador Puente de Wheastone Amplificador Conversor 1 A\D Conversor 2 A\D Señal de referencia Algoritmo Display LCD (Visualización) Conversor analógico-digital: Cumple la función de digitalizar la señal (niveles entre 0 y 5V) entregada por la etapa de acondicionamiento para ingresarla al Módulo de Control Principal Señal de referencia (calibración): Previo al comienzo de cada examen, el equipo lleva a cabo una rutina de calibración, la cual consiste en la medición de una resistencia patrón para obtener el valor aproximado de el tejido a ubicar y tenerla en cuenta en la medición del paciente, disminuyendo así errores por posibles cambios por temperatura o envejecimiento de los componentes. Para ello consta de un potenciómetro de precisión conectado a la entrada del conversor 2. LCD: Posibilitan la lectura de los de los datos de la medición. 47 4.2.3 Diagrama de flujo funcionamiento electrónico. La siguiente figura explica mediante un diagrama de flujo los procesos del circuito electrónico (Ver Figura 11). Figura 11. Diagrama de flujo funcionamiento electrónico. Fuente: Autor. 48 4.2.4 Puente de Wheatstone. Es el encargado de asociar un desbalance en los valores de impedancia a valores de voltaje, Como el valor las resistencias R están balanceadas en 400Ω para permitir un voltaje dentro del rango de 0 a 5V D.C. Permitiendo así al conversor análogo digital comparar los voltajes a la entrada (Ver Figura 12). Figura 12. Circuito Propuesto Fuente: Autor. La ganancia del amplificador AD620 se fija con la ayuda de una resistencia externa llamada RG, o más precisamente por cualquier impedancia ubicada entre los pines 1y 8, este amplificador está diseñado para ganancias con errores del orden de 0.1%–1%, se muestra los valores requeridos en RG para diferentes ganancias (Ver Tabla 3). Nótese que G = 1, la RG se encuentra desconectada (RG = ∞) Cualquier ganancia se puede calcular mediante la siguiente fórmula: 49 Tabla 3. Valores requeridos para RG Fuente: ANALOG DEVICES INC., AD620 Low Cost, Low Power Instrumentation Amplifier Data Sheet, 1999. ERRORES DE MEDICIÓN RELACIONADOS CON EL AMPLIFICADOR: Se atribuyen los errores bajos del AD620 a dos fuentes, la entrada y a los errores del rendimiento. El error del rendimiento es dividido por G cuando se refiere a la entrada. En la práctica, los errores de la entrada dominan a las ganancias altas y los errores del rendimiento dominan a las ganancias bajas. El VOS total para una ganancia dada es calculado como: El Error total RTI = el error de la entrada + (el error/G del rendimiento) El Error total RTO = (el error de la entrada ´ G) + el error del rendimiento PROTECCIÓN DE LA ENTRADA: El AD620 ofrece 400 W de serie la resistencia de película delgada en sus entradas, y resistirá las cargas excesivas de la entrada seguramente de a ±15 V o ±60 mA durante varias horas.22 22 ANALOG DEVICES INC., AD620 Low Cost, Low Power Instrumentation Amplifier Data Sheet, 1999. 50 4.2.5 Esquemático general de conexiones. La configuración de conexión del microcontrolador 16F873 y sus accesorios es la siguiente (Ver Figura 13). Figura 13. Esquemático general de conexiones Fuente: Autor. La señal de referencia es un nivel de voltaje entro 0 y 5V D.C. Ajustable con un potenciómetro, este voltaje se aplica a la entrada de un segundo conversor Análogo-Digital para compararlo con la señal medida. El LED a la salida del Pin 15 se enciende cuando el valor de referencia es igual al valor medido, esto me sirve como un indicador adicional al display LCD. 51 4.3 DESARROLLO MECÁNICO Esta es la posible apariencia del sistema completo, el modelamiento CAD de todas las piezas del sistema se trabajaron con SOLID EDGE V19 licencia académica (Ver Figura 14). Figura 14. Sistema completamente ensamblado Los materiales sugeridos para conformar cada elemento y los factores que se deben considerar en el diseño se explicaran más adelante, el posible comportamiento de los componentes se simula con el software de elementos finitos NASTRAN®; Las Unidades de medida utilizadas son según Sistema Internacional (SI). 52 Figura 15. Partes del Sistema 4.3.1 Sistema de Guía. Para poder tener un control sobre los movimientos angular y lineal o de profundidad trasmitidos de la mano del especialista a el Nano puente. Dado que estos movimientos son muy delicados, se optó por implementar en el diseño una perilla de control manual y no un medio distinto como motores u actuadores (Ver Figura 16). 53 Figura 16. Perilla. Simulación: Una fuerza de 50N es aplicada en la cara externa de la perilla y es soportada por la superficie de la parte superior de la pistola. • Características del material: Material Name ABS Plastic, medium impact Mass Density 1024,000 kg/m^3 54 Young's Modulus 2275269,810 kPa Poisson's Ratio 0,400 Thermal Expansion Coefficient 0,0001 /C Thermal Conductivity 0,002 kW/m-C Yield Strength 43436,969 kPa Ultimate Strength 0,000 kPa • Tipo de Elemento utilizado para el análisis: Mesh Type Tetrahedral Mesh Number of elements 1.134 Number of nodes 2.395 Solver Type Nastran • Análisis de Esfuerzos: Figura 17. Esfuerzos en la Perilla 55 • Análisis de desplazamientos: Figura 18. Deformación en la Perilla • Factor de seguridad: • Análisis de resultados: La carga es distribuida uniformemente y no se compromete el diseño, el borde más delgado ubicado en el eje “Y” de la perilla es la zona con mayor concentración de esfuerzos. Funcionamiento: los movimientos son transmitidos directamente al Nano puente que está en el interior del catéter, La perilla posee un indicador visual de ángulo y una escala de profundidad para facilitar la manipulación por parte del especialista. 56 Figura 19. Perilla de ajuste angular y profundidad. 4.3.2 Cable flexible Guía. Este componente es el encargado de trasmitir los movimientos que se generan con la perilla de ajuste. Para cumplir esto, el cable guía debe ser de tipo Straight Tip es decir de punta recta, el cable guía disponible en el mercado es el modelo Cordis Emerald 502-558 (Ver Tabla 3). Tabla 4. Cables Guía disponibles. Fuente: Cordis Corporation, Emerald Guidewires Ordering Catalog, 2008. La característica más importante de este cable guía es para su correcto funcionamiento, requiere de un bajo coeficiente de fricción entre la superficie interna del catéter y el cable para poder manipular muy suavemente al Nano puente, para poder lograr esto, el cable guía tiene un recubrimiento superficial en teflón ante la imposibilidad de utilizar lubricantes de otro tipo como aceites o grasas y además tiene una textura en anillos muy finos que reducen al área de contacto con el interior del catéter, además de un recubrimiento en heparina que es un compuesto químico hemolítico que previene la obstrucción por trombosis (Ver Figura 20). 57 Figura 20. Cable flexible guía. 4.3.3 Collarín de sujeción del dispositivo. La unión entre el cable guía y el Nano puente es un sub-conjunto denominado “Collarín de sujeción” el cual está compuesto por un cuadrante y un collarín (Ver figura 21). Figura 21. Componentes collarín. Cuadrante Imán cerámico • Cuadrante: La función del cuadrante es auto-alinear la punta del catéter con respecto al Nano puente y así tener un ajuste al eje cuadrado, la parte superior es más ancha que el fondo para facilitar la entrada del dispositivo como una especie de embudo, además permite transmitir los movimientos angulares al Nano puente. 58 • Imán cerámico: Por medio de atracción magnética mantiene unido al Nano puente con el cable guía, por su pequeño tamaño se sugiere un material de alto poder atractivo como el Neodimio (Ver Figura 22). Figura 22. Unión Collarín-Nano puente. Figura 23. Collarín. 59 4.3.4 Diseño del Catéter. Se deben considerar que camino del catéter es a través de la vena subclavia vía vena cava superior, la cual sirve de acceso al endocardio y tiene un diámetro interno de aproximadamente 8 milímetros; la flexibilidad es el parámetro clave para lograr llegar al tejido endocárdico y finalmente al nodo AV, para el diámetro interno del catéter se tiene debe ser coherente con el tamaño del dispositivo y del collarín de unión (Ver Figura 24). Figura 24. Catéter. 4.3.5 Electrodos. Los electrodos son los componentes generalmente metálicos que conducen la señal eléctrica desde el endocardio al circuito electrónico. El diseño y los materiales de los catéteres electrodos influyen en su desempeño, estabilidad y características de manipulación. Para este diseño en particular, la medición de la impedancia del tejido especializado del Nodo AV es la principal tarea a realizar por los electrodos, esta permite la ubicación óptima del dispositivo de estimulación. Para el diseñar los electrodos del catéter, se consideran tres factores principales: Propiedades estructurales, Propiedades eléctricas y costos de fabricación Propiedades Eléctricas Están directamente relacionadas con la estructura molecular del conductor y su facilidad para llevar la corriente si, junto con el otro factor que determina la naturaleza del comportamiento eléctrico que es la forma geométrica del electrodo, de la forma geométrica se destacan el área transversal, la longitud y la superficie activa de contacto como las variables más relevantes. El uso de nuevas formas de poliuretano y silicona para el aislamiento ha permitido desarrollar catéteres electrodos más flexibles y fáciles de manipular, y con ninguno se generan problemas relacionados con su coeficiente de fricción. 60 Factores como la distancia entre electrodos, el tamaño del cátodo, y el material de aislamiento influyen sobre la rigidez del catéter y la transmisión de fuerza sobre la pared miocárdica, provocando traumatismo, inflamación y hasta perforación cardíaca.23 Propiedades Estructurales Los electrodos al ser componentes del catéter, también tienen que ayustarse a los limitantes de diseño del mismo y no afectar ni su flexibilidad ni su resistencia mecánica, tampoco debe afectar las mediciones por una autoinducción generada por la corriente. Diseño Propuesto: Para cumplir con estos requerimientos, se propuso el diseño de doble hélice contraria para los cables que llevan la señal desde los electrodos a la etapa de acondicionamiento de señal, a continuación se explica con mayor profundidad este diseño. El cátodo se une a la pistola por un cable en espiras que va con el sentido de las manecillas del reloj (color plata), y a su vez del ánodo sale otro cable (Dorado) con una hélice con sentido contrario a las manecillas del reloj dorada (Ver Figura 25). Figura 25. Cables electrodos. De esta manera logramos contrarrestar la posible fuerza producida por la inducción de la corriente que pasa por las espiras y además se contribuye a 23 HAYES DL, GRAHAM KJ, IRWIN M, VIDAILLET H, DISLER G, SWEESY M ET AL. Multicenter experience with a bipolar tined polyurethane ventricular lead. Pacing Clinical Electrophysiogy, 1995, 999-1004p. 61 fortalecer la pared del catéter. Puntas de los Electrodos Las puntas de los electrodos son las superficies de exploración que entraran en contacto directo con el tejido del endocardio. Para estas superficies, la configuración más común es de anillo-punta, donde la punta es el ánodo y el anillo distal es cátodo para realizar mediciones endocavitarias, pero como este catéter es de medición y transporte, la configuración cambia (Ver Figura 26). Figura 26. Electrodo. 62 Figura 27. Detalle Electrodo. Este diseño particular propone dos electrodos en forma de anillos, guardando similitud con los electrodos tradicionales, pero reemplaza la punta ciega proximal del catéter por otro anillo, para tener una salida para el canal de transporte del catéter. Los catéteres son fabricados con compuestos de silicona; generalmente son de color Cian (Ver Figura 28). Figura 28. Descripción electrodos. La escala catéter francesa (abreviada como Fr, pero también a menudo como FR o F) normalmente se utiliza para medir el diámetro exterior de instrumentos médicos cilíndricos como los catéteres. La Medida francesa fue inventada por el fabricante Parisino de instrumentos quirúrgicos Joseph-Frédéric-Benoit Charrière en el siglo IXX. En el sistema de la Medida francés como él también es conocido, el diámetro en los milímetros del catéter puede determinarse dividiendo el tamaño francés por 3, así un tamaño francés creciente corresponde con un catéter del diámetro más grande. Las ecuaciones siguientes resumen las relaciones: D(mm) = Fr/3 o Fr = D(mm)*3 Por ejemplo, si el tamaño francés es 9, el diámetro es 3 mm. 63 Para usos industriales se fijaron los valores del 3 al 34 en la escala francesa como el estándar a aplicar para el diseño de catéteres (Ver Tabla 4). Tabla 5. Escala Francesa French Catheter Scale *sizes are Outside Diameter French INCH mm 3 0.039 1 4 0.053 1.35 5 0.066 1.67 6 0.079 2 7 0.092 2.3 8 0.105 2.7 9 0.118 3 10 0.131 3.3 11 0.144 3.7 12 0.158 4 13 0.170 4.3 14 0.184 4.7 15 0.197 5 16 0.210 5.3 17 0.223 5.7 18 0.236 6 19 0.249 6.3 20 0.263 6.7 22 0.288 7.3 24 0.315 8 26 0.341 8.7 28 0.367 9.3 30 0.393 10 32 0.419 10.7 34 0.445 11.3 Fuente:The French Catheter Scale, Dirección URL: http://www.texloc.com/closet/cl_french_scale.html, Última actualizacion enero de 2005 64 Las variables a considerar en las puntas del electrodo son la superficie activa proximal, la superficie activa distal y la distancia entre polos (Ver Tabla 5). Tabla 6. Comparación de las especificaciones de tres modelos de catéteres que utilizan electrodos endocavitarios. Tendril® Capsurefix Novus® 5076 (Medtronic®) Bipolar Transvenoso 52 cm/59 cm 2,4 mm 1488T (St Jude Medical®) Bipolar transvenoso 52 y 58 cm 2,1 mm 8 French 7 French 7 French 5,7 mm2 8,0 mm2 4,2 mm2 35 mm2 16 mm2 22 mm2 11,0 mm 13,8 mm 10,0 mm Activa 1,9 mm Activa 1,8 mm Activa 1,8 mm Sí Sí Sí Silicona Silicona Silicona IS-1 Acetato dexametasona IS-1 Dexametasona fosfato IS-1 Acetato dexametasona Flextend® 4087/4088 (Guidant Corp®) Tipo de electrodo Longitud Diámetro externo Tamaño introductor Superficie activa punta Superficie activa anillo Distancia entre polos Tipo de fijación Tamaño hélix retráctil Hélix activo Aislamiento externo Tipo de conector Esteroides Bipolar transvenoso 52 y 58 cm 2,0 mm Fuente: FRANGINI S Patricia, Ismael Vergara S, Rolando González A, Alejandro Fajuri N, Mariana Baeza La Comparison Of Three Brands Of Intracardiac Pacemarker Leads,. Rev Méd Chile 2006; 134: 1427-1435 Distancia entre Polos: La elección de esta distancia es una medida suficiente como para realimentar el potencial aplicado al tejido, se optó por una distancia comúnmente utilizada que es de 10 milímetros entre los polos del electrodo. 65 Superficie activa distal Con base en el diseño Tendril® 14887 de St. Jude Medical®. Se dimensionan los anillos proximal y distal: Figura 29. Superficie activa. Estos 16 mm2, al tener una superficie relativamente pequeña, la flexibilidad no se ve afectada y es muy sencillo fabricarlos a partir de láminas planas, deben ser materiales de excelente conductividad eléctrica. 4.3.6 Conjunto pistola y caja de circuitos. El diseño propuesto es el de un dispositivo liviano y totalmente desechable (Ver Figura 30). Figura 30. Conjunto pistola Está compuesto por una caja inferior de circuitos y una cubierta superior encargada de mantener unidos la perilla y el catéter como un todo; la caja de circuitos como su nombre lo indica es la encargada de contener los circuitos electrónicos, tiene un diseño anatómico de bordes redondeados para mayor 66 comodidad y fácil manipulación. Simulación: Análisis de presiones de 0,5 KPa aplicadas sobre los costados de la caja de circuitos, simulando un apretón fuerte con la mano. • Características del material: Material Name ABS Plastic, medium impact Mass Density 1024,000 kg/m^3 Young's Modulus 2275269,810 kPa Poisson's Ratio 0,400 Thermal Expansion Coefficient 0,0001 /C Thermal Conductivity 0,002 kW/m-C Yield Strength 43436,969 kPa Ultimate Strength 0,000 kPa • Tipo de Elemento utilizado para el análisis: Mesh Type Tetrahedral Mesh Number of elements 26.868 Number of nodes 54.195 Solver Type Nastran • Análisis de Esfuerzos: 67 Figura 31. Esfuerzos en la Caja de Circuitos • Análisis de desplazamientos: Figura 32. Deformación en la Caja de Circuitos 68 • Factor de seguridad: • Análisis de resultados: La carga es distribuida uniformemente y no se compromete el diseño, El espesor de la pared es suficiente como para garantizar la integridad de la pieza bajo este tipo de cargas. Figura 33. Caja de Circuitos 69 Simulación: Una fuerza de 50N es aplicada sobre la cara externa de la tapa, la restricción es la cara opuesta sobre la caja de circuitos. • Características del material: Material Name ABS Plastic, medium impact Mass Density 1024,000 kg/m^3 Young's Modulus 2275269,810 kPa Poisson's Ratio 0,400 Thermal Expansion Coefficient 0,0001 /C Thermal Conductivity 0,002 kW/m-C Yield Strength 43436,969 kPa Ultimate Strength 0,000 kPa • Tipo de Elemento utilizado para el análisis: Mesh Type Tetrahedral Mesh Number of elements 3.852 Number of nodes 8.201 • Análisis de Esfuerzos: 70 Figura 34. Esfuerzos en la Tapa Frontal • Análisis de desplazamientos: Figura 35. Deformación en la Tapa Frontal 71 • Factor de seguridad: • Análisis de resultados: La deformación es mínima debido a que el apoyo en el borde interno de la tapa sobre la caja de circuitos distribuye de manera uniforme la carga aplicada y restringe los movimientos; la mayor concentración de esfuerzos se observa sobre el borde superior e inferior. Figura 36. Tapa Frontal. 72 La caja se cierra a presión por acción de la tapa (macho) que se une a cuatro soportes ubicados en la caja (hembra) o caja de circuitos (Ver Figura 38). Figura 37. Tapa. Figura 38. Unión Tapa Frontal. La tapa es muy fácil de retirar debido a que no tiene tornillos o uniones móviles; además tiene una apertura para la pantalla LCD y botón de ON-OFF, La caja de circuitos tiene un perfil en su parte superior que permite deslizar la pieza con la perilla y el catéter, esto facilita su ensamblaje y también separar con facilidad los circuitos electrónicos del resto de la pistola (Ver Figura 29). Figura 39. Caja de Circuitos abierta. 73 La parte superior tiene marcas de referencia para el control de profundidad y de ángulo de inclinación, junto con la caja de circuitos es completamente desechable, es transparente para permitir la visualización de la perilla entrando y girando a la vez (Ver Figura 40). Figura 40. Detalle parte superior descartable. Simulación: Analisis bajo una fuerza de compresion de 0.5 kPa aplicada por la perilla sobre la parte superior de la pistola. • Características del material: Material Name ABS Plastic, medium impact Mass Density 1024,000 kg/m^3 Young's Modulus 2275269,810 kPa Poisson's Ratio 0,400 Thermal Expansion Coefficient 0,0001 /C Thermal Conductivity 0,002 kW/m-C Yield Strength 43436,969 kPa Ultimate Strength 0,000 kPa • Tipo de Elemento utilizado para el análisis: Mesh Type Tetrahedral Mesh Number of elements 35.903 Number of nodes 59.969 Solver Type Nastran 74 • Análisis de Esfuerzos: Figura 41. Esfuerzos en la Parte Superior • Análisis de desplazamientos: 75 Figura 42. Deformación en la Parte Superior • Factor de seguridad: • Análisis de resultados: La deformación de la pieza es mínima debido a la solidez del diseño y a las propiedades mecánicas del ABS, el mayor desplazamiento se dio en el mismo eje de compresión y en el eje normal a este con un ensanchamiento; se observa que no hay un lugar específico donde las fuerzas se concentren sino que se distribuyen uniformemente. 76 Figura 43. Parte superior descartable. 77 5. PRESENTACION Y ANALISIS DE RESULTADOS Las mediciones simuladas en NI CIRCUIT DESIGN SUITE VERSION 10.0.1 de National Instruments Corporation ©, para el circuito propuesto arrojaron los siguientes datos (Ver Tabla 6). Tabla 7. Valores de Voltaje a la Salida del Amplificador. Vin (V) 0.904 0.955 1.007 1.217 1.427 1.617 1.807 1.979 2.151 2.307 2.464 2.607 2.750 2.881 3.012 3.132 3.253 3.364 3.475 3.578 LCD (Ω) 450 475 500 525 550 575 600 625 650 675 700 725 750 775 800 825 850 875 900 925 Donde Rg=49kΩ determina un porcentaje de error en la amplificación del orden de 0.1%–1. Incrementando el valor de la resistencia entre los electrodos en un valor constante de 25Ω y luego graficando el valor del voltaje la salida del AD620, podemos analizar cómo se comporta la entrada de voltaje (Ver Figura 32). 78 Figura 44. Relación entre el voltaje y la resistencia. Se observa como la variación de la resistencia respecto al voltaje es la salida del amplificador de instrumentación es muy aproximada la una respuesta linealmente proporcional, el valor del voltaje de 1,007V en la entrada microcontrolador es el apropiado para localizar tejidos especializados de aproximadamente 500Ω, recodemos que generalmente los tejidos vivos tienden a tener un valor de resistencia eléctrica elevada. Cuando los valores medidos son superiores a 925Ω o menores de 450 Ω no son detectados (fuera de rango) porque el conversor análogo digital solo toma voltajes entre 1 y 5V. 79 6. CONCLUSIONES Los voltajes provenientes de señales biológicas son muy débiles y requieren frecuentemente de un amplificador de instrumentación para poder tener niveles de voltaje apropiados para los microcontroladores PIC. La resolución máxima del microcontrolador PIC 16F873 es de 19.56mV por paso, suficiente para realizar la comparación de impedancias, aunque la programación del microcontrolador fija 25Ω como la medida mínima posible, con la ayuda del LED indicador es posible tener una medición un poco más sensible al implementar el sistema. El uso plástico ABS es una excelente opción para fabricar dispositivos descartables por su bajo costo, facilidad de manejo y naturaleza inerte, los recubrimientos superficiales de heparina y teflón son un avance muy importante en la fabricación de catéteres, porque reducen la fricción, evitan riesgos de obstrucción y trombosis. Las herramientas de simulación electrónica son un apoyo útil en el momento de analizar el comportamiento de circuitos no-lineales como puentes de resistencias. El sistema propuesto puede ser fácilmente implementado como complemento a las futuras pruebas con células de endocardio vivas, por razones ajenas a esta investigación estas pruebas no se consiguieron realizar. 80 7. RECOMENDACIONES Para tener una lectura correcta del instrumento y evitar fallos, se recomienda revisar el nivel de carga de la batería o utilizar siempre una nueva, o en su defecto una fuente regulada. Para evitar descargas accidentales de estática, se recomienda disponer de elementos que neutralicen este fenómeno. La calibración del sistema debe realizarse en lo posible con un instrumento de tipo patrón o un multímetro de alta precisión, apoyados previamente siempre de estudios electrofisiológicos. Para futuros estudios el uso de un microcontrolador de mayor capacidad (16 o 32 bits) podría ofrecer una mayor resolución y capacidad de análisis en frecuencia. 81 BIBLIOGRAFIA ANALOG DEVICES INC., AD620 Low Cost, Low Power Instrumentation Amplifier Data Sheet, 1999. ANTZELEVITCH C, Yan GX, Shimizu W, Burashbikov A, Electrical heterogeneity, the ECG, and cardiacarrhythmias, Philadelphia, W.B. Saunders Co., 1999. CHIRIFE, Physiological principles of a new method for rate responsive pacing using the pre-ejection interval, PACE 1988,1545-1554p FYE WB. American Cardiology. The History of a Specialty and Its College. Baltimore, Md: The Johns Hopkins University Press, 1996. Geddes LA, Geddes LE. The Catheter Introducers. Chicago, Ill: Mobium Press, 1993, 38–39p. HAYES DL, GRAHAM KJ, IRWIN M, VIDAILLET H, DISLER G, SWEESY M ET AL. Multicenter experience with a bipolar tined polyurethane ventricular lead, Pacing Clinical Electrophysiogy, 1995, 999-1004p. ICIPC. Introducción a los Materiales Plásticos, Medellín, Julio 1996. MANOLIS, Simeonidou E, Sousani E, Chiladakis J. Alternate sites of permanent cardiac pacing: A randomized study of novel technology, Hellenic J Cardiology 2004, 145-149p. MYERBURG, Kessler KM, Castellanos A, Sudden cardiac death: Structure, function and time-dependence of risk, 1992. OXFORD University, Signal Processing & Neural Networks Group, Dept. of Engineering Science, 2001. PARSONNET V. Bernstein AD, Perry GY.The nuclear pacemaker: Is renewed interest warranted. Am J Cardiol 1990, 837-842p. PUURTINEN Merja. “Bioamplifier Work”. Tampere University of Technology, Ragnar Granit Institute, Medical Electronics Laboratory, 2003 REVISTA CUBANA DE CARDIOLOGÍA, Bloqueo AV Cardiaco, Página: 82 2001, 56-60 p. 82 REYNOLDS Pombo Jorge, 30 Años de Estimulación Cardiaca en Colombia, Ed. Andes, Bogotá, 1988 RYAN TJ, The coronary angiogram and its seminal contribution to cardiovascular medicine over five decades, Circulation. 2002, 752–756p. SCHEINMAN MM,Morady F,Hess DS,Gonzalez R. Catheter-induced ablation of the atriovetricular junction to control refractory supraventricular arrhythmias, JAMA 1982, 851-855p. SCHOENFELD, Compton SJ, Mead RH, Weiss DN, Sherfesee L, Englund J, Mongeon LR Remote monitoring of implantable cardioverter defibrillators: a prospective analysis, PACE, 2004. SUN, W Cameron, S Heymsfield, H Lukaski, D Schoeller, K Friedl, R Kuczmarsyi, K Flegal, C Johnson, V Hubbard, Development of Bioelectrical Impedance Analysis Prediction Equations for Body Composition with the use of a Multicomponent model for use in Epidemiologic Surveys, American Society for Clinical Nutrition, 2003. UNIVERSIDAD DE JAEN, Adquisición de Magnitudes Microcontrolador, Granada, España, Julio de 2000, 83 Físicas Mediante ANEXOS. ANEXO A. Programa microcontrolador List p=16F873 include "p16f873.inc"; __config(_PWRTE_OFF & _XT_OSC & _WDT_OFF & _CP_OFF & _DEBUG_OFF &_CPD_OFF &_LVP_OFF &_BODEN_OFF ) #DEFINE BANK0 BCF STATUS,5 #DEFINE BANK1 BSF STATUS,5 #DEFINE RS PORTC,5 #DEFINE EN PORTC,6 #DEFINE CARRY STATUS,0 #DEFINE ZERO STATUS,2 REG1 EQU 0X20 REG2 EQU 0X21 REGA EQU 0X23 REGB EQU 0X24 REGC EQU 0X25 CounterA EQU 0X26 CounterB EQU 0X27 CounterC EQU 0X28 CONTABLA EQU 0X29 REGSEG EQU 0X2A DEC1 EQU 0X2B UNI1 EQU 0X2C DEC EQU 0X2D CEN EQU 0X2E DAT10 EQU 0X2F DAT11 EQU 0X30 DAT12 EQU 0X31 REGIS EQU 0X32 SETS EQU 0X33 ORG 0X00 GOTO INICIO TABLA1 ADDWF PCL,1 RETLW "R" RETLW "r" RETLW "e" ; PRIMERA LINEA 84 RETLW "f" RETLW "" RETLW "=" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" TABLA2 ADDWF PCL,1 RETLW "R" RETLW "s" RETLW "e" RETLW "n" RETLW "" RETLW "=" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" RETLW "" INICIO ; PRIMERA LINEA BANK1 MOVLW 0XFF ;CONFIGURACION DE PUERTOS MOVWF TRISA CLRF TRISB MOVLW 0X00 MOVWF TRISC MOVLW 0X04 MOVWF ADCON1 ;CONFUGURACION DE AN_0 , AN_1 Y ADRESH BANK0 CALL RETARDO CLRF REG1 CLRF REG2 MOVLW 0X38 CALL SCONTROL 85 MOVLW 0X38 CALL SCONTROL MOVLW 0X38 CALL SCONTROL MOVLW 0X38 CALL SCONTROL MOVLW 0X02 ; CURSOR A CASA CALL SCONTROL MOVLW 0X28 ; 8 BITS 2 LINEA CALL SCONTROL MOVLW 0X06 ; MENSAJE FIJO CALL SCONTROL MOVLW 0X0C ; DISPLAY ON CALL SCONTROL MOVLW 0X01 CALL SCONTROL CALL MENS1 CALL MENS2 ADCMAS CALL RETARDO ;SUBRUTINA DE CONVERSION ANALOGA DIGITAL MOVLW 0X01 MOVWF ADCON0 NOP NOP NOP NOP NOP NOP BSF ADCON0,2 ;GO DONE NOP NOP NOP LLL BTFSC ADCON0,2 GOTO LLL NOP NOP MOVFW ADRESH MOVWF REG1 ;****************************************************************** ADCMENOS 86 MOVLW MOVWF NOP NOP NOP NOP NOP NOP BSF NOP NOP NOP 0X09 ADCON0 BTFSC GOTO NOP NOP ADCON0,2 LLL1 ADCON0,2 ;GO DONE LLL1 MOVFW MOVWF ADRESH REG2 CALL VISU MOVFW REG1 XORWF REG2,0 BTFSS ZERO GOTOLLL2 BSF PORTC,4 GOTO ADCMAS LLL2 BCF PORTC,4 GOTO ADCMAS RETARDO ;Time Delay = .050003 s with Osc = 4.000000 MHz movlw D'65' movwf REGB movlw D'238' movwf REGA loop decfsz REGA,1 goto loop decfsz REGB,1 goto loop RETURN MENS1 87 CLRF CONTABLA MOVLW 0X80 CALL SCONTROL LOOPA MOVF CONTABLA,0 CALL TABLA1 CALL SCDATO MOVF CONTABLA,0 XORLW .13 BTFSC STATUS,2 RETURN INCF CONTABLA,1 GOTOLOOPA MENS2 CLRF CONTABLA MOVLW 0XC0 CALL SCONTROL LOOPB MOVF CONTABLA,0 CALL TABLA2 CALL SCDATO MOVF CONTABLA,0 XORLW .13 BTFSC STATUS,2 RETURN INCF CONTABLA,1 GOTOLOOPB SCONTROL BCF RS GOTO SCDATO BSF RS LOOPX NOP BSF EN MOVWF MOVLW ANDWF NOP SWAPF ANDLW IORWF LOOPX REGSEG 0XF0 PORTC,1 REGSEG,0 0X0F PORTC,1 88 CALL RTX2 BCF EN CALL RTX2 BSF EN MOVLW ANDWF NOP MOVF ANDLW IORWF CALL RTX2 BCF EN CALL RTX2 BSF EN RETURN ; TIEMPO CORTO ; TIEMPO CORTO 0XF0 PORTC,1 REGSEG,0 0X0F PORTC,1 ; TIEMPO CORTO ; TIEMPO CORTO RTX2 ;PIC Time Delay = 0,002 s with Osc = 4.0 MHz movlw D'3' movwf CounterB movlw D'151' movwf CounterA lpr decfsz CounterA,1 goto lpr decfsz CounterB,1 goto lpr return RET_FLA ;PIC Time Delay = 0,2500020 s with Osc = 4 MHz movlw D'2' movwf CounterC movlw D'70' movwf CounterB movlw D'168' movwf CounterA loop1 decfsz CounterA,1 goto loop1 decfsz CounterB,1 goto loop1 decfsz CounterC,1 goto loop1 return VISU 89 MOVFW REG1 MOVWF REGIS CALL CONV BTFSC SETS,0 GOTOVISU1 MOVLW 0X87 CALL SCONTROL MOVLW 0X30 ADDWF DAT10,1 MOVF DAT10,0 CALL SCDATO MOVLW 0X30 ADDWF DAT11,1 MOVF DAT11,0 CALL SCDATO MOVLW 0X30 ADDWF DAT12,1 MOVF DAT12,0 CALL SCDATO VISU1 MOVFW REG2 MOVWF REGIS CALL CONV BTFSC SETS,0 RETURN MOVLW 0XC7 CALL SCONTROL MOVLW 0X30 ADDWF DAT10,1 MOVF DAT10,0 CALL SCDATO MOVLW 0X30 ADDWF DAT11,1 MOVF DAT11,0 CALL SCDATO MOVLW 0X30 ADDWF DAT12,1 MOVF DAT12,0 CALL SCDATO RETURN CONV MOVLW XORWF BTFSS 0X2B REGIS,0 ZERO 90 GOTO$+.6 MOVLW .4 MOVWF DAT10 MOVLW .5 MOVWF DAT11 GOTOCERO MOVLW 0X2D XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .4 MOVWF DAT10 MOVLW .7 MOVWF DAT11 GOTOCINCO MOVLW 0X30 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .5 MOVWF DAT10 MOVLW .0 MOVWF DAT11 GOTOCERO MOVLW 0X3C XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .5 MOVWF DAT10 MOVLW .2 MOVWF DAT11 GOTOCINCO MOVLW 0X46 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .5 MOVWF DAT10 MOVLW .5 MOVWF DAT11 91 GOTOCERO MOVLW 0X4F XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .5 MOVWF DAT10 MOVLW .7 MOVWF DAT11 GOTOCINCO MOVLW 0X59 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .6 MOVWF DAT10 MOVLW .0 MOVWF DAT11 GOTOCERO MOVLW 0X61 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .6 MOVWF DAT10 MOVLW .2 MOVWF DAT11 GOTOCINCO MOVLW 0X6A XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .6 MOVWF DAT10 MOVLW .5 MOVWF DAT11 GOTOCERO MOVLW XORWF 0X72 REGIS,0 92 BTFSS ZERO GOTO$+.6 MOVLW .6 MOVWF DAT10 MOVLW .7 MOVWF DAT11 GOTOCINCO MOVLW 0X7A XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .7 MOVWF DAT10 MOVLW .0 MOVWF DAT11 GOTOCERO MOVLW 0X81 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .7 MOVWF DAT10 MOVLW .2 MOVWF DAT11 GOTOCINCO MOVLW 0X89 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .7 MOVWF DAT10 MOVLW .5 MOVWF DAT11 GOTOCERO MOVLW XORWF BTFSS GOTO$+.6 MOVLW MOVWF 0X8F REGIS,0 ZERO .7 DAT10 93 MOVLW .7 MOVWF DAT11 GOTOCINCO MOVLW 0X96 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .8 MOVWF DAT10 MOVLW .0 MOVWF DAT11 GOTOCERO MOVLW 0X9C XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .8 MOVWF DAT10 MOVLW .2 MOVWF DAT11 GOTOCINCO MOVLW 0XA2 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .8 MOVWF DAT10 MOVLW .5 MOVWF DAT11 GOTOCERO MOVLW 0XA8 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .8 MOVWF DAT10 MOVLW .7 MOVWF DAT11 GOTOCINCO MOVLW 0XAE 94 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .9 MOVWF DAT10 MOVLW .0 MOVWF DAT11 GOTOCERO MOVLW 0XB2 XORWF REGIS,0 BTFSS ZERO GOTO$+.6 MOVLW .9 MOVWF DAT10 MOVLW .2 MOVWF DAT11 GOTOCINCO BSF SETS,0 RETURN CERO MOVLW .0 MOVWF DAT12 BCF SETS,0 RETURN CINCO MOVLW .5 MOVWF DAT12 BCF SETS,0 RETURN END 95
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados