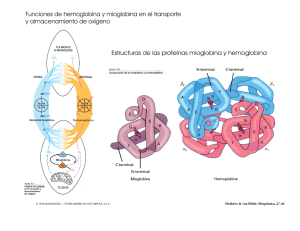
AMINOÁCIDOS Y PROTEÍNAS 1. Son las macromoléculas biológicas más abundantes 2. Se encuentran en todas las células y en todas partes dentro de las células 3. Existen miles de diferentes tipos y tamaños de proteínas 4. Exhiben una gran cantidad diversidad de funciones de Funciones Desempeñan papeles claves en casi todos los procesos biológicos: • • • • • • • catálisis enzimática transporte y almacenamiento (de iones y sust. pequeñas, ej. hemoglobina) movimiento coordinado (contracción muscular, mov. cromosómico, de esperma) soporte mecánico (ej. colágeno) protección inmune (anticuerpos) generación y transmisión de impulsos nerviosos (receptores: responsables de la transmisión de los impulsos en las sinapsis) control del crecimiento y la diferenciación (control secuencial de la expresión: represores) Cada organismo puede construir con esta base de 20 aa diferentes proteínas (aminoácidos proteinogénicos) Enzimas venenos Hormonas colágeno Anticuerpos receptores Transportadores hemoglobina (piel, huesos) Proteínas de leche Queratina lana, uñas (cuernos, escamas, pelos, Aminoácidos • Cada ser vivo sintetiza sus propias proteínas a partir de los aa. • Las plantas superiores sintetizan a su vez todos los aa necesarios, en tanto que los animales no tienen esa capacidad. Cada animal puede sintetizar sólo algunos de los que necesita, y el resto que son necesarios para formar sus proteínas debe incorporarlos de la dieta. Estos se denominan esenciales (no son los únicos necesarios sino que son los que deben estar incluídos en la dieta). Para los humanos son ocho (fenilalanina, isoleucina, leucina, lisina, metionina, treonina, triptofano y valina). Otros dos, arginina e histidina, se sintetizan en forma insuficiente en determinadas etapas. Por ejemplo la histidina es esencial durante el crecimiento pero no para el adulto. Composición • Todas las proteínas contiene C, H, O y N, y casi todas poseen además S. • El contenido de N representa ~ el 16 % de la masa total de la molécula → c / 6,25 g proteína hay 1 g de N. Este factor de 6,25 se utiliza para estimar la cantidad de proteína existente en una muestra a partir de la medición del N de la misma. • Son polímeros de alto peso molecular. Están formadas por unidades estructurales básicas llamadas aminoácidos (aa). Unidades estructurales básicas de las proteínas α- aminoácidos •un grupo amino (-NH2) •un grupo carboxilo (-COOH) •un átomo de H • un grupo distintivo R (cadena lateral) unidos al átomo de carbono α Isomería Excepto para glicina, donde R = H, los aa tienen las 4 valencias del Cα saturadas por grupos diferentes, C asimétrico o quiral. El agrupamiento tetraédrico de 4 átomos diferentes alrededor del C confiere actividad óptica a los aa → las 2 formas especulares se llaman isómero L y D. Solamente los aa L son constituyentes de las proteínas. Isómeros: compuestos diferentes con igual fórmula molecular (número y clase de átomos pero unidos de forma diferente). Algunos aa naturales tienen más de un C asimétrico, por lo tanto pueden existir más de 2 estereoisóimeros, por ej. Treonina, la isoleucina y la cistina (Unión de 2 cisteínas) •Las proteínas de todos los seres vivientes están constituidas 20 aminoácidos unidos covalentemente en diferentes combinaciones y secuencias. •Debido a que cada uno de estos aa posee una cadena lateral diferente, con diferentes propiedades químicas, este grupo de 20 moléculas pueden ser consideradas como el ALFABETO con el que se ESCRIBE el lenguaje de las proteínas. •Gracias a esta variedad las células pueden producir proteínas con propiedades físicas y funcionales totalmente diferentes AMINOÁCIDOS APOLARES AMINOÁCIDOS POLARES NO CARGADOS Tirosina (Tyr) AMINOÁCIDOS CARGADOS AMINOÁCIDOS ALIFÁTICOS NO POLARES Prolina (Iminoácido) AMINOÁCIDOS AROMÁTICOS NO POLAR POLAR NO POLAR POLARES NO CARGADOS POLARES CARGADOS POLARES CARGADOS Aminoácidos modificados Se encuentran de forma poco frecuente en las proteínas). Se producen por modificación enzimática después de que los aminoácidos precursores se han insertado en la cadena polipeptídica. • Fosfoserína • 4-hidroxiprolina • δ-hidroxilisina Colágeno •N-metil-lisina Miosina • Ac. γ carboxiglutamina Protrombina Aminoácidos no proteicos Se conocen unos 150 aminoácidos que se encuentran en distintas células y tejidos en forma libre o combinada, pero nunca en las proteínas. Derivan de los α-aa y se conocen con el nombre de beta-aa, gamma-aa y delta-aa. Ácido-gamma-aminobutírico (GABA), que es un neurotransmisor, Algunos aa no proteicos están en conformación D (acdo D-glutámico), que se encuentra en la pared celular de muchas bacterias, etc…) PROPIEDADES ÁCIDO-BASE de los aminoácidos Todos los aminoácidos poseen un grupo ácido y grupo básico ionizables (que desaparecerán cuando polimericen para formar proteínas) Algunos aminoácidos tienen una cadena lateral ionizable (que NO desaparecerán cuando polimericen para formar proteínas) Las curvas de titulación de los aminoácidos ayudan a comprender su carga en función del pH El punto isoeléctrico se localiza entre los dos pKas que delimitan la zona de pH en que predomina la especie neutra Los aa a pH neutro son IONES DIPOLARES Forma no disociada o no ionizada Forma dipolar iónica o zwetterion o ion híbrido El estado de ionización depende del pH En disolución ACIDA el grupo carboxilo no está inoizado (COOH) aa con carga + En disolución ALCALINA el grupo amino no está ionizado (NH2) aa con carga - Aa = iones dipolares ? Aa ? casi siempre se encuentran disociados, con cargas positivas y negativas sobre la misma molécula. El grupo carboxilo se comporta como ácido o dador de protones: -COOH ? COO- + H+ ? Carácter anfótero El grupo amino se comporta como base o aceptor de protones: -NH2 + H+ ? -NH3+ ? ? En sn. ácida fuerte capta un ión H a nivel del carboxilo ? se comporta como una base ? se convierte en un catión. ? En sn. alcalina fuerte los hidroxilos reaccionan con -NH3+ para formar agua. Carboxilo ? se comporta como ácido ? se convierte en un anión. CURVAS DE TITULACIÓN Capacidad de tamponamiento PUNTO ISOELÉCTRICO Capacidad de tamponamiento Curva de Valoración de la Glicina H2N-CHR-COO9.6 5.97 H3+N-CHR-COO-ÅÆ H2N-CHR-COO- H3+N-CHR-COO- 2.34 H3+N-CHR-COOH ÅÆ H3+N-CHR-COO- H3+N-CHR-COOH www.um.es/.../Quimica/Practica01/Practica01.htm Curva de Valoración de la Histidina (aa básico) Curva de Valoración del ácido glutámico (aa ácido) PROPIEDADES QUÍMICAS DE LOS AMINOÁCIDOS 1.- LIGADAS AL GRUPO –COOH 1.1.- ESTERIFICACIÓN 1.2.- FORMACIÓN DE AMIDAS 1.3.- REDUCCIÓN A ALCOHOL PRIMARIO 2.- LIGADAS AL GRUPO R 2.1.- FORMACIÓN DE PUENTES DISULFURO 3.- LIGADAS AL GRUPO –NH2 3.1.- REACCIÓN CON NINHIDRINA 3.2.- REACCIÓN CON FLUORESCAMINA 3.3.- REACCIÓN DE SANGER Y EDMAN 3.4.- REACCIÓN CON CLORURO DE DANSILO 3.5.- REACCIÓN CON CLORURO DE DABSILO PROPIEDADES QUÍMICAS DE LOS AMINOÁCIDOS 1.- LIGADAS AL GRUPO –COOH 1.- Formación ésteres Reacciones de los aminoácidos Esteres metílicos y etílicos Esteres bencílicos Se utiliza como método para proteger el grupo –COOH de los aminoácidos en la síntesis química de los péptidos Formación de amidas CH2 CH COO NH3 Fenil alanina Suspensión del alcohol con HCl anhidro del aminoácido. CH3OH HCl CH2 CH CO OCH3 NH3 90% Cl Reacciones de los aminoácidos 1.- Formación ésteres Esteres metílicos y etílicos Alcohol bencílico con bencenosulfonato o tosilato como catalizador. Esteres bencílicos Formación de amidas CH 2 OH SO3 H Se utiliza como método para proteger el grupo –COOH de los aminoácidos en la síntesis química de los péptidos H3N CH2 COO Glicina SO3 H3N CH2 CO O CH2 90% Reacciones de los aminoácidos Preferentemente en medio básico y con cloruros de ácido. Esteres metílicos y etílicos Por ejemplo cloruro de benzoilo y sosa concentrada en agua. Esteres bencílicos Formación de amidas 2.- Formación amidas H3N CH COO CH3 CH COCl CH3 4ºC HO 2h H2O CO HN CH COO CH 3 CH Valina CO HN CH COOH CH 3 CH CH 3 HCl CH3 Reacciones de los aminoácidos Esteres metílicos y etílicos Esteres bencílicos 2.- Formación amidas También por reacción con anhídrido acético Formación de amidas H 3N CH3 CH COO CH 2 NH N Histidina CH3 C O C CH3 O O 100ºC 2h C HN CH COOH CH2 O NH 80% N 3.- Reducción a alcohol primario Reducción con borohidruro de litio COOH Después BH4Li de la hidrólisis BH 4Li Se separa el amino-alcohol en medio básico (los demás ionizados y él no) BH4Li CH2OH R NH2 C H Amino alcohol 2.- LIGADAS AL GRUPO R 1.- Formación del puente disulfuro 3.- LIGADAS AL GRUPO –NH2 1.Reacción con la ninhidrina Tiene como objetivo detectar y cuantificar cantidades de aminoácidos libres. Los aminoácidos, en general reaccionan con la ninhidrina (hidrato de hicelohidrindeno) cuando son calentados con un exceso de la misma. Todos los aminoácidos que poseen un grupo amino libre reaccionan y forman dióxido de carbono, amoníaco y un aldehído que contiene un átomo de carbono menos que el compuesto original. Esta reacción da lugar a la formación de un producto color azul o púrpura (que posteriormente puede ser utilizado para cuantificar el aminoácido). En el caso de la prolina, que estructuralmente no posee el grupo amino libre, sino un grupo imino, la coloración final es amarilla. El amoníaco, la mayoría de los polipéptidos y las proteínas pueden desarrollar coloración en esta reacción, pero a diferencia de los aminoácidos, no liberan CO2. Recuerde que la coloración azulada o violeta será proporcional a la concentración del aminoácido 3.- LIGADAS AL GRUPO –NH2 1.Reacción con la ninhidrina La ninhidrina (hidrato de tricetohidrindeno) reacciona con aminoácidos que tengan el grupo amino libre, dando lugar a la formación de amoniaco y anhídrido carbónico, con reducción del reactivo (ninhidrina) a hidrindantina. La hidrindantina reacciona a su vez con el amoniaco y otra molécula de ninhidrina para dar un compuesto de adición doble que presenta una coloración azulpúrpura, con la excepción de la prolina e hidroxiprolina que dan una coloración amarillenta 1.Reacción con la ninhidrina 2.Reacción con la fluorescamina (producto fluorescente) La fluorescamina reacciona rápidamente con los a.a. proporcionando una gran sensibilidad al formar un derivado altamente fluorescente, que permite la detección de a.a. del orden de nanogramos. 3.Reacción con reactivo de Sanger Se forman derivados 2,4 –dinitrofenilados. Dichos compuestos son de color amarillo. Reactivos para identificar NH2 terminales 2,4-dinitrofluorbenceno FDNB Después de la hidrólisis NO2 NO2 F Amarillo, se extrae con cloroformo (los demás productos de hidrólisis ionizados no se extraen) N O S Cl O COOH R NH C H 2,4 dinitrofenilaminoácido DNS-Cl Este método es más sensible que el anterior y es alrededor de 100 veces más sensible que el de Sanger Después de la hidrólisis CH3 CH 3 CH 3 NO2 NO2 4.Reacción con cloruro de dansilo Cloruro de dimetilaminonaftalen-5-sulfonilo Cloruro de dansilo Sanger CH 3 Análogo a FDNB pero fluorescente (detecta cantidades mínimas) COOH N O S O R C H NH PROPIEDADES ESPECTRALES DE LOS AMINOÁCIDOS PROPIEDADES ESPECTRALES DE LOS AMINOÁCIDOS 1.- ENANTIÓMEROS O ESTEREOISÓMEROS Formas D- y L. Depende de la presencia de carbonos quirales o asimétricos 2.- DIASTEREOISÓMEROS Cuando existe más de 1 carbono asimétrico. Aparecen las formas alo- (Thr e Ile) y meso- (cistina) Histidina Estructura resonante TAUTÓMERO A TAUTÓMERO C FORMA ÁCIDA PROPIEDADES ÓPTICAS DE LOS AMINOÁCIDOS Se obtiene luz polarizada en un plano haciendo pasar luz blanca a través de un filtro polarizador. Si el plano de la luz polarizada pasa a través de una sustancia y rota en un ángulo llamado a , se dice que esta sustancia es ópticamente activa. Si el plano de la luz polarizada rota hacia la izquierda, este compuesto se designa como levorrotatorio (-). Si el plano rota hacia la derecha, el compuesto es dextrorrotatorio (+) Como el ángulo a obtenido en el polarímetro depende, además de la naturaleza del compuesto, de la concentración de la muestra y del paso de luz, se ha definido la rotación específica ([a ]D25) que permite caracterizar al compuesto. Rotación específica TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE AMINOÁCIDOS 1.- Técnicas cromatográficas 1.1.- Cromatografía de partición 1.2.- Cromatografía de intercambio iónico 1.3.- Cromatografía líquida de alta presión 2.- Técnicas electroforéticas 3.- Técnicas de identificación Reacciones químicas que forman complejos coloreados o fluorescentes. 1.- Técnicas cromatográficas Cromatografía de partición o de reparto Base del coeficiente de reparto En papel Definición de Rf (Prácticas) Fase móvil Fase estacionaria En columna Definición de coeficiente de reparto 1.- Técnicas cromatográficas Cromatografía de partición o de reparto 1.- Técnicas cromatográficas Cromatografía de partición o de reparto Cromatografía de Intercambio iónico Las moléculas se separan en función basándose en las diferencias de comportamiento ácido-base. La columna se llena con una resina que contiene grupos cargados fijos. Existen de 2 tipos: 1.- Intercambio catiónico, 2.- intercambio aniónico. Se le añade una disolución ácida de aa (carga neta +). Los aminoácidos básicos se Unirán a la resina por fuerzas electrostáticas y los más ácidos se unirán menos. Se eluirán de forma distinta. + + + + + + + + + Intercambio iónico - + - + + - + + + + - Proteínas adsorbidas al intercambiador iónico + + -- - + - - - A baja concentración de sal, se desprenden las proteínas menos electronegativas + + + + + + + + - - - - - - - - A mayor concentración de sal se desprenden las proteínas más electronegativas Cromatografía líquida de alta presión (HPLC) Gases disueltos Desgasificador de disolventes Precolumna Jeringa o válvula para la muestra Introducción de la muestra Espacio térmico Abastecimiento de disolvente Filtro Medidor de presión Bomba Válvula de seguridad y purga Descarga Columna analítica Lectura Amplificador Recolección o descarga En la HPLC el compuesto pasa por la columna cromatogràfica a través de la fase estacionaria (normalmente, un cilindro con pequeñas partículas redondeadas con ciertas características químicas en su superficie) mediante el bombeo de líquido (fase móvil) a alta presión a través de la columna. La muestra a analizar es introducida en pequeñas cantidades y sus componentes se retrasan diferencialmente dependiendo de las interacciones químicas o físicas con la fase estacionaria a medida que adelantan por la columna. El grado de retención de los componentes de la muestra depende de la naturaleza del compuesto, de la composición de la fase estacionaria y de la fase móvil 1.- Cromatografía de fase normal Esta técnica utiliza una fase estacionaria polar y una fase móvil apolar, y se utiliza cuando el compuesto de interés es bastante polar. El compuesto polar se asocia y es retenido por la fase estacionaria. La fuerza de adsorción aumenta a medida que aumenta la polaridad del compuesto y la interacción entre el compuesto polar y la fase estacionaria polar (en comparación a la fase móvil) aumenta el tiempo de retención. 2.- Cromatografía de fase reversa. Consiste en una fase inmóvil apolar y una fase móvil de polaridad moderada. Una de las fases estacionarias más comunes de este tipo de cromatografía es la silica tratada con RMe2SiCl, dónde la R es una cadena alquil tal como C18H37 ó C8H17. El tiempo de retención es mayor para las moléculas de naturaleza apolar, mientras que las moléculas de carácter polar eluyen más rápidamente. 3.- Cromatografía de exclusión molecular. La cromatografía de exclusión molecular, también conocida como cromatografía por filtración en gel, separa las partículas de la muestra en función de su tamaño. Generalmente se trata de una cromatografía de baja resolución de forma que se suele utilizar en los pasos finales del proceso de purificación. También es muy útil para la determinación de la estructura terciaria y la estructura cuaternaria de las proteínas purificadas. 4.- Cromatografía de intercambio iónico En la cromatografía de intercambio iónico, la retención se basa en la atracción electrostática entre los iones en solución y las cargas inmovilizadas a la fase estacionaria. Los iones de la misma carga son excluidos mientras que los de carga opuesta son retenidos por la columna. Algunos tipos de intercambiadores iónicos son: i) Resinas de poliestireno, ii) intercambiadores iónicos de celulosa y dextranos (geles) y iii) Silica porosa o vidrio de tamaño de poro controlado. 5.- Cromatografía basada en bioafinidad Este tipo de cromatografía se basa en la capacidad de las sustancias biológicamente activas de formar complejos estables, específicos y reversibles. La formación de estos complejos implica la participación de fuerzas moleculares como las interacciones de Van der Waals, interacciones electrostáticas, interacciones dipolo-dipolo, interacciones hidrofóbicas y puentes de hidrógeno entre las partículas de la muestra y la fase estacionaria. 2.- Técnicas electroforéticas SEPARACIÓN DE LOS ELEMENTOS DE UNA MEZCLA Separa los diferentes elementos que componen una mezcla compleja en función de la carga eléctrica de los mismos VELOCIDAD DE LAS PARTICULAS Depende de ... La carga de las mismas La intensidad del campo eléctrico y Del coeficiente de fricción de las moléculas con el medio 2.- Técnicas electroforéticas FUNDAMENTO DE LAS SEPARACIONES ELECTROFORETICAS La velocidad de migración de un ion, v, en centímetros por segundo, en el seno de un campo eléctrico, es igual al producto de la intensidad del campo eléctrico E (V cm‐1) por la movilidad electroforética µe (cm2V‐1s‐1 ), esto es: v = µeE La movilidad electroforética es directamente proporcional a la carga eléctrica del analito e inversamente proporcional a los factores de retardo por rozamiento. El campo eléctrico actúa solamente sobre los iones. Si dos especies difieren bien en la carga o en las fuerzas de rozamiento, se moverán a través del tampón y se separan. Las especies neutras no se separan 2.- Técnicas electroforéticas Representación simplificada de la separación electroforética de la alanina, lisina y ácido aspártico a pH = 6. La lisina catiónica es atraída hacia el cátodo, el ácido aspártico aniónico es atraído hacia el ánodo y la alanina se encuentra en su punto isoeléctrico, por lo que no se mueve 2.- Técnicas electroforéticas ENLACE PEPTÍDICO Estas subunidades unidas por ENLACE AMIDA o ENLACE PEPTÍDICO proveen la estructura de las proteínas ENLACE PEPTÍDICO CARACTERÍSTICAS DEL ENLACE PEPTÍDICO caract de doble enlace dipolo eléctrico posición trans Los 6 átomos están en el mismo plano ESTRUCTURA DEL ENLACE PEPTÍDICO El enlace peptídico tiene algunas propiedades muy importantes para la estructura de las proteínas • Más rígido y corto que un enlace C-N simple • Los átomos que participan (O, C, N, H) son coplanares • El grupo de átomos alrededor del enlace peptídico puede darse en dos configuraciones posibles: trans y cis • Caracter parcial de doble enlace: Se le puede considerar un híbrido de resonancia No se permite giro alrededor del enlace -C-N- ESTABILIDAD Y FORMACIÓN DEL ENLACE PEPTÍDICO ΔG=10 KJ/mol Enlace peptídico La reacción sin catalizar es muy lenta EN LA CÉLULA: la formación del enlace peptídico está acoplado a la hidrólisis de ATP Aa + tRNA Aminoacil-tRNA ATP AMP + PPi 2 Pi ENLACE PEPTÍDICO la estabilización por resonancia de una amida da lugar a su gran estabilidad, a la disminución de basicidad del átomo de nitrógeno y a la rotación restringida (carácter de doble enlace parcial) del enlace C-N. En un péptido, el enlace amida se denomina enlace peptídico. Tiene seis átomos en un plano: el C y el O del carbionilo, el N y su H, y los dos átomos de carbono asociados. ENLACE PEPTÍDICO Este enlace es relativamente rígido y no puede girar libremente. Dicha propiedad es de suma importancia con respecto a la conformación tridimensional de las cadenas polipeptídicas ENLACE PEPTÍDICO Podríamos pensar que una proteína puede adoptar miles de conformaciones debidas al giro libre en torno a los enlaces sencillos. Sin embargo, en su estado natural sólo adoptan una única conformación tridimensional que llamamos conformación nativa; que es directamente responsable de la actividad de la proteína. Esto hizo pensar que no podía haber giro libre en todos los enlaces; y efectivamente, mediante difracción de rayos X se vio que el enlace peptídico era más corto que un enlace sencillo normal, porque tiene un cierto carácter (60%) de enlace doble, ya que se estabiliza por resonancia. Descubrimiento de las Estructuras Polipépt. Regulares S. XX 1930. Quim. Linus Pauling Difracción de Rayos X. De aa. y péptidos 1950´s Principios: 1. La longitud y ángulos de enlace deberían desviarse lo menos posible de los hallados por DRX. 2. Dos á tomo no pueden acercarse uno al otro a una distancia menor de la que les permiten sus radios de Van der Waals . Enlace peptídico Plano Amida Gpo. péptido trans 3. El gpo . Amida debe permanecer en un plano de así conf. Trans , es posible la rotaci ón alrededor de los 2 enlaces adya - centes al C -α de cada residuo de aa. 4. Es preciso algún tipo de enlace no covalente para estabilizar un plegado regular ENLACE PEPTÍDICO Péptidos ? Polipéptidos: polímeros formados por más de 10 aa unidos por enlaces peptídicos. ? Proteína: generalmente polímeros de más de 50 aa (~ 6000 Da = masa insulina). ? Por convención se considera al extremo amino libre como el comienzo de la cadena: extremo amino-terminal o N-terminal. El otro extremo posee el grupo carboxilo libre unido al C-a: extremo carboxilo-terminal o C-terminal. ? Los péptidos se nombran de acuerdo al orden de los aa a partir del que posee el grupo amino libre. Por ejemplo el tetrapéptido ala-lys-tyr-cys se denomina alanil-lisil-tirosil-cisteína. Ejemplos ? hormonas (ej. oxitocina, oxitocina, vasopresina, calcitonina) calcitonina) ? glutatió glutatión (ácido glutá glutámicomico-cisteí cisteínana-glicina: en gló glóbulos rojos contribuye a prevenir dañ daños oxidativos). oxidativos). ? encefalinas (sist. sist. nervioso central) ? antibió antibióticos ? ? toxinas (amanitina (amanitina)) PÉPTIDOS Y ENLACE PEPTÍDICO Los péptidos se forman por la unión de los aminoácidos mediante enlaces covalentes de tipo amida llamados enlaces peptídicos Enlace peptídico OLIGOPÉPTIDOS (<20 aa) POLIPÉPTIDOS (20-50 aa) PROTEÍNAS (>50 aa) PÉPTIDOS DE INTERÉS BIOLÓGICO Glutatión (γ-glutamilcistenilglicina). La unión Glu-Cys se da en el C del Glu. Es un tripéptido muy abundante en la naturaleza que es sintetizado sistemáticamente por la célula. Es Ubicuo, se encuentra en diferentes reinos. Tiene diversas funciones: •Carnosina (ß-alanilhistidina). La unión Ala-His se da en el carbono beta de la Ala. Es un dipéptido presente en los músculos esqueléticos. Tirocidina A Péptido cíclico que contiene aa-D. TRH Factor liberador tirotrópico Presente en hormonas tiroideas. Oxitocina Nonapéptido de carácter hormonal implicado en las contracciones de la musculatura lisa del útero en el momento del parto y de la salida de la leche en la lactancia. Vasopresina Nonapéptido de carácter hormonal que se diferencia en pocos residuos aminoacídicos de la oxitocina. Se encarga de la constricción de los vasos sanguíneos aumentando la presión sanguínea. PÉPTIDOS DE INTERÉS BIOLÓGICO DE ORIGEN NO PROTEÍNICO L-Leu Antibiótico D-Phe L-Orn L-Pro L-Pro L-Val D-Phe L-Orn L-Leu Gramicidina S GLUTATION (γ-glutamil-cisteinil-glicina) El enlace peptídico del glutámico es por el resto gammacarboxilo PÉPTIDOS NATURALES DE INTERÉS BIOLÓGICO Hormona humana bradiquinina es un nonapéptido con un grupo -NH3+ en el extremo N terminal y un -COO- libre en el extremo C terminal. La bradiquinina es un potente vasodilatador dependiente del endotelio, que provoca la contracción de músculo liso no vascular, aumenta la permeabilidad vascular y también está relacionado con el mecanismo del dolor. PÉPTIDOS NATURALES DE INTERÉS BIOLÓGICO Oxitocina La oxitocina es un nonapéptido con dos residuos de cisteína (en las posiciones 1 y 16) que unen parte de la molécula formando un gran anillo PÉPTIDOS NATURALES DE INTERÉS BIOLÓGICO HORMONA (nonapéptido) DIFERENCIA CON OXITOCINA EN 2 AMINOÁCIDOS VASOPRESINA PUENTES DISULFURO cys-cys SÍNTESIS EN HIPOTÁLAMO La vasopresina es secretada desde el lóbulo posterior de la glándula pituitaria en respuesta a la reducción del volumen de plasma o en respuesta al aumento de osmolaridad en el plasma PROPIEDADES ÁCIDO BASE DE LOS PÉPTIDOS 1.- Todos los aminoácidos poseen un grupo ácido y grupo básico ionizables (que desaparecerán cuando polimericen para formar proteínas) 2.- Algunos aminoácidos tienen una cadena lateral ionizable (que NO desaparecerán cuando polimericen para formar proteínas) El punto isoeléctrico se localiza entre los dos pKas que delimitan la zona de pH en que predomina la especie neutra PROPIEDADES ÁCIDO BASE DE LOS PÉPTIDOS 1.- PUNTO ISOELÉCTRICO 1.1.- SIN CADENAS LATERALES CON GRUPOS IONIZABLES 1.2.- CON CADENAS LATERALES CON GRUPOS IONIZABLES 2.- TITULACIÓN PROPIEDADES ÓPTICAS DE LOS PÉPTIDOS 1.- En los péptidos cortos la actividad óptica total es una función aditiva de aproximada de las actividades ópticas de los aminoácidos componentes 2.- En los péptidos largos depende de la estructura Secundaria que se produzca PROPIEDADES QUÍMICAS DE LOS PÉPTIDOS 1.- REACCIÓN DE LA NINHIDRINA 2.- REACCIÓN DE BIURET: El tratamiento de un péptido o de una proteína con Cu2+ y álcali produce un complejo Cu2+-péptido que puede medirse en un espectrofotómetro REACCIÓN DE LA NINHIDRINA REACCIÓN DE BIURET La presencia de proteínas en una mezcla se puede determinar mediante la reacción del Biuret. El reactivo de Biuret contiene CuSO4 en solución acuosa alcalina (gracias a la presencia de NaOH o KOH). La reacción se basa en la formación de un compuesto de color violeta, debido a la formación de un complejo de coordinación entre los iones Cu2+ y los pares de electrones no compartidos del nitrógeno que forma parte de los enlaces peptídicos. O C C O HN R CH NH Cu2+ HC R O C C O HN NH R CH HC R Desnaturalización-Hidrólisis ? Desnaturalización de una proteína: pérdida de la conformación nativa y de sus propiedades originales (ej. coagulación por calor de las proteínas de la clara del huevo). ? Hidrólisis de una proteína: escisión en aminoácidos (ruptura de un enlace covalente por adición de agua). Desnaturalización de la ribonucleasa: enzima con puentes disulfuros reducidos y sin actividad enzimática HIDRÓLISIS 1.- TOTAL: Los enlaces peptídicos se hidrolizan con facilidad por calefacción, tanto con un ácido como con una base. 2.- PARCIAL (ENZIMÁTICA) HIDRÓLISIS TOTAL 1.- Hidrólisis ácida. Normalmente se utiliza: HCl 6 N 100-120ºC durante 10-24 h. No produce racemizaciones de los aminoácidos. Problemas: 1.- No se recuperan todos los aminoácidos. a.-Trp se destruye durante el tratamiento b.- Pérdida de alguna cantidad de Ser y Thr c.- Los grupos amida de la Asn y Gln experimentan hidrólisis completa y se convierten en los ácidos correspondientes Asp y Glu. HIDRÓLISIS TOTAL 2.- Hidrólisis básica o alcalina. También se pueden hidrolizar las proteínas con 100ºC con disoluciones concentradas de NaOH Problemas 1.- Provoca la destrucción de la cisteína, cistina, Ser y Thr 2.- Se produce racemización de todos los aminoácidos Ventajas 1.- El Trp no se pierde y es estable en presencia de las bases. Este método se utiliza prácticamente para la valoración por separado del triptófano HIDRÓLISIS PARCIAL Es llevado a cabo por las PROTEASAS, enzimas que hidrolizan el enlace peptídico. Las peptidasas (antes conocidas como proteasas) son enzimas que rompen los enlaces peptídicos de las proteínas. Usan una molécula de agua para hacerlo y por lo tanto se clasifican como hidrolasas. HIDRÓLISIS PARCIAL. Tipos 1.- Tripsina: enzima digestivo secretado por el páncreas al intestino delgado. Cataliza la hidrólisis de los enlaces peptídicos en que la función carbonilo es aportada por el resto de Lys o Arg. Es el más específico 2.- Quimotripsina: Escinde el enlace peptídico de Phe, Trp o Tyr (aminoácido 1) 3.- Pepsina: Escinde el enlace Phe, Trp, Tyr (aminoácido 1) y otros varios 4.- Termolisina: Escinde el enlace Leu, Ile, Val (aminoácido 2). Aa no polares. Ha sido útil para establecer la secuencia de protaminas con gran cantidad de Arg y Lys 5.- Bromuro de cianógeno: Escinde Met (aminoácido 1) HIDRÓLISIS PARCIAL La tripsina hidroliza por la derecha de Arg , Lys La quimotripsina hidroliza por la derecha de Phe, Trp, Tyr La pepsina hidroliza por la izquierda de Phe, Trp, Tyr La termolisina hidroliza por la izquierda de Val, Leu, Ile El bromuro de cianógeno (BrCN) hidroliza por la derecha de la Met HIDRÓLISIS PARCIAL HIDRÓLISIS PARCIAL METIONINA HIDRÓLISIS PARCIAL TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 1.- Técnicas cromatográficas Base del coeficiente a.- Cromatografía de partición o de reparto de reparto En papel Definición de Rf (Prácticas) Fase móvil Fase estacionaria En columna Definición de coeficiente de reparto TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS b.- Cromatografía de intercambio iónico (catiónico y aniónico) TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS c.- Cromatografía de filtración en gel o de exclusión molecular (Prácticas) TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS d.- Cromatografía de afinidad 1.- Factores de transcripción. Utilizar secuencias-consenso 2. Anticuerpos. La proteína A o Gagarosa TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas a.- Electroforesis en gel (SDS-PAGE) TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas a.- Electroforesis en gel (SDS-PAGE) 2.- Técnicas electroforéticas a.- Electroforesis en gel (SDS-PAGE) TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas a.- Electroforesis en gel (SDS-PAGE) TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas b.- isoelectroenfoque TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas c.- electroforesis bidimensional 1.- Primera dimensión: pI 2.- Segunda dimensión: MW TÉCNICAS PARA EL AISLAMIENTO, SEPARACIÓN E IDENTIFICACIÓN DE PROTEÍNAS 2.- Técnicas electroforéticas c.- electroforesis bidimensional SECUENCIACIÓN SECUENCIACIÓN DEGRADACIÓN DE EDMAN 1.- Marcaje del amino terminal con PITC (Fenilisotiocianato) en medio alcalino. Se forma el derivado feniltiocarbamilo 2.- Se hidroliza el enlace peptídico entre el aminoácido 1 y 2 3.- Se identifica el derivado del residuo N-terminal por HPLC Degradación secuencial Análisis de Péptidos Degradación de Edman S N C + H NH CH CO NH CH CO R1 R2 NH CH COOH R3 1ª) Adición en medio básico de isotiocianato de fenilo H S N C NH CH CO NH CH CO 2ª) Hidrólisis suave solo del terminal con HCl en CH3NO2 ó Acético Mejora de este es soportar mediante el COOH a un polímero el péptido e ir degradando secuencialmente R1 NH CH COOH R2 + HOO C O C H CH RR1 CH 1 N S NH N C NH C R3 NH2 CH CO R2 NH CH COOH R3 Puede repetirse el proceso con el resto hasta 30 ó más veces si el péptido es grande S Tiohidantoina feniltiohidantoína Se separa e identifica Degradación de Edman SECUENCIACIÓN La secuencia de aminoácidos de una proteína están determinadas genéticamente: La secuencia de nucleótidos del DNA codifica una secuencia complementaria de nucleótidos en el RNA determina la secuencia de aminoácidos de la proteína estructura espacial función mutaciones alteraciones genéticas La secuencia de aminoácidos de una proteína están determinadas genéticamente Conformación de las proteínas Todas las proteínas poseen un estado NATIVO, una forma tridimiensional característica conocida como CONFORMACIÓN. La conformación se puede describir en términos de niveles estructurales Ordenamiento tridimensional Estructuras 1ria, 2ria, 3ria y 4ria CONFORMACIÓN DE LAS PROTEÍNAS estructura jerárquica Estructura Estructura Estructura Estructura 1ria 2ria 3ria 4ria Secuencia de aa del esqueleto del peptídico y S-S Arreglo / distribución/ordenamiento del esqueleto y las cadenas laterales de la proteína en el espacio Describe el ordenamiento tridimensional de las proteínas Estructura 1ria Se refiere al ordenamietno del esqueleto covalente de la cadena polipeptídica, DADA POR LA SECUENCIA DE aa Será la que determine el ordenamiento tridimensional que adoptará la proteína Diferentes fuerzas intervienen en la estabilización del esqueleto peptídico para alcanzar la conformación tridimensional Puente de hidrógeno NO COVALENTES Interaccines hidrofóbicas Atracción electroestática COVALENTES Puentes S-S Estructuras 2ria, 3ria y 4ria Diferentes arreglos espaciales o estructuras 2rias • α - hélice (semejante a un cilindro) • Hoja β - plegada • Turns (γ, β, ω) • Random coil (desordenada) Estructura 3ria Se refiere al modo en que la cadena polipeptídica se pliega o se curva para formar la estructura plegada o compacta de las proteínas solubles Fuerzas que intervienen en la estabilización de la estructura terciaria Estructura 4ria Solo la alcanzan las proteínas que poseen más de una cadena polipeptídica Pueden intervenir enlaces covalentes y no covalentes ESTRUCTURA SECUNDARIA: PROTEÍNAS FIBROSAS El estudio de las queratinas ha sido especialmente importante al revelar las conformaciones que prevalecen en las cadenas polipeptídicas de las proteínas nativas: 1.- Hélice-α 2.- Conformación ß Existen dos tipos: 1.- QUERATINAS: Proteínas insolubles derivadas del ectodermo. Ej: pelo, lana, escamas, plumas, uñas cuernos y la seda. 1.1.- α-queratinas: 1. Ricas en cisteína 2. Contienen la mayor parte de los aminoácidos corrientes 3.- Se estiran cuando se calientan y se contraen cuando se enfrían. Por ej: el pelo se estira casi al doble cuando se le somete a calor húmedo Ej: Proteínas duras y quebradizas de los cuernos y las uñas (22% Cys) y las queratinas más blandas y flexibles de la piel, pelo y lana (10-14% Cys) 1.2.- ß-queratinas 1.- No contienen cisteína 2.- Ricas en aminoácidos con cadenas laterales pequeñas (Glicocola, Alanina, Serina) 3.- No se estiran Ej: Fibras hiladas por las arañas y los gusanos de seda y en las escamas , garras y picos de los reptiles y pájaros 2.- COLÁGENOS ESTRUCTURA SECUNDARIA: ANÁLISIS POR RAYOS X DE LAS QUERATINAS 1.- Ideas generales de difracción de rayos X 2.- William Astbury (1930) 2.1.- El pelo, la lana y ciertas proteínas fibrosas (α-queratinas) Producen espectros de difracción muy parecidos entre sí 2.2.- Por lo tanto todas ellas deben tener una PERIODICIDAD PRINCIPAL. También denominada unidad repetida (0,5 a 0,55 nm) 2.3.- Conclusión: Todas ellas se hallan plegadas de modo regular 2.4.- La fibroína (ß-queratina de las fibras de la seda) presenta una unidad repetida de 0,7 nm 2.5.- Al estirar la lana y el pelo después de someterlos A la acción del vapor, la difracción de rayos X es semejante a la periodicidad de Las ß-queratinas (0,7 nm) 2.6.- Conclusión: La cadenas peptídicas en las α y ß-queratinas Están plegadas de manera diferente 3.- Linus Pauling y Corey y el descubrimiento de la estructura del enlace peptídico ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS Características: 1.- 3,6 aminoácidos/vuelta 2.- Los grupos R de los aminoácidos se proyectan hacia el exterior de la hélice 3.- La unidad repetida 0,54 nm La elevación por cada resto es de 0,15 nm, que corresponde con la periodicidad menor observada en las difracciones de rayos X 4.- Permite la existencia de enlaces de hidrógeno intracatenarios entre vueltas consecutivas de la hélice. Los vectores eléctricos de los enlaces están orientados de modo que proporcionan casi la máxima fuerza de enlace 5.- Existen distintos tipos de plegamientos helicoidales 6.- Se puede formar con L o con D-aminoácidos pero no a partir de una mezcla 7.- Si se parte de aminoácidos L se puede plegar a derechas y a izquierdas. La dextro es la más estable. 8.- En las α-queratinas del pelo y de la lana se arrollan 3 o 7 de estas hélices α unas a alrededor de las otras, formando cordones de 3 a 7 cabos que se mantienen unidos por puentes disulfuro ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS Características: 9.- Aminoácidos formadores y desestabilizadores de la doble hélice 9.1.- Poli alanina: Los grupos R son pequeños y sin carga forma espontáneamente hélices alfa a pH 7 9.2.- Poli lisina: No forma hélice alfa a pH 7 sino que es irregular. Poseen carga positiva y se repelen y no puente de H. Pero sí la forma a pH12, sin carga 9.3.- Ácido poliglutámico: a pH 7 es totalmente irregular pero a pH 2 sí 10.- La presencia de interacciones debidas a las cargas no constituye el único factor determinante de si se puede formar una hélice. Volumen y tamaño de las cadenas laterales de los aminoácidos. Ej: poli Isoleucina (Cadenas laterales muy voluminosas y no forma α-hélice) 11.- Siempre que en la cadena aparece la Pro o hidroxi-Pro la hélice alfa se interrumpe y se origina una curvatura (No puentes de H y por los anillos rígidos de la cadena lateral) Hélice α ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS ESTRUCTURA SECUNDARIA: HÉLICE-α Y ESTRUCTURA DE LAS α-QUERATINAS PROPIEDADES ÓPTICAS DE LA HÉLICE-α 1.- Las proteínas nativas son significativamente más dextrorrotatorias que la suma de las rotaciones individuales de los aminoácidos (Es máximo en la forma de alfa-helice). Ej: poli-Glu a pH 2 (hélice-alfa) es -15 º y a pH 7 (al azar) es -85º 2.- Las proteínas arrolladas al azar presentan una aditividad en el poder rotatorio. 3.- La capacidad de hacer rotar el plano de la luz polarizada no solo depende de la presencia de los carbonos asimétricos sino que también otras formas de asimetría molecular puede tener actividad óptica aunque no exista ningún C asimétrico 3.1.- Si una molécula puede existir en dos formas diferentes no superponibles (imágenes especulares) tiene actividad óptica. 3.2.- Una hélice alfa formada por L-aminoácidos, la asimetría total de la molécula es la suma de la asimetría portada por los carbonos asimétricos más la contenida por el enrrollamiento alfa-helicoidal, que es asimétrico, ya que es levo o dextro Representaciones de Ramachandran PLEGAMIENTO 1.- Enlace peptídico 2.- Cadenas laterales Representaciones de Ramachandran ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS (Ej: Fibroína de la seda) Características: 1.- También la difracción por rayos X han determinado su estructura 2.- Cuando las alfa-queratinas se someten a calor húmedo se duplicaba el tamaño y presentaban otra estructura, debido a rotura de puentes de hidrógeno intracatenarios y el alargamiento de la hélice-alfa 3.- Adoptan configuración en zig-zag (más extendida que la alfa-hélice) 4.- Las cadenas polipeptídicas paralelas de la conformación ß están dispuestas en láminas plegadas que se unen unas a otras por puentes de hidrógeno intercatenarios 5.- Los grupos R se hallan por encima o por debajo de los planos en zig-zag de la lámina plegada. 6.- La fibroína presenta un aminoácido sí y otro no Gly y la mayoría del resto de los aminoácidos es la alanina (Grupos metilo como cadena lateral). Si fueran con cadena lateral grande existirían interacciones estéricas. 7.- Existen en dos conformaciones: Paralela y Antiparalela a diferencia de las alfaqueratinas (paralela) ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS Antiparalela puente de H entre grupos NH y CO de distintas cadenas polipeptídicas Paralela ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS Fibroína Bombyx mori (Gusano de seda) Grupos metilo ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS Fibroína ESTRUCTURA SECUNDARIA: ß-LÁMINA Y ESTRUCTURA DE LAS ß-QUERATINAS A.A. α-Queratina (lana) Fibroina Colágeno (Seda) (Tendón de Bovino) Elastina (Aorta Porcina) ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO • Principal constituyente del tejido conjuntivo • Principal proteína estructural del reino animal (presente en tendones, cartílagos, matriz orgánica de los huesos y córnea del ojo) • Forma aprox. un 30% de la proteína total del cuerpo ESTRUCTURA: •Tiene 3,3 residuos/vuelta (muy extendida): Gly 33% Ala 11% Pro e Hyp 21% Hidroxi-Lys en menor proporción (lugar de unión a polisacáridos) • Fragmentos comunes: Gly-Pro-Hyp Gly-X-Pro Gly-X-Hyp • Hélice simple y única • Es levógira pero la triple hélice es dextrógira ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO El colágeno es la principal proteína de la matriz extracelular y constituye el 25% de la masa de proteínas de un vertebrado. Está constituido por una triple hélice ordenada hacia la izquierda, con tres residuos aminoacídicos por vuelta. Uno de ellos siempre es glicina y de los otros dos es bastante frecuente que uno sea prolina y otro hidroxiprolina ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO ? 25 % del total de prote ínas en vertebrados (piel, huesos, cart ílagos, tendones, vasos sangu íneos), una de las m ás largas que se conocen. Insoluble en agua y poco digerible; sometido a ebullici ón en agua ? gelatina, soluble y digerible. Existen alrededor de 14 tipos los cuales difieren levemente en su estructura primaria. ? Estructura primaria muy regular y peri ódica: ? proporció ó n de glicina y prolina, , y de hidroxiprolina e proporci prolina hidroxilisina. En vez de h élice a, su estructura secundaria es una h élice m ás extendida y enrollada hacia la izquierda. ? 3 cadenas de alrededor de 1000 aa c/u as í enrolladas ( triplehé triplehélice) lice) ? unidad estructural de superhélice llamada tropocolágeno. La glicina ocupa 1 de c/3 posiciones: es el único aa que por su tamaño puede ubicarse en el interior de esa fibra helicoidal tan compacta. ? Fibras de col ágeno: unidades de tropocolágeno ubicadas en hileras con igual orientaci ón (extremos N-terminales para el mismo lado), escalonadas en un cuarto. Éstas a su vez est án reforzadas por medio de enlaces cruzados. Se producen a veces tambié tropocolá también uniones entre lisinas de tropocolágenos vecinos ? gran resistencia mecá mecánica. ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO SÍNTESIS COLÁGENO PROCOLÁGENO PEPTIDASA ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO SÍNTESIS COLÁGENO Formación de al-lisinas ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Las cadenas de tropocolágeno aparecen unidas unas a otras en la microfibrilla mediante: - Cadena lateral de al-lisina unida a cadena lateral de lisina no modificada a través de base de Schiff y posterior reducción - Cadena lateral de al-lisina unida a otra al-lisina a través de condensación aldólica - Enlaces de hidrógeno entre el grupo -C=O de la prolina y el -N-H de la glicina, siempre intercatenarios ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Hidroxilación de prolina HO OH O N C O N C C O C O 4-Hidroxiprolina (mayoritario) 3-Hidroxiprolina (minoritario) Enzima: procolágeno:prolina monooxigenasa (prolil hidroxilasa), requiere ácido ascórbico La hidroxilación de prolina favorece la formación de enlaces H entre las cadenas ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO NH3+ Hidroxilación de lisina CH2 HC OH CH2 Enzima: Procolágeno:lisina monooxigenasa (lisil hidroxilasa), requiere ácido ascórbico CH2 CH N C H O 5-Hidroxilisina La lisina hidroxilada es el punto de unión de oligosacáridos al colágeno ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Al-Lisina CHO CH2 Enzima: lisil aminooxidasa CH2 CH2 CH N C H O Al-Lisina (Lisina aldehídica) Forma enlaces cruzados (entrecruzamientos) covalentes entre los helicoides del colágeno Es una reacción de desaminación oxidativa (El grupo NH2 se cambia por un grupo aldehído) ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Lisina H O H O H O N C N C N C (CH2)4 (CH2)4 NH3+ N Al-lisina H C O CH2 (CH2)3 (CH2)3 N NH REDUCCIÓN C CHO C (CH2)4 N H C (CH2)3 C N O H Base de Schiff C C O Entrecruzamiento (lisil norleucina) Formación de entrecruzamiento covalente entre cadenas de colágeno a través de lisina y al-lisina, (vía base de Schiff) ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Formación de entrecruzamiento covalente entre cadenas de colágeno a través de lisina y al-lisina, (vía base de Schiff) ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Al-lisina H N O H O C N C (CH2)3 CHO CHO (CH2)3 CH O C C H (CH2)2 (CH2)3 Al-lisina N H C C O N H C C O Entrecruzamiento aldólico Formación de entrecruzamiento covalente entre cadenas de colágeno a través de dos al-lisinas, (vía condensación aldólica) ESTRUCTURA SECUNDARIA: TRIPLE HÉLICE DEL COLÁGENO Tipos de colágeno Tipo I [α1(I)]2α2(I) Mayoritario (huesos, piel, tendones) Tipo II [α1(II)]3 Cartílago, vítreo Tipo III [α1(III)]3 Vasos sanguíneos, cicatrices Tipo IV [α1(IV)]3 [α2(IV)]3 Membrana basal, cristalino Tipo V [α1(V)]2α2(V) [α1(V)]3 [α1(V)][α2(V)][α3(V)] Superficies celulares Tipo VI Íntima de la aorta DEFECTOS GENÉTICOS RELACIONADOS CON EL COLÁGENO Gly-X-Pro • Osteogénesis imperfecta (formación anormal de huesos en bebés) Cys en lugar de Gly • Síndrome de Ehlers-Danlos (debilidad de las articulaciones) Ser en lugar de Gly ESTRUCTURAS SUPERSECUNDARIAS La estructura supersecundaria puede tener una determinada función o simplemente pertenecer a una unidad funcional mayor denominada DOMINIO ESTRUCTURAS SUPERSECUNDARIAS Miohemeritrina Sandwich β Prealbúmina Piruvato quinasa, dominio 1 Cilindro β antiparalelo Proteína de la cubierta del virus del mosaico de tabaco a) Predominantemente hélice α Inmunoglobulina, dominio V2 Hexoquinasa, dominio 2 b) Predominantemente lámina β c) Hélice α y lámina β mezcladas ESTRUCTURAS SUPERSECUNDARIAS ESTRUCTURAS SUPERSECUNDARIAS 1.- Dedos de Zinc (Zn- Fingers) cis cis Zn cis H2N his COOH ESTRUCTURAS SUPERSECUNDARIAS 1.- Dedos de Zinc (Zn- Fingers) • Este motivo consiste en espaciamientos específicos conformados por residuos de cisteínas e histidinas que permiten la unión de cationes Zn2+ a la proteína, produciéndose un enlace coordinativo del metal en el centro de ellos. • Este fenómeno confiere al dominio aspecto de un dedo, por lo cual es llamado comunmente “dedo de zinc”. • Estos dominios pueden encajar en los surcos mayores del ADN. El acople de estos factores regulatorios abarca la mitad de una vuelta de la doble hélice del ADN. • Los ejemplos más típicos son el factor de transcripción de la ARN polimerasa II (TFIIIA) y las proteínas de la superfamilia de receptores de las hormonas permisivas (esteroideas, tiroideas, etc). ESTRUCTURAS SUPERSECUNDARIAS 1.- Dedos de Zinc (Zn- Fingers) ESTRUCTURAS SUPERSECUNDARIAS 2.- Cremalleras de Leucina (Leucine zipper) HOOC H2N COOH uel leu uel leu uel leu uel leu NH2 Puntos de recnocimiento del ADN ESTRUCTURAS SUPERSECUNDARIAS 2.- Cremalleras de Leucina (Leucine zipper) • Es un motivo que se origina por la distribución repetitiva de residuos de leucina espaciados por 7 aminoácidos en una distribución alfa helicoidal de la proteína. • Estos residuos de Leu terminan en una zona con residuos R que protruyen con respecto a la zona helicoidal. Los grupos R se interdigitan con grupos R de otros dominios de este tipo, estabilizando así la homo o heterodimerización. • Los dominios de cierre de lueucina están presentes en proteínas tales como: c-myc, c-fos, c-jun y C/EBP. • La tasa de expresión de un gen es la resultante de la interacción de varios de estos factores de transcripción específicos que inducen o impiden la formación del aparato basal de transcripción (compuesto por los factores de transcripción generales). ESTRUCTURAS SUPERSECUNDARIAS 2.- Cremalleras de Leucina (Leucine zipper) The Fos and Jun proteins Fos Jun Basic regions (DNA contact surfaces that bind to the DNA) • Four leucines ( ) are present at every seventh position in the amphipathic α-helix Leucine zipper (dimerization domain) ESTRUCTURAS SUPERSECUNDARIAS 2.- Cremalleras de Leucina (Leucine zipper) ESTRUCTURAS SUPERSECUNDARIAS 2.- Cremalleras de Leucina (Leucine zipper) ESTRUCTURAS SUPERSECUNDARIAS 3.- Motivos hélice-vuelta hélice • Constituye una zona proteica o dominio compuesto por dos regiones de alfa hélice separadas por una de longitud variable que forma un rulo o bucle entre ellas. • Los dominios alfa helicoidales son similares estructuralmente y necesarios para la interacción con secuencias de la proteína que permiten una conformación simétrica respecto de un eje. • Esta clase de proteínas a menudo contiene una región rica en aminoácidos básicos localizada en el extremo amino terminal que le permite su unión a secuencias del ADN reconocidas específicamente. • Los dominios HLH son necesarios para la homo y heterodimerización. – Ejemplos para las proteínas de unión al ADN con motivos HLH son: Myo D, c-Myc y Max. ESTRUCTURAS SUPERSECUNDARIAS 3.- Motivos hélice-vuelta hélice GIROS 1/3 de los aminoácidos se encuentran en turns o loops donde las CADENAS INVIERTEN su dirección El grupo C=O de un residuo n enlazado por puente de H con el grupo NH del residuo (n+3) β turns GIROS GIROS Muchos de estos cambio de dirección se realizan mediante una unidad estructural común conocida como giro beta o giro reverso. Lo esencial de este giro en horquilla es que el carbonilo de un residuo n enlace con el grupo amino del residuo n+3. En consecuencia la cadena puede cambiar bruscamente de dirección. A menudo los giros beta conectan hojas beta antiparalelas. Se conocen varios tipos de giros. En los giros tipo I, podemos encontrar cualquier tipo de residuos con excepción de la prolina en posición 3. En los giros tipo II, la glicina debe estar en posición i+2 y casi siempre aparece una prolina en posición i+3. Los giros tipo III son una porción de hélice 310, y no hay restricciones en cuanto a la identidad de sus componentes. A veces puede conseguirse un giro completo de la cadena polipeptídica con tan solo dos residuos como es el caso de los giros tipo γ. Εn estos residuos n suele ser la prolina ESTRUCTURA TERCIARIA: MIOGLOBINA CLASIFICACIÓN DE PROTEÍNAS 1.HOLOPROTEÍNAS Formadas solamente por aminoácidos •HETEROPROTEÍNAS o Proteínas Conjugadas Formadas por una fracción protéica y por un grupo no protéico, que se denomina "grupo prostético” ESTRUCTURA TERCIARIA: MIOGLOBINA CLASIFICACIÓN DE PROTEÍNAS Proteínas fibrosas: toda la molécula dispuesta en hélice α o en lámina β. • Elastina. Componente del tejido conjuntivo (paredes de los vasos sanguíneos, ligamentos), capaz de estirarse de modo reversible varias veces su longitud inicial. Al igual que el colágeno es rica en Gly y Pro, pero tiene escasa hidroxiprolina y carece de hidroxilisina. • Queratina. α- queratinas: principales proteínas del pelo y uñas, piel de animales. Generalmente dos hélices α se enrollan sobre si. En uñas, gran cantidad de puentes disulfuro. • β-queratinas: presentan láminas β y se encuentran en plumas y escamas de reptiles. Proteínas globulares: porciones de hélices α y en láminas β y ambas unidas al azar para dar una conformación esferoidal. Por ej. hemoglobina. • Como resultado de acciones de diferentes fuerzas (de atracción o repulsión electroestáticas, enlaces H de cadenas laterales, ptes S-S) ciertas regiones de una proteína presentan asociaciones de hélices α o láminas β comportándose como unidades estructurales y funcionales, dominios. ESTRUCTURA TERCIARIA: MIOGLOBINA Proteínas simples Formadas solamente por aa. ? Albúminas. Proteínas globulares ácidas, de origen animal o vegetal, solubles en agua y de cadena única (ovoalbúmina, lactoalbúmina, legumelina). ? Globulinas. Proteínas globulares de origen animal o vegetal, insolubles en agua pura, generalmente de varias cadenas (ovoglobulinas, lactoglobulinas). ? Histonas. Proteínas básicas, asociadas al ADN, con alta proporción de lisina, arginina e histidina. ? Glutelinas y gliadinas. Granos de cereales (zeína). ? Escleroproteínas. Proteínas fibrosas componentes de tejidos animales de sostén (queratina, colágeno, elastinas). ESTRUCTURA TERCIARIA: MIOGLOBINA Proteínas conjugadas Formadas por una proteína simple (apoproteína) + una porción no proteica (grupo prostético: GP). ? Nucleoproteínas (GP: ácidos nucleicos). ? Cromoproteínas (GP coloreado; hemoglobina, citocromos- procesos de oxidoreducción; rodopsina). ? Gicoproteínas (GP: hidratos de C). ? Fosfoproteínas (GP: fosfatos; caseína de la leche, vitelina de la clara del huevo). ? Lipoproteínas (GP: lípidos, en el plasma sanguíneo transportan lípidos insolubles en medio acuoso). ? Metaloproteínas (GP: metales como Fe, Cu, Mg, Mn) ESTRUCTURA TERCIARIA: MIOGLOBINA Proteínas Conjugadas Proteína Gpo.Prostético / Característico Ejemplo Glucoproteínas Carbohidratos γ−Globulina de la sangre Lipoproteínas Lípidos β−Lipoproteína de la sangre Fosfoproteínas Grupo fosfato Caseína de la leche Hemoproteína Hemo Hemoglobina Flavoproteína Núcleo de Flavina Succinato Deshidrogenasa Metaloproteína Fe, Ferritina Zn Alcohol Deshidrogenasa ESTRUCTURA TERCIARIA: MIOGLOBINA Características generales 1.- Se encarga del almacenamiento de oxígeno en los músculos 2.- Posee una sola cadena polipeptídica con 153 aa 3.- El grupo prostético es un grupo hemo ferroporfirínico o grupo hemo 4.- Es abundante en los músculos esqueléticos y particularmente en los animales buceadores (ballena, foca y morsa) 5.- Está emparentada con la hemoglobina, que contiene 4 cadenas peptídicas y cuatro grupos hemo y por consiguiente un peso molecular alrededor de 4 veces superior 6.- El esqueleto está formado por 8 segmentos (A-H) relativamente rectos constituído por una porción de hélice alfa (7-23 aminoácidos) dextrógiros. 7.- El 75 % de la cadena es hélice alfa 8.- Todos los grupos R polares de los restos aminoácidos se encuentran en la superficie 9.- Casi todos los grupos no polares o hidrofóbicos R se encuentran en el interior de la molécula, protegidos de la exposición al agua ESTRUCTURA TERCIARIA: MIOGLOBINA Características generales 10.- Los restos de prolina solo aparecen en las curvaturas, que también contienen algunos aminoácidos de los que se sabe no forman enrrollamientos en forma de hélice alfa como la isoleucina y la serina 11.- La conformación tridimensional de la cadena peptídica es semejante en las mioglobinas aisladas de diferentes especies, a pesar de que difieren algo en la composición aminoacídica 12.- Presenta una cavidad en el interior en el que están presentes el grupo prostético hemo rodeado por el entorno hidrófobo de la histidina (el anillo imidazólico de la His es una trampa de protones y protege al Fe2+ de la oxidación). Fe 3+ (Grupo HEMINA) pérdida de la capacidad de unir oxígeno. 13.- Almacena oxígeno y facilita su distribución dentro de las miofibrillas musculares, liberándolo cuando las demandas lo requieren 14.- El oxígeno se une de forma reversible 15.- La estructura se estabiliza mediante las siguientes interacciones: 1.- Los enlaces de hidrógeno entre grupos peptídicos 2.- Las interacciones hidrofóbicas entre grupos no polares, que son los más importantes 3.- Enlaces iónicos entre grupos cargados positiva y negativamente ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA GRUPO HEMO Formado por: 1.- Protoporfirina IX (4 anillos pirrólicos unidos por puentes meteno) 1.1.- 4 Grupos metilo 1.2.- 2 Grupos vinilo 1.3.- 2 Grupos ácido propiónico 2.- Ión ferroso: Tiene 6 posiciones de coordinación 2.1.- 4 enlaces con el Nitrógeno 2.2.- 2 enlaces por encima y por debajo del plano del grupo hemo. Por arriba la His proximal (F8) y por debajo la His distal (E7), que sirve como orientación para la unión del oxígeno ANILLO PIRRÓLICO PUENTE METENO GRUPO HEMO ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA El Fe2+ del grupo hemo establece 6 enlaces de coordinación: • 4 con los N del anillo tetrapirrólico (situados en el plano del anillo) • 1 con el N de la His 93 (F8) llamada His F8 ó His proximal • El 6º enlace: • Desoximioglobina: una molécula de agua • Oximioglobina: una molécula de oxígeno, junto a la His distal (número 64, E7) En el entorno hidrófobo del interior de la mioglobina, el hierro no es fácilmente oxidado por el oxígeno. Fuera del ambiente celular, el hierro se oxida lentamente, formando la metamioglobina, incapaz de unir oxígeno une en su lugar una molécula de agua. El CO se une al Fe2+ con mayor afinidad que el O2 ESTRUCTURA TERCIARIA: MIOGLOBINA FORMACIÓN DE LA OXIMIOGLOBINA Está 0,4 Ȧ por encima del plano de la porfirina ESTRUCTURA TERCIARIA: MIOGLOBINA FORMACIÓN DE LA OXIMIOGLOBINA Histidina proximal Histidina distal ESTRUCTURA TERCIARIA: MIOGLOBINA FORMACIÓN DE LA OXIMIOGLOBINA PUENTE DE HIDRÓGENO ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA TERCIARIA: MIOGLOBINA ANÁLISIS DE LA UNIÓN DEL OXÍGENO POR LA MIOGLOBINA La curva de unión de oxígeno a la mioglobina es hiperbólica e indica que tiene una elevada afinidad por el oxígeno ya que P50 es muy baja (unos 4 mm de Hg) En los capilares (PO2 30 mm Hg): La Mb estaría saturada En los tejidos (PO2 baja): La Mb capta O2 de la Hb de la sangre arterial circulante y luego lo cede a los orgánulos celulares que consumen oxígeno (mitocondrias) PO2 Mb + O2 MbO2 PO2 “Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002 ESTRUCTURA TERCIARIA: MIOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA Características generales 1.- Presenta estructura cuaternaria. Es una proteína oligomérica y cuyas estructuras terciaria y cuaternaria fueron conocidas gracias al análisis por rayos X. Fue conseguido por Perutz y colaboradores en Inglaterra tras 25 años de estudio. 2.- La hemoglobina contiene 2 cadenas α (141 restos) y 2 cadenas ß (146 restos) a cada uno de las cuales se halla unido un resto hemo mediante enlace no covalente 3.- Las cadenas α y ß poseen alrededor de un 70 % de carácter helicoidal, como también ocurre en la mioglobina 4.- La estructura terciaria de las cadenas α y ß es muy semejante a la de la estructura de la cadena única de la hemoglobina, en consonancia con la semejante función biológica. 5.- Hay muy poco contacto entre las 2 cadenas alfa y entre las 2 cadenas ß pero son numerosos los contactos de grupos R entre los pares correspondientes a cadenas diferentes. 6.- Cada uno de los 4 grupos hemo se halla parcialmente encerrado de grupos con R apolares 7.- Durante la desoxigenación de la hemoglobina, las cadenas alfa experimentan una rotación de unos 9º y las cadenas ßde cercea de 7º. Por lo tanto la unión de las 4 moléculas de oxígeno provoca un cambio profundo en la estructura cuaternaria de la molécula 8.- La representación gráfica del porcentaje de saturación de la hemoglobina frente a laa presión parcial de oxígeno es SIGMOIDAL, lo que significa una baja afinidad ESTRUCTURA CUATERNARIA: HEMOGLOBINA Características generales 9.- El diámetro de la proteína es 5,5 nm= 55 Å 10.- Contacto entre cadenas α y ß es mediante interacciones hidrofóbicas e iónicas 11.- Proteína transportadora de oxígeno por los glóbulos rojos 12.- La curva de saturación de la hemoglobina es de tipo COOPERATIVO 13.- El porcentaje de homología entre la mioglobina y la hemoglobina es de alrededor del 24 % y se mantiene una buena conservación de residuos en las histidina proximal y distal ESTRUCTURA CUATERNARIA: HEMOGLOBINA Hemoglobina: proteína globular, conjugada y oligomérica - Grupo prostético: hemo hemo: protoporfirina IX + ion ferroso Fe2+ - Cuatro subunidades, iguales dos a dos: Hemoglobina A1 (HbA1): α2β2 Hemoglobinas Hemoglobina A2 (HbA2): α2δ2 adultas Hemoglobina fetal Hemoglobinas embrionarias Hemoglobina F (HbF): α2γ2 Hemoglobina fetal (HbF): α2γ2. Hemoglobina Gower 1: ζ2ε2 Hemoglobina Gower 2: α2ε2 Hemoglobina Portland: ζ2γ2 97% 2% 1% Gran afinidad por el oxígeno - Se conoce, además, un gran número de hemoglobinas mutantes. ESTRUCTURA CUATERNARIA: HEMOGLOBINA α1 β1 β2 α2 Hemoglobina A1 (forma T, desoxi-) ESTRUCTURA CUATERNARIA: HEMOGLOBINA α1 β2 β1 α2 Hemoglobina A1 (forma R, oxi-) ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA Modelo MWC Forma R, oxiKR s Monod-Wyman-Changeaux (MODELO CONCERTADO) s s s s s Se favorece mucho el estado T s s s s Se favorece mucho el estado R i KT i Forma T, desoxi- i i i i i i i i ESTRUCTURA CUATERNARIA: HEMOGLOBINA MODELO SECUENCIAL En este modelo cada tetrámero puede estar en dos estados, el T y el R. La unión de un ligando a un centro del ensamblaje aumenta la afinidad de unión de centros vecinos, sin que se induzca la completa conversión del estado T en R Realmente ninguno de los dos modelos describe mejor la unión cooperativa del oxígeno a la hemoglobina. Se requiere un MODELO COMBINADO. La conducta de la Hb es concertada en las moléculas con 3 centros ya ocupados por el oxígeno y cuya estructura cuaternaria está casi siempre en estado R. El restante centro de unión desocupado presenta una afinidad que es 20 veces superior a la que tenía la Hb totalmente desoxigenada. Sin embargo, la conducta no es totalmente concertada, puesto que cuando la Hb se ha unido en sólo 1 de los centros de unión, su estructura cuaternaria permanece mayoritariamente en estado T. Esta molécula enlaza oxígeno con 3 veces más de afinidad a como lo haría totalmente desoxigenada, lo que concuerda con un modelo SECUENCIAL ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA COMPARACIÓN Mb vs Hb en el transporte de oxígeno 1.- La Hb es mejor transportadora de oxígeno 2.- La Mb es mejor almacenadora de oxígeno ESTRUCTURA CUATERNARIA: HEMOGLOBINA H+, CO2, 2,3 BPG ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO DEL pH Y DEL CO2 ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO BOHR A menor pH la afinidad de la Hb por el oxígeno disminuye y tiene una mayor capacidad para cederlo a los tejidos periféricos ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO BOHR ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO BOHR Cadena α Puente salino ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO BOHR ANHIDRASA CARBÓNICA El CO2 es capaz de hacer la liberación de oxígeno por parte de la Hb de 2 maneras: 1.- Disminuye el pH dentro del hematíe por la acción de la anhidrasa carbónica 2.- Interacción química directa entre CO2 y la Hb formando carbamatos ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO BOHR Contacto α−β, desoxihemoglobina α H 2N A rg 9 2 C L ys 4 0 C (C H 2 ) 3 C NH (C H 2 ) 4 N H 3 + N H 2+ - - OOC + OOC CH CH2 C H 2 C G lu 4 3 CH2 HN NH H is 1 4 6 (C -t) β ESTRUCTURA CUATERNARIA: HEMOGLOBINA Contacto α−α, desoxihemoglobina α Arg 141 C H 2N (CH2)3 C NH2+ NH COO- + H 3N + H 3N C - OOC CH2 C Asp 126 (CH2)4 Val 1 C Lys 127 α ESTRUCTURA CUATERNARIA: HEMOGLOBINA Contacto β−β, desoxihemoglobina β Asp 94 - C CH2 COO + HN NH CH2 C His 146 β ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO DEL BPG ESTRUCTURA CUATERNARIA: HEMOGLOBINA EFECTO COOPERATIVO ESTRUCTURA CUATERNARIA: HEMOGLOBINA 1.- ALTERACIONES CUALITATIVAS DE LA HEMOGLOBINA HEMOGLOBINAS MUTANTES: ANEMIA FALCIFORME ESTRUCTURA CUATERNARIA: HEMOGLOBINA HEMOGLOBINAS MUTANTES: ANEMIA FALCIFORME M u tació n p u n tu a l se d eb e a u n cam b io en el co d ó n G A C n o rm al, q u e p a sa a G T G , q u e d a co m o resu ltad o la su stitu ció n d el am in o ácid o : ácid o glu tám ico p o r valin a, en la p o sició n 6 d e la cad en a b eta lo caliz ad a en el cro m o so m a 11 En e stu d io s re alizad o s e n p a d re s d e n iñ o s co n d re p an o cito sis revelan q u e hasta u n 4 0 % d e su h e m o glo b in a e s an o rm al ESTRUCTURA CUATERNARIA: HEMOGLOBINA HEMOGLOBINAS MUTANTES: ANEMIA FALCIFORME Estos glóbulos rojos falciformes no son flexibles y forman tapones en los vasos sanguíneos pequeños, produciendo una interrupción de la circulación de la sangre que puede dañar los órganos de cualquier parte del cuerpo *afecta a los glóbulos rojos de la sangre *cambian su forma a la de una hoz o media luna ESTRUCTURA CUATERNARIA: HEMOGLOBINA HEMOGLOBINAS MUTANTES: ANEMIA FALCIFORME • Glutamico por valina en la cadena beta. • Se la denomina hemoglobina S disminuyendo la solubilidad de la proteína desoxiHb y las hemoglobinas tienden a polimerizar generando la forma característica • Produce anemia drepanocítica o de células falciformes, con hematíes en forma de hoz. • Se favorece por la hipoxia y hay hemolisis • Mas frecuente en la raza negra. • Diagnóstico por electroforesis. RELACIÓN CON LA MALARIA ESTRUCTURA CUATERNARIA: HEMOGLOBINA 2.- ALTERACIONES CUANTITATIVAS DE LA HEMOGLOBINA TALASEMIA Las talasemias son un grupo muy heterogéneo de anemias hereditarias caracterizadas por la disminución o ausencia total de la síntesis de una o varias cadenas de la hemoglobina. Según qué cadena de globina esté sintetizada en menor cantidad (aunque siempre globina de características normales) se llamará 1.- Talasemia alfa (a ) 2.- Talasemia beta (b ). Y según la severidad del cuadro: 1.- Talasemia mayor (se heredan las dos copias del gen con una alteración importante en cada copia o alelo), intermedia (se heredan dos copias con dos alteraciones moderadas o una alteración importante y una moderada) 2.- Talasemia minor (también conocida como rasgo talasémico, se debe a la herencia de un alelo alterado y otro normal). ESTRUCTURA CUATERNARIA: HEMOGLOBINA HEMOGLOBINA M Presencia de Fe3+ en vez de Fe2+. La Metahemoglobina, se genera por la Oxidación de las Fracciones Hemo al Estado Férrico, lo que provoca un Color Azulado – Pardo, similar a la cianosis. La Metahemoglobina tiene una Afinidad tan Alta por el Oxígeno, que prácticamente No Libera Nada a los Tejidos. Las Concentraciones Mayores del 50 al 60%, a menudo, son Mortales. La Metahemoglobinemia Congénita, surge como Consecuencia de Mutaciones de la Globina que Estabilizan el Hierro en Estado Férrico [Hb Iwata (α 87 His → Tyr)], o por Mutaciones que Alteran las Enzimas que Reducen la Metahemoglobina a Hemoglobina [por ejemplo, Metahemoglobina Reductasa, NADP Diaforasa]. La Metahemoglobinemia Adquirida, se debe a Toxinas que Oxidan el Hierro del Hemo, especialmente, los Compuestos que contienen Nitratos o Nitritos. ESTRUCTURA CUATERNARIA: HEMOGLOBINA HEMOGLOBINA FETAL 1.- Tiene una gran afinidad por el O2 2.- Existe una modificación de la His 143 de la subunidad ß por una Ser 143 3.- Dicha modificación afecta al sitio de unión del BPG a la hemoglobina 4.- Se eliminan cargas positivas del centro donde se produce la unión disminuyendo la afinidad de la HbF por el 2,3 BPG 5.- Por lo tanto tiene una mayor afinidad que la Hb materna para unirse al O2 6.- Existe una transferencia muy eficaz de los hematíes maternos a los fetales DESNATURALIZACIÓN DE PROTEINAS Consiste en la pérdida de la estructura cuaternaria, terciaria por romperse los puentes que forman dicha estructura Todas las proteínas desnaturalizadas tienen la misma conformación muy abierta y con una interacción máxima con el disolvente una proteína soluble en agua cuando se desnaturaliza se hace insoluble precipita La desnaturalización se puede producir por cambios temperatura (> 60-70 ºC) variaciones del pH. salinidad Urea En algunos casos, si las condiciones se restablecen, una proteína desnaturalizada puede volver a su anterior plegamiento o conformación, proceso que se denomina renaturalización. DESNATURALIZACIÓN DE PROTEINAS Qué ocurre durante el calentamiento de las proteínas ? DESNATURALIZACIÓN DESNATURALIZACIÓN DE PROTEINAS MUCHAS PROTEÍNAS SÓLO RETIENE SU ACTIVIDAD BIOLÓGICA DENTRO DE UNA FLUCTUACIÓN LIMITADA DE pH y TEMPERATURA SECUENCIACIÓN DEGRADACIÓN DE EDMAN 1.- Marcaje del amino terminal con PITC (Fenilisotiocianato) en medio alcalino. Se forma el derivado feniltiocarbamilo 2.- Se hidroliza el enlace peptídico entre el aminoácido 1 y 2 3.- Se identifica el derivado del residuo N-terminal por HPLC SECUENCIACIÓN Degradación secuencial Análisis de Péptidos Degradación de Edman S N C + H NH CH CO NH R1 CH CO R2 N H C H C OOH R3 1ª) Adición en medio básico de isotiocianato de fenilo H S N C 2ª) Hidrólisis suave solo del terminal con HCl en CH 3 NO 2 ó Acético Mejora de este es soportar mediante el COOH a un polímero el péptido e ir degradando secuencialmente NH CH CO NH R1 CH CO N H C H COOH R2 + H OO C O C H C H RR 1 C H 1 S N N NH C NH C R3 NH2 CH R2 CO N H C H C OOH R3 Puede repetirse el proceso con el resto hasta 30 ó más veces si el péptido es grande S Tiohidantoina feniltiohidantoína Se separa e identifica SECUENCIACIÓN SECUENCIACIÓN PLEGAMIENTO DE PROTEÍNAS Experimento de Anfinsen - ß-mercaptoetanol - Urea + Urea P2 P2 Bis + ß-mercaptoetanol - ß-mercaptoetanol - Urea P1 P1 Bis Anfinsen cogió ribonucleasa, una proteína pequeña (14000 Daltons) y que tiene 4 puentes disulfuro. Desnaturalizó el enzima con urea y bmercaptoetanol la solución resultante la dividió en dos alícuotas P1 y P2. A la alícuotas P1 le eliminó primero el bmercaptoetanol, dejo reposar y le eliminó luego la urea (alícuota resultante P1bis). A la alícuotas P2 le eliminó primero la urea, y luego el b-mercaptoetanol (alícuota resultante P2b). Una vez hecho esto miro la actividad enzimática de P1bis y P2bis. Encontró que la alícuota P2b había mucha actividad enzimática, mientras que en P1b prácticamente no había nada. Son las interacciones no-enlazantes y no las enlazantes (puentes disulfuro) las que guían el plegamiento. PLEGAMIENTO DE PROTEÍNAS ENFERMEDAD DE ALZHEIMER Otras enfermedades (priones, diabetes, etc…)
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados