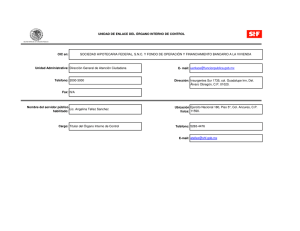
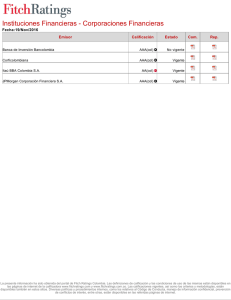
Ficha, Informe y Evaluación (Doc. PDF=361 Kb)
Anuncio

Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica MEDICAMENTOS INFORMACIÓN Y EVALUACIÓN DE NOVEDADES TERAPÉUTICAS INFORME Nº: 21 Principio activo: ELETRIPTÁN Especialidades: RELPAX, RELERT® Fecha de la última revisión: Mayo 2003 Revisores: Horga JF, Más Serrano P, Peiró AM, Zapater P CONTENIDO Ficha informativa Informe y Evaluación Ficha Técnica remitida por el laboratorio: • Relpax, Relert® ELABORADO POR: Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 1 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica FICHA INFORMATIVA FICHA Nº: 21 ELETRIPTÁN (DCI); Relpax®, Relert® Última Actualización: Abril 2003 EFICACIA El porcentaje de pacientes que respondieron, con una reducción del dolor de cabeza de moderado o severo a leve o no dolor (variable: “respuesta analgésica a las 2 horas”), con eletriptán comparado con placebo a las dosis de 20 mg fue 45 vs. 22,1; a la dosis de 40 mg 59,2 vs. 24,5 y con la dosis de 80 mg 62,5 vs. 24,5, respectivamente. Y para la variable “respuesta analgésica sostenida durante 24 horas” (respuesta analgésica a las 2 horas mantenida durante las 24 horas siguientes al tratamiento (sin recurrencia del dolor a moderado o severo) y sin la necesidad de utilizar mediación de rescate o una segunda dosis de la mediación de estudio) comparado con placebo fue 39 vs. 19; 46 vs. 18 y 53 vs. 18 para las dosis de eletriptán 20, 40 y 80 mg, respectivamente. En los estudios de comparación directa con otros fármacos, para la variable “respuesta analgésica a las 2 horas”, eletriptán 80 mg fue significativamente superior a sumatriptán 100 mg (77% vs. 55%). En otro de estos estudios, eletriptán 40 y 80 mg fue significativamente superior a sumatriptán 50 y 100 mg (64% y 67% vs. 50% y 53%, respectivamente). TOXICIDAD MÁS RELEVANTE Los eventos adversos generales que aparecen con una frecuencia >1/100 y <1/10 fueron: astenia, síntomas torácicos (dolor, opresión), cefalea, dolor abdominal, dolor de espalda y escalofríos, opresión en la garganta. COSTE / EFICACIA El coste del tratamiento de un ataque agudo de migraña con eletriptán (40-80 mg) es de 7,98 – 15,97 euros/día. Se ha estimado que la mediana de pérdida de trabajo en pacientes tratados con eletriptán, 40 y 80 mg, fue de 4 horas, mientras que para el grupo placebo fue de 9 horas. Dichas pérdidas suponen un coste asociado de 4722, 5701 y 10510 euros para los grupos eletriptán 40 mg, 80 mg y placebo, respectivamente, en una cohorte de 100 pacientes británicos. INDICACIONES AUTORIZADAS Migraña: Tratamiento agudo de la fase de cefalea de los ataques de migraña con o sin aura. APORTACIONES PRINCIPALES En base a los datos publicados hasta la fecha, eletriptán comparado con sumatriptán logra mejores porcentajes de respuesta, tanto en el inicio de la respuesta (variable “respuesta analgésica” a las 2 horas) como en su mantenimiento (variable “respuesta analgésica sostenida durante 24 horas”). Una vez que se publiquen ensayos clínicos comparativos de eletriptán con otros triptanos se podrá establecer con mayor precisión si eletriptán representa o no un avance terapéutico significativo y dentro de su grupo. 2 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Mecanismo de Acción y Farmacocinética Pauta terapéutica e indicaciones Eletriptán es un agonista selectivo de los receptores 5HT (conocidos como triptanos) y posee alta afinidad por los receptores 5-HT1B, 1D y 1F. La acción fundamental consiste en un efecto vasoconstrictor del territorio arterial carotídeo afectando a la arteria cerebral media, el árbol arterial meníngeo y la arteria basilar. Esta acción sobre el tono vascular craneal parece que es, junto con una acción antiinflamatoria perivascular del territorio inervado por el trigémino la responsable de su efecto terapéutico fundamental, la responsable de la mejoría del ataque agudo de migraña. Migraña: Tratamiento agudo de la fase de cefalea de los ataques de migraña con o sin aura. Dosis inicial 40 mg. Si hay respuesta inicial pero la cefalea reaparece en menos de 24 h siguientes, administrar otros 40 mg dejando un intervalo entre dosis de al menos 2 h. Si no se obtiene respuesta inicial en 2 h con la primera dosis, no se deberá tomar una segunda dosis para el mismo ataque. En pacientes con insuficiencia renal leve o moderada se recomienda una dosis inicial de 20 mg y una dosis máxima diaria de 40 mg. No se recomienda su uso en insuficiencia renal grave. No se requieren ajustes de dosis insuficiencia hepática leve o moderada. Debido a que no se ha estudiado en insuficiencia hepática grave, no se recomienda el uso en este caso. Tampoco se recomienda su utilización en pacientes ancianos (>65 años) (Ficha técnica: Eletriptán. Pfizer Inc., 2002b). Eletriptán se absorbe rápidamente a través de la barrera gastrointestinal tras su administración oral (Pfizer Laboratories Limited, 2002). Su biodisponibilidad absoluta vía oral es aproximadamente de un 50%, el Tmáx de 1-1,5 horas, su farmacocinética es lineal dentro del rango de dosis utilizadas (20 y 80 mg) (Milton y col., 2002. J.Clin Pharmacol., 42, 528-539) y la comida rica en grasas favorece su absorción. Se une en un 85% a proteínas y posee un volumen de distribución de 2-2,5 L/kg. El metabolismo hepático es el responsable del 90% del aclaramiento total de eletriptan, vía citocromo P-450 (CYP3A4) (Drugdex drug evaluation. Eletriptán., 2002), siendo las concentraciones plasmáticas del metabolito activo un 10-20% del fármaco total, por lo que no parece contribuir a la acción terapéutica del eletriptán (Pfizer Laboratories Limited, 2002). El aclaramiento renal tras su administración vía oral es de aproximadamente 3,9 L/h y se excreta un 9% de forma inalterada. La vida media de eliminación es de 4 a 5 horas. Los ensayos clínicos realizados muestran que los pacientes que no responden al tratamiento de un ataque pueden aún responder al tratamiento de un ataque posterior. Los pacientes que no obtengan eficacia satisfactoria con 40 mg, (con buena tolerancia y sin respuesta al tratamiento en 2 ataques de 3), podrán ser tratados con 80 mg en ataques de migraña posteriores, sin poder administrarse una segunda dosis de 80 mg en las siguientes 24 h. Dosis máxima: 80 mg/día (Ficha técnica: Eletriptán. Pfizer Inc., 2002b). Está contraindicado la administración conjunta de fármacos derivados de ergotamina y otros agonistas 5HT1 con eletriptán en las 24 h siguientes a su administración. Asimismo, deberán transcurrir al menos 24 h tras la administración de un fármaco que contenga ergotamina antes de poder administrar eletriptán. No se recomienda el uso de eletriptán junto con eritromicina, ketoconazol y otros inhibidores de CYP3A4, como mínimo en las primeras 72 horas (Ficha técnica. FDA). Eficacia El porcentaje de pacientes que respondieron a la variable “respuesta analgésica a las 2 horas” con eletriptán comparado con placebo a las dosis de 20 mg fue 45 vs. 22,1; a la dosis de 40 mg 59,2 vs. 24,5 y con la dosis de 80 mg 62,5 vs. 24,5, respectivamente. Y para la variable “respuesta analgésica sostenidadurante 24 horas” comparado con placebo fue 39 vs. 19; 46 vs. 18 y 53 vs 18 para las dosis de eletriptán 20, 40 y 80 mg, respectivamente (Smith y col., 2001. Cochrane. Database. Syst. Rev., CD003224). Coste del tratamiento El coste del tratamiento de un ataque agudo de migraña con eletriptán es de (40-80 mg) 7,98 – 15,97 euros/día. Se ha estimado que la mediana de pérdida de trabajo en pacientes tratados con eletriptán, 40 y 80 mg, fue de 4 horas, mientras que para el grupo placebo fue de 9 horas. Dichas pérdidas suponen un coste asociado de 4722, 5701 y 10510 euros para los grupos eletriptán 40 mg, 80 mg y placebo, respectivamente, en una cohorte de 100 pacientes estudiada en Inglaterra (Wells y Steiner, 2000. Pharmacoeconomics, 18:557-566). En los estudios de comparación directa entre eletriptán y sumatriptán, para la variable “respuesta analgésica a las 2 horas”, eletriptán 80 mg fue significativamente superior a sumatriptán 100 mg (77% vs. 55%) (Goadsby y col., 2000. Neurology, 54:156-163). En otro estudio, eletriptán 40 y 80 mg fue significativamente superior a sumatriptán 50 y 100 mg (64% y 67% vs. 50% y 53%, respectivamente) (Sandrini y col., 2002. Neurology, 54:156-163). Un estudio de modelización, remitido por el promotor, realizado a partir de los datos de eficacia de un metaanálisis de ensayos clínicos de distintos triptanes y con los costes del mercado español, sugiere una disminución del coste total por ataque tratado con éxito con eletriptán. Seguridad En general, eletriptán se tolera bien, siendo la mayoría de las reacciones adversas leves y transitorias. La incidencia de eventos adversos no se ve influida por factores como la edad, sexo o raza de los pacientes. En estudios clínicos aleatorizados en los que se utilizaron dosis de 20, 40 y 80 mg, se ha puesto de manifiesto que la incidencia de reacciones adversas es dosis dependiente. Las reacciones adversas más frecuentes son astenia, náusea, mareos y somnolencia. Lugar en la terapéutica En base a los datos publicados hasta la fecha, eletriptán comparado con sumatriptán logra mejores porcentajes de respuesta, tanto en el inicio de la respuesta (variable “respuesta analgésica” a las 2 horas) como a su mantenimiento (variable “respuesta analgésica sostenida durante 24 horas”). Una vez que se publiquen ensayos clínicos comparativos de eletriptán con otros triptanos se podrá establecer con mayor precisión si eletriptán representa o no un avance terapéutico significativo y dentro de su grupo. Los eventos adversos generales que aparecen con una frecuencia >1/100 y <1/10 fueron: astenia, síntomas torácicos (dolor, opresión), cefalea, dolor abdominal, dolor de espalda y escalofríos, opresión en la garganta (Ficha técnica: Eletriptán. Pfizer Inc., 2002b). 3 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica INFORME Y EVALUACIÓN Informe Nº: 21 Fármaco: ELETRIPTÁN Denominación química: 3-[[(R)-1-metil-2-pirrolidinil]metil]-5-[2-(fenilsulfonil)etil]indol Composición cuantitativa: C 69.08% H 6.85% N 7.32% O 8.36% S 8.38% Fórmula empírica: C22H26N2O2S Peso molecular: 382,50 Fuente: http://www.portalfarma.com/home.nsf Especialidades comercializadas en España que contienen ELETRIPTAN: Clase Código Nombre ESPEC. 955724 RELERT 20 MG 2 COMPRIMIDOS ESPEC. 960633 RELERT 20 MG 4 COMPRIMIDOS ESPEC. 965483 RELERT 40 MG 2 COMPRIMIDOS ESPEC. 965491 RELERT 40 MG 4 COMPRIMIDOS ESPEC. 987214 RELPAX 20 MG 2 COMPRIMIDOS ESPEC. 954867 RELPAX 20 MG 4 COMPRIMIDOS ESPEC. 954875 RELPAX 40 MG 2 COMPRIMIDOS ESPEC. 954883 RELPAX 40 MG 4 COMPRIMIDOS Fuente: http://www.portalfarma.com/home.nsf 4 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Indicaciones autorizadas en España: Migraña: Tratamiento agudo de la fase de cefalea de los ataques de migraña con o sin aura. (Fuente: ficha técnica del producto) Grupo Terapéutico: N02CC: ANTIMIGRAÑOSOS: AGONISTAS SELECTIVOS RECEPTORES 5-HT1 Coste de las especialidades de Eletriptán comercializadas en España: Especialidad Laboratorio PVP (IVA incl.): Fecha de alta RELERT 20 MG 2 COMPRIMIDOS 456: PFIZER 10,15 EUR 01/07/2001 RELERT 20 MG 4 COMPRIMIDOS 456: PFIZER 19,96 EUR 01/07/2001 RELERT 40 MG 2 COMPRIMIDOS 456: PFIZER 16,24 EUR 01/07/2001 RELERT 40 MG 4 COMPRIMIDOS 456: PFIZER 31,93 EUR 01/07/2001 RELPAX 20 MG 2 COMPRIMIDOS 456: PFIZER 10,15 EUR 01/07/2001 RELPAX 20 MG 4 COMPRIMIDOS 456: PFIZER 19,96 EUR 01/07/2001 RELPAX 40 MG 2 COMPRIMIDOS 456: PFIZER 16,24 EUR 01/07/2001 RELPAX 40 MG 4 COMPRIMIDOS 456: PFIZER 31,93 EUR 01/07/2001 Fuente: http://www.portalfarma.com/home.nsf 5 DE Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica INDICE INDICE.........................................................................................................................................6 A) INTRODUCCIÓN ....................................................................................................................8 1.- Mecanismo de acción y grupo farmacológico ...............................................................8 2.- Farmacocinética ..........................................................................................................11 2.1.- Absorción ..........................................................................................................................................11 2.2.- Distribución .......................................................................................................................................11 2.3.- Metabolismo y excreción...................................................................................................................12 2.4.- Eliminación .......................................................................................................................................12 2.5.- Farmacocinética: potenciales factores modificadores........................................................................12 B) EFICACIA .............................................................................................................................13 1.- Diseño de los estudios.................................................................................................13 2.- Características de la población de estudio..................................................................18 3.- Resultados: eficacia frente a placebo..........................................................................20 Respuesta analgésica..................................................................................................................................21 Respuesta libre de dolor.............................................................................................................................21 Respuesta analgésica sostenida durante 24 horas.......................................................................................21 4.- Eficacia frente a otros fármacos: Sumatriptán ............................................................24 Respuesta analgésica..................................................................................................................................24 Respuesta libre de dolor.............................................................................................................................29 Respuesta analgésica sostenida durante 24 horas.......................................................................................32 5.- Eficacia frente a otro fco: cafeína + ergotamina..........................................................34 Respuesta analgésica..................................................................................................................................34 Respuesta libre de dolor.............................................................................................................................34 6.- Eficacia frente a otros triptanos distintos a sumatriptán..............................................34 Respuesta analgésica..................................................................................................................................34 Respuesta libre de dolor.............................................................................................................................38 Respuesta analgésica sostenida durante 24 horas.......................................................................................38 C) SEGURIDAD ........................................................................................................................39 1.- Descripción ..................................................................................................................39 Mutagénesis, carcinogénesis e infertilidad.................................................................................................39 Teratogénesis .............................................................................................................................................40 Eventos adversos .......................................................................................................................................40 Intoxicación ...............................................................................................................................................45 2.- Contraindicaciones y precauciones.............................................................................46 Contraindicaciones ....................................................................................................................................46 Precauciones ..............................................................................................................................................46 3.- Interacciones ...............................................................................................................47 6 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Fármacos derivados de ergotamina............................................................................................................47 Inhibidores CYP3A4..................................................................................................................................48 Inhibidores de la MAO ..............................................................................................................................48 Propranolol, verapamilo y fluconazol ........................................................................................................48 Otros agonistas 5HT1 ................................................................................................................................48 D) PAUTA TERAPÉUTICA E INDICACIONES ........................................................................49 Adultos, oral: .............................................................................................................................................49 Dosis en situaciones especiales:.................................................................................................................49 E) FARMACOECONOMÍA........................................................................................................51 1.- Estudios de Farmacoeconomía...................................................................................51 2.- Precios comparativos ..................................................................................................51 F) CONCLUSIONES .................................................................................................................52 REFERENCIAS BIBLIOGRÁFICAS.........................................................................................52 7 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica A) Introducción 1.- Mecanismo de acción y grupo farmacológico La migraña es una alteración neurovascular incapacitante, crónica, que se caracteriza por crisis agudas de cefaleas, y en el que una serie de eventos neurales conllevan una dilatación de los vasos, que como consecuencia, provocan dolor y una activación nerviosa. Estos cambios están desencadenados por la liberación de serotonina (5-HT) (Goadsby y col., 2002). Existen tres tipos principales de receptores de 5-HT: 5-HT1, 5-HT2 y 5-HT3 (se han identificado hasta 7 clases distintas). A su vez los receptores 5-HT1 se subdividen en los subtipos A, B, C, D y E. • Los receptores 5-HT1 se encuentran principalmente en el SNC, neuronas entéricas y vasos sanguíneos. Los efectos neuronales son inhibitorios. • Los receptores 5-HT2 se encuentran en el SNC, músculo liso y plaquetas. Los efectos neuronales y sobre el músculo liso son excitatorios. • Los receptores 5-HT3 se encuentran en el sistema periférico, especialmente en las neuronas aferentes nociceptivas, y en las neuronas entéricas. Los efectos son excitatorios. Eletriptán es un agonista selectivo de los receptores 5HT (conocidos como triptanos), posee alta afinidad por los receptores 5-HT1B, 1D y 1F, modesta sobre los receptores 5-HT1A, 1E, 2B y T7, y nula afinidad sobre los receptores 5-HT2A, 2C, 3, 4, 5A y 6. Eletriptán no posee afinidad ni actividad farmacológica sobre los receptores alfa1, alfa2 o beta adrenérgicos; dopaminérgicos D1 o D2; muscarínicos u opioides (Pfizer Inc., 2002a). La acción fundamental consiste en un efecto vasoconstrictor del territorio arterial carotídeo afectando a la arteria cerebral media, el árbol arterial meníngeo y la arteria basilar. Esta acción sobre el tono vascular craneal parece que es, junto con una acción antiinflamatoria perivascular del territorio inervado por el trigémino la responsable de su efecto terapéutico fundamental: la mejoría del ataque agudo de migraña. La acción vasoconstrictora craneal depende fundamentalmente de la 8 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica activación de receptores 5-HT1B, en tanto que en la inhibición de la inflamación perivascular participan los receptores 5-HT1D y 5-HT1F (Gawel y Grujich, 2001). Eletriptán es químicamente similar al zolmitriptán y al rizatriptán. El perfil farmacológico in vitro del eletriptán, como otros triptanos, muestra alta afinidad por los receptores recombinantes humanos 5-HT1B, 5-HT1D y 5-HT1F. Parece ser que el eletriptán posee cinco veces más afinidad por el receptor 5-HT1D que el sumatriptán (Drugdex (R) Editorial Staff, 2002). Los estudios in vitro han demostrado que tanto eletriptán como sumatriptán son igual de efectivos en la respuesta contráctil que ejercen sobre la arteria media meníngea humanas aisladas y sobre la venas safenas. Sin embargo, eletriptán es menos potente que sumatriptán en la evocación de las respuestas contráctiles en la arteria coronaria aislada de humanos (Gawel y Grujich, 2001). En general los triptanos son efectivos en el tratamiento agudo de las crisis de migraña, disminuyendo el dolor, las náuseas y los vómitos. Comparados con los alcaloides derivados de la ergotamina, el efecto farmacológico de los triptanos parece estar limitado a los receptores de la familia 5HT1. Los triptanos son mucho más selectivos que los alcaloides derivados de la ergotamina ya que interaccionan potencialmente con los receptores 5HT1D y 5HT1B y tienen una afinidad baja o nula con otros subtipos de receptores 5HT. Las dosis efectivas clínicas de triptanos y alcaloides ergóticos no se correlacionan bien con sus afinidades con los receptores 5HTA y 5HT1E, pero se correlacionan bien con sus afinidades con los receptores 5HT1B y 5HT1D. Los datos que se tienen actualmente son consistentes con la hipótesis de que los 5HT1B y/o 5HT1D son los receptores que parecen estar relacionados con el mecanismo de acción de los fármacos antimigrañosos (Goadsby y col., 2002; Sanders-Bush E. y Mayer S.E., 2001). Existen dos hipótesis que han sido propuestas para explicar la eficacia de los agonistas de los receptores 5HT1B/1D en el tratamiento de la migraña. Una hipótesis sugiere que el estímulo de estos receptores causa vasoconstricción de los vasos intracraneales incluidas las anastomosis arteriovenosas. De acuerdo con los modelos fisiopatológicos de la migraña, durante una crisis aguda, aproximadamente el 80% de la sangre arterial carotídea se desvía a través de anastomosis carotídeas arterio-venosas, localizadas principalmente en la piel craneal, y disminuyendo transitoriamente la perfusión cerebral total, produciendo isquemia e hipoxia cerebral. 9 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Basado en este modelo, un antimigrañoso efectivo cerraría estas anastomosis y restablecería el flujo sanguíneo al cerebro. De hecho, ergotamina, dihidroergotamina y sumatriptán comparten la habilidad de producir este efecto vascular (Sanders-Bush E. y Mayer S.E., 2001). Una hipótesis alternativa está relacionada con la observación de que tanto los receptores 5HT1B como los 5HT1D sirven como autorreceptores presinápticos, modulando la liberación de neurotransmisores en las terminaciones neuronales. Los agonistas 5HT1 bloquearían la liberación de neuropéptidos proinflamatorios a nivel de las terminaciones nerviosas en el espacio perivascular. Ergotamina, dihidroergotamina y sumatriptán se han mostrado capaces de bloquear el desarrollo de extravasación neurogénica del plasma en la duramadre tras la despolarización de los axones perivasculares tras la inyección de capsaicina o la estimulación del nervio trigémino. La habilidad de los agonistas 5HT1 de inhibir la liberación de los neurotransmisores endógenos en el espacio perivascular podría estar relacionado con su eficacia en el tratamiento del ataque agudo de migraña (Sanders-Bush E. y Mayer S.E., 2001). Eletriptán se caracteriza por una alta afinidad por los receptores 5HT1B y 5HT1D, y ha demostrado una rápida asociación y una lenta disociación del receptor 5HT1D in vitro. Igualmente, ha demostrado mayor selectividad por los vasos craneales que por los cardíacos en modelos animales y en tejido humano aislado (Stark y col., 2002). Eletriptán también posee una alta afinidad por el receptor 5HT1F que puede contribuir a su actividad antimigrañosa. Estudios en animales con eletriptán han demostrado una gran selectividad por la carótida, en contraposición con el sumatriptán que poseía selectividad por los lechos vasculares coronarios y femorales. Además el eletriptán ha demostrado inhibir la inflamación neurogénica en la duramadre de animales. Tanto la habilidad de producir vasocontracción de los vasos sanguíneos intracraneales y su acción inhibidora de la inflamación neurogénica puede contribuir a su acción antimigrañosa en humanos (Pfizer Laboratories Limited, 2002). 10 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 2.- Farmacocinética 2.1.- Absorción Eletriptán se absorbe rápidamente a través de la barrera gastrointestinal tras su administración oral (Pfizer Laboratories Limited, 2002). Su biodisponibilidad absoluta vía oral es aproximadamente de un 50% (Milton y col., 2002). Ésta representa la biodisponibilidad en sujetos sanos y en paciente con migraña durante periodos libre de migraña. La biodisponibilidad es mayor que la del sumatriptán vía oral y similar a la del rizatriptán y zolmitriptán, y menor que la del naratriptán (Pfizer Inc., 2002b). El Tmáx se encuentra entre 1 y 1,5 horas tras su administración oral y ha demostrado una farmacocinética lineal dentro del rango de dosis utilizadas (20 y 80 mg) (Milton y col., 2002). La absorción del eletriptán se reduce ligeramente, tanto en la cantidad como en la velocidad de absorción (AUC un 30%, Tmáx se incrementa a 2,8 horas) durante los periodos de ataque agudo de migraña, al igual que ocurre con otros agonistas de los receptores 5HT1, comparado con los periodos libre de migraña. Esta diferencia se ha atribuido a fenómenos de estasis gástrico (Drugdex (R) Editorial Staff, 2002). La comida favorece la absorción de eletriptán. Tras la administración de una comida rica en grasa, tanto el AUC como la Cmáx se incrementaron en un 20-30% (Pfizer Laboratories Limited, 2002). Tras la administración de dosis repetidas (20 mg TID) durante 5-7 días, la farmacocinética del eletriptán se mantiene lineal y su acumulación es predecible. En administración múltiple de dosis altas (40 mg TID y 80 mg BID), la acumulación del fármaco durante 7 días fue un 40% superior a lo que cabría esperar (Pfizer Laboratories Limited, 2002). 2.2.- Distribución Eletriptán se une un 85% a proteínas y posee un volumen de distribución de 2-2,5 L/kg, tras la administración del fármaco vía i.v. en pacientes migrañosos durante el periodo libre de migraña (Drugdex (R) Editorial Staff, 2002). 11 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 2.3.- Metabolismo y excreción El metabolismo hepático es el responsable del 90% del aclaramiento total de eletriptán. Los estudios in vitro indican que su metabolismo está mediado por el citocromo P-450 a través del CYP3A4 (Drugdex (R) Editorial Staff, 2002). Se han identificado dos metabolitos importantes en la circulación sistémica. El metabolito formado por N-desoxidación que no ha mostrado actividad en modelos animales. Sin embargo, el metabolito formado por N-desmetilación sí ha mostrado ser activo en modelos animales. Las concentraciones plasmáticas de este metabolito activo representan solo un 10-20% del fármaco total, por lo que no parece contribuir a la acción terapéutica del eletriptán (Pfizer Laboratories Limited, 2002). 2.4.- Eliminación El aclaramiento total de eletriptán tras una administración i.v. es de 36 L/h (6,5 ml/min/kg), en sujetos sanos y en pacientes con migraña durante períodos sin dolor. El aclaramiento renal tras su administración vía oral es de aproximadamente 3,9 L/h, se excreta un 9% de forma inalterada. El aclaramiento no renal representa un 90% del aclaramiento total, indicando que el eletriptán se elimina principalmente por metabolismo (Pfizer Laboratories Limited, 2002)(Milton y col., 2002). La vida media de eliminación es de 4 a 5 horas, independientemente de la vía utilizada (oral ó i.v.) (Drugdex (R) Editorial Staff, 2002). 2.5.- Farmacocinética: potenciales factores modificadores Sexo Un metaanálisis realizado de los estudios farmacocinéticos con eletriptán demostró que el sexo no tiene ninguna influencia en las concentraciones plasmáticas de eletriptán (Pfizer Laboratories Limited, 2002). Insuficiencia hepática Una insuficiencia hepática grado A/B Child-Pugh provoca un incremento del 34% en la vida media y AUC y un pequeño incremento en Cmáx (18%). No se dispone de datos que indiquen que estos cambios son clínicamente relevantes. (Pfizer Inc., 2002a; Pfizer Laboratories Limited, 2002). Insuficiencia renal 12 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica La insuficiencia renal leve (Clcr 61-89 ml/min), moderada (Clcr 31-60 ml/min) o grave (Clcr <30 ml/min) no provoca alteración significativa alguna de Cmáx, AUC, vida media o unión a proteínas plasmáticas. En pacientes con insuficiencia renal, eletriptán incrementa la presión sanguínea en un mayor grado que en sujetos sanos (Pfizer Laboratories Limited, 2002). Población geriátrica La farmacocinética de eletriptán no se modifica en función de la edad. Existe una pequeña reducción en el aclaramiento (16%) asociado con una disminución estadísticamente significativa de la vida media (de 4,4 a 5,7 horas) entre pacientes ancianos (65-93 años) y sujetos adultos jóvenes (18-45 años) (Pfizer Laboratories Limited, 2002). Población adolescente La farmacocinética de eletriptán en pacientes adolescentes jóvenes (40-80 mg) es similar a la vista en sujetos sanos adultos (Pfizer Laboratories Limited, 2002). Población pediátrica El aclaramiento de eletripán no se modifica en niños (7-11 años) comparados con adolescentes. Si bien el volumen de distribución es menor en niños, con el consiguiente incremento en los niveles plasmáticos (Pfizer Laboratories Limited, 2002). B) Eficacia 1.- Diseño de los estudios En la tabla 1 se detallan los ensayos clínicos de eletriptán incluidos en esta revisión, y sus principales características se han recogido en la tabla 2. La intensidad del dolor se ha clasificado por los investigadores utilizando una escala de cuatro puntos: 0 = no dolor, 1 = dolor leve, 2 = dolor moderado y 3 = dolor severo. Las definiciones de las variables utilizadas son comunes a todos los estudios analizados y se detallan a continuación: Respuesta analgésica a un tiempo determinado (0,5, 1, 2 ó 4 horas): reducción del dolor de cabeza de moderado o severo a leve o no dolor. 13 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Respuesta libre de dolor a un tiempo determinado (0,5, 1, 2 ó 4 horas): reducción del dolor de cabeza de moderado o severo a no dolor. Respuesta analgésica sostenida durante 24 horas: respuesta analgésica a las 2 horas mantenida durante las 24 horas siguientes al tratamiento (sin recurrencia del dolor a moderado o severo) y sin la necesidad de utilizar mediación de rescate o una segunda dosis de la mediación de estudio. Tabla 1. Ensayos clínicos incluidos en la revisión Nombre de Referencia Estudio A (Diener y col., 2002) B C D E F Comparación Eletriptán vs. ergotamina + cafeína vs. placebo (Goadsby y col., 2000) Eletriptán vs. sumatriptán vs. placebo (Sandrini y col., 2002) Eletriptán vs. sumatriptán vs. placebo Información no publicada, Eletriptán vs. citada por (Smith y col., sumatriptán vs. 2001) placebo (Stark y col., 2002) Eletriptán vs. placebo Información no publicada, Eletriptán vs. citada por (Smith y col., placebo 2001) 14 Tipo de estudio Ensayo clínico aleatorizado doble ciego controlado con placebo Ensayo clínico aleatorizado doble ciego controlado con placebo Ensayo clínico aleatorizado doble ciego controlado con placebo Ensayo clínico aleatorizado doble ciego controlado con placebo Ensayo clínico aleatorizado doble ciego controlado con placebo Ensayo clínico aleatorizado doble ciego controlado con placebo Tipo de publicación Artículo Artículo Artículo Metaanálisis Artículo Metaanálisis Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 2: Características generales de los diseños de los estudios Estudio Pacientes A (Diener y col., Migraña con o sin 2002) aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-65 años B (Goadsby y col., Migraña con o sin 2000) aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-71 años Grupos de tratamiento (nº pacientes) Eletriptán: 80 mg (214) 40 mg (210) Ergotamina 2 mg + cafeína 200 mg (203) Placebo (106) Eletriptán: 80 mg (118) 40 mg (117) 20 mg (129) Sumatriptán 100 mg (115) Placebo (142) Procedimiento del estudio Variables estudiadas Estudio de un único ataque de migraña (de intensidad moderada como mínimo). Seguimiento para evaluación: 7-14 días post-tratamiento. Período de lavado: 48 h para triptanos o ergotamina y 6 h para analgésicos o antieméticos. Medicación de rescate: si no responde a las 2 h o experimenta recurrencia entre las 2 y las 24 h post-tratamiento, se puede administrar una segunda dosis del estudio. Se puede utilizar medicación de rescate (distinta de der. ergóticos o sumatriptán) transcurridas 2 h tras administración de la 2ª dosis. Estudio de un único ataque de migraña (de intensidad moderada como mínimo). Seguimiento para evaluación: 7 días post-tratamiento. Periodo de lavado: mismas características que el estudio A. Medicación de rescate: según las necesidades analgésicos o antieméticos 2h tras administración de la medicación de estudio. No se pueden utilizar sumatriptán o der. ergóticos hasta 24h postadministración. Si no responde a las 2h o experimenta recurrencia entre las 2 y las 24h posttratamiento, se puede administrar una segunda dosis del estudio. 1aria: respuesta analgésica a las 2h. 2aria: respuesta analgésica tras 1h; respuesta libre de dolor; presencia de: náusea, vómitos, fotofobia y fonofobia; daño funcional; tiempo en recaer; utilización de medicación de rescate; tasa de respuesta sostenida de dolor; tasa de respuesta sostenida libre de dolor y aceptación del tratamiento. 15 1aria: respuesta analgésica a las 2 h. 2aria: respuesta analgésica a 0,5, 1 y 4h; respuesta libre de dolor; presencia de: náusea, vómitos, fotofobia y fonofobia; daño funcional; impresión global a las 24 h (Global Impression of Efficacy); recurrencia; tiempo en recaer; tiempo en utilización de medicación de rescate y aceptación del tratamiento. Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Estudio Pacientes C (Sandrini y col., Migraña con o sin 2002) aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-76 años D (Smith y col., Migraña con o sin 2001) aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-65 años E (Stark y col., Migraña con o sin 2002) aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-68 años Grupos de tratamiento (nº pacientes) Eletriptán: 80 mg (164) 40 mg (175) Sumatriptán: 100 mg (170) 50 mg (181) Placebo (84) Eletriptán: 80 mg (138) 40 mg (124) Sumatriptán: 50 mg (113) 25 mg (99) Placebo (42) Eletriptán: 80 mg (462) 40 mg (453) Placebo (238) Procedimiento del estudio Estudio de tres ataques consecutivos de migraña (de intensidad moderada como mínimo). Seguimiento para evaluación: 7 días posttratamiento. Periodo de lavado: mismas características que el estudio A. Medicación de rescate: mismas características que el estudio A. Variables estudiadas 1aria: respuesta analgésica tras 1h del 1er ataque. 2aria: medida a las 0,5, 1, 2, 4 y 24 de severidad del dolor; respuesta libre de dolor; respuesta funcional; presencia de fotofobia, fonofobia o náuseas; consistencia de la respuesta; administración de 2ª dosis de mediación; utilización de mediación de rescate y aceptación del tratamiento. 1aria: respuesta analgésica tras 1 y Estudio de hasta tres ataques consecutivos de migraña (de intensidad moderada como mínimo). 2h; respuesta libre de dolor a 2h; alivio sostenido durante 24h. Periodo de lavado: mismas características que el estudio A. 2arias: respuesta analgésica a las Medicación de rescate: si no responde a las 2 h o 0,5h; respuesta libre de dolor a las 0,5 experimenta recurrencia entre las 2 y las 24 h y 1h; presencia de fotofobia, fonofobia post-tratamiento, se puede administrar una y náuseas; respuesta funcional; segunda dosis del estudio. utilización de medicación de rescate y calidad de vida (SF36). 1aria: respuesta analgésica a las 2h Estudio de hasta tres ataques consecutivos de migraña (de intensidad moderada como mínimo). del 1er ataque. 2arias: respuesta analgésica a las 0,5 Seguimiento para evaluación: 1-7 días posttratamiento del 1er ataque de migraña y tras el 3er y 1h del 1er ataque; daño funcional; ataque a los 7-14 días para evaluación final o a las presencia de: fotofobia, fonofobia y náuseas; recurrencia; utilización de 2ª 16 semanas tras la evaluación basal. Periodo de lavado: mismas características que A. dosis de estudio; utilización de Medicación de rescate: mismas características que medicación de rescate; eficacia en los 3 ataques; aceptación del tratamiento. el estudio A. 16 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Estudio F (Smith 2001) y Pacientes col., Migraña con o sin aura diagnosticada según los criterios de la IHS. Hombres y mujeres no gestantes. Edad: 18-78 años (Smith y col., 2001) Migraña con o sin aura diagnosticado según los criterios de la IHS (moderada o severa). Hombres y mujeres no gestantes. IHS: International Headache Society. Grupos de tratamiento (nº pacientes) Eletriptán: 80 mg (208) 40 mg (167) 20 mg (142) Placebo (71) Eletriptán 80 mg 40 mg 20 mg Placebo Procedimiento del estudio Variables estudiadas Estudio de hasta tres ataques consecutivos de migraña (de intensidad moderada como mínimo). Periodo de lavado: mismas características que el estudio A. Medicación de rescate: si no responde a las 4 h o experimenta recurrencia entre las 4 y las 24 h post-tratamiento, se puede administrar una segunda dosis del estudio. 1aria: respuesta analgésica tras 1 y 2h; respuesta libre de dolor a 2h; alivio sostenido durante 24h. 2arias: respuesta analgésica a las 0,5 y 4h; respuesta libre de dolor a las 0,5, 1 y 4h. Estudio de un único ataque de migraña (de intensidad moderada como mínimo) Los estudios incluidos en el metaanálisis deben contener un grupo placebo y como mínimo un grupo en el que eletriptán se administraba en dosis única en un único ataque de migraña. Medicación de rescate: permitida 2h (como mínimo) después de administrar el fco estudio. Estudios incluidos: A, B, C, D, E y F 1aria: respuesta analgésica tras 1 y 2h; respuesta libre de dolor a 2h; alivio sostenido durante 24h; efectos adversos. 2arias: respuesta analgésica a las 0,5 y 4h; respuesta libre de dolor a las 0,5, 1 y 4h. 17 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 2.- Características de la población de estudio Los criterios de inclusión para todos los ensayos clínicos revisados son bastante uniformes, pudiéndose resumir como sigue: ! Edad 18-65 años ! Hombres o mujeres ! Migraña con o sin aura (definido por la International Headache Society IHS) diagnosticado como mínimo hace 1 año y antes de los 40 años de edad de intensidad moderada o severa usando una escala estandarizada de cuatro puntos. ! Frecuencia de ataque migrañoso como mínimo 1 cada 6 semanas pero no más de 6 al mes Los criterios de exclusión principales son: ! Dolores de cabeza no migrañosos frecuentes (> 6 / mes) ! Migraña atípica que no responda a tratamiento médico ! Migraña con aura prolongada ! Migraña hemipléjica “familiar” ! Infarto migrañoso ! Enfermedad arterial coronaria ! Migraña basilar ! Arritmias cardiacas ! Insuficiencia cardiaca ! Hipertensión arterial no controlada ! Enfermedad vascular periférica o Síndrome de Raynaud ! Enfermedad sistémica activa clínicamente significativa (renal, hepática, gastrointestinal, neurológica, endocrino, metabólico o psiquiátrico) ! Absorción GI limitada ! Alergias a fármacos graves ! Abuso de alcohol u otras sustancias ! Utilización excesiva y regular de analgésicos o ergotamina ! Mujeres embarazadas, lactantes o en riesgo de quedar embarazada La información relativa a las características de estudio se recoge en la tabla 3 y los datos sobre comorbilidades y abandonos se especifican a continuación. 18 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 3: Características de las poblaciones de los estudios Estudio Grupo Placebo Cafergot Eletriptán 40 mg Eletriptán 80 mg Placebo Sumatriptán 100 mg B (Goadsby Eletriptán 20 mg y col., 2000) Eletriptán 40 mg Eletriptán 80 mg Placebo Sumatriptán 50 mg C (Sandrini Sumatriptán 100 mg y col., 2002) Eletriptán 40 mg Eletriptán 80 mg Placebo E (Stark y Eletriptán 40 mg col., 2002) Eletriptán 80 mg A (Diener y col., 2002) Edad media (años) 42 40 40 40 41 40 40 41 40 37,5 37,4 38,2 38 39,9 42 42 42 % hombres 14 14 14 10 20 16 18 15 19 11 10 13 12 13 19 17 15 Tipo de migraña (%) Con y sin Con aura Sin aura aura 13 59 27 18 52 30 13 65 21 10 61 29 11 70 18 11 73 16 13 69 19 12 66 22 13 65 22 12 63 25 10 71 18 15 64 22 14 57 30 10 68 23 7 64 29 9 67 24 8 64 28 19 Dolor de cabeza severo (%) 48 46 46 46 46 43 43 47 43 Tto previo con sumatriptán (%) 58 59 52 57 61 54 49 67 55 42 39 41 69 71 72 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 3.- Resultados: eficacia frente a placebo Actualmente, existe un debate sobre cuál es la mejor medida para la valoración de fármacos antimigrañosos y qué variable es la más representativa de la eficacia. Oldman y colaboradores (Oldman y col., 2002) han publicado un metaanálisis en el que se compara la eficacia analgésica de distintos tratamientos farmacológicos (entre los que se incluyen los triptanos) para el ataque agudo de migraña en pacientes con dolor migrañoso de intensidad moderada a severa. Las variables utilizadas por los autores para poder valorar la eficacia del tratamiento, fueron por una parte una serie de medidas a corto plazo y por otra el número de pacientes con respuesta analgésica a las 2 horas y que se mantuvieron libre de dolor durante las siguientes 22 horas. Según otros autores (Ferrari, 1999) la aproximación más útil sería el número de pacientes libres de dolor a las 2 horas y que permanecen libre de dolor durante 24 horas sin ayuda de otros analgésicos adicionales. Sin embargo, esta variable no aparece en ningún EC. La guía para los ensayos clínicos controlados en migraña (Tfelt-Hansen y col., 2000) cita como variables apropiadas para la evaluación de la eficacia de fármacos antimigrañosos la respuesta analgésica sostenida y la respuesta libre de dolor sostenida. Esta guía afirma que la respuesta libre de dolor sostenida es la respuesta ideal de un fármaco para el tratamiento del ataque agudo de migraña y que debería ser el objetivo final en el desarrollo de estos fármacos. Estudios y metaanálisis recientes (Ferrari y col., 2001; Gruffyd-Jones y col., 2001; Oldman y col., 2001) utilizan ambas variables como medidas de eficacia. La variable principal de medida de eficacia de los EC publicados fue respuesta analgésica a 1 hora o a las 2 horas de administrar el fármaco. Se han extraído del metaanálisis publicado por Smith y col. (Smith y col., 2001), los resultados de las variables: respuesta analgésica, respuesta libre de dolor y respuesta analgésica sostenida durante 24 horas de eletriptán vs. placebo, el cual incluye los resultados individuales de todos los EC realizados hasta el momento con eletriptán (A, B, C, D, E y F) y cuyos resultados fueron facilitados a los autores de 20 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica dicho estudio por Pfizer ®, algunos de los cuales no han sido publicados por el momento. Respuesta analgésica En la tabla 4 se muestran los resultados de respuesta analgésica a distintos tiempos (0,5, 1, 2 y 4 horas) con distintas concentraciones de eletriptán (20, 40 y 80 mg) frente a placebo. Tal y como refleja el NNT (número de pacientes necesario a tratar para lograr una respuesta en un paciente) cuanto mayor es la dosis y mayor es el periodo de tiempo transcurrido tras la administración del fármaco menor NNT y por lo tanto mayor eficacia (Smith y col., 2001). Respuesta libre de dolor En la tabla 5 se muestran los resultados de respuesta libre de dolor a distintos tiempos (0,5, 1, 2 y 4 horas) con distintas concentraciones de eletriptán (20, 40 y 80 mg) frente a placebo. Al igual que ocurre con la variable “respuesta analgésica” la respuesta es dosis y tiempo dependiente (Smith y col., 2001). Respuesta analgésica sostenida durante 24 horas En la tabla 6 se detallan los resultados de la variable respuesta analgésica sostenida durante 24 horas de eletriptán frente a placebo. Siendo de nuevo la eficacia dosis dependiente (Smith y col., 2001). 21 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 4: Nº de pacientes que responden al dolor a distintos tiempos de eletriptán vs. placebo (Smith y col., 2001). Dosis (mg) Eletriptán 20 40 80 Tiempo (h) Tto Control RR (IC 95%) NNT (IC 95%) Nº estudios 0,5 17 / 349 17 / 353 1,01 (0,52-1,95) - 2 1 78 / 349 40 / 353 1,98 (1,39-2,82) 12 (7,2-40) 2 2 157 / 349 78 / 353 2,04 (1,62-2,56) 4,4 (3,4-6,2) 2 4 224 / 349 106 / 353 2,13 (1,79-2,55) 2,9 (2,4-3,7)) 2 0,5 74 / 1050 30 / 694 1,65 (1.08-2.52) 37 (21-179) 5 1 378 / 1224 105 / 779 2,33 (1,91-2,84) 5,6 (4,8-7,2) 6 2 724 / 1224 191 / 779 2,38 (2,09-2,72) 2,9 (2,6-3,3) 6 4 251 / 360 106 / 353 2,33 (1,96-2,78) 2,5 (2,2-3,0) 2 0,5 100 / 1051 30 / 694 2,26 (1,51-3,38) 22 (14-51) 5 1 408 / 1221 105 / 779 2,48 (2,03-3,02) 5,0 (4,3-6,1) 6 2 763 / 1221 191/ 779 2,50 (2,19-2,85) 2,6 (2,4-3,0) 6 4 261 / 365 106 / 353 2,39 (2,01-2,84) 2,4 (2,1-2,9) 2 RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 22 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 5: Nº de pacientes con respuesta libre de dolor a distintos tiempos de eletriptán vs. placebo (Smith y col., 2001). Dosis (mg) Eletriptán 20 40 80 Tiempo (h) Tto Control RR (IC 95%) NNT (IC 95%) Nº estudios 0,5 - - 2,02 (0,19-22,1) - 2 1 12 / 349 5 / 353 2,43 (0,87-6,82) - 2 2 52 / 349 17 / 353 3,09 (1,82-5,24) 9,9 (6,9-18) 2 4 117 / 349 45 / 353 2,63 (1,93-3,58) 4,8 (3,7-6,8) 2 0,5 - - 1,63 (0,38-7,05) - 5 1 71 / 1224 9 / 779 5,00 (2,54-9,85) 22 (16-32) 6 2 365 / 1224 38 / 779 5,96 (4,30-8,27) 4,0 (3,6;4,5) 6 4 151 / 360 45 / 353 3,30 (2,45-4,45) 3,4 (2,8-4,3) 2 0,5 - - 4,50 (1,20-16,91) 70 (47-143) 5 1 138 / 1221 9 / 779 9,67 (5,00-18,71) 10 (8,3-12) 6 2 386 / 1221 38 / 779 6,40 (4,62-8,85) 3,7 (3,4-4,2) 6 4 165 / 365 45 / 353 3,55 (2,64-4,77) 3,1 (2,6-3,8) 2 RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 23 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 6: Nº de pacientes con respuesta analgésica sostenida durante 24 horas de eletriptán vs. placebo (Smith y col., 2001). Dosis (mg) Eletriptán Tto Control RR (IC 95%) NNT (IC 95%) Nº estudios 20 53 / 136 26 / 134 2,01 (1,34-3,01) 5,1 (3,3-11,1) 1 40 526 / 1157 117 / 662 2,55 (2,14-3,05) 3,6 (3,1-4,2) 5 80 618 / 1160 117 / 662 3,01 (2,53-3,58) 2,8 (2,5-3,2) 5 RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 4.- Eficacia frente a otros fármacos: Sumatriptán Respuesta analgésica Los dos únicos EC disponibles en los que se comparan eletriptán vs. sumatriptán son los realizados por Goadsby y col. y Sandrini y col. (Goadsby y col., 2000). Los(Sandrini y col., 2002) resultados de la variable “respuesta analgésica” se detallan en la tabla 7. En el estudio de Goadsby y col. (Goadsby y col., 2000) eletriptán fue significativamente superior a sumatriptán 100 mg a las dosis de 40 y 80 mg 1 hora post administración del fármaco y a la dosis de 80 mg 2 horas post administración. En el otro estudio eletriptán 80 mg 1 hora post administración fue significativamente superior a sumatriptán 50 mg y eletriptán 40 y 80 mg 2 horas post administración superior a sumatriptán 50 y 100 mg (Sandrini y col., 2002). En el metaanálisis realizado por Oldman y col. (Oldman y col., 2002) los resultados de eficacia se obtuvieron de EC en los que tanto los criterios de diagnóstico como el grado de dolor al inicio del tratamiento fueron similares en todos ellos. Además la definición de las variables fueron también similares y todos los EC utilizaron placebo como comparación. Todo esto permitió a los autores calcular una serie de variables de eficacia para distintos tratamientos farmacológicos entre lo que se encuentran sumatriptán y otros triptanos. Según los autores la eficacia relativa de 24 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica estos fármacos obtenida a través de la comparación indirecta se sustenta tanto por la relación dosis dependiente observada en el estudio como por la similitud de los resultados obtenidos por comparación directa en otros EC con tamaños maestrales grandes (parte de estos estudios han sido incluidos en dicho metaanálisis). En la tabla 9 se detallan los resultados de respuesta analgésica de sumatriptán (6 mg sc; 50 y 100 mg vo) y eletriptán (40 y 80 mg) frente a placebo. Se observa, de nuevo que la eficacia para sumatriptán administrado vía oral es también dosis y tiempo dependiente al igual que ocurre con eletriptán, y que sumatriptán administrado vía parenteral es el tratamiento más eficaz y posee el inicio de acción más corto. Los límites del IC 95% del NNT de eletriptán 80 mg a las 2 horas no se superpone con el del sumatriptán 100 y 50 mg vo al igual que ocurre con los límites de eletriptán 40 mg vs. sumatriptán 50 mg, de lo que se deduce que existen diferencias clínicas importantes entre ambos tratamientos farmacológicos, a favor de eletriptán. 25 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 7: Respuesta analgésica de eletriptán vs. sumatriptán. Resultados expresados en porcentaje (nº pacientes) Estudio B (Goadsby y col., 2000) C (Sandrini y col., 2002) T (h) Placebo 0,5 Sumatriptán (mg) 50 Eletriptán (mg) 100 20 40 80 6% (8/136) 10% (12/126) 6% (9/143) 5% (4/25) 12% (17/137) 1 12% 20% 24%1 38%1,3 41%1,3 2 24% 55% 54%1 65%1 77%1,3 1 12% 24% (43/177)1 27% (44/165)1 30% (52/172)1 37% (58/157)1,2 2 31% (25/80) 50% (88/176)1 53% (85/160)1 64% (108/169)1,2,3 67% (107/160)1,2,3 1 p<0,05 vs., placebo; 2 p<0,05 vs. sumatriptán 50 mg; 3 p<0,05 vs., sumatriptán 100 mg Tabla 8: Respuesta libre de dolor de eletriptán vs. sumatriptán. Resultados expresados en porcentaje (nº pacientes). Estudio T (h) Placebo B (Goadsby y col., 2000) 1 C (Sandrini y col., 2002) Sumatriptán (mg) 50 Eletriptán (mg) 100 20 40 80 2% 6% 2% 8% 17% 2 6% 23% 19% 29%1 37%1,3 1 1% 5% 7% 6% 13%1,2 2 4% 19%1 18%1 31%1,2,3 37%1,2,3 1 p<0,05 vs., placebo; 2 p<0,05 vs. sumatriptán 50 mg; 3 p<0,05 vs., sumatriptán 100 mg 27 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 9: Respuesta analgésica de eletriptán y sumatriptán expresado en nº paciente, extraído del metaanálisis publicado por Oldman y col. (Oldman y col., 2002). Fármaco y dosis Sumatriptán 6 mg sc Sumatriptán 50 mg vo Sumatriptán 100 mg vo Eletriptán 40 mg Eletriptán 80 mg T (h) Nº estudios Tto (nº ptes) Placebo (nº ptes) RR (IC 95%) NNT (IC 95%) 1 12 1278/1815 216/1001 3,2 (2,8-3,6) 2,1 (1,9-2,2) 2 8 379/477 131/461 2,8 (2,4-3,3) 2,0 (1,8-2,2) 1 4 268/934 77/398 1,4 (1,1-1,8) 11 (7,1-22) 2 6 532/1042 137/510 1,9 (1,6-2,2) 4,1 (3,4-5,2) 1 7 501/1628 119/678 1,6 (1,3-1,9) 7,6 (5,9-10) 2 13 1346/2311 336/1211 2,0(1,8-2,2) 3,3 (3,0-3,7) 1 6 378/1224 105/779 2,3 (1,9-2,8) 5,8 (4,8-7,2) 2 6 724/1224 191/779 2,4 (2,1-2,7) 2,9 (2,6-3,3) 1 6 408/1221 105/779 2,5 (2,0-3,0) 5,0 (4,3-6,1) 2 6 763/1221 191/779 2,5 (2,2-2,9) 2,6 (2,4-3,0) RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 28 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Respuesta libre de dolor De nuevo los dos únicos EC disponibles en los que se comparan eletriptán vs. sumatriptán son los estudios de Goadsby y col. y Sandrini y col. (Goadsby y col., 2000; Sandrini y col., 2002) cuyos resultados de la variable respuesta libre de dolor se detallan en la tabla 8. En el estudio de Goadsby y col. (Goadsby y col., 2000) eletriptán fue superior a sumatriptán 100 mg a las dosis de 80 mg 2 hora post administración del fármaco. En el EC de Sandrini y col. la dosis de eletriptán 80 mg 1 hora post administración fue significativamente superior a sumatriptán 50 mg; y las dosis de 40 y 80 mg 2 horas post administración de eletriptán fueron superiores a ambas dosis de sumatriptán (50 y 100 mg) (Sandrini y col., 2002). En el metaanálisis de Oldman y col. (tabla 10), eletriptán (40 y 80 mg) fue superior a sumatriptán 50 mg vo, 2 horas post-administración del fármaco (tal y como refleja el hecho de que los IC 95% del NNT de eletriptán no se solapan con los de sumatriptán). Siendo de nuevo sumatriptán administrado sc el más eficaz en cuanto a la respuesta libre de dolor a las 2 horas (Oldman y col., 2002). 29 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 10: Respuesta libre de dolor a las 2 horas de eletriptán, sumatriptán y otros triptanos, expresado en nº pacientes, extraído del metaanálisis publicado por Oldman y col. (Oldman y col., 2002). Dosis y vía Nº estudios Tto (nº ptes) Placebo (nº ptes) RR (IC 95%) NNT (IC 95%) 6 mg, sc 6 206/345 41/338 4,4 (3,2-6,0) 2,1 (1,9-2,4) 50 mg, vo 4 131/711 21/372 3,3 (2,1-5,2) 7,8 (6,1-11) 100 mg, vo 8 415/1461 53/744 3,6 (2,8-5,5) 4,7 (4,1-5,5) 40 mg, vo 6 335/1224 38/779 5,6 (4,0-7,7) 4,5 (3,9-5,1) 80 mg, vo 6 386/1221 38/779 6,4 (4,6-8,9) 3,7 (3,4-4,2) Naratriptán 2,5 mg, vo 1 44/213 9/107 2,5 (1,3-4,8) 8,2 (5,1-21) Rizatriptán 5 mg, vo 4 284/933 65/713 3,4 (2,6-4,4) 4,7 (4,0-5,7) 10 mg, vo 7 720/1783 83/987 4,8 (3,8-5,9) 3,1 (2,9-3,5) 2,5 mg, vo 2 109/438 17/213 3,1 (1,9-5,1) 5,9 (4,5-8,7) 5 mg, vo 4 298/943 17/285 5,1 (3,3-8,1) 3,9 (3,4-4,6) Fármaco Sumatriptán Eletriptán Zolmitriptán RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 31 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Respuesta analgésica sostenida durante 24 horas Mientras que en el EC de Goadsby y col. no existen diferencias entre los distintos grupos (eletriptán vs. sumatriptán) en la tasa de recurrencias y en la utilización de medicación de rescate (Goadsby y col., 2000), en el EC de Sandrini y col. ambas dosis de eletriptán ensayadas (40 y 80 mg) fueron estadísticamente superiores a sumatriptán (50 y 100 mg) (Sandrini y col., 2002). En el metaanálisis publicado por Oldman y col. (tabla 11), eletriptán también fue superior a sumatriptán vo (los IC95% del NNT de eletriptán 80 mg no se solapan con los de sumatriptán 100 mg vo) e igual frente a sumatriptán administrado vía sc (Oldman y col., 2002). 32 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 11: Respuesta analgésica sostenida durante 24 horas de eletriptán, sumatriptán y otros triptanos expresado en nº pacientes, extraído del metaanálisis publicado por Oldman y col. (Oldman y col., 2002). Dosis y vía Nº estudios Tto (nº ptes) Placebo (nº ptes) RR (IC 95%) NNT (IC 95%) Ergotamina + cafeína 2 mg + 200 mg, vo 1 60/203 15/105 2,1 (1,2-3,5) 6,6 (4,1-16) Sumatriptán 6 mg, sc 2 70/144 28/160 2,7 (1,9-3,9) 3,2 (2,4-4,8) 50 mg, vo 2 157/362 47/177 1,7 (1,3-2,2) 6,0 (4,0-12) 100 mg, vo 4 472/1190 109/442 1,6 (1,3-1,9) 6,7 (5,0-9,9) 40 mg, vo 5 526/1157 117/662 2,6 (2,1-3,0) 3,6 (3,1-4,2) 80 mg, vo 5 618/1160 117/662 3,0 (2,5-3,6) 2,8 (2,5-3,2) 5 mg, vo 3 280/803 148/647 1,5 (1,3-1,8) 8,3 (6,0-14) 10 mg, vo 3 420/1030 148/647 1,7 (1,5-2,0) 5,6 (4,5-7,4) 5 mg 1 180/498 14/56 1,5 (0,91-2,3) - Fármaco y dosis Eletriptán Rizatriptán Zolmitriptán RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 33 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 5.- Eficacia frente a otro fco: cafeína + ergotamina Respuesta analgésica En el estudio de Diener y col., 142 de 209 pacientes (68%) en el grupo eletriptán 80 mg, 111 de 209 pacientes (54%) en el grupo eletriptán 40 mg y 65 de 197 pacientes (33%) a los que se les administró una combinación de cafeína + ergotamina obtuvieron respuesta analgésica a las dos horas de la administración del fármaco (p<0,01 para todas las combinaciones de eletriptán vs. cafeína + ergotamina) (Diener y col., 2002). Respuesta libre de dolor Al igual que ocurre con la variable respuesta analgésica a las dos horas, también una mayor proporción de pacientes en el grupo eletriptán obtuvieron respuesta libre de dolor a las dos horas (eletriptán 80 mg: 79/209, 38%; eletriptán 40mg: 58/206, 28%) comparado con el grupo al que se les administró cafeína + ergotamina (5/102; 5%) (p<0,001 para todas las comparaciones de eletriptán vs. cafeína + ergotamina) (Diener y col., 2002). 6.- Eficacia frente a otros triptanos distintos a sumatriptán Hasta el momento no existe ningún ensayo clínico publicado en el que se haya realizado una comparación directa de eletriptán vs. otros triptanos. Así pues, los resultados de las distintas variables que se detallan a continuación se han extraído del metaanálisis publicado por Oldman y colaboradores (Oldman y col., 2002). Existen dos comunicaciones tipo póster en los que se compara eletriptán 40 y 80 mg vs. zolmitriptán 2,5 mg (Steiner y col., 2002) y eletriptán 40 mg vs. naratriptán 2,5 mg (Garcia-Ramos y col., 2002). Respuesta analgésica 34 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Los NNTs para la respuesta analgésica a las 2 horas entre los distintos triptanos comparados con placebo (tabla 12) varían entre 2,6 (2,4-3,0), para la dosis de eletriptán 80 mg, y 5,4 (3,8-9,2), para la dosis de naratriptán 2,5 mg. En el casos de las dosis altas, la diferencia entre los distintos triptanos es baja (rango de NNTs: de 2,6 (2,4-3,0) a 3,3 (2,4-3,0)) al igual que ocurre con las dosis bajas (rango de NNTs: de 2,9 (2,6-3,3) a 4,1 (3,4-5,2)). Naratriptán (disponible únicamente a la dosis de 2,5 mg) fue menos eficaz que todas las dosis altas de triptanos y que la dosis menor de eletriptán (Oldman y col., 2002). Para la variable respuesta analgésica 1 hora post-administración del fármaco, comparado con placebo, los NNTs varían entre 4,9 (4,2-6,0) para rizatriptán 10 mg y 8,5 (4,2-38) para naratriptán 2,5 mg. Los NNTs para las dosis altas de los triptanos el rango se sitúa entre 4,9 (4,2-6,0) y 5,9 (4,4-8,8), y para las dosis bajas entre 5,8 (4,8-7,2) y 7,3 (4,7-16) (Oldman y col., 2002). Los resultados de las dos comunicaciones tipo póster sugieren que, para la variable respuesta analgésica 2 hora post-administración del fármaco, en el estudio de Steiner y col. un mayor porcentaje de pacientes respondían con eletriptán 80 mg vs. zolmitriptán 2,5 mg (74 vs. 60%, respectivamente, p<0,0001) mientras que eletriptán 40 mg obtuvo porcentajes similares a zolmitriptán 2,5 mg (64 vs. 60%, respectivamente) (Steiner y col., 2002). En el estudio de Garcia-Ramos y col. eletriptán 40 mg obtuvo mejores porcentajes de respuesta que naratriptán 2,5 mg (56 vs. 42%, respectivamente, p<0,01) (Garcia-Ramos y col., 2002). 35 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 12: Respuesta analgésica de eletriptán y otros triptanos expresado en nº paciente, extraído del metaanálisis publicado por Oldman y col. (Oldman y col., 2002). Fármaco y dosis Naratriptán 2,5 mg Rizatriptán 5 mg Rizatriptán 10 mg Zolmitriptán 2,5 mg Zolmitriptán 5 mg Eletriptán 40 mg Eletriptán 80 mg T (h) Nº estudios Tto (nº ptes) Placebo (nº ptes) RR (IC 95%) NNT (IC 95%) 1 1 59/213 17/107 1,7 (1,1-2,8) 8,5 (4,8-38) 2 2 154/340 61/229 1,7 (1,3-2,2) 5,4 (3,8-9,2) 1 4 349/933 167/713 1,6 (1,4-1,9) 7,2 (5,4-10) 2 4 548/933 234/713 1,8 (1,6-2,0) 3,9 (3,3-4,7) 1 7 761/1783 221/987 1,9 (1,6-2,1) 4,9 (4,2-6,0) 2 7 1216/1783 303/987 2,2 (2,0-2,4) 2,7 (2,4-2,9) 1 2 173/438 55/213 1,5 (1,2-2,0) 7,3 (4,7-16) 2 2 279/438 74/213 1,8 (1,5-2,2) 3,5 (2,7-4,7) 1 4 355/943 59/285 1,9 (1,5-2,5) 5,9 (4,4-8,8) 2 4 583/943 85/285 2,1 (1,7-2,5) 3,1 (2,6-3,9) 1 6 378/1224 105/779 2,3 (1,9-2,8) 5,8 (4,8-7,2) 2 6 724/1224 191/779 2,4 (2,1-2,7) 2,9 (2,6-3,3) 1 6 408/1221 105/779 2,5 (2,0-3,0) 5,0 (4,3-6,1) 2 6 763/1221 191/779 2,5 (2,2-2,9) 2,6 (2,4-3,0) RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 37 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Respuesta libre de dolor Para la variable respuesta libre de dolor a las 2 horas (Oldman y col., 2002), los NNTs de los distintos triptanos, varían entre 3,1 (2,9; 3,5) para rizatriptán 10 mg y 8,2 (5,1; 23) para naratriptán (tabla 10). Al igual que ocurre con la variable “respuesta analgésica”, apenas existe diferencia entre los distintos triptanos cuando se comparan entre sí y de forma individual, las dosis altas (eletriptán 80 mg, rizatriptán 10 mg y zolmitriptán 5 mg), como las dosis bajas (eletriptán 40 mg, rizatriptán 5 mg y zolmitriptán 2,5 mg). Los resultados de las comunicaciones tipo póster sugieren al igual que ocurre con la variable respuesta analgésica que, en el estudio de Steiner y col. eletriptán 80 mg obtiene mejores porcentajes de respuesta que zolmitriptán 2,5 mg (44 vs. 26%, respectivamente, p<0,0001), no así con la dosis de eletriptán 40 mg (32 vs. 26%) (Steiner y col., 2002). En el estudio de Garcia-Ramos y col. eletriptán 40 mg también obtiene mejores porcentajes de respuesta que zolmitriptán 2,5 mg (35 vs. 18%, respectivamente, p<0,0005) (Garcia-Ramos y col., 2002). Respuesta analgésica sostenida durante 24 horas La respuesta analgésica sostenida durante 24 horas definida como respuesta analgésica a las 2 horas sin que se produzca ninguna recurrencia durante las siguientes 24 horas, varía para el grupo tratamiento entre 30-53% y para el grupo placebo entre 14-27% (tabla 11). De los resultados disponibles, zolmitriptán a la dosis de 5 mg, es el único que respecto a placebo no obtuvo diferencias estadísticamente significativas. Entre los distintos triptanos los NNTs varían entre 2,8 (2,5-3,2) y 8,3 (6,0-14), siendo en esta variable la intervención más efectiva eletriptán 80 mg y la que menos rizatriptán 5 mg. Además, se observa una relación dosis dependiente, tanto para eletriptán (40 mg vs. 80 mg; p=0,004) como para rizatriptán (10 mg vs. 5 mg; p=0,035) (Oldman y col., 2002). Los resultados de las comunicaciones tipo póster sugieren que, en el estudio de Steiner y col. eletriptán 40 y 80 mg obtiene mejores porcentajes de respuesta que zolmitriptán 2,5 mg (44 y 47 vs. 35%, p<0,01 y p<0,0001, respectivamente) 38 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica (Steiner y col., 2002). En el estudio de Garcia-Ramos y col. eletriptán 40 mg también obtiene mejores porcentajes de respuesta que zolmitriptán 2,5 mg (38 vs. 27%, respectivamente, p<0,05) (Garcia-Ramos y col., 2002). C) Seguridad 1.- Descripción Mutagénesis, carcinogénesis e infertilidad En los ensayos in vitro efectuados (en bacterias y en células de mamíferos), eletriptán no mostró poder mutagénico ni clastogénico. Los estudios de carcinogenicidad se llevaron a cabo en ratones y ratas durante 104 semanas administrándoles eletriptán junto con la dieta. En ratas, la incidencia de adenomas de células intersticiales se incrementó a la dosis más alta (75 mg/kg/día). La estimación de la exposición (AUC) a eletriptán a esa dosis equivale aproximádamente a 6 veces a la que se alcanza en humanos cuando se administra la dosis máxima diaria recomendada (DMDR) de 80 mg y la dosis de 15 mg/kg/día equivale a 2 veces la que se alcanza al administrar la DMDR. En ratones, la incidencia de adenomas hepatocelulares se incrementó cuando se administró la dosis máxima (400 mg/kg/día, equivalente a 18 veces la que se alcanza administrando la DMDR), siendo la dosis que no produjo daño hepático la de 90 mg/kg/día (equivalente a 7 veces la concentración que se alcanza en humanos cuando se administra la DMDR) (Pfizer Inc., 2002a). Se realizaron estudios sobre la fertilidad en ratas y sobre el desarrollo embrionario, sugiriendo una inhibición parcial de la ovulación causada por eletriptán. No se observó ningún efecto sobre la fertilidad en los machos y ningún otro sobre la fertilidad de las hembras a las dosis estudiadas (50, 100 y 200 mg/kg/día, equivalente a una exposición a eletriptán, basado en el AUC, de 4, 8 y 16 veces la alcanzada al administrar la DMDR en machos y 7, 14 y 28 veces la alcanzada en hembras) (Pfizer Inc., 2002a). 39 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Teratogénesis Categoría C de la FDA (Cuando los estudios realizados en animales han mostrado efectos adversos en el feto (teratógenos, embriocidas u otros) y no existen estudios comparativos en mujeres, o cuando no existen estudios disponibles ni en mujeres ni en animales. Sólo deben administrarse si el beneficio potencial justifica el riesgo para el feto.). En los estudios de toxicidad en ratas y conejos, la administración oral de eletriptán se asoció una disminución del peso fetal (a las dosis estudiadas, equivale a 6-12 veces las alcanzadas en humanos cuando se administra la DMDR) e incremento de la incidencia de anormalidades estructurales de los fetos (equivalente bien, a 12 veces la DMDR en ratas, bien a la misma que cuando se administra la DMDR en conejos). Cuando se administró eletriptán a ratas preñadas durante el periodo de organogénesis a dosis de 10, 30 ó 100 mg/kg/día, el peso fetal disminuyó y la incidencia de alteraciones vertebrales y esternales se incrementó a la dosis de 100 mg/kg/día (aprox. 12 veces la DMDR). La dosis de 100 mg/kg/día también fue tóxica para la rata preñada, ya que disminuyó la ganancia de peso durante la gestación. A la dosis de 30 mg/kg/día, las ratas no desarrollaron toxicidad durante la organogénesis (equivalente a 4 veces la DMDR). También disminuyó el peso fetal cuando se administró eletriptán 50 mg/kg/día (equivalente a 12 veces la DMDR; dosis ensayadas: 5, 10 y 50 mg/kg/día) a conejos blancos de Nueva Zelanda durante la organogénesis. La inicencia de vértabras fusionadas y desviación de vena cava se incrementó en todos los grupos. No se desarrolló toxicidad materna en ningún grupo y no se pudo calcular la dosis a la que no se desarrolla toxicidad en el conejo, siendo la dosis de 5 mg/kg/día equivalente a la DMDR (Pfizer Inc., 2002a). No se han realizado estudios controlados en mujeres embarazadas, por lo que, eletriptán debería usarse durante el embarazo solo si el beneficio potencial justifica los riesgos. Eventos adversos En la tabla 13 se resumen la incidencia de los eventos adversos más frecuentes aparecidos en el grupo experimental (con una incidencia superior al 2%) 40 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica (Pfizer Inc., 2002a). En general, eletriptán se tolera bien, siendo la mayoría de las reacciones adversas leves y transitorias. La incidencia de eventos adversos no se ve influida por factores como la edad, sexo o raza de los pacientes y las frecuencias de éstas son las mismas en presencia de fármacos administrados de forma concomitante para la profilaxis de la migraña (por ejemplo, inhibidores de la recaptación de serotonina, betabloqueantes, bloqueantes de los canales de calcio, antidepresivo tricíclicos), tratamiento de sustitución con estrógenos o anticonceptivos orales. Tabla 13: Incidencia de eventos adversos en ensayos clínicos controlados con placebo. Tipo de evento adverso Placebo (n=988) Eletriptán 20 mg (n=431) Eletriptán 40 mg (n=1774) Eletriptán 80 mg (n=1932) Parestesia 2% 3% 3% 4% Sensación de calor 2% 2% 2% 2% Pecho – dolor / presión 1% 1% 2% 4% Abdominal – dolor / molestia / dolor de estómago 1% 1% 2% 2% Boca seca 2% 2% 3% 4% Dispepsia 1% 1% 2% 2% Disfagia 0,2% 1% 2% 2% Nausea 5% 4% 5% 8% Mareo 3% 3% 6% 7% Somnolencia 4% 3% 6% 7% Dolor de cabeza 3% 4% 3% 4% Sensaciones atípicas Dolor y sensación de presión Digestivo Neurológico Otros 41 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tipo de evento adverso Placebo (n=988) Eletriptán 20 mg (n=431) Eletriptán 40 mg (n=1774) Eletriptán 80 mg (n=1932) 3% 4% 5% 10% Astenia En la tabla 15 se resumen los principales eventos adversos, expresados como riesgo relativo (RR) y NNH (number-needed-to-harm), para cada dosis de eletriptán estudiada. Los principales eventos adversos se han clasificado como efectos adversos (EA) serios, leves e individuales. Los EA serios se han definido como el número de pacientes en cada grupo de tratamiento en los que se informó de cualquier efecto adverso que provocó muerte o enfermedad grave, o cualquier efecto adverso lo suficientemente severo para provocar el abandono del ensayo. Los EA leves se definieron como el número de pacientes en los que se produjo cualquier efecto adverso. También se estudiaron EA individuales como náuseas, vómitos, astenia, mareos, dolor de cabeza, somnolencia, boca seca o miastenia (en la tabla resumen se muestran solo los EA individuales para los que existía diferencias significativas entre el grupo experimental y el control) (Smith y col., 2001). En la tabla 14 se han extraído los resultados de eventos adversos de dos comunicaciones tipo póster en los que se compara eletriptán 40 mg vs. naratriptán 2,5 mg (Garcia-Ramos y col., 2002) y eletriptán 40 y 80 mg vs. zolmitriptán 2,5 mg (Steiner y col., 2002). Tabla 14: Eventos adversos relacionados con la medicación con una incidencia >3% Estudio Zolmitriptán 2,5 mg Eletriptán 40 mg (n=192) 3,6 4,2 5,7 1,6 5,2 Eletriptán 80 mg (n=144) 0 4,2 1,4 (n=405) 2,5 4,2 1,5 (n=392) 3,1 4,1 1,5 (n=396) 8,1 4,0 4,3 1,4 0,2 2,3 3,3 Placebo GarciaRamos y col. Astenia Náusea Mareos Vómitos Somnolencia Steiner y col. Astenia Náusea Mareos Síntomas torácicos (n=92) 1,1 5,4 3,3 4,3 2,2 Naratriptán 2,5 mg (n=199) 1,0 3,5 2,0 2,0 4,0 42 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 15: Eventos adversos de eletriptán, expresados en nº de pacientes, extraído del metaanálisis publicado por Smith y col. (Smith y col., 2001). Dosis eletriptán 20 mg 40 mg 80 mg Evento adverso Nº Estudios Tratamiento Control RR (IC 95%) NNH (IC 95%) Grave 2 3 / 278 3 / 205 0,70 (0,19-2,63) - Menor 2 67 / 278 30 / 205 1,57 (1,08-2,28) 11 (6,2-39) Grave 7 18 / 1120 5 / 356 0,64 (0,26-1,56) - Menor 7 372 /1120 67 / 356 1,51 (1,20-1,90) 7,0 (5,2-11) Mareo 7 58 / 1120 5 / 356 2,54 (1,14-5,67) 27 (18-50) Grave 6 26 / 976 5 / 326 1,08 (0,49-2,42) - Menor 6 453 / 976 62 / 326 2,04 (1,63-2,56) 3,7 (3,1-4,5) Mareo 6 68 / 976 5 / 326 3,14 (1,38-7,14) 18 (13-50) Astenia 6 102 / 976 7 / 326 3,28 (1,69-6,35) RR: Riesgo relativo de respuesta de tratamiento vs. Control; NNT: Nº de pacientes a tratar con eletriptán para logra una respuesta; IC (95%): Intervalo de confianza del 95% 43 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica En estudios clínicos aleatorizados en los que se utilizaron dosis de 20, 40 y 80 mg, se ha puesto de manifiesto que la incidencia de reacciones adversas es dosis dependiente. Las reacciones adversas más frecuentes son astenia, náusea, mareos y somnolencia. Las reacciones adversas observadas con eletriptán que se consideran relacionadas con el tratamiento o provocadas por éste, con una incidencia superior a la obtenida con placebo son las siguientes (Pfizer Inc., 2002b) - Generales: Frecuentes (>1/100, <1/10): Astenia, síntomas torácicos (dolor, opresión, presión), cefalea, dolor abdominal, dolor de espalda y escalofríos, opresión en la garganta. Poco frecuentes (>1/1000, <1/100): Malestar, edema facial. Raras (>1/10000, <1/1000): Shock. - Cardiovascular: Frecuentes (>1/100, <1/10): Sensación de calor o rubor, palpitaciones, taquicardia. Poco frecuentes (>1/1000, <1/100): Trastorno vascular periférica. Raras (>1/10000, <1/1000): Bradicardia. - Digestivo: Frecuentes (>1/100, <1/10): Náuseas, sequedad de boca, dispepsia. Poco frecuentes (>1/1000, <1/100): Diarrea, anorexia y glositis. Raras (>1/10000, <1/1000): Estreñimiento, esofagitis, edema en la lengua y eructos. - Hematológico y linfático: Raras (>1/10000, <1/1000): Linfadenopatía. - Metabólico y nutricional: Poco frecuentes (>1/1000, <1/100): Sed, edema y edema periférico. Raras (>1/10000, <1/1000): Bilirrubinemia e incremento de la AST. - Músculo esquelético: Frecuentes (>1/100, <1/10): Miastenia, mialgia. Poco frecuentes (>1/1000, <1/100): Artralgia, artrosis y dolor de huesos. Raras (>1/10000, <1/1000): Artritis y miopatía. - Nervioso: Frecuentes (>1/100, <1/10): Somnolencia, mareo, hormigueo o sensación anormal, sensación de opresión o rigidez, hipoestesia y vértigo. Poco frecuentes (>1/1000, <1/100): Temblor, hiperestesia, pensamiento anormal, agitación, insomnio, confusión, ataxia, despersonalización, euforia, hipocinesia, alteraciones del habla, depresión y estupor. Raras (>1/10000, <1/1000): Labilidad emocional y espasmos musculares. - Respiratorio: Frecuentes (>1/100, <1/10): Faringitis. Poco frecuentes (>1/1000, <1/100): Disnea, rinitis, alteración respiratoria y bostezo. Raras (>1/10000, <1/1000): Asma, infección del tracto respiratorio y alteración de la voz. 44 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica - Piel y anejos: Frecuentes (>1/100, <1/10): Sudoración. Poco frecuentes (>1/1000, <1/100): Erupción y prurito. Raras (>1/10000, <1/1000): Alteraciones de la piel y urticaria. - Sentidos especiales: Poco frecuentes (>1/1000, <1/100): Visión anormal, dolor de oídos, dolor de ojos, fotofobia, alteración del gusto, tinnitus y alteración del lagrimeo. Raras (>1/10000, <1/1000): Conjuntivitis. - Urogenital: Poco frecuentes (>1/1000, <1/100): Frecuencia urinaria, alteración del tracto urinario y poliuria. Raras (>1/10000, <1/1000): Dolor de mamas y menorragia. Algunos de los síntomas comunicados como reacciones adversas pueden ser síntomas asociados al ataque de migraña. Las reacciones adversas habituales observadas con eletriptán son típicas de reacciones adversas registradas con el grupo de los agonistas del receptor 5-HT1. Intoxicación Algunos pacientes han recibido dosis únicas de 120 mg sin efectos adversos significativos. Sin embargo, teniendo en cuenta la farmacología de este grupo terapéutico, podría aparecer hipertensión u otros síntomas cardiovasculares más graves tras una sobredosis. En caso de sobredosis, se deben adoptar las medidas de apoyo estándar requeridas. La semivida de eliminación de eletriptán es de aproximadamente 4 h, y por tanto, la monitorización de los pacientes y la administración de un tratamiento de apoyo general después de una sobredosis con eletriptán debe continuar durante al menos 20 h o mientras persistan los signos y síntomas. No existe un antídoto específico para eletriptán. Se desconoce el efecto que tienen la hemodiálisis o la diálisis peritoneal sobre las concentraciones plasmáticas de eletriptán (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). 45 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica 2.- Contraindicaciones y precauciones Contraindicaciones Contraindicado en caso de (Ficha técnica: Relpax (R). Pfizer Inc., 2002b): - Hipersensibilidad a bromhidrato de eletriptán o a cualquiera de los excipientes. - Insuficiencia hepática o renal grave. - Hipertensión grave o moderadamente grave, o hipertensión leve no tratada. - Enfermedad coronaria confirmada: incluyendo cardiopatía isquémica (angina de pecho, infarto de miocardio previo o isquemia silente confirmada), síntomas objetivos o subjetivos de cardiopatía isquémica o angina de Prinzmetal. - Arritmias significativas o insuficiencia cardiaca. - Enfermedad vascular periférica. - Accidente cerebrovascular o ataque isquémico transitorio: antecedentes. Precauciones - Migraña hemipléjica, oftalmopléjica o basilar. - Cefaleas "atípicas: cefaleas que pueden estar relacionadas con una patología posiblemente grave (accidente cerebrovascular, rotura de aneurisma) en los que la vasoconstricción cerebrovascular puede ser perjudicial. - Enfermedad cardiaca no diagnosticada o riesgo de enfermedad coronaria (EC) (por ejemplo, pacientes con hipertensión arterial, diabéticos, fumadores o sometidos a un tratamiento de sustitución de la nicotina, postmenopáusicas varones y mayores pacientes con de 40 años, antecedentes mujeres familiares importantes de EC): no administrar sin una evaluación previa. Puede que los exámenes cardiacos no identifiquen a todos los pacientes que padecen una enfermedad cardiaca y, en casos muy 46 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica raros, han tenido lugar alteraciones cardiacas graves en pacientes sin enfermedad cardiovascular subyacente cuando se han administrado agonistas del receptor 5-HT1 (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Hipertensión: Se han observado incrementos ligeros y transitorios de la tensión arterial con dosis de eletriptán de 60 mg o superiores pero sin asociación con secuelas clínicas. El efecto fue mucho más pronunciado en sujetos con insuficiencia renal y en ancianos (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Efectos sobre la capacidad para conducir y utilizar máquinas: La migraña o el tratamiento con eletriptán puede producir somnolencia o mareo en algunos pacientes. Deberá advertirse a los pacientes que evalúen su capacidad para realizar tareas complejas, como conducir, durante el ataque de migraña y tras la administración de eletriptán (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Advertencias especiales de uso (Ficha técnica: Relpax (R). Pfizer Inc., 2002b): - Sólo debe utilizarse cuando se establezca un diagnóstico claro de migraña. - La administración de eletriptán puede asociarse a síntomas transitorios incluyendo dolor y opresión torácicos que pueden ser intensos y extenderse a la garganta. Si tales síntomas se consideraran indicativos de cardiopatía isquémica, no deberá administrarse ninguna dosis adicional y se deberá realizar una evaluación adecuada. 3.- Interacciones Fármacos derivados de ergotamina Los fármacos derivados de ergotamina pueden ocasionar reacciones vasoespásticas prolongadas. En ensayos clínicos con cafeína/ergotamina por vía oral administrado 1 y 2 h después de eletriptán, se observaron pequeños 47 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica incrementos en la tensión arterial, acumulables en el tiempo y predecibles según la farmacología de ambos fármacos. Por consiguiente, no se recomienda la administración conjunta en las 24 h siguientes a la administración de eletriptán. Asimismo, deberán transcurrir al menos 24 h de la administración de un fármaco que contenga ergotamina antes de poder administrar eletriptán (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Inhibidores CYP3A4 Eletriptán se metaboliza primariamente por el CYP3A4. En estudios con eritromicina (1000 mg) y ketoconazol (400 mg) y otros inhibidores de CYP3A4 (ketoconazol, itraconazol, eritromicina, claritromicina, josamicina e inhibidores de la proteasa (ritonavir, indinavir y nelfinavir)) se observaron aumentos significativos en la Cmax (2 y 2,7 veces) y en el AUC (3,6 y 5,9 veces) respectivamente. Este aumento de la exposición se asoció con un incremento en la t1/2 de eletriptán desde 4,6-7,1 h para eritromicina y de 4,8-8,3 h para ketoconazol. Por tanto, no se recomienda el uso de eletriptán junto con estos medicamentos, como mínimo en las primeras 72 horas (Pfizer Inc., 2002a). Inhibidores de la MAO Eletriptán no es un sustrato de la MAO, por lo que no se espera ningún tipo de interacción entre eletriptán y los IMAO (Pfizer Inc., 2002a). Propranolol, verapamilo y fluconazol En estudios clínicos con estos fármacos la Cmax de eletriptán se incrementó 1,1 veces, 2,2 veces y 1,4 veces respectivamente. El aumento del AUC de eletriptán fue de 1,3, 2,7 y 2,0 veces respectivamente. Estos efectos no se consideran clínicamente significativos puesto que no hubo un aumento de la tensión arterial ni de los efectos adversos en comparación con la administración de eletriptán sólo (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Otros agonistas 5HT1 No se recomienda el uso concomitante de otros agonistas 5HT1 dentro de las 24 horas siguientes (Pfizer Inc., 2002a). 48 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica D) Pauta terapéutica e indicaciones Adultos, oral: Dosis inicial 40 mg. Si hay respuesta inicial pero la cefalea reaparece en menos de 24 h siguientes, administrar otros 40 mg dejando un intervalo entre dosis de al menos 2 h. Si no se obtiene respuesta inicial en 2 h con la primera dosis, no se deberá tomar una segunda dosis para el mismo ataque. Los ensayos clínicos realizados muestran que los pacientes que no responden al tratamiento de un ataque pueden aún responder al tratamiento de un ataque posterior. Los pacientes que no obtengan eficacia satisfactoria con 40 mg, (con buena tolerancia y sin respuesta al tratamiento en 2 ataques de 3), podrán ser tratados con 80 mg en ataques de migraña posteriores, sin poder administrarse una segunda dosis de 80 mg en las siguientes 24 h. Dosis máxima: 80 mg/día (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Dosis en situaciones especiales: - Alteración renal – Puesto que los efectos de eletriptán sobre la tensión arterial se incrementan en caso de insuficiencia renal, se recomienda una dosis inicial de 20 mg en pacientes con insuficiencia renal leve o moderada y una dosis máxima diaria de 40 mg. No se recomienda el uso en insuficiencia renal grave (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Alteración hepática – No se requieren ajustes de dosis insuficiencia hepática leve o moderada. Debido a que no se ha estudiado en insuficiencia hepática grave, no se recomienda el uso en este caso (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Ancianos – La eficacia y seguridad de eletriptán en pacientes mayores de 65 años no ha sido sistemáticamente evaluada dado el escaso número de estos pacientes incluidos en los ensayos clínicos (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Eletriptán se ha administrado solo a 50 pacientes mayores de 65 años. En estos pacientes la presión sanguínea se incrementó en mayor medida que en los pacientes jóvenes. En ensayos clínicos (n=50), no parece que exista diferencias, en cuanto a la eficacia o la incidencia de efectos adversos, entre pacientes con edad mayor de 65 años y pacientes con edad menor de 65 años (Pfizer Inc., 2002a). Existe 49 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica una pequeña reducción sin significación estadística (16%) en el aclaramiento asociada con un incremento estadísticamente significativo de la semivida (de 4,4 h a 5,7 aproximadamente) entre los ancianos (6593 años) y los adultos más jóvenes. Uso no recomendado (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Niños y adolescentes – La eficacia de eletriptán no ha sido establecida en adolescentes (12-17 años), tampoco se ha evaluado la seguridad y eficacia en niños hasta 11 años. El volumen de distribución de eletriptán es inferior en niños, dando lugar a niveles plasmáticos más altos de lo que cabría esperar tras la administración de la misma dosis en adultos. Uso no recomendado en este grupo de edad (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Madres embarazadas – Los estudios en animales no muestran efectos perjudiciales directos o indirectos relativos al embarazo, desarrollo embrionario/fetal, parto o desarrollo postnatal. No se dispone de datos clínicos sobre eletriptán en el embarazo humano. El uso de este medicamento durante el embarazo sólo se recomienda en caso de ausencia de alternativas terapéuticas más seguras (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). - Madres lactantes – Eletriptán se excreta en la leche materna. En un estudio de 8 mujeres que recibieron una dosis única de 80 mg, la cantidad media total de eletriptán en la leche materna a lo largo de 24 h fue del 0,02% de la dosis. Sin embargo, debe tenerse precaución cuando se considere la administración de eletriptán a mujeres en periodo de lactancia. La exposición del niño puede minimizarse evitando la lactancia durante las 24 h posteriores al tratamiento (Ficha técnica: Relpax (R). Pfizer Inc., 2002b). Normas para la correcta administración: administrar tan pronto como sea posible tras el inicio de la cefalea migrañosa, aunque también son eficaces si se toman con posterioridad durante un ataque de migraña. Sólo debe administrarse durante la fase de cefalea de la migraña ya que no ha mostrado eficacia durante la fase de aura. No utilizar de manera preventiva. Ingerir enteros con un poco de agua. 50 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica E) Farmacoeconomía 1.- Estudios de Farmacoeconomía En el estudio de Wells y Steiner, se estudió la eficacia de eletriptán vs. placebo en la reducción de la pérdida de trabajo producido durante un único ataque de migraña. La evaluación de dicha pérdida de trabajo se realizó a través de un cuestionario cumplimentado durante las siguientes 24 horas tras la última dosis administrada tras el ataque de migraña. La mediana de pérdida de trabajo en el grupo de pacientes tratados con eletriptán, 40 y 80 mg, fue de 4 horas, mientras que para el grupo placebo fue de 9 horas (p<0,001). Dichas pérdidas suponen un coste asociado de 3373, 4072 y 7507 libras para los grupos eletriptán 40 mg, 80 mg y placebo, respectivamente, en una cohorte de 100 pacientes (Wells y Steiner, 2000). En un estudio de modelización, remitido por el promotor (Pfizer S.A., 2003), realizado a partir de los datos de eficacia de un metaanálisis (Ferrari y col., 2002) de EC de triptanos y con los precios del mercado español, el análisis coste/efectividad sugiere un menor coste total por ataque de migraña tratado con éxito (es decir, para lograr un ataque tratado con éxito e incluye el coste de la medicación de rescate y el tratamiento de la recurrencia a las 24 horas) comparado con los triptanos existentes en el mercado español: 26,54 € con eletriptán 40 mg frente a 29,69 € con rizatriptán 10 mg, 30,61 € con sumatriptán 100 mg, 32,41 € con naratriptán 2,5 mg, 36,06 € con rizatriptán 2,5 mg ó 45,95 € con Almotriptán 12,5 mg. No hay disponible información sobre estudios farmacoeconómicos prospectivos en los que se compare eletriptán con otros agonistas 5HT1. 2.- Precios comparativos En la tabla 15 se indica el coste diario de un tratamiento con eletriptán comparado con el de otros agonistas 5HT1 orales disponibles en el mercado español. 51 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Tabla 15. Coste diario de un tratamiento para el tratamiento agudo de la migraña calculado con las dosis iniciales establecidas para algunos de los fármacos más utilizados en nuestro país. Fármaco Eletriptán Especialidad (Laboratorio) Pfizer ® Dosis diaria total 40 – 80 mg Coste (Euros) tratamiento/día Envase. Precio (Euros). Compr. 20 mg (env. 2) Compr. 20 mg (env. 4) Compr. 40 mg (env. 2) Compr. 40 mg (env. 4) – 10,15 – 19,96 – 16,24 – 31,93 7,98 – 15,97 8,86 – 35,44 12,5 – 50 mg Compr. 12,5 mg (env. 4) Compr. 12,5 mg (env. 6) – 35,44 – 53,17 Naratriptán Almirall ® Prodesfarma Uriach ® Glaxo Smithkline ® 2,5 – 5 mg Merck Sharp Dohme ® 10 – 20 mg – 34,72 – 16,24 – 47,92 5,79 – 11,57 Rizatriptán Compr. 2,5 mg (env. 6) Compr. o liotabs 10 mg (env. 2) Compr. o liotabs 10 mg (env. 6) Compr. 50 mg (env. 4) – 26,90 6,73 – 40,35 Compr. 2,5 mg (env. 3) Compr. 2,5 mg (env. 6) Compr. disp. 2,5 mg (env. 6) – 20,26 – 40,08 – 40,08 6,68 – 13,36 Almotriptán Alter ® Sumatriptán Abbott Laboratorios ® Zolmitriptán Glaxo Smithkline ® Ferrer Internacional ® Astrazeneca Farmaceutica Spain ® 50 – 300 mg 2,5 – 5 mg 7,98 – 15,96 Los precios considerados son los de especialidades de referencia de cada uno de los productos en el año 2002. De muchos de los productos existen especialidades genéricas que pueden tener precios inferiores a los aquí reseñados. Existen otras preparaciones de cada uno de los fármacos que pueden tener precios distintos. Precios (PVP IVA incluido) tomados de la Base de datos del medicamento del Consejo General de Colegios Farmacéuticos de España: http://www.portalfarma.com/home.nsf F) Conclusiones En base a los datos disponibles hasta la fecha, eletriptán 40 mg, comparado con sumatriptán 50 y 100 mg, y naratriptán 2,5 mg, logra mejores porcentajes, en lo que se refiere al inicio de la respuesta (variable “respuesta analgésica” a las 2 horas) como a su mantenimiento (variable “respuesta analgésica sostenida durante 24 horas”). La dosis de eletriptán 80 mg también fue significativamente más eficaz que la dosis de zolmitriptán 2,5 mg para estas variables, sin embargo, el porcentaje de casos de astenia se incrementó del 2,5% al 8,1% en el grupo tratado con eletriptán. No se han realizado ensayos clínicos que comparen directamente eletriptán con distintas dosis / triptanes presentes en el mercado español. REFERENCIAS BIBLIOGRÁFICAS 52 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Diener, H. C., Jansen, J. P., Reches, A., Pascual, J., Pitei, D. & Steiner, T. J. (2002) Efficacy, tolerability and safety of oral eletriptan and ergotamine plus caffeine (Cafergot) in the acute treatment of migraine: a multicentre, randomised, doubleblind, placebo-controlled comparison. Eur.Neurol., 47(2): 99-107. Drugdex (R) Editorial Staff . Eletriptan. Drugdex Drug Evaluation. MICROMEDEX(R) Healthcare Series Vol. 115. 2002. Ferrari, M. (1999) How to assess and compare drugs in the management of migraine: success rates in terms of response and recurrence. Cephalalgia, 19 Suppl 23: 2-4. Ferrari, M. D., Goadsby, P. J., Roon, K. I. & Lipton, R. B. (2002) Triptans (serotonin, 5-HT1B/1D agonists) in migraine: detailed results and methods of a meta-analysis of 53 trials. Cephalalgia, 22(8): 633-658. Ferrari, M. D., Roon, K. I., Lipton, R. B. & Goadsby, P. J. (2001) Oral triptans (serotonin 5-HT(1B/1D) agonists) in acute migraine treatment: a meta-analysis of 53 trials. Lancet, 358(9294): 1668-1675. Garcia-Ramos, G., MacGregor, E. A., Hilliard, B. & Hettiarachchi, J. (2002) Comparison of the efficacy and safety of eletriptan and naratriptan for the treament of a sigle migraine attack: results of a multicenter, randomized, placebo-cotrolled trial (abstract nº P04.077). 54th Annual Meeting of the American Academy of Neurology, Denver, Colo, 13-20 Apr 2002. Neurology, 58 (Suppl 3): A289. Gawel, M. J. & Grujich, N. N. (2001) Eletriptan. Expert.Opin.Investig.Drugs, 10(10): 1869-1874. Goadsby, P. J., Ferrari, M. D., Olesen, J., Stovner, L. J., Senard, J. M., Jackson, N. C. & Poole, P. H. (2000) Eletriptan in acute migraine: a double-blind, placebocontrolled comparison to sumatriptan. Eletriptan Steering Committee. Neurology, 54(1): 156-163. Goadsby, P. J., Lipton, R. B. & Ferrari, M. D. (2002) Migraine--current understanding and treatment. N.Engl.J.Med., 346(4): 257-270. 53 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Gruffyd-Jones, K., Kies, B., Middleton, A., Mulder, L. J., Rosjo, O. & Millson, D. S. (2001) Zolmitriptan versus sumatriptan for the acute oral treatment of migraine: a randomized, double-blind, international study. Eur.J.Neurol., 8(3): 237-245. Milton, K. A., Scott, N. R., Allen, M. J., Abel, S., Jenkins, V. C., James, G. C., Rance, D. J. & Eve, M. D. (2002) Pharmacokinetics, pharmacodynamics, and safety of the 5-HT(1B/1D) agonist eletriptan following intravenous and oral administration. J.Clin Pharmacol., 42(5): 528-539. Oldman, A. D., Smith, L. A., McQuay, H. J. & Moore, R. A. (2001) Rizatriptan for acute migraine. Cochrane.Database.Syst.Rev.,(3): CD003221. Oldman, A. D., Smith, L. A., McQuay, H. J. & Moore, R. A. (2002) Pharmacological treatments for acute migraine: quantitative systematic review. Pain, 97(3): 247-257. Pfizer Inc. Eletriptan. Relpax (TM) - U.S. Package insert. US Food and Drug Administration.Center for Drug Evaluation and Research. Web: http://www.fda.gov/cder/approval/index.htm (fecha de acceso: 2003a). http://www.fda.gov/cder/foi/label/2002/21016_relpax_lbl.pdf. Última revisión: 1-12002a. Pfizer Inc. Ficha tecnica: Eletriptan. 2002b. Pfizer Laboratories Limited. Product information: Relpax (R), eletriptan hydrobromide. Medsafe.New Zeland Medicines and Medical Devices Safety and Authority. Web: http://www.medsafe.govt.nz/index.asp (fecha de acceso: 12-22003). http://www.medsafe.govt.nz/profs/datasheet/r/relpaxtab.htm. Última revisión: 9-1-2002. Pfizer S.A. Evaluación farmacoeconómica de Relpax (R) (Eletriptán). Investigación de resultados en Salud, Unidad Médica. 2003. Sanders-Bush E. & Mayer S.E. (2001) 5-Hydroxytryptamine (serotonin): Receptor agonists and antagonists. En: Goodman and Gilman's The Pharmacological Basis of Therapeutics (eds J. G. Hardman, L. E. Limbird & A. G. Gilman), pp. 269-290. McGraw-Hill Companies, Inc., International Edition. 54 Unidad de Farmacología Clínica Hospital General Universitario de Alicante Dirección General para la Prestación Farmacéutica Sandrini, G., Farkkila, M., Burgess, G., Forster, E. & Haughie, S. (2002) Eletriptan vs sumatriptan: a double-blind, placebo-controlled, multiple migraine attack study. Neurology, 59(8): 1210-1217. Smith, L. A., Oldman, A. D., McQuay, H. J. & Moore, R. A. (2001) Eletriptan for acute migraine. Cochrane.Database.Syst.Rev.,(3): CD003224. Stark, R., Dahlof, C., Haughie, S. & Hettiarachchi, J. (2002) Efficacy, safety and tolerability of oral eletriptan in the acute treatment of migraine: results of a phase III, multicentre, placebo- controlled study across three attacks. Cephalalgia, 22(1): 2332. Steiner, T., Diener, H. C., Schoenen, J., Muirhead, N. & Sikes, C. (2002) The efficacy of eletriptan in comparison with zolmitriptan for the acute treament of migraine: results of a multicenter, randomized clinical trial (abstract nº F61). 44th Annual Scientific Meeting, American Scientific Society, June 21-23, 2002, Seattle, Washington. Headache, 42(5): 400. Tfelt-Hansen, P., Block, G., Dahlof, C., Diener, H. C., Ferrari, M. D., Goadsby, P. J., Guidetti, V., Jones, B., Lipton, R. B., Massiou, H., Meinert, C., Sandrini, G., Steiner, T. & Winter, P. B. (2000) Guidelines for controlled trials of drugs in migraine: second edition. Cephalalgia, 20(9): 765-786. Wells, N. E. & Steiner, T. J. (2000) Effectiveness of eletriptan in reducing time loss caused by migraine attacks. Pharmacoeconomics, 18(6): 557-566. 55