Capítulo I Compuestos Monodimensionales de Cationes Trivalentes
Anuncio

Capítulo I
Compuestos Monodimensionales de Cationes
Trivalentes con Etilendiamina y Flúor:
(C2N2H10)[M(HPO3)F3]
(M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
32
Capítulo I
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
33
I.1 SÍNTESIS Y CARACTERIZACIÓN
I.1.1 SÍNTESIS
Las fases (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr) se han
obtenido por síntesis solvotermal en condiciones suaves (170 ºC y presión autógena
próxima a 10 bares), empleando para ello recipientes de teflón con carcasas de acero y
mezclas agua-etanol como disolvente.
En la síntesis se han utilizado sales solubles de los cationes metálicos
correspondientes y ácido fosforoso, disueltos en 10 cm3 de agua e introducidos en el
recipiente de teflón, añadiendo a continuación el ácido fluorhídrico. Para la preparación de
las fases de vanadio se partió de una disolución previa de 1g de óxido de vanadio(III),
1.1cm3 de ácido sulfúrico, 1.6 cm3 de ácido hipofosforoso y 4 g de ácido fosforoso en
agua. Esta particularidad en la síntesis de los compuestos de vanadio se debe a que las
sales de vanadio trivalente se oxidan fácilmente en presencia del aire y por la humedad
ambiental durante la pesada, dando lugar a precipitados insolubles de color pardo al
disolver el resto del reactivo en agua.
Simultáneamente, se mezclaron las cantidades correspondientes de etilendiamina,
agua y etanol. Esta mezcla se añadió sobre la disolución anterior, manteniéndola en
agitación suave. El pH resultante de la disolución obtenida es ligeramente ácido en todas
las síntesis, hallándose dentro del intervalo comprendido entre 5 y 7. Únicamente en el
caso de la síntesis del compuesto de galio se observó en esta etapa la aparición de
precipitado sólido. En la Tabla I.1 se muestran las cantidades de reactivos empleadas en
cada caso.
Posteriormente, se cerraron los recipientes de reacción, introduciéndolos en sus
carcasas. Los recintos reaccionales así preparados se colocaron en una estufa a 170 ºC,
manteniéndolos durante 5 días a esta temperatura. Después de este periodo de tiempo se
dejaron enfriar al aire, abriéndolos una vez alcanzada la temperatura ambiente. Se midió el
pH del medio de reacción resultante, lo que permitió comprobar que el mismo no mostraba
variaciones apreciables respecto al de la disolución inicial.
Todos los productos, obtenidos en forma de monocristales, se han lavado por
decantación con agua y acetona, dejándolos secar al aire y recogiéndolos posteriormente
con ayuda de una espátula.
34
Capítulo I
Tabla I.1 - Reactivos empleados en la síntesis de los compuestos (C2N2H10)[M(HPO3)F3]. En el caso
de los compuestos que contienen V, el número de moles indicados de ácido fosforoso
contabilizan tanto el añadido como el número de moles de ácidos fosforoso e
hipofosforoso que contiene el volumen de disolución de V empleado.
M
sal metálica, cantidad
H3PO3
HF(48%)
C 2N 2H 8
agua
V
disolución, 5.6 cm3
(0.75 mmol)
0.873 g
(15 mmol)
1.0 cm3
(28 mmol)
1.50 cm3
(23 mmol)
12 cm3
10 cm3
Cr
Cr(NO3)3·9H2O, 1.001 g
(2.5 mmol)
1.230 g
(15 mmol)
1.0 cm3
(28 mmol)
1.0 cm3
(15 mmol)
10 cm3
9 cm3
Fe
FeCl3·6H2O, 0.406 g
(1.5 mmol)
1.230 g
(15 mmol)
1.8 cm3
(50 mmol)
1.54 cm3
(23 mmol)
17 cm3
10 cm3
V0.28Fe0.72
disolución, 5.2 cm3 /
FeCl3·6H2O, 0.190 g
(0.7 mmol / 0.7 mmol)
0.885 g
(15 mmol)
1.8 cm3
(50 mmol)
1.50 cm3
(23 mmol)
17 cm3
5 cm3
Ga2(SO4)3, 0.666 g. /
Cr(NO3)3·9H2O, 0.025 g
(1.6 mmol / 0.063 mmol)
1.230 g
(15 mmol)
1.8 cm3
(50 mmol)
1.55 cm3
(23 mmol)
17 cm3
10 cm3
Ga: 2.3%Cr
etanol
Los estudios realizados sobre las condiciones de síntesis indican que estas fases se
pueden preparar con relativa facilidad. La mayoría de ellas se pueden obtener puras en un
amplio intervalo de pH, que suele estar comprendido entre 1.5 y 8. A pH mayores se
obtienen las fases correspondientes con mayor o menor cantidad de impurezas, o incluso
no se obtiene ningún producto sólido.
La proporción entre agua y etanol de la mezcla empleada como disolvente influye
drásticamente sobre la calidad y el tamaño de los monocristales obtenidos. Además, el
empleo de una cantidad demasiado reducida de etanol, prescindir de él o emplear otro
codisolvente orgánico produce la aparición de impurezas, (caso de la síntesis del
compuesto de hierro), o la no aparición de producto sólido (caso de los compuestos de
vanadio y de cromo). El aumento de la cantidad de ácido fluorhídrico empleada suele estar
relacionado con el aumento de tamaño de los monocristales obtenidos y la disminución de
su cantidad. Sin embargo, esta última variación no suele contribuir a una mejora de la
calidad de los mismos y si se emplea una cantidad excesiva, es frecuente observar el efecto
contrario. La reducción de la cantidad de ácido fluorhídrico empleada conduce a la
disminución de tamaño de los monocristales obtenidos y a la aparición de impurezas.
Sin haber llegado a realizar un estudio exhaustivo de la influencia de los diversos
parámetros en el proceso de síntesis, se ha tratado de optimizar el mismo, de tal manera
que se obtengan los compuestos en forma de monocristales de la mejor calidad posible, y
libres de impurezas. En las ocasiones en que las condiciones de síntesis necesarias para
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
35
satisfacer estos dos requisitos son diferentes, se han detallado en la Tabla I.1 las que
conducen a la obtención de los compuestos sin impurezas.
La síntesis de la fase de cromo ha resultado ser particularmente complicada y, con
frecuencia, poco reproducible. Ha sido preciso emplear una cantidad relativamente elevada
de sal metálica para obtener un producto sólido. Generalmente, se ha obtenido la fase en
forma de agregados de monocristales de pequeño tamaño, acompañados de impurezas. En
alguna de las preparaciones se pudo aislar una pequeña cantidad de monocristales de
calidad suficiente para su empleo en estudios por difracción de rayos X sobre monocristal.
Finalmente, y tras muchos ensayos modificando las cantidades de reactivos empleadas, se
obtuvieron una serie de preparaciones libres de impurezas que pudieron ser destinadas a
realizar las medidas de sus propiedades físicas.
I.1.2 ANÁLISIS QUÍMICO
El análisis químico del contenido en metal de transición y de P se ha llevado a cabo
por medio de Espectroscopía de Emisión Atómica de Plasma Acoplado Inductivamente
(Inductively Coupled Plasma – Atomic Emission Spectroscopy, ICP-AES). El contenido en
C, N, H se ha obtenido por análisis elemental, y el de F a partir de la medición de la
concentración de iones fluoruro en una disolución del producto de concentración conocida
con un electrodo selectivo de iones F-. En la Tabla I.2 se muestran los resultados para todos
los compuestos analizados. Los porcentajes determinados están en buen acuerdo con las
fórmulas propuestas. Para los compuestos bimetálicos de Fe y V, y el de Ga dopado con
Cr, la proporción de los metales presentes en la fórmula se ha calculado a partir de los
datos de análisis químico.
Tabla I.2 - Datos de análisis químico de los compuestos (C2N2H10)[M(HPO3)F3].
M
C(%)
N(%)
H(%)
F(%)
M(%)
P(%)
Exp. Calc.
Exp. Calc.
Exp. Calc.
Exp. Calc.
Exp. Calc.
Exp. Calc.
V
9.1
9.6
11.2 11.2
4.2
4.4
22.7 22.8
20.1
20.4
12.0 12.4
Cr
9.5
9.6
11.2 11.2
4.3
4.4
22.5 22.7
20.5
20.7
12.2 12.3
Fe
9.1
9.4
10.8 11.0
4.2
4.4
22.1 22.4
20.8
21.1
11.9 12.2
V0.28Fe0.72
9.3
9.5
11.0 11.1
4.0
4.4
22.0 22.5
V: 5.5 5.6
Fe: 15.6 15.9
11.8 12.2
Ga: 2.3%Cr
8.7
9.0
10.4 10.4
3.9
4.1
21.1 21.2
Ga: 25.2 25.5
Cr: 0.38 0.39
11.3 11.5
36
Capítulo I
I.2 ESTUDIO ESTRUCTURAL
I.2.1 TOMA DE DATOS Y RESOLUCIÓN ESTRUCTURAL
Los cristales de las fases (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga:
2.3%Cr) presentan, en general, morfología de prismas de base rómbica, más alargados los
de los compuestos de vanadio y cromo, siendo las dimensiones del de galio dopado con
cromo comparables entre si.
Para llevar a cabo la toma de intensidades de difracción, se ha seleccionado un
monocristal de tamaño y calidad adecuados de cada fase, mediante observación de la
correspondiente preparación bajo luz polarizada en una lupa. A continuación, se ha situado
el monocristal seleccionado en el difractómetro automático, procediendo a llevar a cabo la
toma de datos de difracción de rayos X según el método indicado para cada difractómetro
en el Anexo A.3.1. La recogida de datos se ha efectuado a temperatura ambiente, salvo en
el caso del compuesto de cromo que se midió a 100 K.
Una vez finalizado el proceso de toma de datos, se ha realizado la reducción de los
mismos, que incluye las correcciones de Lorentz y de polarización, así como la de
absorción. En el caso de las fases de vanadio y de cromo se ha prescindido de la corrección
de absorción debido al reducido tamaño de los monocristales empleados en el experimento
de difracción.
El método seguido para efectuar la reducción de datos depende del difractómetro
empleado, y se ha descrito en el Anexo A.3.1. Este proceso ha finalizado con la obtención
de los factores de estructura al cuadrado para todas las reflexiones medidas.
La resolución estructural se ha llevado a cabo, en todos los casos, empleando
métodos directos (SHELXS971) seguidos de síntesis de Fourier, lo que ha proporcionado
un modelo inicial que contenía las coordenadas de todos los átomos, a excepción de los de
hidrógeno. A continuación, se ha procedido al afinamiento estructural (SHELXL972) de
dicho modelo por el método de mínimos cuadrados de la matriz completa, con el empleo
de factores térmicos isotrópicos para todos los átomos. Durante el mismo, se han logrado
identificar los átomos de flúor diferenciándolos de los de oxígeno en base a la carencia de
enlaces con átomos de fósforo, y a que presentaban unos factores térmicos ligeramente
1 Sheldrick, G. M. SHELXS 97: Program for the solution of crystal structures; University of Göttingen,
Germany, 1997.
2 Sheldrick, G. M. SHELXL 97: Program for the refinement of crystal structures; University of Göttingen,
Germany, 1997.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
37
menores. Una vez alcanzada convergencia en esta etapa del afinamiento, se ha continuado
el mismo introduciendo factores térmicos anisotrópicos para todos los átomos del modelo
estructural, lo que ha conducido a la localización del átomo de hidrógeno del grupo fosfito
en el mapa de densidad electrónica residual en todos los casos. Los átomos de hidrógeno
del catión etilendiamonio no se han localizado en dicho mapa, por lo que se procedió a
realizar el cálculo geométrico de sus posiciones.
Tras introducir en el modelo las coordenadas de todos los átomos de hidrógeno y
fijar la distancia P-H a su valor teórico3 de 1.31(8) Å, se ha proseguido con el afinamiento
estructural, que ha finalizado con la obtención de factores de acuerdo aceptables en todos
los casos, y ha proporcionado el modelo estructural final para cada compuesto. A partir de
el mismo se han realizado los correspondientes cálculos geométricos (PARST4), de
valencias de enlace por el método propuesto por Brown5,6, así como las representaciones
de la estructura cristalina (ATOMS7).
Los procesos de resolución y afinamiento estructural se han llevado a cabo mediante
el sistema de programas WINGX8(versión 1.63). Se muestran en la Tabla I.3 los
parámetros cristalográficos correspondientes a la toma, reducción de datos, resolución y
afinamiento estructural para todos los compuestos. Las tablas de coordenadas atómicas,
factores térmicos, distancias, ángulos de enlace y los resultados de los cálculos de
valencias de enlace se presentan en el Anexo B.1.
3 Loub, J. Acta Cryst., B47, 468 (1991).
4 Nardelli, M. J. Appl. Cryst., 28, 659 (1995).
5 Brown, I. D.; Wu, K. K. Acta Cryst., 32, 1957 (1976).
6 Brown, I. D.; Altermatt, D. Acta Cryst., B41, 244 (1985).
7 Dowty, E. ATOMS: A Computer Program for Displaying Atomic Structures; Shape Software, 521 Hidden
Walley Road, Kingsport, TN (1993).
8 Farrugia, L. J. J. Appl. Cryst., 32, 837 (1999).
38
Capítulo I
Tabla I.3 – Datos crista
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
39
I.2.2 DESCRIPCIÓN DE LA ESTRUCTURA CRISTALINA
Las fases (C2N2H10)[M(HPO3)F3] presentan una estructura cristalina de marcado
carácter monodimensional, formada por el apilamiento de cadenas dobles de fórmula
[M(HPO3)F3]2- que se extienden en la dirección [001]. Las interacciones iónicas y enlaces
de hidrógeno que se establecen entre las cadenas aniónicas y los cationes etilendiamonio
dan lugar al empaquetamiento observado en la estructura de estos compuestos (Fig. I.1).
El metal de transición presenta una coordinación octaédrica y se encuentra enlazado
a tres átomos de oxígeno y tres de flúor. En estos octaedros mer-[MO3F3] dos átomos de
oxígeno están en posición trans, y tres átomos de flúor y uno de oxígeno en el mismo
plano. A su vez, el átomo de fósforo se encuentra unido a tres átomos de oxígeno y a uno
de hidrógeno, dando lugar a una topología de tetraedro distorsionado característica del
grupo fosfito (Fig. I.2 y Fig. I.3).
[M(HPO3)F3]2-
Enlace de
hidrógeno
(C2N2H10)2+
b
c
a
Fig. I.1 - Estructura cristalina de los compuestos (C2N2H10)[M(HPO3)F3] vista a lo largo de la
dirección [001].
40
Capítulo I
O(1)
O(3)
F(2)
F(1)
H(1)
O(1)
O(2)
[MO3F3]
O(3)
F(3)
(HPO3)
c
a
b
Fig. I.2 - Estructura de las cadenas dobles [M(HPO3)F3] paralelas a la dirección [001].
La sucesión alternada de los octaedros mer-[MO3F3] y los tetraedros (HPO3) da lugar
a cadenas infinitas, en las que cada octaedro comparte los dos átomos de oxígeno O(1) y
O(3) situados en trans con los tetraedros más cercanos. La distancia M-M a lo largo de la
cadena corresponde al parámetro c y está dentro del intervalo comprendido entre 6.37 y
6.51 Å para los diferentes compuestos estudiados.
Cada octaedro mer-[MO3F3] comparte, además, el átomo de oxígeno O(2) con un
tetraedro (HPO3) perteneciente a una cadena vecina, originando las cadenas dobles de
fórmula [M(HPO3)F3]2- (Fig. I.2). Dependiendo del metal que contengan, la menor
distancia entre dos átomos metálicos situados en dos cadenas sencillas vecinas diferentes
está dentro del intervalo comprendido entre 4.82 y 4.88 Å.
Las cadenas dobles [M(HPO3)F3]2- y los cationes etilendiamonio se encuentran
empaquetados dentro de la estructura de tal manera que cada cadena está rodeada de seis
cationes orgánicos dispuestos en las direcciones [101] y [ 1 01] y cada uno de éstos está
rodeado de tres cadenas (Fig. I.1). Los dos grupos NH3+ de cada catión orgánico se
encuentran muy próximos a las cadenas dobles aniónicas. De esta manera tiene lugar el
establecimento de tres y cuatro enlaces de hidrógeno entre los atomos de nitrógeno N(1) y
N(2), respectivamente, de los cationes etilendiamonio, y los átomos de flúor y oxígeno de
las cadenas aniónicas. Estos enlaces son de carácter considerablemente fuerte, con
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
41
distancias N-O y N-F inferiores a 3 Å. Aunque el empaquetamiento adoptado por las fases
esté determinado, mayormente, por las interacciones iónicas entre las cadenas aniónicas y
los cationes orgánicos, es probable que el carácter direccional de los enlaces de hidrógeno
haya ocasionado la estabilización de la estructura observada frente a otras con la misma (o
incluso mayor) eficiencia de empaquetamiento iónico.
Las cadenas dobles [M(HPO3)F3]2- poseen como elementos de simetría un eje binario
helicoidal que relaciona las dos cadenas simples que la integran. No obstante, presentan
una fuerte pseudosimetría consistente en planos m perpendiculares al eje de las cadenas y
que pasan por los átomos de metal y fósforo, generando pseudocentros de inversión
situados sobre los ejes y entre los poliedros de coordinación (Fig. I.3).
Eje 21
M
d (M-Mc. vecina)
Plano m
Centro
d (M-Mcadena)
Plano m
O(1)
O(3)
H(1)
F(3)
O(2)
P
O(1)
M
F(1)
Centro
F(2)
O(3)
F(1)
O(2)
F(2)
F(3)
M
Plano m
P
c
H(1)
O(1)
a
b
O(3)
Fig. I.3 - Poliedros de coordinación de M y P y elementos de simetría (color negro) y
2pseudosimetría (color gris) presentes en las cadenas de fórmula [M(HPO3)F3] .
Las cadenas dobles que forman parte de la estructura de las fases
(C2N2H10)[M(HPO3)F3] constituyen un motivo estructural que se puede hallar en
compuestos relacionados, tales como el fosfito de vanadilo [VO(HPO3)(H2O)2]·3H2O9, el
9 Zakharova, B. S.; Ilyukhin, A. B.; Chudinova, N. N. Zhurnal Neorganicheskoi Kimii, 39, 1443 (1994).
42
Capítulo I
hidrógenofosfato de vanadilo VO(HPO4)·4H2O10, el hidrógenofosfato de molibdeno
MoO2(HPO4)·H2O11, el fosfonato Zr2(O3PCH2CH2-viológeno-CH2CH2PO3)F6·2H2O12, o el
polioxovanadato
híbrido
orgánico-inorgánico
conteniendo
fenantrolina
[V4O10(C12H8N2)2]13. En todos ellos, se puede apreciar la pseudosimetría descrita
anteriormente (plano m y centros de simetría), y sólo en el caso del hidrógenofosfato de
molibdeno ésta se corresponde con la simetría real de las cadenas (grupo espacial P 21/m).
Las cadenas que forman parte del fosfonato Zr2(O3PCH2CH2-viológenoCH2CH2PO3)F6·2H2O son las que presentan mayor semejanza con las de las fases
estudiadas (C2N2H10)[M(HPO3)F3]. Tanto unas como otras incluyen sólamente un eje
binario helicoidal como elemento de simetría y los poliedros de coordinación del metal son
similares, incluyendo tres átomos de oxígeno y tres de flúor en la misma disposición. La
diferencia más importante tiene que ver con el papel que juega la molécula orgánica en la
estabilización de la estructura cristalina. Este catión orgánico enlaza todas las cadenas en
una dirección, dando lugar a una estructura laminar para el fosfonato, mientras que en los
compuestos (C2N2H10)[M(HPO3)F3], las interacciones iónicas entre las cadenas aniónicas y
los cationes orgánicos establecen un entramado tridimensional. En ambos casos, se puede
relacionar la simetría y pseudosimetría de las cadenas con el efecto ejercido por la parte
orgánica. En las cadenas pertenecientes al resto de compuestos citados en la bibliografía no
se observa ningún elemento de simetría.
Los otros dos ejes binarios helicoidales que contiene la estructura de las fases
(C2N2H10)[M(HPO3)F3], en las direcciones de los ejes z e y, generan el empaquetamiento
de las cadenas aniónicas y los cationes etilendiamonio.
Estos compuestos son quirales. El análisis de las coordenadas atómicas permite
concluir que todos los cristales medidos (salvo el del compuesto de galio dopado con
cromo) presentan la misma configuración absoluta. No obstante, dado que se ha partido de
reactivos no quirales, no se puede descartar la presencia de mezclas racémicas en las
preparaciones de los diferentes compuestas. Ello implicaría que el enantiómero de cada
fase depende del individuo escogido para la toma de datos de difracción, lo que es una
cuestión de azar.
10 Leonowicz, M. E.; Johnson, J. W.; Brody, J. F.; Shannon, H. F. Jr.; Newsam, J. M. J. Solid State Chem.,
56, 370 (1985).
11 Biot, C.; Leclaire, A.; Borel, M. M.; Raveau, B. Zeitschrift für Kristallog., 212, 792 (1997).
12 Poojary, D. M.; Vermeulen, L. A.; Vicenzi, E.; Clearfield, A.; Thompson, M. E. Chem. Mater., 6, 1845
(1994).
13 Li, Y.; Wang, E.; Zhang, H.; Luan, G.; Hu, G. J. Solid State Chem., 163, 10 (2002).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
43
I.3 ESTUDIOS TÉRMICOS
Se ha realizado el análisis termogravimétrico de todas las fases estudiadas en este
capítulo, empleando atmósfera de aire sintético y una velocidad de calentamiento de 5
ºC/min, desde temperatura ambiente hasta 800 ºC. Los estudios térmicos se han
completado en el caso de las fases (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe) con análisis
termodifractométricos. Para ello se han registrado en atmósfera de aire diagramas de
difracción de rayos X sobre muestra policristalina desde 30 ºC hasta 810 ºC, en intervalos
de 15 ºC, empleando una velocidad de calentamiento de 5 ºC/min. Los difractogramas se
han medido empleando un paso de 0.02 en º2θ y un tiempo de contaje de 1 s por paso.
I.3.1 FASE (C2N2H10)[V(HPO3)F3]
En el termograma de este compuesto de vanadio (Fig. I.4) se puede apreciar que no
tiene lugar ningún proceso a temperaturas menores que 300 ºC, aproximadamente. Por
encima de esta temperatura se da una continua pérdida de masa, que finaliza a 670 ºC,
aproximadamente.
8
90
4
ATD
80
0
ATD (ºC)
% Masa
TG
100
70
-4
60
0
100
200
300
400
500
600
700
-8
800
T(ºC)
Fig. I.4 - Termograma del compuesto (C2N2H10)[V(HPO3)F3].
La primera etapa de este proceso entre 300 y 360 ºC es rápida y exotérmica. Sin
embargo, la ausencia de meseta posterior o cambio brusco de pendiente indica que esta
etapa se solapa con las que suceden a continuación. El final del pico exotérmico que se
observa en la curva ATD (Análisis Térmico Diferencial) tiene lugar a una temperatura de,
44
Capítulo I
aproximadamente, 360 ºC y corresponde a una pérdida de masa del 25.5 % de la masa
inicial. Estos datos, junto con la temperatura a la que tiene lugar, permiten asignar esta
etapa a la pérdida de la molécula de etilendiamina (24.0 % teor.).
Durante el resto del proceso de descomposición no se observa ningún otro accidente
notable en la curva ATD, a excepción de unos pequeños picos exotérmicos, lo que permite
suponer un comportamiento térmico complejo para el sistema a temperaturas superiores a
360 ºC, con etapas redox y de descomposición. Este comportamiento complejo coincide
con el que muestran comúnmente los sistemas V-P-O14, y es la base de la utilidad de este
tipo de compuestos como catalizadores para la oxidación selectiva del n-butano a anhídrido
maléico.
A la temperatura a la cual la masa de muestra es mínima (680 ºC, aproximadamente)
ésta corresponde a un 59.3 % de la masa de muestra inicial. Este valor concuerda con la
formación del pirofosfato de vanadilo (IV), (VO)2P2O7 (61.56 % teórico). Esta fase, que ha
sido identificada en los estudios sobre descomposición térmica de fosfatos15, fosfonatos15
y fosfitos de vanadilo16, está relacionada con una mayor selectividad de los catalizadores
de sistemas V-P-O para la reacción anteriormente citada. Se puede proponer la Ecuación
[I.1] para todo el proceso.
(C 2 N 2 H 10 )[V(HPO 3 )F3 ] +
3
1
O 2 → C 2 N 2 H 8 + 3HF + (VO) 2 P2 O 7
4
2
[I.1]
Por encima de 680 ºC tiene lugar una ligera y progresiva ganancia de masa de,
aproximadamente, un 1 % de la masa inicial. Esta ganancia se puede asignar, al comienzo
del proceso de oxidación del pirofosfato de vanadilo (IV) a fosfato de vanadilo (V), según
la Ecuación [I.2]. En los estudios presentes en la bibliografía, este proceso de oxidación
comienza a 330 ºC para el caso del fosfito de vanadilo VO(HPO3)·1.5H2O y a 630º C para
el fosfato de vanadilo VO(HPO4)·0.5H2O.
(VO) 2 P2 O 7 +
1
O 2 → 2 (VO)PO 4
2
[I.2]
La obtención de un residuo final compacto y fuertemente adherido al crisol ha
impedido llevar a cabo su identificación por difracción de rayos X sobre muestra
policristalina.
14 Guliants, V. V.; Benziger, J. B.; Sundaresan, S. J. Catal., 156, 298 (1995).
15 Guliants, V. V.; Benziger, J. B.; Sundaresan, S. ; Wachs, I. E.; Jehng, J.-M. Chem. Mater., 7, 1493 (1995).
16 Guliants, V. V.; Benziger, J. B.; Sundaresan, S. Chem. Mater., 7, 1485 (1995).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
45
El estudio termodifractométrico (Fig. I.5) muestra que en los difractogramas
registrados a temperaturas menores que 255 ºC se pueden observar los máximos de
difracción correspondientes a la fase inicial, (C2N2H10)[V(HPO3)F3]. En los difractogramas
obtenidos entre 255 ºC y 450 ºC no aparece ningún máximo, y presentan un fondo más
elevado que los de temperaturas más bajas. Estos resultados indican que la estructura
cristalina de la fase (C2N2H10)[V(HPO3)F3] se desmorona a una temperatura notablemente
inferior a la que tiene lugar el comienzo de pérdida de la molécula orgánica, dando lugar a
un compuesto amorfo.
Fig. I.5 - Diagramas de difracción de Rayos X correspondientes al estudio termodifractométrico
del compuesto (C2N2H10)[V(HPO3)F3]. Se han indicado las temperaturas a las que
tienen lugar los cambios de fase, las fases identificadas y los procesos observados en el
análisis termogravimétrico.
Entre 450 ºC y 705 ºC se pueden identificar tres polimorfos del fosfato de
vanadilo(V), VO(PO4). Los primeros máximos de difracción que aparecen a 450 ºC
corresponden a la fase ω-VO(PO4)17a (tetragonal, a = 6.839 Å, c = 8.420 Å). Por encima de
480 ºC aproximadamente, se observan los máximos pertenecientes al compuesto βVO(PO4)17b (rómbico, Pnma, a = 7.78 Å, b = 6.13 Å, c = 6.97 Å). Este polimorfo del
fosfato de vanadilo (V) constituye la fase mayoritaria en la fracción cristalina de la muestra
en el intervalo comprendido entre 480 ºC y 705 ºC. A temperaturas superiores a 480 ºC se
observa la desaparición paulatina de los máximos de difracción correspondientes al
polimorfo ω-VO(PO4) y su sustitución por la fase alfa17c (tetragonal, P4/n, a = 6.014 Å, c =
4.434 Å). Estas dos fases son minoritarias a estas temperaturas.
17 “Powder Diffraction File – Inorganic and Organic”, Fichas nº 37-809(a), 27-948(b), 70-1535(c). ICDD.
Pennsylvania, USA (2001).
46
Capítulo I
Estos resultados son muy diferentes de los obtenidos en el análisis
termogravimétrico, en el que el valor mínimo de la masa de muestra alcanzado a 680 ºC
(59.3 % de la inicial) descarta que se trate de cualquier polimorfo del fosfato de
vanadilo(V) (66.7 % teórico), aunque se ha propuesto su formación por encima de esta
temperatura. Las diferencias observadas se pueden atribuir a la conjunción de factores
cinéticos y termodinámicos, estando originadas por la diferente velocidad relativa de
calentamiento empleada en ambas técnicas.
Los máximos de difracción correspondientes a los diversos polimorfos del fosfato de
vanadilo (V) desaparecen a temperaturas superiores a 705 ºC, lo que indica una fusión de
la muestra a esta temperatura. En efecto, el residuo final obtenido es compacto y estaba
fuertemente adherido al portamuestras, lo que correspondería a un compuesto amorfo,
resultado de la rápida solidificación de un fundido, como ocurría en el análisis
termogravimétrico.
I.3.2 FASE (C2N2H10)[Cr(HPO3)F3]
El termograma de la fase de cromo se muestra en la Figura I.6. Se observa un
proceso continuo de pérdida de masa que comienza a temperatura ambiente, finalizando a
600 ºC, aproximadamente. Dicho proceso está formado por varias etapas solapadas, que se
distinguen por las diferentes pendientes mostradas por la curva de pérdida de masa, y por
su carácter exotérmico o endotérmico.
En la primera etapa, la masa de muestra disminuye en un 2.3%, teniendo lugar entre
temperatura ambiente y 100 ºC. Esta etapa posee carácter endotérmico y corresponde a la
pérdida del agua adsorbida por el compuesto.
A continuación comienza una etapa de pérdida de masa progresiva, que se acelera a
partir de 300 ºC, temperatura a la cual la masa se ha reducido en un 5.8%. Entre 300 ºC y
380 ºC continúa este proceso de manera más rápida. La curva ATD indica que se trata de
un proceso endotérmico. La pérdida de masa asociada a estas dos etapas es de un 19.0 %, y
corresponde, aproximadamente, a la eliminación de la molécula de etilendiamina (23.9 %
teor.). Las diferencias encontradas entre la pérdida de masa real y el porcentaje teórico
indican que la reacción no ha finalizado a 380 ºC, solapándose con la siguiente.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
47
8
TG
100
7
6
ATD
5
4
80
3
70
ATD (ºC)
% Masa
90
2
1
60
0
100
200
300
400
500
600
700
0
800
T(ºC)
Fig. I.6 - Termograma del compuesto (C2N2H10)[Cr(HPO3)F3].
Entre 380 ºC y 600 ºC tienen lugar la pérdida de ácido fluorhídrico, así como la
descomposición y oxidación del grupo fosfito.
En el intervalo de temperaturas comprendido entre 600 ºC y 770 ºC,
aproximadamente, no se produce variación de masa, manteniéndose en un 62.5 % de la
masa de muestra inicial. La curva ATD no registra ningún proceso térmico. En este
intervalo cabría esperar una composición para la muestra de fosfato de Cr(III), CrPO4
(58.53 % teor.), dada la estequiometría del compuesto analizado. El hecho de que su masa
real sea mayor que la teórica indicaría que se ha producido una oxidación parcial del ion
Cr(III) durante las etapas anteriores. El exceso de masa encontrado correspondería a otro
anión que compensa la carga del Cr, probablemente óxido procedente del oxígeno del aire,
o parte del ion fluoruro que no se ha perdido en la etapa correspondiente.
A temperaturas superiores a 770 ºC se produce una disminución de masa exotérmica
que corresponde a la pérdida de anhídrido fosfórico (punto de ebullición18 605 ºC). El
residuo obtenido a 800 ºC ha sido caracterizado por difracción de rayos X sobre muestra
policristalina. Se trata de una mezcla de un compuesto amorfo (fondo significativamente
elevado) y del óxido de Cr(III) Cr2O319 (trigonal, P-3c, a = 4.951 Å, c = 13.598 Å). La
18 Lide, D. R.; Frederikse, H. P. R.(eds.) “CRC Handbook of Chemistry and Physics”, 77th Edition, CRC
press, Boca Raton, USA (1996).
19 “Powder Diffraction File – Inorganic and Organic”, Ficha nº 84-1616. ICDD. Pennsylvania, USA
(2001).
48
Capítulo I
altura del fondo en el difractograma indica que la fracción amorfa de la muestra es
probablemente mayoritaria, conteniendo cromo en estados de oxidación mayores que tres.
En los difractogramas medidos a temperaturas menores que 285 ºC (Fig. I.7) se
pueden identificar los máximos de difracción correspondientes al compuesto inicial
(C2N2H10)[Cr(HPO3)F3]. Por encima de dicha temperatura desaparecen todos los máximos
de difracción, lo que indica la destrucción térmica de la estructura cristalina del compuesto.
A diferencia de lo que ocurría con el compuesto de vanadio, el paso a un producto amorfo
tiene lugar después de comenzar la eliminación de la molécula orgánica, cuando la masa ya
ha disminuido un 4.5%, aproximadamente.
En el intervalo de temperaturas comprendido entre 285 ºC y 810 ºC no se observa
ningún máximo de difracción, por lo que la muestra es amorfa. Estos hechos contrastan
con los resultados de la caracterización del residuo del termograma a 800 ºC en el que se
identificó una pequeña cantidad óxido de Cr(III). Estas diferencias podrían estar
relacionadas con la diferente velocidad relativa a la que se produce el incremento térmico
en las dos técnicas empleadas.
Fig. I.7 - Diagramas de difracción de rayos X correspondientes al estudio termodifractométrico
del compuesto (C2N2H10)[Cr(HPO3)F3]. Se han indicado las temperaturas a las que
tienen lugar los procesos observados en el análisis termogravimétrico.
I.3.3 FASE (C2N2H10)[Fe(HPO3)F3]
El termograma de esta fase (Fig. I.8) muestra un primer proceso de pérdida de masa
exotérmico que tiene lugar a una temperatura de 310 ºC, aproximadamente. Esta
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
49
temperatura se encuentra dentro del intervalo habitual para los procesos de pérdida de
molécula orgánica en fosfatos de metales de transición con estructuras abiertas y diaminas
orgánicas20. El valor de la pérdida de masa (24.4 %) se corresponde con el de una
molécula de etilendiamina (23.6 % teor.).
Entre 290 ºC y 500 ºC se produce un proceso de disminución de masa gradual que
culmina con una pérdida repentina y exotérmica a 500 ºC, aproximadamente. En el
intervalo comprendido entre 500 ºC y 800 ºC no tiene lugar ningún otro proceso, y la masa
se mantiene constante (55.8 % de la muestra inicial).
El residuo final ha sido identificado por difracción de rayos X sobre muestra
policristalina como una mezcla de fosfato de hierro FePO421a (trigonal, P3121, a = 5.027 Å,
c = 11.234 Å) y oxifosfato de hierro Fe3(PO4)O321b (trigonal, R3m, a = 8.006 Å, c = 6.863
Å) como fase minoritaria.
25
TG
100
20
15
10
80
5
70
ATD (ºC)
% Masa
90
ATD
0
60
-5
50
0
100
200
300
400
500
600
700
-10
800
T(ºC)
Fig. I.8 - Termograma del compuesto (C2N2H10)[Fe(HPO3)F3].
Por lo tanto, la pérdida de masa que tiene lugar entre 320 ºC y 500 ºC se debe a
procesos solapados con pérdida de flúor, así como a la oxidación del grupo fosfito a
fosfato, de carácter exotérmico y con pérdida brusca de masa (el hidrógeno del fosfito
eliminado en forma de agua) a 500 ºC.
20 Walton, R. I.; Millange, F.; O’Hare, D. Chem. Mater., 12, 1977 (2000).
21 “Powder Diffraction File – Inorganic and Organic”, Fichas nº 84-876(a), 76-1761(b). ICDD.
Pennsylvania, USA (2001).
50
Capítulo I
La obtención del fosfato de hierro FePO4 como único residuo correspondería a una
masa final de 59.2 %. La existencia del oxifosfato de hierro Fe3(PO4)O3 como fase
minoritaria en dicho residuo implica la pérdida de una pequeña parte del fósforo,
probablemente como P2O5. Se puede proponer la Ecuación [I.3] para el proceso global de
descomposición térmica del compuesto (C2N2H10)[Fe(HPO3)F3].
(C 2 N 2 H 10 )[Fe(HPO 3 )F3 ] +
1
x
x
O 2 → C 2 N 2 H 8 + 3HF + (1 − x)FePO 4 + Fe 3 (PO 4 )O 3 + P2 O 5
2
3
3
[I.3]
Los diagramas de difracción obtenidos a temperaturas menores que 240 ºC (Fig. I.9)
corresponden al compuesto inicial, (C2N2H10)[Fe(HPO3)F3]. La desaparición de los
máximos de difracción indica que a esta temperatura tiene lugar el colapso de la estructura
cristalina que conduce a la formación de un compuesto amorfo. Al igual que sucede en el
compuesto de vanadio, este proceso tiene lugar a una temperatura más baja que la que
marca el inicio de la pérdida de la molécula de etilendiamina en el termograma (310 ºC).
Fig. I.9 - Diagramas de difracción de rayos X correspondientes al estudio termodifractométrico
del compuesto (C2N2H10)[Fe(HPO3)F3]. Se han indicado las temperaturas a las que
tienen lugar los cambios de fase y los procesos observados en el análisis
termogravimétrico.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
51
Por encima de 510 ºC se observa la aparición de los máximos de difracción
correspondientes al fosfato de hierro FePO422a (rómbico, Cmcm, a = 5.227 Å, b = 7.770 Å,
c = 6.322 Å).
A la temperatura de 600 ºC tiene lugar un cambio de fase, en el que desaparecen los
máximos de difracción del fosfato de hierro, y aparecen los correspondientes al fosfato de
hierro polimorfo FePO422b (trigonal, P3121, a = 5.027 Å, c = 11.234 Å) y al oxifosfato de
hierro Fe3(PO4)O322c (trigonal, R3m, a = 8.006 Å, c = 6.863 Å), éste último minoritario.
Estas dos fases son las que se obtienen como residuo del termograma.
En el intervalo comprendido entre 600 ºC y 810 ºC no se observan cambios en los
diagramas de difracción de rayos X, en buen acuerdo con las fases identificadas en el
residuo del termograma.
I.3.4 FASE (C2N2H10)[Ga(HPO3)F3]: 2.3%Cr
En el análisis termogravimétrico realizado a esta fase (Fig. I.10) se observa un
proceso continuo de pérdida de masa entre 250 ºC y 670 ºC, caracterizado por varias etapas
con pendientes diferentes.
TG
100
6
ATD
4
80
70
2
ATD (ºC)
% Masa
90
60
0
50
40
0
100
200
300
400
500
600
700
-2
800
T(ºC)
Fig. I.10 - Termograma del compuesto (C2N2H10)[Ga(HPO3)F3]:2.3%Cr.
22 “Powder Diffraction File – Inorganic and Organic”, Fichas nº 30-659(a), 84-876(b), 76-1761(c). ICDD.
Pennsylvania, USA (2001).
52
Capítulo I
La primera etapa consiste en una pérdida endotérmica de un 33.6 %, mucho mayor
que la correspondiente a la masa de la molécula de etilendiamina (22.4 % teor.). No
obstante, esta etapa tiene lugar dentro del intervalo de temperaturas habitual para esta
reacción, según se ha observado en los estudios sobre las fases isoestructurales presentados
en este capítulo. Este hecho se debe a que la pérdida de la molécula orgánica tiene lugar
simultáneamente con otra reacción de descomposición.
A una temperatura de 325 ºC, aproximadamente, se observa un cambio de pendiente
con el que comienza una etapa de pérdida de masa más lenta que la anterior. Por encima de
375 ºC vuelve a aumentar la pendiente y se observa una sucesión de pequeños picos
endotérmicos y exotérmicos en la curva ATD. Después de alcanzar temperaturas
superiores a 670 ºC la masa de muestra permanece constante, y corresponde al 43.7 % de
la masa inicial de muestra.
El residuo final obtenido a 800 ºC es amorfo, no presentando máximos en su
diagrama de difracción de rayos X. Se puede proponer la formación del oxifosfato de galio
Ga3(PO4)O3 (43.7 % teor.) como producto final, ya que concuerda con la masa de producto
final (43.7 %). Esto supondría una pérdida de fósforo como P2O5 en alguna etapa del
proceso de descomposición, según queda reflejado en la ecuación [I.4].
(C 2 N 2 H 10 )[Ga(HPO 3 )F3 ] +
1
1
1
O 2 → C 2 N 2 H 8 + 3HF + Ga 3 (PO 4 )O 3 + P2 O 5
2
3
3
[I.4]
I.3.5 FASE (C2N2H10)[V0.28Fe0.72(HPO3)F3]
El termograma de esta fase bimetálica (Fig. I.11) muestra una ligera disminución del
1.3 % de masa entre temperatura ambiente y 180 ºC, atribuible a la pérdida del agua
adsorbida por el compuesto. Entre 270 y 350 ºC se produce una pérdida exotérmica del
24.4 % de masa. Por comparación con el comportamiento térmico del correspondiente
compuesto homometálico de hierro (Fig. I.8), se puede asignar este proceso a la pérdida de
la molécula de etilendiamina (23. 7 % teor.).
A 350 ºC tiene lugar un cambio de pendiente en la curva, temperatura a la cual
comienza una pérdida de masa compuesta de dos etapas. La primera de ellas es lenta, y
durante la misma, la curva ATD no registra ningun intercambio térmico. Esta etapa finaliza
a 440 ºC, donde comienza la segunda etapa (más rápida y de carácter exotérmico) que
continua hasta 600 ºC. A esta última temperatura se observa un pico endotérmico en la
curva ATD.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
53
12
TG
100
10
8
6
ATD
80
4
2
ATD (ºC)
% Masa
90
70
0
-2
60
0
100
200
300
400
500
600
700
-4
800
T(ºC)
Fig. I.11 - Termograma del compuesto (C2N2H10)[V0.28Fe0.72(HPO3)F3].
Por encima de 600 ºC la masa se mantiene a un valor constante del 58.0 %. No se ha
podido recuperar el residuo formado a 800 ºC debido a que quedó fuertemente adherido al
crisol empleado, lo cual ha impedido su caracterización.
Por comparación con el comportamiento térmico de los compuestos homometálicos
de vanadio y hierro (Fig. I.4 y Fig. I.8) se puede asignar la última pérdida de masa a
reacciones de condensación y procesos redox que conducen, probablemente, a la
formación de fosfatos de hierro y vanadio. Debido al desconocimiento acerca del estado de
oxidación final del vanadio y a la carencia de información sobre la composición del
residuo final, no se ha propuesto ninguna reacción para estos últimos procesos.
En cualquier caso, el comportamiento térmico del compuesto bimetálico
(C2N2H10)[V0.28Fe0.72(HPO3)F3] se encuentra más cercano al del compuesto homometálico
de hierro, como cabría esperar por su mayor contenido en este metal.
I.3.6 DISCUSIÓN
En la Tabla I.4 se muestra un resumen del comportamiento térmico de los
compuestos estudiados en este Capítulo.
El compuesto de Cr es el que mantiene su estructura cristalina hasta una mayor
temperatura ( 285 ºC), mayor que la de comienzo de su descomposición térmica. En el
54
Capítulo I
resto de compuestos estudiados por termodifractometría (M = V, Fe) se destruye la
estructura cristalina a una temperatura aproximadamente 40 ºC menor que la del comienzo
de su descomposición térmica.
Tabla I.4 - Resumen del comportamiento térmico de las fases (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe,
Ga: 2.3%Cr, V0.28Fe0.72).
M
Comienzo
(TG)
Pérdida
Cristalinidad
Residuo TG
Cambios de fase
V
300
255
-
amorfo → β − VO(PO4 ) → amorfo
Cr
100*
285
amorfo +
Cr2O3
amorfo en todo el intervalo
Fe
280
240
FePO4 +
Fe3(PO4)O3
amorfo → FePO 4 → FePO 4 (trig.)
480ºC
705º C
510ºC
600º C
(romb.)
Ga
250
-
-
-
V0.28Fe0.72
270
-
-
-
+ Fe3 (PO 4 )O3
* Perdida continua de masa a partir de temperatura ambiente. Hasta 100 ºC se ha asignado al agua
adsorbida.
El compuesto de vanadio es el que resiste mayores temperaturas sin descomponerse,
mientras que el de galio dopado con cromo comienza su descomposición a temperaturas
menores. Los estudios térmicos de los compuestos de vanadio y de hierro muestran que la
aparición de fases cristalinas tras su descomposición térmica tiene lugar a temperaturas
cercanas a 500 ºC, produciéndose algún cambio de fase a mayores temperaturas. El
compuesto de cromo muestra un comportamiento anómalo, no detectándose ninguna fase
cristalina a altas temperaturas.
La temperatura de inicio de la descomposición térmica de la fase bimetálica de hierro
y vanadio es semejante a la del compuesto de hierro. Sin embargo, parece que el vanadio
que contiene determina que el residuo final del análisis termogravimétrico quede
fuertemente adherido al crisol, como ocurre con el compuesto homometálico de dicho ion.
I.4 ESTUDIOS ESPECTROSCÓPICOS
I.4.1 ESPECTROSCOPÍA INFRARROJA Y RAMAN
Se han registrado los espectros infrarrojos de las fases estudiadas en este capítulo en
el intervalo de longitudes de onda comprendido entre 400 y 3600 cm-1 (Fig. I.12).
Con el objeto de obtener información complementaria a la proporcionada por los
espectros infrarrojos se han medido los de Raman de las fases (C2N2H10)[M(HPO3)F3]
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
55
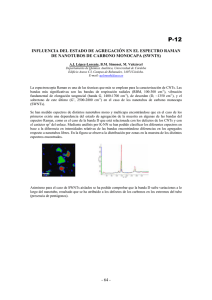
(M=Fe, Cr, Ga: 2.3%Cr) (Fig. I.13). La medida del espectro de los compuestos que
contienen vanadio no mostraron señal apreciable, degradándose al incrementar ligeramente
la intensidad de radiación aplicada. Dicho comportamiento se debe a la absorción de la
radiación empleada.
M=V
Transmitancia (u. a.)
M = Cr
M = Fe
M=V
Fe
0.28
0.72
M = Ga: 2.3 %Cr
γ(NH );
+
3
δ(CH )
γ(CH2)
2
ν(N-H); ν(C-H)
3600
3200
2800
δ(PO )
δ(NH +)
ν(P-H)
2400
3
2000
ν(C-N)
1600
ν(PO ); δ(P-H)
3
3
1200
800
400
ν (cm )
-1
Fig. I.12 – Espectros infrarrojos de los compuestos (C2N2H10)[M(HPO3)F3].
En efecto, en el caso de los compuestos que contienen vanadio, la longitud de onda
del láser de neodimio empleado en la medida de los espectros Raman (9398 cm-1) coincide,
aproximadamente, con el máximo de absorción de una banda del espectro de reflectancia
difusa como se describirá en el apartado correspondiente. Este hecho indica que, por una
parte, la mayoría de la radiación láser suministrada va a sufrir absorción, en vez de
dispersión Raman. Por este motivo hace falta una intensidad mayor de radiación láser para
obtener una señal registrable en la medida de éstos compuestos en comparación con los
56
Capítulo I
demás. Sin embargo, la absorción de una gran cantidad de energía por la muestra irradiada
puede conducir fácilmente a su degradación. Estos fenómenos explicarían el
comportamiento observado durante la medida de los espectros Raman de los compuestos
que contienen vanadio.
En la Tabla I.5 se muestran la frecuencia, intensidad y asignación de las bandas que
se observan en los espectros infrarrojos y Raman de las fases (C2N2H10)[M(HPO3)F3]. Se
observa que la mayoría de las bandas están situadas, aproximadamente, en los mismos
valores de frecuencia en las dos series de espectros, mostrando intensidades diferentes.
La diferencia en la frecuencia a la que aparece alguna banda en el espectro infrarrojo
y en el espectro Raman puede ser explicada teniendo en cuenta que, en ocasiones,
coinciden varios modos de vibración en los que intervienen enlaces del mismo tipo,
algunos activos en espectroscopía infrarroja y otros en Raman.
La primera banda que se observa en algunos espectros infrarrojos está situada a 3440
cm , aproximadamente. Esta banda, ancha y con intensidad débil, no se observa en los
espectros Raman, y corresponde a la vibración de tensión del enlace O-H del agua
adsorbida por el compuesto.
-1
ν(P-H)
ν(PO ); δ(P-H)
3
3
ν(N-H); ν(C-H)
Intensidad (u. a.)
δ(PO )
δ(NH +)
3
δ(CH )
2
γ(NH +);
3
γ(CH )
2
M = Cr
M = Fe
M = Ga: 2.3% Cr
3600
3200
2800
2400
2000
1600
1200
800
400
-1
Desplazamiento Raman (cm )
Fig. I.13 – Espectros Raman de los compuestos (C2N2H10)[M(HPO3)F3] (M=Cr, Fe, Ga: 2.3%Cr).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
57
-1
Tabla I.5 – Asignaciones de las bandas (cm ) de los espectros infrarrojos y Raman de los
compuestos (C2N2H10)[M(HPO3)F3]
M
V
Cr
Fe
V0.28Fe0.72
Ga: 2.3%Cr
IR
IR
Raman
IR
Raman
IR
IR
Raman
υ(N-H); υ(CH)*
3175,
3040fa
3195,
3050fa
3015,
2980ms
3165,
3040fa
3015,
2980ds
3170,
3035fa
3165,
3040fa
3020,
2980ms
Molécula
δ(NH3+)*
1615,
1540ms
1625,
1540fs
1620ms, 1615ma,
1520ds 1540ms,
1615da
1615ma,
1540ms
1625,
1540fs
1620ds
Orgánica
δ(CH2)*
1480,
1460ds
1480,
1455ds
1460,
1345ms
-
1460,
1345ds
1480,
1350ds
-
1460,
1350ds
υ(C-N)
1170ms
1170ms
-
1170ms
-
1170ms
1180fs
-
γ(NH3+);
γ(CH2)
795ds
800ds
865ms
795ds
925ds
795ds
795ds
925ms
υ(P-H)
2375ms
2375ms
2380fs
2380ms
2380fs
2380ms
2385fs
2385fs
Grupo
υas(PO3)
1080fa
1085fa
1110ma
1085fa
1080ma
1085fa
1110fa
1110ds
Fosfito
υs(PO3)
1045ms
1050ms
1060fs
1045ms
1060,
1040ms
1045ms
1045ms 1065ms,
1045ds
δ(P-H)
1025ds
1025ds
1025ms
1025ds
1030,
1020ms
1025ms
1025ms 1030ms,
δs(PO3)
595ms
605ms
590ds
590ms
580ds
590ms
600ms
585ds
505ma
530fa
530ms
480ma
480ds
500ma
510ds
525ds
δas(PO3)
Las características de cada banda se denotan como: f=fuerte, m= media, d=débil, a=ancha,
s=estrecha. *Varias bandas, se indican los dos máximos principales, h: se aprecia como un
hombro en una banda adyacente.
Entre 3300 y 2700 cm-1 aparece en los espectros infrarrojos una banda muy intensa,
ancha y con multitud de máximos (los principales a 3170 y 3040 cm-1). En los espectros
Raman, la banda tiene intensidad media y sus máximos, situados a 3020 y 2980 cm-1,
aproximadamente, se encuentran mejor resueltos. Esta banda es el resultado del
solapamiento de todos los modos de vibración de tensión de los enlaces N-H y C-H del
catión etilendiamonio.
Aproximadamente a 2380 cm-1 existe una banda muy estrecha, de intensidad media
en los espectros infrarrojos y muy intensa en los espectros Raman, que corresponde a la
vibración de tensión del enlace P-H del grupo fosfito. Como ya se ha puesto de manifiesto
en el estudio estructural, las fases (C2N2H10)[M(HPO3)F3] poseen un solo grupo fosfito
cristalográficamente independiente, por lo que esta banda es única.
A menores frecuencias, entre 1650 y 1500 cm-1, se observan dos bandas con algún
hombro, que corresponden a las frecuencias de los modos de vibración de deformación
δ(NH3+) de los cationes orgánicos. Estas bandas presentan intensidad media en los
58
Capítulo I
espectros infrarrojos, mientras que en los espectros Raman la primera muestra intensidad
media y la segunda es débil (en algún caso no se observa). La complejidad de esta zona del
espectro, se debe al elevado número de modos de deformación δ(NH3+) esperado de los
cationes etilendiamonio. La posición de la primera de estas bandas indica que la molécula
de etilendiamina está protonada23,24.
El intervalo comprendido entre 1500 y 1340 cm-1 es propio de los modos de
vibración de deformación δ(CH2). En esta zona se observan dos bandas de intensidad
media con hombros, así como algunas zonas de débil absorción. Tal como ocurría en el
caso anterior, esta complejidad está provocada por los distintos modos de vibración de
deformación δ(CH2) que poseen los cationes etilendiamonio.
Entre 1190 y 980 cm-1 aparecen un grupo de bandas solapadas muy intensas, tanto en
los espectros infrarrojos como en los espectros Raman. Pertenecen a los modos de tensión
simétrica y asimétrica de los enlaces P-O, y de flexión del enlace P-H del grupo fosfito.
Dado que el grupo fosfito no posee ningún elemento de simetría, las bandas
correspondientes a esos modos de vibración están desdobladas.
Los modos de vibración γ(NH3+) y γ(CH2) de la molécula orgánica dan lugar a una
banda estrecha de intensidad media que se observa en los espectros Raman a 925 cm-1,
aproximadamente (la banda aparece a 865 cm-1 en el caso del compuesto de cromo), y una
banda débil a 795 cm-1, aproximadamente, en el espectro infrarrojo.
Finalmente, las dos bandas observadas a 590 y 520 cm-1, aproximadamente, en los
dos tipos de espectros (más intensas en el espectro infrarrojo que en el Raman)
corresponden a los modos de flexión simétrica y asimétrica del grupo fosfito. En algunos
casos, la última banda presenta mayor anchura (o se encuentra desdoblada en dos) debido a
la degeneración del modo de flexión asimétrica.
I.4.2 ESPECTROSCOPÍA ULTRAVIOLETA-VISIBLE
Se han registrado los espectros de reflectancia difusa de todas las fases estudiadas en
este Capítulo. Además, se han medido los espectros luminiscentes de emisión y de
excitación de los compuestos que contienen cromo, ya que las fases que contienen este ion
pueden presentar fenómenos de luminiscencia.
23 Gharbi, A.; Jouini, A.; Averbuch-Pouchot, M. T.; Durif, A. J. Solid State Chem., 111, 330 (1994).
24 Dolphin, D.; Wick, A. E. “Tabulation of Infrarred Spectral Data”, John Wiley & Sons, New York (1997).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
59
Dado que cada ion metálico presenta características distintas, a continuación se
presentan los resultados obtenidos para los compuestos agrupados en tres conjuntos:
aquellos que contienen vanadio, los que contienen cromo, finalizando con el compuesto de
hierro. Concluiremos el apartado con un estudio comparativo.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, V0.28Fe0.72).
Los espectros de reflectancia difusa de las fases que contienen vanadio (Fig. I.14)
muestran las dos bandas características del ion V3+ en un entorno octaédrico, centradas
aproximadamente a 14000 cm-1 y 22000 cm-1. Estas bandas aparecen en la región del
visible, y son las responsables del color verde que muestran los compuestos. Se ha
empleado el diagrama de niveles de energía25,26 correspondiente a un sistema con
configuración electrónica d2 para realizar su asignación, lo que permite comprobar que las
bandas corresponden a las transiciones permitidas de espín desde el estado fundamental
3
T1g(3F) hasta los estados excitados 3T2g(3F) y 3T1g(3P).
Absorbancia (u. a.)
M=V
M=V
Fe
0.28
8000
12000
16000
20000
24000
0.72
28000
ν (cm )
-1
Fig. I.14 – Espectros
de
reflectancia
(C2N2H10)[M(HPO3)F3] (M=V, V0.28Fe0.72).
difusa
de
los
compuestos
En el espectro del compuesto que sólo contiene V, de color verde claro, las bandas
presentan mayor intensidad. Para el compuesto de V y Fe, la banda situada sobre 22000
cm-1 es más ancha. Estas características son la causa del color verde pálido amarillento que
presenta este compuesto bimetálico.
25 Tanabe, Y.; Sugano, S. J. Phys. Soc. Japan., 9, 753 (1954).
26 Orgel, L. E. J. Chem. Phys., 23, 1004 (1955).
60
Capítulo I
A 10000 cm-1, aproximadamente, se observa una banda algo más débil que las
anteriores que está originada por las transiciones prohibidas de espín entre el estado
fundamental 3T1g(3F) y los estados excitados 1E2g(1D) y 1T2g(1D).
En la región de números de onda mayores que 26000 cm-1, se puede apreciar una
acumulación de bandas muy anchas, considerablemente intensas y parcialmente solapadas
con la banda observada a 22000 cm-1. Dichas bandas de absorción se deben a
transferencias de carga entre el catión metálico y los ligandos.
En el caso del compuesto bimetálico que contiene V y Fe, no se ha observado
ninguna banda asignable a alguna de las transiciones propias del ion hierro(III). Sus
bandas, prohibidas de espín, se encontrarán probablemente obscurecidas por las bandas
pertenecientes al catión V3+.
Para realizar el ajuste de los espectros de reflectancia difusa se han empleado las
ecuaciones [I.5]-[I.8], lo cual ha permitido calcular los números de onda a los que se dan
las transiciones. Estas ecuaciones se han obtenido por diferencia entre las ecuaciones de los
niveles fundamental y excitados27.
9 B2
+ 0.5 225B2 + 100Dq2 + 180DqB
10Dq
1
Eg,1T2g(1D)←3T1g(3F); υ1 = 1.5B − 5Dq + 2C −
3
T2g(3F) ← 3T1g(3F);
υ2 = 5Dq − 7.5B + 0.5 225B2 + 100Dq 2 + 180DqB
[I.6]
3
T1g(3P) ← 3T1g(3F);
υ3 = 225B2 + 100Dq 2 + 180DqB
[I.7]
3
A2g(3F) ← 3T1g(3F);
υ4 = 15Dq − 7.5B + 0.5 225B2 + 100Dq 2 + 180DqB
[I.8]
[I.5]
En el caso de la fase que sólo contiene V, los mejores ajustes (Fig. I.15) se han
obtenido para los valores del parámetro de desdoblamiento del campo cristalino Dq = 1560
cm-1, y de los parámetros de Racah B = 550 cm-1 y C = 3060 cm-1. Los ajustes de la fase
bimetálica conducen a unos valores de Dq = 1540 cm-1, B = 540 cm-1 y C = 3140 cm-1.
Todos los parámetros se encuentran dentro del intervalo habitual para compuestos de
V(III) en un entorno octaédrico28,29,30. Los parámetros B son un 64 % y 62 % del
correspondiente al del ion libre31 (861 cm-1) para las fases de V, y bimetálica,
27 Lever, A. B. P. “Inorganic Electronic Spectroscopy”, Elsevier Science Publishers B. V., Amsterdam,
Nederlands (1984).
28 Mason, W. R.; Gray, H. B. J. Amer. Chem. Soc., 90, 5721 (1968).
29 Rush, R. M.; Martin, D. S.; LeGrand, R. G. Inorg. Chem., 14, 2543 (1975).
30 Sutton, J .E.; Krentzien, H.; Garner, C. S. Inorg. Chem., 19, 2425 (1980).
31 Griffith, J. S. “The Theory of Transition-Metal Ions”, Cambridge University Press, Londres (1964).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
61
respectivamente. Estos valores indican un grado notable de covalencia para los enlaces VO y V-F.
Absorbancia (u. a.)
a
M=V
3
3
3
2g
1
1
1
3
3
3
E , T ( D)<- T ( F)
2g
2g
1g
3
3
3
3
1g
3
T ( P)<- T ( F)
1g
3
3
A ( F)<- T ( F)
1g
3
T ( F)<- T ( F)
2g
1g
2-
3+
π(O )->t (V )
2g
8000
12000
16000
20000
24000
28000
ν (cm )
-1
Absorbancia (u. a.)
b
M=V
0.28
Fe
0.72
3
3
3
2g
1
1
1
3
3
3
E , T ( D)<- T ( F)
2g
2g
3
12000
3
1g
2-
2g
1g
16000
3+
π(O )->t (V )
3
T ( F)<- T ( F)
2g
8000
3
3
1g
T ( P)<- T ( F)
1g
1g
3
3
3
A ( F)<- T ( F)
20000
24000
28000
ν (cm )
-1
Fig. I.15 – Mejores ajustes obtenidos de los espectros de reflectancia difusa de los compuestos
(a) (C2N2H10)[V(HPO3)F3] y (b) (C2N2H10)[V0.28Fe0.72(HPO3)F3].
Para realizar los ajustes se introdujeron dos bandas adicionales, que dan cuenta de la
transferencia de carga ligando-metal. Estas bandas se encuentran solapadas con las de las
transiciones d-d del catión metálico y su posición final tras el ajuste (26000 cm-1 y 49900
cm-1 para el compuesto de V; 25800 cm-1 y 45100 cm-1 para el compuesto de V y Fe) está
62
Capítulo I
en razonable acuerdo con la energía esperada para las primeras transiciones π(O2-)
→t2g(V3+) (32000 cm-1) y π(O2-)→eg(V3+) (47700 cm-1). Estos valores teóricos han sido
obtenidos mediante cálculos realizados a partir de las electronegatividades ópticas de los
ligandos y los cationes metálicos, y las energías de apareamiento de espín, empleando el
tratamiento de Jørgensen32.
Por último, hay que hacer notar que los ajustes han permitido determinar la posición
de la banda de absorción debida a la transición desde el estado fundamental al estado
excitado 3A2g(3F), que generalmente es de difícil observación, (Ecuación [I.8]). Esta
transición es de dos electrones, por lo que da origen a una banda que suele presentar una
intensidad muy reducida.
Compuestos (C2N2H10)[M(HPO3)F3] (M=Cr, Ga: 2.3%Cr).
Absorbancia (u. a.), I (u. a.)
Los espectros de reflectancia difusa de las fases que contienen cromo se muestran en la
Figura I.16. Las dos bandas de absorción más intensas aparecen a 15200 y 22400 cm-1.
M = Ga: 2.3%Cr
M = Cr, emisión
M = Cr
12000
16000
20000
24000
28000
32000
36000
ν (cm )
-1
Fig. I.16 – Espectros de reflectancia difusa de los compuestos (C2N2H10)[M(HPO3)F3]
(M=Cr, Ga: 2.3%Cr) (linea contínua) y espectro de emisión del compuesto
(C2N2H10)[Cr(HPO3)F3] (línea de puntos).
Estas bandas son características del ion Cr3+ en un entorno octaédrico, y son
responsables del color verde que presentan los compuestos. Se han asignado a las
transiciones permitidas de espín que tienen lugar entre el estado fundamental 4A2g(4F) y los
estados excitados 4T2g(4F) y 4T1g(4F), respectivamente. Muestran las mismas características
32 Jørgensen, C. K. en: Jørgensen, C. K.; Neilands, J. B.; Nyholm, R. S.; Reinen, D.; Williams, R. J. P. (eds.)
“Structure and Bonding”,Vol. 1, Springer-Verlag, Berlín (1966).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
63
en ambos compuestos, siendo su intensidad considerablemente menor en la fase de galio
dopado con cromo.
La primera banda observada muestra, en ambos espectros, dos pequeñas bandas muy
estrechas en la zona cercana al máximo de absorbancia, a 14800 y 15400 cm-1,
aproximadamente. Además, a números de onda mayores que 33000 cm-1 aparece una zona
de alta absorción asignable a transiciones de transferencia de carga entre los ligandos y el
catión Cr3+.
Según el diagrama de niveles de energía (Fig. I.17) correspondiente a un sistema con
configuración d3 en un entorno octaédrico, las bandas características se ajustan a un valor
de Dq/B de 2.1, aproximadamente. Tanto el estado 4T2g(4F) como los estados 2Eg(2G) y
2
T1g(2G) poseen, aproximadamente, la misma energía para este valor de Dq/B. Por lo tanto,
la estructura en bandas menores que aparecen sobre la primera banda de absorción,
corresponde a las transiciones prohibidas de espín entre el estado fundamental 4A2g(4F) y
los dos estados doblete 2Eg(2G) y 2T1g(2G).
3
Fig. I.17 – Diagrama de energías33 para un ion con configuración electrónica d en un entorno
octaédrico.
El diagrama de energías muestra que, además de las dos transiciones permitidas de
espín observadas, tiene lugar una transición permitida de espín entre el estado fundamental
y el estado excitado 4T1g(4P). La banda correspondiente a esta transición debería aparecer
aproximadamente a 35000 cm-1, en la zona donde se observan las bandas de transferencia
33 Tanabe, Y.; Sugano, S. J. Phys. Soc. Japan., 9, 753 (1954).
64
Capítulo I
de carga entre los ligandos y el metal. Probablemente, esta transición corresponda a la
inflexión observada sobre 33000 cm-1.
Como ya se ha indicado anteriormente, se procedió a registrar el espectro
luminiscente de emisión del compuesto de cromo (Fig. I.16). La medida se realizó a la
temperatura del He líquido, empleando una longitud de onda de excitación de 22200 cm-1
(coincidente con la transición desde el estado fundamental al estado excitado 4T1g(4F), ver
Figura I.19). El espectro de emisión muestra parte de una banda. Las características del
equipo empleado han impedido llevar a cabo la toma de datos por debajo de 12500 cm-1, lo
que no ha permitido registrar la banda completa, cuyo máximo se encuentra a números de
onda menores que 12500 cm-1.
La banda observada en el espectro de emisión corresponde a la transición entre el
estado excitado 4T2g(4F) y el estado fundamental 4A2g(4F). Dicha transición también da
lugar a una absorción en el espectro de reflectancia difusa, pero a un valor de energía
notablemente mayor (15200 cm-1), según se observa en la Figura I.16. Esta diferencia,
descrita en la bibliografía34, se explica en base al principio de Frank-Condon.
Para el registro del espectro de excitación del compuesto (C2N2H10)[Cr(HPO3)F3],
también llevado a cabo a la temperatura del He líquido (Fig. I.18) se ha seleccionado una
longitud de onda (12600 cm-1) cercana al límite inferior del intervalo de medida del
espectro de emisión, dentro de la banda mostrada por el mismo.
El espectro muestra dos bandas. La primera de ellas, situada a 22000 cm-1, coincide
aproximadamente con la segunda observada en el espectro de reflectancia difusa. La
segunda aparece a 33500 cm-1 Dichas bandas corresponden a las transiciones entre el
estado fundamental y los estados excitados 4T1g(4F) y 4T1g(4P), en buen acuerdo con el
diagrama de niveles de energía para la misma relación Dq/B de 2.1 empleada en la
asignación de máximos del espectro de reflectancia difusa.
34 Lever, A. B. P. “Inorganic Electronic Spectroscopy”, Elsevier Science Publishers B. V., Amsterdam,
Nederlands (1984).
65
Intensidad (u. a.)
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
20000
25000
30000
35000
ν (cm )
-1
Fig. I.18 – Espectro de excitación de la fase (C2N2H10)[Cr(HPO3)F3].
El ajuste de los espectros de reflectancia difusa y de excitación ha permitido
determinar el valor del parámetro de desdoblamiento del campo cristalino Dq y los
parámetros de Racah B y C. Para el cálculo de los números de onda de las transiciones
observadas se han empleado las Ecuaciones [I.9]-[I.13].
4
T2g(4F) ← 4A2g(4F);
υ 1 = 10Dq
2
Eg(2G) ← 4A2g(4F);
υ 2 = 9 B + 3C −
50 B 2
10 Dq
[I.10]
2
T1g( G) ← A2g( F);
24 B 2
υ 3 = 9 B + 3C −
10 Dq
[I.11]
4
T1g(4F) ← 4A2g(4F);
υ 4 = 15Dq + 7.5 B − 0.5 225B 2 + 100 Dq 2 − 180 DqB
[I.12]
4
T1g(4P) ← 4A2g(4F);
υ 5 = 15Dq + 7.5B + 0.5 225B 2 + 100 Dq 2 − 180 DqB
[I.13]
2
4
4
[I.9]
Estas expresiones se han obtenido por diferencia entre las ecuaciones de los niveles35
fundamental y excitados correspondientes a las bandas asignadas. Se ha utilizado el mismo
conjunto de parámetros en los espectros de excitación y reflectancia difusa del compuesto
(C2N2H10)[Cr(HPO3)F3], lo que ha permitido utilizar en el ajuste las cinco bandas que se
pueden identificar claramente en alguno de los dos espectros. En el caso del compuesto de
35 Lever, A. B. P. “Inorganic Electronic Spectroscopy”, Elsevier Science Publishers B. V., Amsterdam,
Nederlands (1984).
66
Capítulo I
Ga dopado con cromo, se ha partido de los parámetros obtenidos en el ajuste de los
espectros del compuesto de cromo.
Absorbancia (u. a.)
a
M = Cr
2
2
2g
4
4
2
4
4
E , T ( G)<- A ( F)
4
1g
2g
Intensidad (u. a.)
Para la fase homometálica de cromo el mejor ajuste (Fig. I.19) se obtiene para un
valor del parámetro de desdoblamiento del campo cristalino de Dq = 1380 cm-1, y de los
parámetros de Racah B = 780 cm-1 y C = 3410 cm-1.
4
20000
T ( F)<- A ( F)
2g
25000
4
4
4
30000
ν (cm )
2g
-1
35000
4
T ( F)<- A ( F)
1g
2g
2-
3+
π(O )->e (Cr )
g
4
4
1g
12000
16000
20000
24000
28000
4
4
T ( P)<- A ( F)
32000
2g
36000
ν (cm )
-1
4
b
M = Ga: 2.3% Cr
4
Absorbancia (u. a.)
1g
2
2
2
4
4
4
T ( P)<- A ( F)
2g
4
E , T ( G)<- A ( F)
2g
1g
2g
2-
3+
π(O )->e (Cr )
g
4
4
4
4
T ( F)<- A ( F)
2g
2g
4
4
1g
12000
16000
4
4
T ( F)<- A ( F)
20000
2g
24000
28000
32000
36000
ν (cm )
-1
Fig. I.19 – Mejores ajustes obtenidos de los espectros de reflectancia difusa de los compuestos
(C2N2H10)[Cr(HPO3)F3] (a) y (C2N2H10)[Cr(HPO3)F3]:2.3% Cr (b). El mejor ajuste para el
espectro de excitación del compuesto de Cr se muestra en un inserto en (a).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
67
El espectro del compuesto de galio dopado con cromo se simula satisfactoriamente
sin realizar cambios significativos en los valores de los parámetros. Dichos valores se
encuentran dentro del intervalo habitual para compuestos de Cr3+ en un entorno
octaédrico36,37.
El valor del parámetro B de Racah constituye un 76 % del correspondiente al ion
(1030 cm-1), lo cual indica un cierto carácter de covalencia en los enlaces Cr-O y
Cr-F de los compuestos.
libre38
En los ajustes de los espectros de reflectancia difusa se han introducido dos bandas
adicionales, que dan cuenta de la transferencia de carga ligando-metal. Estas bandas se
encuentran solapadas con las de las transiciones d-d del catión metálico. Su posición final
tras el ajuste (39600 cm-1 y 48300 cm-1 para el compuesto de Cr; 39800 y 48000 cm-1 para
el compuesto de galio dopado con Cr) está en acuerdo razonable con la energía esperada
para las primeras transiciones π(O2-)→eg(Cr3+) (41800 cm-1) y π(O2-)→t2g(Cr3+) (49500
cm-1), según el tratamiento de Jørgensen39.
Compuesto (C2N2H10)[Fe(HPO3)F3].
La Figura I.20 muestra el espectro de reflectancia difusa de la fase
(C2N2H10)[Fe(HPO3)F3]. Está compuesto de varias bandas muy débiles situadas en la zona
de números de onda menores que 30000 cm-1. En la zona de mayores energías tiene lugar
un aumento del fondo del espectro, debido a las transferencias de carga entre los ligandos y
el catión metálico.
Los máximos situados a 14000 cm-1, 19400 cm-1, 24800 cm-1 y 27600 cm-1 son
asignables a transiciones típicas de un sistema con configuración electrónica d5 en un
entorno octaédrico de alto espín. Tales bandas son responsables del color violeta pálido
que presenta el compuesto y tienen su origen en las transiciones electrónicas prohibidas de
espín desde el estado fundamental 6A1g(6S) hasta los estados excitados 4T1g(4G), 4T2g(4G),
4
T2g(4D) y 4Eg(4D), respectivamente. En la zona de 22500 cm-1 puede apreciarse un fondo
más elevado en el espectro, que corresponde a la transición a los estados excitados 4A1g y
36 Weber, M. J.; Brawer, S. A.; Degroot A. J. Phys. Rev. B., 23, 11 (1981).
37 Cuadrado, M.C.; Alamo, J. Mat Res. Bull., 24, 7 (1989).
38 Griffith, J. S. “The Theory of Transition-Metal Ions”, Cambridge University Press, Londres (1964).
39 Jørgensen, C. K. en: Jørgensen, C. K.; Neilands, J. B.; Nyholm, R. S.; Reinen, D.; Williams, R. J. P. (eds.)
“Structure and Bonding”, Vol. 1, Springer-Verlag, Berlín (1966).
68
Capítulo I
4
Eg(4G). La asignación ha sido realizada de acuerdo con el diagrama de niveles de
energía40,41 de un sistema con configuración d5 para un valor de Dq/B de 1.4.
Absorbancia (u. a.)
El ajuste del espectro se ha realizado empleando las Ecuaciones [I.14] a [I.18] para el
cálculo de las energías de las transiciones42.
12000
16000
20000
24000
28000
ν (cm )
-1
Fig. I.20 – Espectro de reflectancia difusa del compuesto (C2N2H10)[Fe(HPO3)F3].
T1g( G)← A1g( S);
26B 2
υ1 = −10Dq + 10B + 6C −
10Dq
[I.14]
4
T2g(4G)← 6A1g(6S);
υ 2 = −18Dq + 10B + 6C −
38B 2
10Dq
[I.15]
4
A1g,4Eg(4G) ← 6A1g(6S); υ 3 = 10B + 5C
[I.16]
4
T2g(4D) ← 6A1g(6S);
υ 4 = 13B + 5C
[I.17]
4
Eg(4D) ← 6A1g(6S);
υ 5 = 17B + 5C
[I.18]
4
4
6
6
40 Tanabe, Y.; Sugano, S. J. Phys. Soc. Japan., 9, 753 (1954).
41 Orgel, L. E. J. Chem. Phys., 23, 1004 (1955).
42 Lever, A. B. P. “Inorganic Electronic Spectroscopy”, Elsevier Science Publishers B. V., Amsterdam,
Nederlands (1984).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
69
El mejor acuerdo entre los datos experimentales y el espectro calculado (Fig. I.21)
conduce a unos valores del parámetro de desdoblamiento del campo cristalino de Dq
=1030 cm-1, y de los parámetros de Racah de B = 720 cm-1 y C = 3080 cm-1. Los valores
obtenidos para los parámetros de Racah se encuentran dentro del intervalo habitual para
compuestos de Fe(III) en un entorno octaédrico de alto espín43,44.
2-
3+
Absorbancia (u. a.)
π(O )->t (Fe )
2g
4
4
6
6
E ( D)<- A ( S)
g
4
4
6
1g
6
T ( D)<- A ( S)
2g
4
4
4
1g
6
6
A , E ( G)<- A ( S)
4
4
6
1g
6
g
1g
T ( G)<- A ( S)
1g
1g
4
4
6
6
T ( G)<- A ( S)
2g
12000
16000
1g
20000
24000
28000
ν (cm )
-1
Fig. I.21 – Mejor ajuste obtenido para el espectro de reflectancia difusa del compuesto
(C2N2H10)[Fe(HPO3)F3].
Mención especial merece el parámetro de desdoblamiento del campo cristalino Dq,
ya que el valor obtenido es sensiblemente menor que el de los compuestos citados en la
bibliografía. Este hecho puede ser debido a que dichos compuestos son óxidos mixtos. El
ion óxido está situado en una posición más avanzada en la serie espectroquímica de los
ligandos45 que los oxoaniones CrO42- y IO32- y el anión F-. A pesar de que los oxoaniones
del fósforo no están presentes en dicha serie, los resultados obtenidos parecen indicar que
el campo cristalino creado por los iones fluoruro y fosfito es menor que el creado por el ion
óxido.
No existen en la bibliografía muchos estudios realizados sobre las propiedades
ópticas de compuestos de Fe3+ en un entorno octaédrico de alto espín, lo cual impide la
43 Lenglet, M.; Hochu, F.; Music, S. Solid State Commun., 94, 211 (1995).
44 Sherman, D. M.; Waite, T. D. Am. Mineral., 70, 1262 (1985).
45 Jørgensen, C. K. en: Jørgensen, C. K.; Neilands, J. B.; Nyholm, R. S.; Reinen, D.; Williams, R. J. P. (eds.)
“Structure and Bonding”,Vol. 1, Springer-Verlag, Berlín (1966).
70
Capítulo I
comparación con los resultados obtenidos por otros autores. Esta ausencia de datos
bibliográficos probablemente se deba a la dificultad de obtener espectros de este catión.
Este hecho tiene su origen en las siguientes características del ion Fe3+:
i.
Todas las transiciones posibles entre su nivel fundamental y los niveles
excitados en un campo octaédrico débil son prohibidas de espín y dan lugar a
bandas muy débiles.
ii.
El carácter moderadamente oxidante del ion Fe3+ trae como consecuencia
que las bandas de transferencia de carga ligando-metal aparecen a energías
relativamente bajas, enmascarando muchas de las bandas originadas por las
transiciones entre los orbitales d.
Uno de los pocos estudios46 que incluyen espectros de reflectancia difusa de fosfatos
de Fe(III) (anión químicamente semejante al fosfito) muestra que las posiciones de las tres
primeras bandas del espectro son muy cercanas a las encontradas en el presente trabajo.
Sin embargo, el estudio citado no incluye el cálculo de los parámetros de desdoblamiento
del campo cristalino y de Racah, por lo que no pueden realizarse las comparaciones
oportunas.
El valor obtenido para el parámetro de Racah B constituye un 63% del
correspondiente al ion libre47 (1144 cm-1), lo cual indica que los enlaces Fe-O y Fe-F
presentan carácter intermedio entre un enlace covalente y un enlace iónico.
Al igual que en el caso de los sistemas anteriormente descritos, se han introducido en
el ajuste dos bandas adicionales, que dan cuenta de la transferencia de carga ligando-metal.
Su posición final tras el ajuste (35700 cm-1 y 46200 cm-1) está en acuerdo razonable con la
energía esperada para las primeras transiciones48 π(O2-) → t2g(Fe3+) (37800 cm-1) y π(O2-)
→ eg(Fe3+) (49800 cm-1) según el tratamiento de Jørgensen.
Estudio Comparativo
46 Losilla, E. R.; Bruque, S.; Aranda, M. A.G.; Moreno-Real, L.; Morin, E.; Quarton, M. Solid State Ionics,
112, 53 (1998).
47 Griffith, J. S. “The Theory of Transition-Metal Ions”, Cambridge University Press, Londres (1964).
48 Jørgensen, C. K. en: Jørgensen, C. K.; Neilands, J. B.; Nyholm, R. S.; Reinen, D.; Williams, R. J. P. (eds.)
“Structure and Bonding”,Vol. 1, Springer-Verlag, Berlín (1966).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
71
Dado que los cromóforos presentes en todos los compuestos poseen el mismo
entorno de ligandos, se pueden establecer comparaciones entre los valores obtenidos para
los diferentes compuestos. En la Tabla I.6 se presenta un resumen de los resultados del
estudio por espectroscopía ultravioleta-visible de las fases (C2N2H10)[M(HPO3)F3] (M = V,
Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr).
Los parámetros de desdoblamiento del campo cristalino se ordenan según la serie
espectroquímica de los cationes48: V(III)>Cr(III)>Fe(III).
Los parámetros de Racah y la energía de la primera banda de transferencia de carga
entre los ligandos y el catión metálico siguen el orden: Cr(III)>Fe(III)>V(III). Por otra
parte, el porcentaje de reducción del parámetro B respecto al correspondiente al ion libre es
mayor para el ion Cr(III) que para el Fe(III), en buen acuerdo con la posición relativa de
los mismos en la serie nefelauxética. El catión V(III) no aparece en dicha serie en las
fuentes bibliográficas consultadas48.
Tabla I.6 – Posiciones de las bandas tras los ajustes, asignaciones y parámetros de desdoblamiento
del campo cristalino y de Racah obtenidos en los estudios por espectroscopía ultravioletavisible de los compuestos (C2N2H10)[M(HPO3)F3] (M = V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr).
Cromóforo
octaedro [VO3F3]
octaedro [CrO3F3]
octaedro [FeO3F3]
Conf. elec.
d2
d3
d5
3
E. fund.
M
T1g(3F)
V
4
V0.28 Fe0.72
A2g(4F)
Cr
6
A1g(6S)
Ga:
Fe
2.3%Cr
1
E. excitado,
ν (cm )
1
Eg, T2g ( D)
9820
4
T2g( F)
T2g( F)
14450
14290
2
3
T1g(3P)
21580
21210
2
A2g(3F)
30030
29690
4
4
3
3
9770
4
3
-1
15160
15160
4
4
T1g(4F)
Eg( G)
14640
14720
T1g(2G)
15439
15420
T1g(4F)
22120
22120
4
T2g(4D)
24760
T1g(4P)
33660
33660
4
Eg(4D)
27640
4
4
14070
2
T2g( F)
19230
A1g,4Eg(4G)
22600
→t2g(V3+)
26000
25800
→eg(Cr3+)
39600
39800
→t2g(Fe3+)
35700
→eg(V3+)
49900
45100
→t2g(Cr3+)
48300
48000
→eg(Fe3+)
46200
Dq
1560
1540
1375
1375
1030
B
550
535
780
780
720
C
3060
3140
3410
3420
3080
64
62
76
76
63
L-M: π(O2-)
Par.
1
B/B(ion libre)
I.5 PROPIEDADES MAGNÉTICAS
72
Capítulo I
I.5.1 ESPECTROSCOPÍA DE RESONANCIA DE ESPÍN ELECTRÓNICO
Los espectros de resonancia de espín electrónico (RSE) en banda X de los
compuestos (C2N2H10)[M(HPO3)F3] (M = Cr, Fe) fueron medidos a diversas temperaturas,
en el intervalo comprendido entre 5 K y 290 K. También se midieron los espectros RSE
del compuesto de galio dopado con cromo en banda X y en banda Q a temperatura
ambiente.
Compuesto (C2N2H10)[Cr(HPO3)F3].
Los espectros RSE de la fase de cromo muestran una señal isotrópica centrada a un
valor de campo magnético de, aproximadamente, 3400 G, típico de un entorno octaédrico
poco distorsionado para el ion Cr3+. La señal observada apenas se modifica al descender la
temperatura desde 290 K hasta 20 K. Por debajo de 20 K la señal se ensancha ligeramente
y aumenta su intensidad (Fig. I.22).
dX''/dH
290 K
20 K
9K
4K
2800
3000
3200
3400
3600
3800
4000
H(G)
Fig. I.22 – Espectros RSE del compuesto (C2N2H10)[Cr(HPO3)F3] en banda X a 4K, 9K, 20K y
290K.
Se ha realizado un ajuste de los espectros, simulados con la derivada de una curva
lorentziana. De esta manera se pudo deducir el factor giromagnético g, la anchura de línea
y la intensidad integrada de cada espectro. El valor obtenido para g es de 1.975, constante
con la temperatura. Dicho valor se encuentra dentro del intervalo habitual (1.91-2.01) para
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
73
un ion Cr3+49. La Figura I.23 muestra la evolución de la intensidad y la anchura de línea
con la temperatura.
La intensidad de la señal aumenta al disminuir la temperatura, de forma más acusada
por debajo de 100 K. A temperaturas inferiores a 6 K vuelve a disminuir la pendiente. La
anchura de línea disminuye ligeramente hasta alcanzar un mínimo a 100 K. Por debajo de
esta temperatura la tendencia se invierte, aumentando notablemente la anchura de línea a
temperaturas inferiores a 20 K.
La disminución de la anchura de línea al descender la temperatura desde 290 K hasta
100 K se debe, normalmente, al aumento del tiempo de relajación espín-red. El incremento
posterior de la anchura, observado por debajo de 100 K, indica la existencia de una fuerte
correlación de espín. Estas características ponen de manifiesto la existencia de
interacciones antiferromagnéticas débiles en el compuesto.
220
Intensidad (u. a.)
Anchura de línea (G)
240
200
180
160
140
0
50
100
150
200
250
300
T(K)
Fig. I.23 – Evolución térmica de la intensidad y la anchura de línea de los espectros RSE del
compuesto (C2N2H10)[Cr(HPO3)F3] en banda X.
49 Carlin, R. L. “Magnetochemistry.”, Springer-Verlag, Berlin Heidelberg (1986).
74
Capítulo I
Compuesto (C2N2H10)[Fe(HPO3)F3].
Los espectros RSE de esta fase (Fig. I.24) presentan una señal ancha, isotrópica y
centrada a un valor de campo magnético de, aproximadamente, 3370 G. Al disminuir la
temperatura desde 290 K hasta 50 K, se aprecia un aumento de la intensidad de la señal sin
cambio de su anchura. Por debajo de 50 K, la señal se ensancha progresivamente, siendo
difícil de detectar a 4 K.
Tras el ajuste de los espectros el valor obtenido para g es de 2.004, habitual para el
ion Fe3+ de alto espín50. Dicho valor no varía, significativamente, con la temperatura. La
intensidad de la señal aumenta al disminuir la temperatura (Fig. I.25), con un máximo
situado a, aproximadamente, 14 K. A temperaturas inferiores vuelve a disminuir la
intensidad. Por otra parte, la anchura de línea disminuye ligeramente con un mínimo a 50
K. A más bajas temperaturas se produce un incremento tan acusado que la señal se vuelve
prácticamente indetectable a 4 K. Este hecho indica que existe una fuerte correlación de
espín, al igual que en el caso del compuesto de Cr.
La existencia de un máximo en la evolución térmica de la intensidad de la señal pone
de manifiesto el establecimiento de un orden antiferromagnético de largo alcance por
debajo de, aproximadamente, 14 K.
dX''/dH
290 K
50 K
15 K
4K
2800
3000
3200
3400
3600
3800
4000
H(G)
Fig. I.24 – Espectros RSE del compuesto (C2N2H10)[Fe(HPO3)F3] en banda X a 4K, 15K, 50K y
290K.
50 Carlin, R. L. “Magnetochemistry.”, Springer-Verlag, Berlin Heidelberg (1986).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
75
Intensidad (u. a.)
500
400
0
300
5
10
15
20
25
30
35
Intensidad (u. a.)
Anchura de línea (G)
600
40
T(K)
200
100
0
50
100
150
200
250
300
T(K)
Fig. I.25 – Evolución térmica de la intensidad y la anchura de línea de los espectros RSE del
compuesto (C2N2H10)[Fe(HPO3)F3] en banda X. En un inserto se muestra en detalle la
evolución de la intensidad de la señal a temperaturas menores que 40 K.
A modo de resumen se indicará que los espectros de RSE de las fases homometálicas
de cromo y de hierro revelan que en ambas fases predominan las interacciones
antiferromagnéticas, estando la fase de hierro magnéticamente ordenada por debajo de 14
K.
Compuesto (C2N2H10)[Ga(HPO3)F3]: 2.3%Cr.
Los espectros de RSE en banda X y en banda Q del compuesto de galio dopado con
cromo se muestran en la Figura I.26. En ambos se observan varias señales, la mayoría de
ellas relacionadas con el desdoblamiento a campo nulo del ion Cr3+. La dilución de los
iones Cr3+ que presenta esta fase impide el ensanchamiento de la señal causado por
acoplamientos entre los momentos magnéticos, como ocurría en el espectro RSE del
compuesto de cromo, en el que solamente se observaba una señal ancha.
En efecto, el estado fundamental del ion Cr3+ en un entorno octaédrico corresponde
al nivel 4A2g(4F), con S=3/2. En un entorno axial, se rompe la degeneración entre los
niveles correspondientes a los diferentes valores de MS, siendo los de menor energía el
doblete de Kramers MS= ±1/2, y teniendo mayor energía el resto (MS= ±3/2). La diferencia
de energías viene determinada por el parámetro D. Si el entorno presenta distorsión
rómbica, el desdoblamiento también muestra dependencia de otro parámetro (E), cuyo
valor está comprendido entre 0 y 1 D. Los espectros RSE del ion Cr3+ pueden ser descritos
3
en términos del Hamiltoniano de Espín (Ecuación [I.19]) para S=3/2.
76
[
Capítulo I
]
Η = g // µ B H zSz + g ⊥µ B (H x Sx + H yS y + D S2z − 13 S(S + 1) + E(S 2x − S2y )
[I.19]
a
H
dX''/dH
H
H ,H
z1
∆M =2
y1
z2
x1
s
H
H ,H
z3
y2
y3
β
0
1000
2000
3000
4000
5000
6000
H(G)
H
b
dX''/dH
H
H ,H
z1
y1
z2
x1
H ,H
z3
H
y3
y2
β
10000
11000
12000
13000
14000
15000
H(G)
Fig. I.26 - Espectros RSE del compuesto (C2N2H10)[Ga(HPO3)F3]: 2.3%Cr en banda X (a) y en
banda Q (b) a temperatura ambiente. Se ha indicado la asignación de las señales
observadas.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
77
El desdoblamiento a campo nulo determina la aparición de señales en el espectro
RSE a tres campos magnéticos H1, H2 y H3 (Fig. I.27). Con frecuencia se observa alguna
señal prohibida originada por transiciones con ∆MS=2, a menor campo magnético.
MS+3/2
E
∆ M S =2
4 A ( 4F)
2g
MS ±3/2
MS ±1/2
2D
MS+1/2
hν
hν
MS-1/2
hν
MS -3/2
H=0
H1
H2
H3
H
Fig. I.27 - Desdoblamiento a campo nulo, y en presencia de un campo magnético H en la dirección
3+
del eje z, de los niveles energéticos de espín del estado fundamental del ion Cr en un
entorno axial. Se han indicado las tres señales H1, H2 y H3 que se observan en los
espectros RSE debidas a transiciones permitidas (∆MS=1) y alguna señal debida a
transiciones prohibidas (∆MS=2).
Los espectros RSE sobre muestra policristalina constituyen la envolvente de los
espectros con todas las orientaciones, lo que determina la aparición de hasta 12 señales,
correspondientes a las orientaciones según los ejes x, y, z y algunas orientaciones
intermedias (βx, βy, βz). Algunas de estas señales (Hz2, βx y βy) no se suelen observar.
En el caso de los espectros RSE del compuesto (C2N2H10)[Ga(HPO3)F3]: 2.3%Cr se
observa una pequeña señal en el espectro en banda X a un campo magnético de 950 G
correspondiente a una transición prohibida con ∆MS=2, no observada en el espectro en
banda Q. El resto de señales, a mayor campo magnético, corresponden a las transiciones
permitidas, con ∆MS=1, y aparecen en ambos espectros, aunque en banda X se observan
mejor.
El hecho de que se observen menos señales que las habituales concuerda con un
valor de E = 1 D el cual determina la coincidencia de las señales Hx1 con Hz1, y Hy3 con
3
Hz3. Estos dos grupos de señales aparecen muy separados del centro del espectro, a 1800 y
5000 G, respectivamente, en el espectro en banda X. La separación de las señales Hz1 y Hz3
78
Capítulo I
sólo depende del parámetro D y permite calcular su valor D = 734·10-4 cm-1, que se
encuentra dentro del intervalo habitual51 (0-4000 ·10-4 cm-1) para el Cr3+ en un entorno
octaédrico distorsionado. El punto intermedio entre estas dos señales corresponde al valor
de gz = 1.957, menor que el g promedio hallado para el compuesto de Cr (1.975). Este
hecho indica que gx y gy deberán tener un valor comprendido entre 1.975 y 2.000.
El resto de señales aparecen en la zona central del espectro, entre 3100 y 4000 G en
el espectro en banda X, como se puede observar en la Figura I.26.
I.5.2 MEDIDAS DE SUSCEPTIBILIDAD MAGNÉTICA
La
variación
térmica
de
la
susceptibilidad
magnética
de
las
fases
(C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72) se registró bajo un campo magnético H
de 1000 G, con dos tipos de enfriamientos previos: en presencia de campo magnético (field
cooling, FC) y a campo nulo (zero field cooling, ZFC).
En todos los casos, las medidas realizadas con enfriamientos bajo campo y a campo
nulo coinciden. En adelante se presentarán las curvas obtenidas en los enfriamientos a
campo nulo, registradas entre 2 K y 300 K.
La evolución térmica de la inversa de la susceptibilidad magnética (Fig. I.28) sigue
una ley de Curie-Weiss (Ecuación [I.20]) a temperaturas mayores que 100 K, para los
compuestos de V y de Fe, 10 K para el compuesto de Cr, y 20 K para el bimetálico de V y
Fe.
En todos los casos la temperatura de Weiss es negativa, lo que indica que las
interacciones predominantes en los compuestos son de carácter antiferromagnético. Dado
que la constante de Curie está relacionada con el momento magnético efectivo, empleando
la Ecuación [I.21] se ha realizado un cálculo de dicho momento magnético efectivo, así
como del factor giromagnético g.
1
1
=
(T − θ)
χ M Cm
µ ef =
3k B
Cm ;
NA
[I.20]
µ ef = gµ B S(S + 1)
51 Pedersen, E.; Toftlund, H. Inorg. Chem., 13, 1603 (1974).
[I.21]
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
79
350
M=V
3
1/χ
χ m(mol/cm )
300
250
200
M = Cr
150
M=V
100
0.28
50
Fe
0.72
M = Fe
0
0
50
100
150
200
250
300
T(K)
Fig. I.28 – Evolución térmica de la inversa de la susceptibilidad magnética de las fases
(C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72) y ajuste de las rectas correspondientes
a leyes de Curie-Weiss.
Puesto que la susceptibilidad magnética es una magnitud escalar aditiva y
macroscópica, la constante de Curie de la fase bimetálica es una media ponderada de las
contribuciones correspondientes a los iones V3+ y Fe3+(Ecuación [I.22]). Utilizando las
constantes de los compuestos homometálicos se estimó la fracción molar de V y Fe. Los
resultados obtenidos se muestran en la Tabla I.7.
C m = X Fe C m(Fe) + (1 − X Fe )C m(V)
[I.22]
Tabla I.7 – Valores obtenidos tras los ajustes a leyes de Curie-Weiss de la evolución térmica del
inverso de la susceptibilidad magnética de las fases (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe,
V0.28Fe0.72).
M
S
θ (K)
Cm (cm3K/mol)
µef (µB)
g
V
1
-5.768
1.004
2.83
2.00
Cr
3/2
-4.556
1.844
3.84
1.98
Fe
5/2
-27.99
4.381
5.92
2.00
V0.28Fe0.72
1, 5/2
-1.128
3.414
Fracción de Fe (XFe): 0.71
80
Capítulo I
Los momentos magnéticos efectivos se encuentran dentro del intervalo habitual para
el ion correspondiente52 (2.8-2.9 para el V3+, 3.7-3.9 para el Cr3+ y 5.8-6.0 para el Fe3+ de
alto espín).
El valor del factor giromagnético para todos los compuestos es próximo a 2.00, y los
de los compuestos de Cr y Fe concuerdan con los obtenidos de los espectros RSE.
Dado que la evolución térmica de la susceptibilidad magnética molar (χm) presenta
características diferenciadas en el caso del compuesto de hierro y del resto de las fases
(C2N2H10)[M(HPO3)F3] (M=V, Cr, V0.28Fe0.72), a continuación se analizarán por separado.
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, V0.28Fe0.72).
Las curvas de χm y del producto χmT se muestran en la Figura I.29. La susceptibilidad
magnética molar de estos tres compuestos aumenta al descender la temperatura, mientras
que el producto χmT disminuye.
3.5
0.2
χ T, M = Cr
χm, M = V0.28 Fe0.72
χmT, M = V0.28 Fe0.72
2.5
m
3
χ (cm /mol)
m
m
2
m
χ , M = Cr
χ T (cm K/mol)
χmT, M = V
m
0.15
3
χ ,M=V
3
0.1
1.5
1
0.05
0.5
0
0
0
50
100
150
200
250
300
T(K)
Fig. I.29 – Variación de χm y χmT para los compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, V0.28Fe0.72).
Los valores del producto χmT a temperatura ambiente son los esperados para los
iones correspondientes: 0.98, 1.81 y 3.40 cm3K/mol para las fases de V, Cr y bimetálica de
52 Carlin, R. L. “Magnetochemistry.”, Springer-Verlag, Berlin Heidelberg (1986).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
81
V-Fe, respectivamente. Estos valores concuerdan con los deducidos a partir de la constante
de Curie (ver Tabla I.7).
Los valores de χmT alcanzados a bajas temperaturas son mucho menores que los
esperados para los iones correspondientes en estado paramagnético, debido a la existencia
de acoplamientos antiferromagnéticos. La ausencia de máximos u otras características en
las curvas de susceptibilidad impide obtener información sobre la dimensionalidad de los
acoplamientos magnéticos de estas fases.
Compuesto (C2N2H10)[Fe(HPO3)F3].
La variación térmica de la susceptibilidad magnética molar se muestra en la Figura
I.30. Al igual que ocurre con el resto de fases, el producto χmT disminuye al descender la
temperatura, desde un valor de 3.99 cm3K/mol a 300 K hasta alcanzar 0.156 cm3K/mol a
2K. El valor observado a alta temperatura se encuentra cercano al de un ion Fe3+ de alto
espín (4.38 cm3K/mol), y concuerda con el valor de la constante de Curie (4.381
cm3K/mol).
0.1
4
0.08
χ (cm /mol)
m
3
3
χ (cm /mol)
m
0.5
0.06
0.04
0.055
0
10
20
30
3
1
0.065
3
m
1.5
0.07
m
2
3
χ T (cm K/mol)
0.06
2.5
0.08
0.075
χ T (cm K/mol)
3
0.085
2
0
40
T(K)
1
0.02
0
0
0
50
100
150
200
250
300
T(K)
Fig. I.30 – Evolución de la susceptibilidad magnética y del producto χmT con la temperatura para el
compuesto (C2N2H10)[Fe(HPO3)F3].
La susceptibilidad magnética muestra un máximo a 14 K. Por debajo de esta
temperatura se produce un leve descenso de la susceptibilidad, volviendo a aumentar a
temperaturas inferiores a 6 K. Como cabría esperar, la evolución térmica de la intensidad
82
Capítulo I
de la señal de RSE (Fig. I.25) reproduce con exactitud la curva de susceptibilidad
magnética, a excepción del incremento a muy bajas temperaturas.
Estos hechos indican el establecimiento de un orden antiferromagnético de largo
alcance por debajo de la temperatura del máximo, 14 K. La coincidencia entre las curvas
de susceptibilidad medidas tras enfriamiento a campo nulo y con un campo magnético de
1000 G, descarta que el incremento mostrado por la curva de susceptibilidad a
temperaturas menores que 6 K esté relacionada con fenómenos de ferromagnetismo débil o
canting. Dicho comportamiento está probablemente originado por la contribución de una
impureza paramagnética a muy baja concentración.
El análisis de la estructura cristalina del compuesto permite proponer tres caminos
posibles de canje magnético en el interior de las dobles cadenas: una longitudinal y dos
oblícuas (Fig. I.31). En la Tabla I.8 se han detallado los ángulos entre los enlaces que los
forman.
O(1)
O(3)
Fe
Fe
O(1)
O(2)
O(3)
Fe
P
P
O(2)
O(2)
P
O(2)
O(2)
P
P
Fe
O(3)
O(1)
Fe
O(3)
O(1)
(A)
(B) {
Fig. I.31 – Posibles caminos de
(C2N2H10)[Fe(HPO3)F3].
canje
magnético
entre
Fe-O(1)-P-O(3)-Fe
Fe-O(1)-P-O(2)-Fe
Fe-O(2)-P-O(3)-Fe
iones
Fe
3+
en
el
compuesto
Tabla I.8 – Ángulos entre los enlaces que forman los posibles caminos de canje y distancias Fe-Fe
para los mismos en el compuesto (C2N2H10)[Fe(HPO3)F3].
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
Camino
(a) (b)
83
Ángulo
Ángulo
Ángulo
Fe-O(a)-P O(a)-P-O(b) P-O(b)-Fe
Distancia
Fe-Fe
Fe-O(1)-P-O(3)-Fe (3) (1)
141.9º
108.6º
143.4º
6.44 Å
Fe-O(1)-P-O(2)-Fe (1) (2)
141.9º
114.7º
143.5º
4.89 Å
Fe-O(2)-P-O(3)-Fe (2) (3)
143.5º
114.3º
143.4º
4.89 Å
(A) El camino longitudinal Fe-O(1)-P-O(3)-Fe conecta a los átomos de Fe en la
dirección de la doble cadena, unidos mediante un sólo grupo fosfito. La distancia
entre los átomos de Fe a través de este camino de canje es de, aproximadamente,
6.44 Å.
(B)
Los caminos Fe-O(1)-P-O(2)-Fe y Fe-O(2)-P-O(3)-Fe son oblicuos y conectan
átomos de Fe de manera transversal dentro de la doble cadena. Cada camino de
canje corresponde a la unión a través de cada grupo fosfito, y la distancia Fe-Fe a
través de estos caminos es similar, de aproximadamente 4.89 Å.
Con el objetivo de plantear un posible modelo para el comportamiento magnético de
esta fase (Fig. I.32), se han realizado las siguientes consideraciones:
i)
Las interacciones
despreciables.
ii)
A los acoplamientos magnéticos de tipo (A) entre los iones Fe3+ en la
dirección de las cadenas (camino de canje Fe-O(1)-P-O(3)-Fe) se les ha
asignado la constante de acoplamiento J1.
iii)
Los acoplamientos magnéticos entre los iones Fe3+ de tipo (B) en dirección
transversal (caminos de canje Fe-O(1)-P-O(2)-Fe y Fe-O(2)-P-O(3)-Fe) son
comparables. Se ha asignando la constante J2 al promedio de estos dos
acoplamientos.
magnéticas
entre
dobles
cadenas
distintas
son
84
Capítulo I
J1
J2
Fig. I.32 - Acoplamientos magnéticos propuestos para el compuesto (C2N2H10)[Fe(HPO3)F3].
No se ha hallado en la bibliografía ningún modelo magnético para este sistema. Dado
que la deducción de un nuevo modelo para el mismo es complicada, situándose fuera de
los objetivos de este trabajo, se han considerado los casos simplificados en los que uno de
los acoplamientos magnéticos es mucho más fuerte que el otro, lo que da lugar a que
J1>>J2, o bien, J2>>J1. Esto conduce, en los dos casos, a asimilar el comportamiento
magnético de esta fase a sistemas de cadenas aisladas de espín S=5/2, que pueden ser
modelados mediante la ecuación de Fischer y Dingle53,54 (Ecuaciones [I.23]).
N A g 2 µ B (1 − n)
;
χ=
3k BT (1 + n)
n=
T
T
− coth
;
T0
T0
T0 =
2JS(S + 1)
kB
[I.23]
siendo kB la constante de Bolzmann, NA el número de Avogadro, µB el
magnetón de Bohr, y J la constante del acoplamiento magnético más fuerte (sea
J1 o J2).
Un sistema como éste de cadenas aisladas no permite un buen ajuste entre los datos
experimentales y el modelo teórico en la zona cercana al máximo, como se muestra en la
Figura I.33.
El empleo de la aproximación del campo molecular55 permite considerar el
acoplamiento magnético más débil, entre un espín y los dos vecinos no considerados en el
modelo inicial. A pesar de mejorar el ajuste, esta corrección no da cuenta de la tendencia
ascendente mostrada por la susceptibilidad magnética. Como ya se ha mencionado, este
incremento está probablemente causado por la presencia de una impureza paramagnética.
53 Fischer, M. E. Am. J. Phys., 32, 343 (1964).
54 Dingle, R.; Lines, M. E.; Holt, S. L., Phys. Rev., 187 (1969).
55 Carlin, R. L. “Magnetochemistry.”, Springer-Verlag, Berlin Heidelberg (1986).
Compuestos (C2N2H10)[M(HPO3)F3] (M=V, Cr, Fe, V0.28Fe0.72, Ga: 2.3%Cr)
85
0.1
4
χ (cm /mol)
3
m
1.5
0.07
1
0.065
2
0.5
0.06
0.04
3
0
40
0.055
0
10
20
30
T(K)
m
2
0.075
3
χ T (cm K/mol)
0.06
2.5
0.08
m
3
3
0.085
3
χ T (cm K/mol)
χ (cm /mol)
m
0.08
1
0.02
0
0
0
50
100
150
200
250
300
T(K)
Fig. I.33 – Ajustes de las curvas de evolución térmica de la susceptibilidad magnética y del
producto χmT para compuesto (C2N2H10)[Fe(HPO3)F3]. En las tres simulaciones
mostradas se ha empleando la ecuación de Fischer y Dingle: sin introducir (...) e
introduciendo(- - -) la aproximación del campo molecular para el resto de interacciones y
___
sumando la contribución de una impureza paramagnética ( ).
La suma al modelo anterior de un 0.76 % de impureza paramagnética con S = 5/2 ha
permitido obtener un buen ajuste entre los datos experimentales y el modelo teórico (Fig
I.31). Las constantes de acoplamiento magnético obtenidas son J = -3.81 K y J’ = -0.38 K,
empleando el valor de g = 2.004 hallado por espectroscopía RSE.
Los resultados logrados indican que, por debajo de 14 K se establece un orden
antiferromagnético monodimensional.
No obstante, se comprueba que uno de los dos acoplamientos magnéticos es
significativamente más fuerte que el otro. Las diferencias geométricas entre los caminos de
canje longitudinal (A) y oblicuos (B) (Tabla I.8) se limitan al valor del ángulo O(a)-PO(b), que es de 108.6º en el caso del canje en la dirección de las cadenas, y cercano a
114.3º para el canje en la dirección transversal. Aunque ésta es, probablemente, la causa de
las diferencias en la magnitud de las interacciones magnéticas a través de uno u otro
camino, con la información disponible actualmente no se ha logrado identificar cuál de
ellos es el que da lugar a las interacciones más fuertes.
Finalmente, hay que destacar las diferencias entre el comportamiento magnético del
compuesto de hierro frente al resto de compuestos estudiados en este capítulo, cuya curva
86
Capítulo I
de susceptibilidad magnética no muestra ningún máximo. Dado que todos ellos tienen la
misma estructura cristalina, con caminos de canje semejantes, las diferencias observadas se
pueden atribuir al menor valor de los momentos magnéticos del resto de iones, que causan
una reducción de la magnitud de las interacciones antiferromagnéticas. Por todo ello se
puede suponer que en el resto de compuestos se da el establecimiento de un ordenamiento
magnético de largo alcance a temperaturas menores que 2 K, situándose el máximo en las
curvas de susceptibilidad magnética por debajo de dicha temperatura.