protocolo nacional de terapia antiretroviral para adultos chile 1999
Anuncio

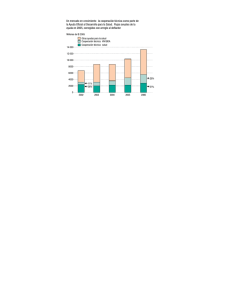
1 BOLETIN EPIDEMIOLOGICO TRIMESTRAL C O N A S I D A J U N I O D E 1 9 9 9 PRESENTACION El presente número del Boletín Epidemiológico Trimestral de CONASIDA, N° 9, incluye la información epidemiológica del VIH/SIDA, hasta Junio de 1999. Siguiendo con la incorporación de artículos de índole técnico en esta edición se ha incorporado el documento técnico “Protocolo Nacional de Terapia Antiretroviral para Adultos, Chile 1999. 2 CARACTERIZACION EPIDEMIOLOGICA DEL VIH/SIDA EN CHILE ”La sensibilidad del sistema de vigilancia pasiva de SIDA existente en nuestro país, se estimó en un 86% en 1997, por el proceso que se ha establecido de revisión de certificados de defunción iniciado en 1991 y que ha entregado resultados similares en todos los años estudiados. Gráfico 1. Como en oportunidades anteriores, es necesario aclarar que los certificados de defunción no constituyen notificación de nuevos casos por sí solos, a diferencia de otros países de la región. La revisión se hace para conocer el número de personas que fallecieron a causa del SIDA y verificar si habían sido notificados como caso de SIDA, es decir para conocer la magnitud de la subnotificación y corregir tasa de mortalidad. Además la información contenida en los certificados de defunción sirve para complementar los datos en los casos conocidos o solicitar la notificación en los casos que no habían sido declarados. La información epidemiológica mostrada en el presente boletín considera como definitivas las cifras correspondientes al año 1997, manteniéndose como preliminares las de 1998, debido a la latencia de la notificación observada en casos de SIDA. El primer caso de SIDA se notificó en 1984; hasta el 30 de Junio de 1999 se han notificado 3.150 enfermos y 3.8571 portadores asintomáticos en las trece regiones del país. Se ha informado el fallecimiento de 2.112 personas. La tasa de incidencia acumulada de SIDA en Chile alcanza a 23.5 por 100.000 habitantes, el análisis por año muestra una tendencia al aumento que se mantiene en el tiempo. El incremento de casos de SIDA en el último quinquenio fue de 20.4% promedio anual. Gráfico 2. Las tasas de incidencia acumulada por 100.000 habitantes más elevadas corresponden a: Región Metropolitana (41.3), V (31.0), II (16.3) y I (12.9). Gráfico 3. La Tabla 1 muestra los casos y tasas de incidencia en hombres y mujeres por Servicio de Salud de ocurrencia, definido como el Servicio que realizó el primer diagnóstico y notificación de cada persona. Las atenciones se concentran en los Servicios de Salud de la Región Metropolitana. Los Servicios de Salud Arauco y Araucanía Sur, no han establecido aún la atención y por ende la notificación de pacientes residentes en su área, manteniéndose estas actividades en los Servicios de origen (Concepción y Araucanía Norte respectivamente). 1 Se refiere al número de portadores notificados, y no refleja necesariamente la situación real de la infección asintomática por VIH. 3 El 90% de los casos SIDA son hombres y el 10% mujeres. Gráfico 4, Tabla 2. Sin embargo, existe un crecimiento mayor de casos de SIDA en mujeres en relación a los hombres, incluyendo todos los mecanismos de transmisión (sexual y sanguínea por drogadicción intravenosa). Esto se refleja en la proporción entre hombres y mujeres, cuya brecha se ha acortado a través del tiempo, llegando a 8.5:1 en 1997. El porcentaje de incremento promedio anual de casos de SIDA fue de 28.6% en mujeres y de 21.4% en hombres. Gráfico 5. Los principales grupos de edad afectados están entre los 20 y 49 años y concentran el 85.3% de los casos. Los menores de 20 años representan el 2.6% y los mayores de 50 el 12.1%, no existiendo diferencias significativas entre ambos sexos. Gráfico 6. Categorías de exposición: Gráfico 7. • Sexual: Es la principal categoría de exposición, declarada en un 92.8% de los casos. El mayor número de casos corresponde a transmisión homo/bisexual en hombres, que constituye el 72.3% de los casos transmitidos por vía sexual, tendencia que se mantiene en el tiempo. Los casos de SIDA declarados por transmisión heterosexual son el 27.7% entre hombres y mujeres. Gráfico 8. • Sanguínea: Alcanza a 5.6% desde el inicio de la epidemia. La detección de anticuerpos anti VIH se implementó en los bancos de sangre a partir del segundo semestre de 1987, frenando la exposición por transfusiones de sangre y otros productos hemoderivados. Sin embargo, se observa un aumento de casos en personas usuarias de drogas intravenosas, vía que hoy es la fundamental dentro de la transmisión sanguínea (76% de esta vía). Gráfico 9. • Vertical: Corresponde al 1.5% dentro del total de casos. La transmisión del VIH de la madre a su hijo alcanza a 29%, cifra acumulada desde el inicio de la epidemia. La cifra de niños que se mantienen en estudio fue de 9%, producto de una revisión de las edades de ellos. Gráfico 10. El porcentaje de transmisión vertical mencionado, corresponde a la cifra global, sin evaluación de la eficacia del Protocolo ACTG 076, cuya aplicación comenzó en nuestro país en 1996. En la actualidad se está diseñando el estudio para evaluar esta medida de prevención. Tendencia de los parámetros socioeconómicos registrados en la notificación de personas con VIH/SIDA: Para medir tendencia de estas variables se comparó la situación de 1992 con la de 1997, eligiéndose este período porque 1997 es el último año cerrado con información completa. Se consideraron en conjunto los casos de SIDA y VIH+ notificados, por el pequeño número de casos de SIDA en mujeres, que de otro modo impediría hacer cálculos de significación estadística. Escolaridad: Al analizar esta variable en mujeres de 15 a 49 años en los dos años, se observa que aumenta la declaración de escolaridad básica (de 29% a 38%), y disminuye la escolaridad media (de 63% a 52%) y superior (de 9% a 7%), sin embargo, ninguno de los cambios anteriores alcanzan significación estadísti- 4 ca. Gráfico 11. En el caso de los hombres, aunque también hay diferencias entre ambos años, estas no son estadísticamente significativas, mostrando que ellos presentan los mismos niveles de educación a través del tiempo. Gráfico 12. Ocupación: El análisis de esta variable es concordante con lo observado en el análisis de la escolaridad en ambos sexos. En mujeres, las categorías de oficinistas y operarias disminuye y aumenta la cantidad de mujeres que declaran ser dueñas de casa, todas diferencias sin significación estadística. Gráfico 13. En hombres se observan diferencias significativas en la ocupación de tipo profesional que disminuye de 17% a 12% (p= 0.06) y la de operario que aumenta entre los dos años analizados de 49% a 56% (p= 0.04). Gráfico 14. Enfermedades marcadoras en casos de SIDA: Se analizaron las enfermedades definidas como marcadoras, según definición de caso CDC 1987 y año de diagnóstico de SIDA, considerando los años 1992 y 1997. Se evaluó la tendencia de estas patologías, observando la importancia relativa que tuvo cada una de ellas en esos años. Las patologías más frecuentes en el año 1992 eran: neumonia por pneumocystis carinii y sindrome de emaciación, cuyo orden en importancia se invierte en 1997, pero manteniéndose ambas en los primeros lugares como patología marcadora de SIDA. En el quinquenio estudiado disminuye, además de la neumonia por pneumocystis carinii, la tuberculosis extrapulmonar, candidiasis esofágica, sarcoma de Kaposi, criptococosis y toxoplasmosis cerebral, aumentando el sindrome de emaciación y demás patologías. Tabla 3. El grupo denominado demás patologías se refiere a enfermedades poco frecuentes que incluye: criptosporidiasis, encefalopatía por VIH, leucoencefalopatía multifocal progresiva, linfoma no Hodking, neumonia intersticial linfoide, infección por citomegalovirus, demencia por VIH, entre otras, pero que sumadas todas ellas alcanzan un aumento importante en el período. Mortalidad: Se analizó la mortalidad por SIDA en hombres de 15 a 49 años, por ser este grupo poblacional el más afectado por la epidemia. Se observa una tendencia al crecimiento sostenido a lo largo de los años, que experimenta un notorio aumento en 1997, probablemente debido al tratamiento antiretroviral. El AZT comienza a usarse en 1992 como monoterapia y tiene un impacto en el mediano plazo que se agota, lo que se evidencia durante 1997. La biterapia se inicia en 1997, y su efecto se reflejará en los próximos años. Gráfico 15. Debido a que las personas afectadas son jóvenes, su muerte impacta fuertemente en el indicador Años de Vida Potenciales Perdidos (AVPP), que son los años que la persona perdió de vivir debido a muerte prematura, el cual muestra una tendencia al aumento que se mantiene en el tiempo, pasando de 3.382 AVPP a 11.019 en el último quinquenio con información completa. Gráfico 16. Se realizó el análisis de las diez primeras causas de muerte ocurridas en 1997 en Chile en ambos sexos de personas fallecidas entre 20 y 44 años de edad. En los hombres el SIDA ocupa el 5to. lugar, con una tasa de 0.94 por 10.000 (en 1996 se situaba en el 6to. lugar), demostrando el impacto de esta patología. Las causas que lo anteceden son exclu- 5 sivamente de tipo accidentales y entre las diez primeras causas es la única de tipo transmisible. Tabla 4. En el caso de las mujeres, el SIDA se ubica en el onceavo lugar (tasa de 0,13 por 10.000), antecedido por causas neoplásicas y accidentales. Tabla 5. Corrección de la tasa de mortalidad: El proceso de revisión de los certificados de defunción ha permitido conocer el número de casos VIH/ SIDA que no fueron notificados y que fallecieron por causas asociadas a la infección y así corregir la tasa de mortalidad. Gráfico 17. La diferencia entre ambas curvas es mí- nima y demuestra que la subnotificación en casos de SIDA e infección VIH es baja, estando frente a un sistema de alta sensibilidad que alcanzó a 86% en 1997, de acuerdo a revisión de certificados de defunción. Letalidad: Se refiere al porcentaje de casos fallecidos del total de enfermos vivos durante ese año. En los primeros años de la enfermedad este indicador era muy alto, mostrando una cierta estabilidad entre 1991 y 1996 en aproximadamente 30%, en 1997 experimenta un aumento que puede deberse a la razón explicada previamente para el aumento en la mortalidad. Gráfico 18. EN RESUMEN, EL VIH/SIDA SE DEFINE EN CHILE COMO: Tipología incipiente. Se caracteriza como: Predomina en hombres homo/bisexuales Localización urbana. No hay marginalización. Pauperización en las mujeres Tendencia a la feminización. 6 7 8 9 10 11 12 13 14 15 16 17 18 PROTOCOLO NACIONAL DE TERAPIA ANTIRETROVIRAL PARA ADULTOS CHILE 1999 La Comisión Nacional del SIDA del Ministerio de Salud, invitó a trabajar a médicos especialistas en atención de PVVIH, con el objeto de elaborar participativamente el Protocolo Nacional de Tratamiento Antiretroviral. Además de ello se ha elaborado un programa de trabajo que busca acompañar y evaluar desde el nivel central la aplicación del protocolo y su impacto en las personas que viven con VIH/SIDA. Este protocolo se ha enviado a la Coordinadora de Quienes Viven y Trabajan con VIH/SIDA -Vivo Positivo- para su conocimiento y revisión. La definición de una política nacional de terapia antiretroviral (TARV) tiene, sin dudas, un gran impacto en la Salud Pública Nacional y en la evolución del SIDA en el país, mejorando la calidad de vida de las personas que viven con VIH/SIDA, la sobrevida, y calidad de atención. Independiente de ello, el énfasis en la prevención debe mantenerse con la misma o mayor intensidad, por cuanto la existencia de tratamientos efectivos contra el VIH podría crear una falsa seguridad en la disminución de la transmisión del VIH y desfavorecer así la adhesión a los programas de prevención. En Chile, las recomendaciones se han basado en nuestra realidad nacional, buscando la mayor eficiencia Existe en la actualidad 3 familias de antiretrovirales. En Chile los fármacos que están disponibles son: 1. INHIBIDORES NUCLEOSIDOS DE LA TRANSCRIPTASA REVERSA ( NRTI) Zidovudina: (AZT); Lamivudina (3TC); Didanosina (ddI); Stavudina ( d4T); Zalcitabina (ddC); Abacavir (ABC) 2. INHIBIDORES NO NUCLEOSIDO DE LA TRANSCRIPTASA REVERSA (NNRTI): Nevirapina (NVP); Delavirdina (DLV); Efavirenz (EFV); 3. INHIBIDORES DE PROTEASA (PI) : Saquinavir (SQV); Ritonavir (RTV); Indinavir (IDV); Nelfinavir (NFV); Amprenavir Cada una de las drogas indicadas tiene características farmacológicas propias que determinan ciertas formas de administración en relación a las comidas e intervalos de dosis, reacciones adversas e interacciones farmacológicas que pueden llegar incluso a ser fatales, por lo que su uso debe ser reservado a médicos familiarizados con su manejo. En general, el uso de TARV de alta potencia involucra la ingesta diaria de un número alto de tabletas u otras formulaciones farmacéuticas y tiene un impacto significativo en la calidad de vida de las personas que las ingieran. 19 Las recomendaciones para el uso de esquemas de TARV deben basarse en su potencia, en las reacciones adversas e interacciones medicamentosas, en su impacto en la calidad de vida y la adherencia al tratamiento y deben considerar el uso previo de drogas y la evolución de los patrones locales de resistencia. Las triterapias son, en la actualidad, consideradas el mejor esquema de TARV. Se han utilizado distintos esquemas siendo los más ampliamente probados los que incluyen 2 NRTI y un PI El conocimiento actual de los mecanismos de resistencia viral ha permitido ciertas recomendaciones generales como: • Intentar siempre el mayor grado de supresión de la carga viral. • Evitar drogas que generan resistencia de alto nivel con una sola mutación, en esquemas de TARV débiles. • Frente a fracasos clínicos, efectuar cambios completos de TARV para evitar monoterapia secuencial. En los cambios de terapia, evitar en lo posible el uso secuencial de drogas con resistencia cruzada y, de preferencia, iniciar con drogas cuya resistencia no induzca resistencia cruzada a otras de la misma familia. Ej: Nelfinavir (NFV). La falta de adherencia es responsable del 50% de falla de tratamiento. El uso de fármacos en dosis subóptima, o de forma irregular acelera el proceso de aparición de cepas resistentes; por ese motivo antes de concluir que se debe a falla terapéutica por resistencia viral y de cambiar esquemas terapéuticos es importante verificar que la persona está realmente haciendo uso de los medicamentos en las dosis adecuadas. Problemas de adhesión motivados por aspectos relacionados con hábitos de vida, toxicidad y/o interacciones medicamentosas pueden estar interfiriendo en mantención de niveles adecuados antiretrovirales en sangre u otros compartimentos corporales. En caso que algunos de esos problemas sea identificado, se sugiere corregirlos y después de algunas semanas realizar evaluación clínica y de laboratorio antes de modificar el esquema terapéutico. Se debe considerar las limitaciones en las opciones terapéuticas y que la decisión de cambiar un esquema terapéutico, invariablemente restringe, por lo tanto, las opciones futuras. El análisis del conocimiento científico actual y su aplicación a la realidad nacional nos permite sugerir la definición de 3 grandes grupos de pacientes de acuerdo a la categoría de progresión, la que está relacionada con etapa de la infección, recuento de linfocitos y determinación de carga viral: (Ver punto II) 1. Alta probabilidad de progresión a SIDA y/o muerte por VIH en el corto plazo(1año). Tratar con triterapia. 2. Probabilidad intermedia de progresión en el corto plazo. Tratar con Biterapia 20 3. Baja probabilidad de progresión en el corto plazo. No tratar. A las personas en riesgo intermedio de progresión, se les debe explicar claramente que están accediendo a una terapia efectiva pero limitada y que en caso de fracaso de la biterapia (no debida a falta de adherencia) y riesgo alto de progresión, tendrán acceso a la terapia completa. A aquellos pacientes que tengan posibilidad de conseguir la tercera droga, recomendarles la terapia triple convencional desde el inicio. Con frecuencia no es fácil clasificar a un paciente en alguna de estas categorías por discordancia entre la clínica y/o los recuentos linfocitarios y/ o carga viral, por influencia de patologías intercurrentes, vacunas, etc. y mala clasificación por patologías oportunistas en etapa de infección aguda. Es recomendable la existencia de 2 recuentos linfocitarios y, al menos una Carga Viral/VIH concordantes, antes de establecer el riesgo de progresión del paciente. En consideración al costo de los fármacos, la disponibilidad presupuestaria y buscando optimizar el uso de ellos es que se elaboró un Protocolo de Tratamiento Antiretroviral como una recomendación marco que debe ser aplicada de acuerdo a la historia y condiciones clínicas de cada paciente. I. CRITERIOS DE INCLUSION SOCIALES y ADMINISTRATIVOS 1. Paciente debe ser beneficiario del SNSS y controlado en un hospital o Centro de Enfermedades de Transmisión Sexual (CETS) perteneciente a algún Servicio de Salud. 2. Residencia: Los pacientes antiguos continuarán atendiéndose en el mismo servicio de salud que lo han hecho hasta ahora, sin considerar la comuna de residencia. En los pacientes nuevos se sectorizará por comuna de residencia. 3. Asistencia regular a controles médicos correspondientes. 4. Diagnóstico serológico VIH (+), confirmado por el Instituto de Salud Pública, ISP. 5. Notificación del paciente a la autoridad epidemiológica local y Comisión Nacional del SIDA usando la clasificación de CDC 1987. 21 II.- CRITERIOS DE INCLUSION TECNICOS CATEGO RIA DE PR OGRESION BAJA PR OBABILIDAD DE PROG RES ION CLINICA: • Asintomá ticos, Etapa A 1 INDICACION DE TER APIA ANTIRETROVIRAL No inicia r antire t ro viral CD4 > 5 00 CD 4/ m m3 CAR GA VIRAL: < 1 0.000 copia s/ml). Est e grupo tiene un riesgo de progresión al año inferior a 2 0% según Mellors. MANE JO CLINICO t e rapia Controles clínicos cada 4 o 6 meses. Control de li nfocitos CD4 y carga viral cada 6 meses. Tratamiento d e enfermedades intercurrentes, en e special enteroparasit osis y ETS. Vacunación antineumocóccica. Profilaxis TBC si procede. Refuer z o y e ducación conti nua en prevenció n secundariade la transmisión del VIH y a dherencia a t ratamient os En m ujeres c o n t r ol ginecológico y PAP cada 6. CD4: Recuento de Linfocitos CD4 CV/VIH: Determinación de carga viral para VIH. Desde el punto de vista clínico, la categoría de progresión se basa en la Clasificación de CDC 1993. PR OBABILIDAD INTER MED IA PR OGRESION 22 DE CV/ V H I > 10.000y < 5 0 . 000: CLINICA: A s in tomático AZT+3TC; Etapa A 2 D4T + DDI; AZT+DDI; CD4: E n t re 3 5 0y D4T+3TC 4 99mm3 Carga Viral 10 .000 a 5 0 .000 copias/ ml, Est e grupo tiene un riesgo de progresión al año de 20a 4 0% según Mellors. Subgrupo de pacientes Subgrupo. asin to mático, CD4 > TARV triasociado 3 50, pero Carga Viral >50.000 copias /m l. ) Controles clínicos cada 1 ó 2 meses Contr ol de linfocitos CD4 y Carga Viral inicial y cada 4 meses. Controles h ematológicos y bioquímicos m e n suales inicialment e Tratamiento de enfermedades intercurrentes Vacunación ant ineumocóccica. Profilaxis TBC si procede Refuerzo y educación continua en p revención secundaria de t ransmisión del VIH y adherencia a tra tamientos. En mujeres cont r ol ginecológico y PAP cada 6 meses. CD4: Recuento de Linfocitos CD4 CV/VIH: Determinación de carga viral para VIH. Desde el punto de vista clínico, la categoría de progresión se basa en la Clasificación de CDC 1993. AL T A PROBAB ILIDAD DE PROG RES ION CLINICA: Etapas A3, B1, 1 .- SIN USO PREVIO DE TARV B2, B3, C1, C2, C3 . CV/VIH >50.000:⇒ AZT+ CD4: < 3 5 0 CD4 /po r 3TC+ IDV mm3. CV/VIH < 50.000 ⇒ AZT+ 3TC+NVP CAR GA VIRAL > 50.000 copias /m l, y a veces > de 2 .-CON FRACASO DE 10.000 copias/ ml BITERAP IA PRE VIA (CV/VIH > 5.000 ) : También se c onsideran en a l to riesgo los -USO PREVIO DE AZT+3 TC pacientes en CV/VIH> 50.000 ⇒ d4T+DDI+ IDV Et apa A2 yCD 4 entre 20 0 CV/VIH< 50.000 ⇒ 3 y 349 célu las/mm d 4T+DDI+NVP -USO PREVIO DE AZT+ DDI o DDC CV> 50.000 ⇒ d4T + 3TC + IDV CV< 50.000 ⇒ d4T + 3TC + NVP Controles c línicos mensuales Control de li nfocit os CD4 y CV/VIH inicial y cada 4 meses. Controles hematológicos y bioquímicos m e n suales inicialment e Tratamiento d e enfermedades intercurrentes Profilaxis d e patologías oportunistas Refuerzo y e ducación contínua en prevención del VIH y adh erencia a t ratamient os. En mujeres c ont r ol ginecológico y PAP cada 3 meses. -USO PREVIO DE D4T– 3TC CV/VIH> 50.000 ⇒ AZT + DDI + IDV CV/VIH< 50.000 ⇒ AZT+DD I+NVP CD4: Recuento de Linfocitos CD4 CV/VIH: Determinación de carga viral para VIH. Desde el punto de vista clínico, la categoría de progresión se basa en la Clasificación de CDC 1993. 23 III.- CRITERIOS DE CAMBIO DE TERAPIAS 1. Intolerancia a los medicamentos. 2. Reacciones adversas severas a drogas (toxicidad neurológica, hematológica, pancreatitis, litiasis renal, otros) 3. Disminución de CD4 o incremento de carga viral sugerente de resistencia, en 2 controles. 4. Progresión de la enfermedad con patología oportunista de mal pronóstico IV.1. 2. 3. 4. 5. 6. CRITERIOS DE SUSPENSION O EXCLUSION DE TERAPIAS Falta de adherencia al tratamiento. Falta al cumplimiento de indicaciones. Falla reiterada a 2 o más controles, sin aviso previo o justificación. Inasistencia a retirar fármacos sin causa justificada o aviso previo. Comercialización o destinación de las drogas a otros efectos. Obtención de fármacos en mas de 1 centro asistencial u otra instancia del sector público o privado. 24 25 Documento realizado por CONASIDA Teléfono: 6300673 Mac-Iver 541