MEDICIÓN DE POTENCIAL HÍDRICO EN PAPA Uno de los
Anuncio
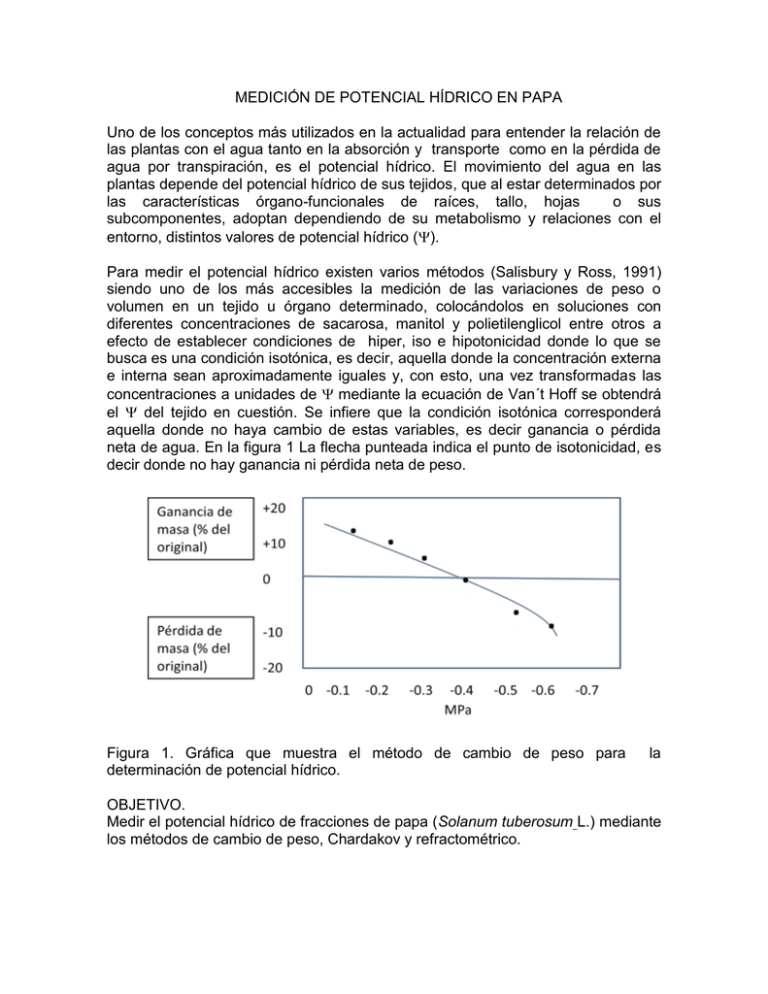
MEDICIÓN DE POTENCIAL HÍDRICO EN PAPA Uno de los conceptos más utilizados en la actualidad para entender la relación de las plantas con el agua tanto en la absorción y transporte como en la pérdida de agua por transpiración, es el potencial hídrico. El movimiento del agua en las plantas depende del potencial hídrico de sus tejidos, que al estar determinados por las características órgano-funcionales de raíces, tallo, hojas o sus subcomponentes, adoptan dependiendo de su metabolismo y relaciones con el entorno, distintos valores de potencial hídrico (). Para medir el potencial hídrico existen varios métodos (Salisbury y Ross, 1991) siendo uno de los más accesibles la medición de las variaciones de peso o volumen en un tejido u órgano determinado, colocándolos en soluciones con diferentes concentraciones de sacarosa, manitol y polietilenglicol entre otros a efecto de establecer condiciones de hiper, iso e hipotonicidad donde lo que se busca es una condición isotónica, es decir, aquella donde la concentración externa e interna sean aproximadamente iguales y, con esto, una vez transformadas las concentraciones a unidades de mediante la ecuación de Van´t Hoff se obtendrá el del tejido en cuestión. Se infiere que la condición isotónica corresponderá aquella donde no haya cambio de estas variables, es decir ganancia o pérdida neta de agua. En la figura 1 La flecha punteada indica el punto de isotonicidad, es decir donde no hay ganancia ni pérdida neta de peso. Figura 1. Gráfica que muestra el método de cambio de peso para determinación de potencial hídrico. la OBJETIVO. Medir el potencial hídrico de fracciones de papa (Solanum tuberosum L.) mediante los métodos de cambio de peso, Chardakov y refractométrico. MATERIAL 7 frascos gerber, 21 tubos de ensayo de 25 ml, gradilla, pipeta Pasteur, pipeta de 10 ml, balanza (precisión de 0.01g), refractómetro para azúcares en grados Brix, navaja, 2 servitoallas, 50 mL de cada una de las soluciones de sacarosa siguientes 0.0, 0.10, 0.20, 0.30, 0.40, 0.50, 0.60 molal, piseta con agua destilada, cutter o sacabocados con un diámetro de 1 cm de luz interior y dos papas grandes. MÉTODO Vierta en tubos de ensayo las cantidades indicadas en la tabla 1 de cada solución. A la denominada tercera serie de cada uno de las concentraciones, adicione una gota de rojo neutro. Soluciones de sacarosa (m) Primera serie Segunda serie Tercera serie Con 1 fracción de Con 1 fracción de sin fracción de papa por tubo de papa por tubo de papa (mL). ensayo donde ensayo donde permanecerá 1.5 permanecerá 1.5 horas en cada horas en cada concentración (mL) concentración (mL) 0.0 15 15 15 0.1 15 15 15 0.2 15 15 15 0.3 15 15 15 0.4 15 15 15 0.5 15 15 15 0.6 15 15 15 Tabla 1. Distribución de series de tubos con las distintas concentraciones necesarias para la determinación de tres métodos de medición de Con ayuda de un cutter o sacabocados obtenga 14 fracciones de 3 cm de largo X 0.5 cm de diámetro. Inmediatamente después de obtener las fracciones de papa péselas en una balanza con una precisión mínima de 0.01 g colóquelas en la solución que le corresponda y espere 1.5 horas. Mientras transcurre el tiempo de espera, elabore con ayuda del refractómetro una curva de calibración (Grados Brix vs MPa correspondientes a cada concentración de sacarosa) con las soluciones de la serie 3. Una vez elaborada la curva de calibración, agregue dos o tres gotas de colorante (safranina) a cada tubo de la serie 3. Transcurridas las 1.5 horas de incubación, saque las fracciones de cada solución (con ayuda de los frascos gerber), séquelas ligeramente con una servitoalla y péselas nuevamente. Repita este procedimiento con todas las fracciones incubadas en las soluciones en el orden cronológico en que fueron inicialmente colocadas, sin desechar las soluciones de donde las extrajo. Calcule el porcentaje de cambio de peso utilizando la fórmula siguiente: peso final - peso inicial % cambio de peso = ------------------------------- x 100 peso inicial Construya una gráfica con el porcentaje de cambio peso (en el eje de las ordenadas) contra la equivalencia en MPa de cada concentración de sacarosa (eje de las abscisas). = - miRT donde: m = molalidad de la solución i = constante de ionización R= constante de los gases (0.0083 MPa Kg-1 mol-1°K-1) T= temperatura absoluta (°K) Con los datos del % de cambio de peso determine por interpolación en la gráfica la concentración en la cual no haya ocurrido un cambio de peso neto en las fracciones de papa. Método de medición de por refractometría. Con una gota de cada una de las soluciones que contuvieron las fracciones de papa (serie 1), realice las lecturas con el refractómetro e interpole en la curva de calibración original que realizó previamente con los datos de la serie 3. Método de medición de Chardakov. Ordene la tercer serie de soluciones que tiño con rojo neutro junto con las soluciones restantes de la serie 2. 0.0 m 0.0 m Tubos sin rojo neutro (Serie 2) 0.1 m 0.2 m 0.3 m 0.4 m 0.5 m Tubos con una gota de rojo neutro (Serie 3) 0.1m 0.2 m 0.3 m 0.4 m 0.5 m 0.6 m 0.6 m Tabla 2. Preparación y distribución de tubos con y sin rojo neutro para la medición del en fracciones de papa. Con una pipeta Pasteur tome un pequeño volumen de cada solución teñida con rojo neutro e introduzca la punta de la misma con la gota, sin soltarla, hasta la mitad del tubo que contuvo la fracción de papa y libere una gota sin “empujarla” y anote si su desplazamiento es ascendente, descendente o estático (Figura 2). Figura 2. Método de Chardakov. Serie 1. Soluciones de Peso Peso % Cambio de sacarosa (mL) MPa Inicial Final peso g g [Sacarosa] Grados Brix Chardakov Ascensodescenso de gotas teñidas [Sacarosa] Grados Brix Chardakov Ascensodescenso de gotas teñidas 0.0 0.1 0.2 0.3 0.4 0.5 0.6 Serie 2. Soluciones de Peso Peso % Cambio de sacarosa (mL) MPa Inicial Final peso g g 0.0 0.1 0.2 0.3 0.4 0.5 0.6 Tabla 3. Resultados obtenidos en los tres métodos de medición de en fracciones de papa Discuta respecto a las diferencias o coincidencias entre estos métodos. Cuestionario 1. ¿Cuál es el fundamento de los métodos de medición de potencial hídrico utilizados en ésta práctica? 2 ¿Cómo mediría el potencial hídrico de un exudado de floema? 3. Describa un método para la medición de potencial hídrico en epidermis de cebolla. 4. La expresión siguiente: “ solución de sacarosa = solución de sacarosa” ¿es correcta o incorrecta. Justifique su respuesta? REFERENCIAS Azcón-Bieto, J. y Talón, M. 2000. Fundamentos de Fisiología Vegetal. Interamericana-McGraw-Hill, Madrid. Moore, T.C.1974. Research experiences in plant physiology. A laboratory manual. Springer-Verlag. New York. pp 20-23.Redwood City, California. Salisbury, F.B. y Ross, C.W. 1991. Plant Physiology. Wadsworth Publishing. California. Taiz, l. y Zeiger, E. 2006. Plant Physiology. Sinauer Associates, Sunderland, MA, USA. Web: http://www.plantphys.net