Problemas de parciales relacionados con el tema cifras significativas
Anuncio

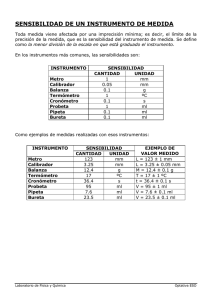
Problemas de parciales relacionados con el tema cifras significativas- tp usos de materiales 1) a) Al colocar un termómetro en dos baños de agua, uno a 30,00 ºC y otro a 40,00 ºC, su columna de mercurio alcanza alturas de 17,2 cm y 22,2 cm respectivamente por encima del bulbo. Calcule la sensibilidad y la precisión del termómetro sabiendo que la menor diferencia de altura que puede apreciarse en la columna de mercurio es de 0,5 mm. b) Se prepara una solución mezclando 10,00 ml de solución de hidróxido de potasio 2,7 %p/v y 260 ml de otra solución de hidróxido de potasio 0,39 M. Luego se disuelven 0,0205 g y 1,30 g de hidróxido de potasio sólido en la solución resultante. ¿Cuál es la masa de soluto presente en la solución final?. La solución final se lleva a volumen en un matraz de 500 ml con 0,1 ml de precisión, calcule su molaridad. Exprese todos los resultados con las cifras correctas. 2) a) En una experiencia como la del tp para determinar la densidad de una solución de sulfato de cúprico se obtuvieron los siguientes datos: Volumen (ml): v1=10, 20; v2=12,35; v3=19,45, v4=18,35, v5=15,70 Masa (g): m1=11,0154; m2=13,1788; m3=21,1133; m4=19,1083; m5=17,1297. i) Expresar correctamente la densidad.ii) Calcular (con el nro correcto de c.s.) la molalidad de la solución si para preparar 100,0 ml de la misma se pesaron 12, 9624 g de soluto (considere que el PMR no limita el nro de c.s.) b) i) Se pesó una masa de hidróxido de sodio, obteniéndose un valor de 43, 780 g. Teniendo en cuenta que el ojo humano promedio es capaz de distinguir 0,5 divisiones, establecer (justificando adecuadamente) con cúal(es) de las siguientes balanzas pudo haberse realizado correctamente dicha medida. Sensibilidades: balanza 1: 0,1 div/mg; balanza 2: 1 div/mg; balanza 3: 0,5 div/mg; balanza 4: 0,05 div/mg. ii) La masa del inciso anterior se disolvió en agua hasta un volumen de 500,0 ml. Se tomaron 10,00 ml y se titularon con una solución de ácido clorhídrico, gastándose 12,50 ml de esta última. ¿ Cuál era la concentración molar de la solución de ácido?. Expréselo con el nro correcto de c.s. Los PMR no limitan el nro de c.s. 3) a) Se pesan dos masas diferentes de hidróxido de sodio, cinco veces cada una en dos balanzas distintas. Los resultados obtenidos son: Balanza 1 (masa 1): 2,535 g; 2,241 g; 2,742 g; 2,451 g; 2,398 g Balanza 2 (masa 2): 2,1523 g; 2,1524 g; 2,1526 g; 2,1522 g; 2,1522 g Las dos masas se colocan juntas en un vaso de precipitados de precisión ± 1 ml y se disuelven en 50 ml de agua. Posteriormente la solución se trasvasa a un matraz de 500 ml de precisión ± 0,1 ml y se lleva a volumen. Expresando correctamente los resultados con el nro correcto de c.s, conteste: i) ¿cuál es la balanza más precisa?, ii) ¿cuál es la concentración molar de la solución final?, iii) ¿qué volumen de ácido sulfúrico 0,258 N será necesario para neutralizar 20,0 ml de la mezcla? b) Un termómetro se sumerge en dos baños de agua a 25,00 ºC y 32,00 ºC (temperaturas medidas con otro termómetro). La columna de mercurio alcanza alturas de 7,25 cm y 10,35 cm, respectivamente. Calcule la sensibilidad del termómetro. ii) Calcular la precisión del termómetro sabiendo que la menor diferencia de altura que puede apreciarse en la columna de mercurio es de 0,5 mm. 4) a) Un volumen de una solución es medido con tres instrumentos volumétricos distintos obteniendo los siguientes valores (en ml): I1: 11,265; 11,271; 11,284; 11,232; 11,290 I2: 11,453; 11,460; 11,459; 11,452; 11,455 I3: 11,001; 11,372; 11,771; 11,224; 11,299 Exprese correctamente la lectura de cada instrumento. b) Se determinó la masa de un vaso de precipitados vacío y del mismo vaso con el volumen de solución al que se hace referencia en el inciso anterior. Los valores fueron 83,4456 y 94,905 g respectivamente. Si la densidad de la solución es 1,02321 g/ml, calcule el volumen de solución contenida en el vaso. Si éste es el valor aceptado, indique y justifique cuál de los tres instrumentos del inciso anterior es el más exacto y cuál es el más preciso. 5) a) Un volumen de solución de cloruro de sodio es medido varias veces con tres instrumentos volumétricos distintos, obteniéndose los siguientes resultados (en ml): Instrumento 1: 12,598; 12,676; 12,502; 12,722 Instrumento 2: 12,217; 12,220; 12,209; 12,212 Instrumento 3: 12,439; 12,477; 12,459; 12,411 i) Expresar correctamente el resultado con cada instrumento. Ii) Si el valor aceptado era 12,5932 ml (medido con otro instrumento), justifique cuál de los instrumentos volumétricos era el más preciso y cuál era el más exacto. b) Una cierta masa de hidróxido de potasio es disuelta en agua y llevada a un volumen en un matraz de 100 ml con precisión 0,1 ml. Se toman 10,00 ml de esa solución y se titulan con una solución de ácido clorhídrico 0,39527 M, gastandose 13,15 ml. ¿ Cuál es la masa de hidróxido de potasio que se había pesado?. Exprésela con el nro correcto de c.s. c) ¿Cuál es la sensibilidad de un termómetro (con el nro correcto de c.s) si la altura de la columna de mercurio es de 16,55 cm a 34,00 ºC y de 12,60 cm a 23,00 ºC?. 6) Se pesa un objeto en dos balanzas diferentes, obteniéndose los siguientes resutados: Balanza 1: 9,7834g; 9,7629 g; 9,7987 g; 9,7950 g; 9,7890 g Balanza 2: 9,7627 g; 9,7628 g; 9,7636 g; 9,7639 g; 9,7638 g a) Expresar correctamente ambas pesadas. b) Indicar cuál es más precisa y cuál es la más exacta, si el peso aceptado del objeto es de 9.7500 g. c) En la balanza más precisa se pesa una masa de 8 g de cloruro de sodio, se la disuelve y se lleva a 100 ml en un matraz (precisión 0,2 ml). Se toman 5 ml con pipeta de doble aforo (precisión 0,01ml) y se agrega nitrato de plata 0,1933 M hasta que no se observa precipitación de cloruro de plata, gastándose 20,65 ml. Calcular la pureza de la muestra (expresar todos los resultados con las c. s correctas). 7) a) En una experiencia como la del tp para determinar la densidad de una solución de permanganato de potasio se obtuvieron los siguientes datos: Masa (en g): m1=13,6178; m2=12,8564; m3=10,5697; m4=18,9315; m5=15,5238. Volumen (ml): v1=13,25; v2=12,60; v3=10,40, v4=18,35, v5=15,10 i) Expresar correctamente la densidad. Ii) Calcular (con el nro correcto de c.s) la concentración en %p/p de la solución si para preparar 100,0 ml se pesaron 13,6942 g de soluto. b) Cuando un termómetro se sumerge en dos baños de agua a 25, 0 ºC y 38,0 ºC la columna de mercurio alcanza alturas de 12,15 cm y 18,65 ml, respectivamente. i) Calcular la sensibilidad del termómetro. ii) ¿Cuál será la precisión del termómetro sabiendo que la menor diferencia de altura que puede apreciarse en la columna de mercurio es de 0,5cm. iii) ¿Cuál o cuáles de las siguientes temperaturas pudieron haberse medido con ese termómetro? . 8) a) Se prepara una solución mezclando 25,00 ml de una solución de sulfato de potasio 4,5%p/v y 270 ml de otra solución 0,044 M del mismo soluto. Luego se disuelven 0,0185 g y 0,411 g de sulfato de potasio sólido en la solución resultante. ¿ Cuál es la masa presente en la solución final?. Expréselo con las cifras significativas correctas. La solución final se lleva a volumen en un matraz de 500 ml con 0,1 ml de precisión. Calcule la molaridad de la solución final (expresadas con las cifras correctas). b) Cierto volumen de agua medido en tres instrumentos volumétricos diferentes ( A, B y C) obteniendo los siguientes resultados (en ml): IA: 9,90; 10,40; 10,25; 9,60 IB: 9,90; 9,82; 9,89; 9,86 I.C: 11,10; 10,80; 11,00; 10,80 Exprese correctamente el volumen medido en cada caso. Para obtener el valor aceptado para ese volumen, éste se pesa en una balanza analítica obteniendo el resultado 9,8488±0,0001 g. Si la densidad del agua es 0,999875 g/ml, calcule el valor aceptado e indique y justifique adecuadamente cuál de los instrumentos es más preciso y cuál más exacto.