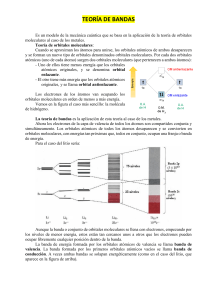
Para las siguientes molécula
Anuncio
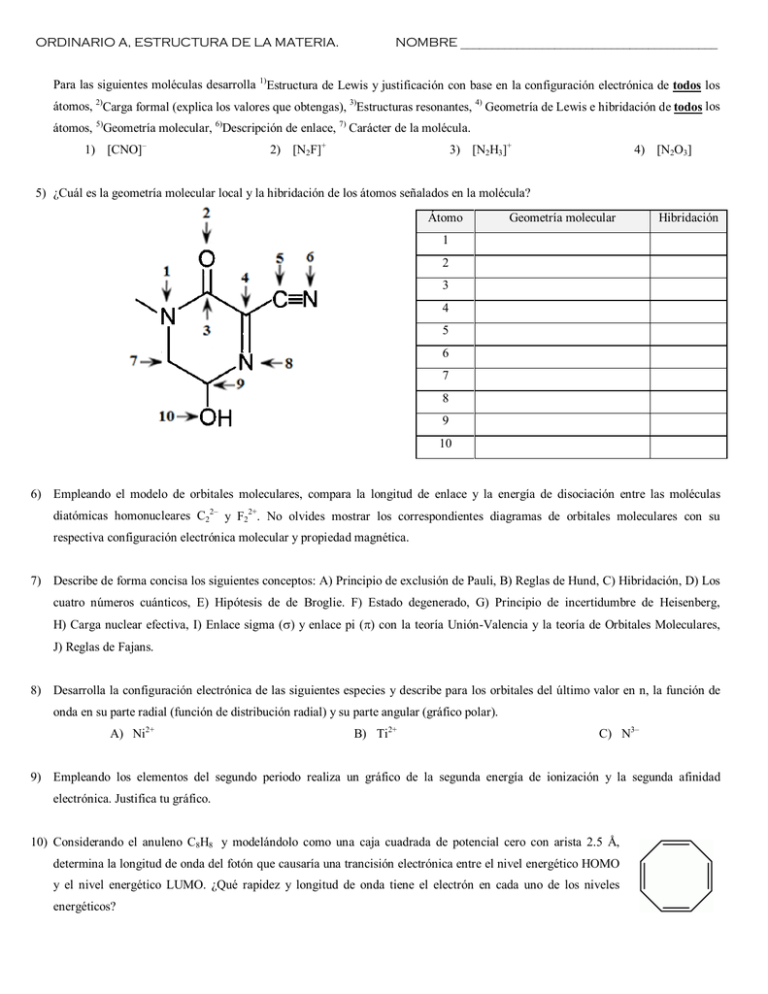
ORDINARIO A, ESTRUCTURA DE LA MATERIA. NOMBRE _________________________________________ Para las siguientes moléculas desarrolla 1)Estructura de Lewis y justificación con base en la configuración electrónica de todos los átomos, 2)Carga formal (explica los valores que obtengas), 3)Estructuras resonantes, 4) Geometría de Lewis e hibridación de todos los átomos, 5)Geometría molecular, 6)Descripción de enlace, 7) Carácter de la molécula. 1) [CNO]– 2) [N2F]+ 3) [N2H3]+ 4) [N2O3] 5) ¿Cuál es la geometría molecular local y la hibridación de los átomos señalados en la molécula? Átomo Geometría molecular Hibridación 1 2 3 4 5 6 7 8 9 10 6) Empleando el modelo de orbitales moleculares, compara la longitud de enlace y la energía de disociación entre las moléculas diatómicas homonucleares C22– y F22+. No olvides mostrar los correspondientes diagramas de orbitales moleculares con su respectiva configuración electrónica molecular y propiedad magnética. 7) Describe de forma concisa los siguientes conceptos: A) Principio de exclusión de Pauli, B) Reglas de Hund, C) Hibridación, D) Los cuatro números cuánticos, E) Hipótesis de de Broglie. F) Estado degenerado, G) Principio de incertidumbre de Heisenberg, H) Carga nuclear efectiva, I) Enlace sigma (σ) y enlace pi (π) con la teoría Unión-Valencia y la teoría de Orbitales Moleculares, J) Reglas de Fajans. 8) Desarrolla la configuración electrónica de las siguientes especies y describe para los orbitales del último valor en n, la función de onda en su parte radial (función de distribución radial) y su parte angular (gráfico polar). A) Ni2+ B) Ti2+ C) N3– 9) Empleando los elementos del segundo periodo realiza un gráfico de la segunda energía de ionización y la segunda afinidad electrónica. Justifica tu gráfico. 10) Considerando el anuleno C8H8 y modelándolo como una caja cuadrada de potencial cero con arista 2.5 Å, determina la longitud de onda del fotón que causaría una trancisión electrónica entre el nivel energético HOMO y el nivel energético LUMO. ¿Qué rapidez y longitud de onda tiene el electrón en cada uno de los niveles energéticos?