REMOCIÓN DE COLORANTES SINTÉTICOS
Anuncio

REMOCIÓN DE COLORANTES SINTÉTICOS UTILIZADOS EN LA INDUSTRIA Informe final COORDINACIÓN DE TRATAMIENTO Y CALIDAD DEL AGUA Jefe de proyecto: Dra. Gabriela E. Moeller Chávez Participantes: M. en I. Luciano Sandoval Yoval Dra. Petia MijaylovaNacheva Colaboradores: M. en I. Erika Miranda Mandujano Ing. Mónica Mejía López Ing. Ma. de los Angeles Farfán Guerrero Ing. Alberto Mendoza Esquivel Ing. Ernesto Bahena Castro Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx ÍNDICE GENERAL ÍNDICE GENERAL 0 ÍNDICE DE FIGURAS iii ÍNDICE DE TABLAS v Resumen Ejecutivo viii 1.- Objetivos: 1 1.1 Objetivo General 1 1.2 Particulares 1 2.- Antecedentes 2 3.- La industria textil en México 5 3.1.-Colorantes utilizados en la industria textil en México 6 3.1.1.- Colorantes naturales 7 3.1.2 Colorantes artificiales 8 3.1.2.1 Colorantes ácidos 8 3.1.2.2.-Colorantes básicos 8 3.1.2.3.- Colorantes directos 9 3.1.2.5.- Colorantes dispersos 10 3.1.2.6.- Colorantes sulfurosos 11 3.2.- Características de las aguas residuales de la industria textil con colorantes 13 3.3.- Regulación de descargas de aguas residuales de la industria textil 14 4.- Colorantes del tipo azo 15 4.1.- Clasificación de los colorantes azo 16 4.2 .- Características de los colorantes azo 17 5.- Tecnologías utilizadas para el tratamiento de aguas residuales de la industria textil con colorantes 18 5.1.- Tratamientos biológicos 19 5.1.1.- Tratamiento biológico convencional 19 5.1.2 Tratamiento biológico no convencional 23 5.1.2.1.- Tratamiento fúngico 23 5.1.2.2. Tratamiento con enzimas del tipo de las peroxidasas 28 5.2 Tratamientos fisicoquímicos: Procesos avanzados de oxidación 33 5.2.1.- Procesos no fotoquímicos 34 5.2.2.- Procesos fotoquímicos 37 5.2.3.- Proceso de oxidación de Fenton 40 6.- Metodología 43 6.1.- Selección y Caracterización de las aguas residuales 43 6.1.1. Aguas residuales de la Empresa Gutterman 43 6.1.2.- Aguas residuales de la Empresa lavadora de mezclillas 44 6.2.- Pruebas de tratabilidad 44 6.2.1.- Tratamiento biológico convencional: Proceso acoplado Anaerobio- Aerobio 44 6.2.1.1.- Sistema experimental 44 6.2.1.2.- Procedimiento experimental 47 6.2.1.3.- Muestreo y análisis físico-químicos 48 6.2.2.- Tratamiento biológico no- convencional 49 6.2.2.1.- Tratamiento fúngico 49 6.2.3.- Tratamiento Fisicoquímico: Oxidación Avanzada (Pruebas de Fenton) 58 7.- Resultados 59 7.1.- Caracterización de las aguas residuales 59 7.1.1. Preparación de aguas residuales sintéticas y colorantes utilizados para las pruebas de tratabilidad fisicoquímicas. 59 7.2.- Pruebas de tratabilidad 61 7.2.1.- Tratamiento biológico convencional: Procesos acoplado anaerobio-aerobio 61 7.2.1.1.-Seguimiento del proceso en el reactor UASB y LA 63 Conclusiones 77 Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx 7.2.2.- Tratamiento biológico no- convencional 7.2.2.1.- Tratamiento fúngico 7.2.2.2 Tratamiento enzimático Conclusiones 7.2.3. - Tratamiento Fisicoquímico: Procesos avanzados de oxidación (procesos Fenton) 7.2.3.1 Pruebas con agua residual industrial 7.2.3.2 Análisis de resultados de pruebas de agua residual industrial 7.2.3.3 Diseño de prototipo Conclusiones CONCLUSIONES REFERENCIAS Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx 79 79 86 93 105 113 124 129 130 131 132 ÍNDICE DE FIGURAS Figura 3.1 Estructuras químicas con representación de grupos cromóforos y auxocromóforos 6 Figura 3.2 Composición química del índigo 7 Figura 3.3 Madeja de hilo de seda teñido con índigo natural. Buri Ram, Surín Tailandia. 2010 7 Figura 3.4 Colorantes azóicos 8 Figura 3.5 Colorantes a la tina 10 Figura 3.6 Colorantes sulfurosos 11 Figura 5.1 Pleurotus ostreatus 25 Figura 5.2 Mecanismo de reacción general de las peroxidasas (Welinder, 1992). 31 Figura 5.3. Variedades de soya producida en México 32 Figura 5.4. Mecanismo de oxidaciónUV/peryodato 39 Figura 5.5 Mecanismo de oxidación fotocatálisis heterogénea 40 Figura 6.1 Esquema y dimensiones del reactor UASB. 46 Figura 6.2 Esquema y dimensiones del reactor LA. 47 Figura 6.3 -Biofiltros empacados. 49 Figura 6.4 -Estructura del colorante Negro Terasil SRL ( http://www.lookchem.com/). 50 Figura 6.5 Hilos después del proceso de teñido con el colorante negro terasil. 51 Figura 7.1 Variación de los valores de la DQO 64 Figura 7.2 Remociones de DQO 65 Figura 7.3 Variaciones de las cargas orgánicas volumétricas en los reactores UASB y LA. 65 Figura 7.4 Variación de las concentraciones de SST 68 Figura 7.5 Variación de las concentraciones de SSV 68 Figura 7.6 Remociones de SST y SSV en el reactor UASB 69 Figura 7.7 Remociones de SST y SSV en el reactor LA. 69 Figura 7.8 Variación de las concentraciones de SSTLM y SSVLM en el reactor LA. 70 Figura 7.9 Variación de las concentraciones del N-NH4 en el influente y efluente del reactor UASB 72 Figura 7.10 Variación de las concentraciones del N-NH4 en el influente y efluente del reactor LA. 73 Figura 7.11 Remoción del N-NH4 en los dos reactores UASB y LA. 73 Figura 7.12 Variación de las concentraciones de los nitritos 74 Figura 7.13 Variación de las concentraciones de los nitratos 74 Figura 7.14 Variación de las concentraciones del PT 76 Figura 7.15 Remoción del PT en los dos reactores UASB y LA. 76 Figura 7.16 Comportamiento del color aparente en los efluentes de los reactores 1 y 4 con respecto al influente 79 Figura 7.17 Comportamiento de color aparente en los efluentes de los reactores 2 y 3 con respecto al influente 80 Figura 7.18 Comportamiento del color verdadero en los efluentes de los reactores 1 y 4 con respecto al influente 81 Figura 7.19 Comportamiento del color verdadero en los efluentes de los reactores 2 y 3 con respecto al influente 81 Figura 7.20 Comportamiento de la concentración de color en los efluentes de los reactores 1 y 4 con respecto al influente 83 Figura 7.21 Comportamiento de la concentración de color en los efluentes de los reactores 2 y 3 con respecto al influente 83 Figura 7.22 Comportamiento de la demanda química de oxígeno en el reactor con turba sin esterilizar (R1) y el reactor con turba sin esterilizar inoculado con P.O. (R4) 85 Figura 7.23 Comportamiento de la demanda química de oxígeno en el reactor con turba que pasó por un proceso de esterilización (R3) y el reactor con turba estéril inoculado con P.O. (R2) 85 Figura 7.24 Decoloración del colorante AND en pruebas en discontinuo a diferentes concentraciones iniciales: ( ) 10 40 mg/L. 86 Figura 7.25 Linealización de los datos experimentales de velocidades de degradación del colorante AND mediante un modelo de inhibición por substrato 88 Figura 7.26 Comprobación del modelo cinético de inhibición por substrato ( ) datos experimentales: (--) modelo cinético. 89 Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx Figura 7.27 decoloración del colorante AND en pruebas a diferentes velocidades de adición de H2O2: ( ) 1.25 µmol/Lmin; ( ) 8 µmol/L-min y diferentes concentraciones de colorante: (a) 40 mg/L; (b) 30 mg/L; (c) 20 mg/L; (d) 10 mg/L 91 Figura 7.28 Comprobación del modelo cinético en función de la concentración del colorante AND y la velocidad de --) datos simulados por el modelo cinético 93 Figura 7.29 Muestra de agua residual inicial 113 Figura 7.30 muestra de agua residual final 113 Figura 7. 31 Prueba No 4 Muestra de agua residual. 115 Figura 7. 32 Vista de prueba 3 en jarras 115 Figura 7. 33 Apariencia del agua inicial de prueba No. 7 118 Figura 7. 34 Prueba No. 7 en curso 118 Figura 7. 35 Agua inicial de prueba 10 120 Figura 7.36 Condiciones finales de prueba 10 120 Figura 7. 37 Agua inicial de prueba No.11 121 Figura 7. 38 Agua final de prueba No.11 121 Figura 7. 39 Agua de inicio prueba No.12 122 Figura 7. 40 Agua final de prueba No.12 122 Figura 7. 41 Relación pH vs Conductividad 125 Figura 7. 42 Relación color inicial vs pH 125 Figura 7. 43 Relación color inicial vs conductividad 126 Figura 7. 44 Color Vs dosis empleadas 126 Figura 7. 45 Porcentaje de remoción de color vs color inicial 127 Figura 7.46 Relación DQO inicial vs pH y conductividad 128 Figura 7. 47 Relación DQO inicial vs peróxido de hidrógeno y sulfato ferroso 129 Figura 7. 48 Remoción de DQO 129 Figura 7. 49 Prototipo de prueba 130 Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx ÍNDICE DE TABLAS Tabla 3.1 Clasificación de colorantes de acuerdo a su grupo cromóforo Tabla 3.2 Clasificación de colorantes de acuerdo a su forma de aplicación Tabla 3.3 Carga contaminante que aportan los colorantes 11 12 14 Tabla 5.1 Procesos físicos empleados en el tratamiento de efluentes de la industria textil 20 Tabla 5.2 Procesos químicos empleados en el tratamiento de efluentes de la industria textil 21 Tabla 5.3 Procesos biológicos convencionales empleados en el tratamiento de efluentes de la industria textil 22 Tabla 5.4 Algunos procesos no convencionales utilizados para el tratamiento de aguas residuales de la industria textil (Casos de estudio sobre las tecnologías usadas para la remoción de colorantes por P. ostratus) 27 Tabla 5.5 Enzimas y su principal aplicación en el tratamiento de residuos orgánicos 29 Tabla 5.6 Trabajos realizados con peroxidasas de mayor aplicación. 30 Tabla 5.7 Factores que influyen en la capacidad catalítica de las enzimas. 32 Tabla 5.8 Tecnologías avanzadas de oxidación (TAO) 34 Tabla 5.9. Trabajos realizados utilizando el proceso de Fenton para la oxidación de colorantes 41 Tabla 6.1 Parámetros de operación del reactor UASB. Tabla 6.2. Características del material de empaque de los biofiltros Tabla 6.3. Características de los influentes utilizados para la alimentación de los biofiltros Tabla 6.4. Características de los influentes utilizados. Tabla 6.5. Parámetros de medición, puntos y frecuencia de muestreo para los biofiltros. Tabla 6.6. Parámetros analizados y sus técnicas de análisis. Tabla 6.7. Aditivos utilizados en la preparación de mezclas para teñido de hilos Tabla 6.8. Parámetros a evaluar en la degradación enzimática de agua artificialmente contaminada y efluente real. Tabla 6.9. Concentraciones de preparación. 48 50 51 52 54 54 57 57 58 Tabla 7.1. Características del agua residual sintética 60 Tabla 7.2 Aguas residuales de la empresa lavadora de mezclillas. 60 Tabla 7.3. Características de las aguas residuales utilizadas en el estudio. 62 Tabla 7.4 Remoción de color aparente 80 Tabla 7.5 Remoción de color verdadero 82 Tabla 7.6 Remoción de color 84 Tabla 7.7. Remoción de materia orgánica 86 Tabla 7.8. Parámetros cinéticos de la degradación del colorante AND a diferentes concentraciones iniciales 87 Tabla 7.9. Parámetros cinéticos del modelo de inhibición por substrato 88 Tabla 7.10. Velocidades de degradación del colorante AND a diferentes concentraciones de colorante y diferentes velocidades de adición de H2O2 91 Tabla 7.11. Parámetros cinéticos de la degradación del colorante AND a diferentes velocidades de adición de H2O2. 92 Tabla 7.12. Parámetros del modelo cinético en función de la concentración del colorante AND y la adición de H2O2. 93 Tabla 7.13. Características del agua de la prueba 1ª 105 Tabla 7.14. Características del agua de la prueba 1b 105 Tabla 7.15. Características del agua de la prueba No.2 106 Tabla 7.16. Características finales del agua de la prueba No.2 106 Tabla 7.17. Características del agua de la prueba No. 3 107 Tabla 7.18. Características finales del agua de la prueba No. 3 107 Tabla 7.19. Características del agua de la prueba No.4 108 Tabla 7.20. Características finales del agua de la prueba No. 4 108 Tabla 7.21. Características del agua de la prueba No. 5 109 Tabla 7.22. Características finales del agua de la prueba No.5 (2h de sedimentación) 109 Tabla 7.23. Características finales del agua de la prueba No.5 (4h sedimentación) 110 Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx Tabla 7.24. Características finales del agua de la prueba No.5 (5h sedimentación) Tabla 7.25. Características finales del agua de la prueba No. 5(6h sedimentación) Tabla 7.26. Características del agua de la prueba No. 6 Tabla 7.27. Características finales del agua de la prueba No. 6 (2h sedimentación) Tabla 7.28. Características finales del agua de la prueba No. 6(Filtrado) Tabla 7.29. Características iniciales muestra No.1 Tabla 7.30. Características finales de la muestra 1 Tabla 7.31. Características iniciales muestra No. 2 Tabla 7.32. Características finales de la muestra No.2 Tabla 7.33. Características iniciales muestra 3 Tabla 7.34. Características finales de la muestra No.3 Tabla 7.35. Características iniciales muestra 4 Tabla 7.36. Características finales de la muestra 4 Tabla 7.37. Características iniciales muestra No.5 Tabla 7.38. Características finales de la muestra No.5 Tabla 7.39. Características iniciales muestra No.6 Tabla 7.40. Características finales de la muestra No.6 Tabla 7.41. Características iniciales muestra No.7 Tabla 7.42. Características finales de la muestra No.7 Tabla 7.43. Características iniciales muestra 8 Tabla 7.44. Características finales de la muestra No.8 Tabla 7.45. Características iniciales muestra No.9 Tabla 7.46. Características finales de la muestra No.9 Tabla 7.47. Características iniciales muestra No.10 Tabla 7.48. Características finales de la muestra No.10 Tabla 7.49. Características iniciales muestra No.11 Tabla 7.50. Características finales de la muestra 11 Tabla 7.51. Características iniciales muestra No.12 Tabla 7.52. Características finales de la muestra 12 Tabla 7.53. Características iniciales muestra No.13 Tabla 7.54. Características finales de la muestra No.13 Tabla 7.55. Características iniciales muestra No.14 Tabla 7.56. Características finales de la muestra No.14 Tabla 7.57. Características iniciales muestra No.15 Tabla 7.58. Características finales de la muestra No.15 Tabla 7.59. Calidad de agua en remoción de color Tabla 7.60. Calidad de agua en remoción de DQO. Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx 110 110 111 111 112 113 114 114 114 114 115 115 115 116 116 116 117 117 117 118 118 118 119 119 119 120 120 121 121 122 122 123 123 123 123 124 127 Resumen Ejecutivo Se evaluaron a nivel laboratorio varios métodos de tratamiento que la literatura refiere como posibles para el tratamiento de las aguas residuales de la industria textil, con énfasis en la remoción de los colorantes que contienen. Los métodos convencionales probados fueron el fisicoquímico mediante oxidación avanzada utilizando el método de Fenton y el biológico acoplado anaerobio aerobio. Como métodos no convencionales se iniciaron las investigaciones probando la efectividad de la biofiltración con el medio de empaque inoculado con hongos conteniendo enzimas del tipo de las peroxidasas.(Biológico fúngico). La matriz o medio de empaque utilizado fue la turba, que fue inoculada con una cepa del hongo Pleurotus ostreatus. El segundo método no convencional que abarcó este estudio fue el biológico enzimático utilizando enzimas también del tipo de las peroxidasas. Se desarrolló un método para la obtención de las peroxidasas provenientes del frijol de soya a partir de un desecho generado durante la fabricación de la leche de soya. Las aguas residuales probadas se obtuvieron de diferentes fuentes: lavadoras de mezclilla, fabricación de playeras y producción de hilos. El efluente que se genera en la producción de textiles que utilizan colorantes son en general aguas con características de alta carga orgánica, alta variabilidad en sus características, baja biodegradabilidad y altamente coloridas. Estas características las hace difíciles de tratar. El proceso biológico convencional (sistema acoplado anaerobio - aerobio.(UASB-Lodos activados))no resultó muy apropiado por el efecto inhibitorio de las aguas residuales y su alta variabilidad. La carga orgánica aplicada de 5.3 kg DQO.m-3.d-1 y con un TRH de 11.1 h en el reactor UASB. permitió alcanzar una remoción de 67% después de 46 días de operación. El agua residual descargada directamente de la tina de teñido en la industria con una DQO promedio de 7,739±3,180 mg/L, casi tres veces mayor que la DQO del efluente general de la industria textil. Esta agua residual es fuertemente inhibitoria para la biomasa granular del reactor UASB. Operando el reactor con una carga orgánica de 8.3 ±1.8 kg DQO m-3 d-1 y con un TRH de 18.2 h durante más de un mes se obtuvo una remoción promedio de DQO de tan solo 16±5% con tendencia de incremento. Con respecto al tratamiento aerobio utilizado, el reactor de lodos activados usado como segunda etapa del tratamiento biológico del agua residual de la tina de teñido de la industria textil, operado con una carga orgánica volumétrica de 6.51±1.27 kgDQO.m-3.d-1y un TRH de 14.0 h, permitió obtener una remoción promedio de 14.9±7.7%. La aclimatación de la biomasa al sustrato presente en el agua residual efluente del UASB es difícil, con problemas de intoxicación de la biomasa e inhibición de la degradación de la materia orgánica y del crecimiento de la biomasa, sin embargo, fue posible superar la intoxicación en unos 10 días, pero la remoción aumenta muy lentamente. El promedio de la remoción global de la DQO (en los dos reactores) durante los últimos 30 días de operación fue de 28.7±7.3% con una tendencia de incremento. Se necesita seguir el proceso de aclimatación y estabilización del proceso en ambos reactores. Referido a los procesos biológicos no convencionales: Es importante el considerar que la extracción de la enzima peroxidasa se realizó a partir del residuo de la obtención de la leche de soya, ADES (Okara), lo cual se considera como algo no realizado con anterioridad. Se utilizaron para estos experimentos no el agua residual del efluente general o de la tina, sino sólo el colorante azul negro directo , AND., esto para tener un mayor control del proceso. La oxidación enzimática del colorante AND mediante la enzima Peroxidasa constituye un método muy efectivo para su degradación. Las condiciones en las cuales la oxidación es más rápida y la actividad enzimática se ve menos afectada. Aun cuando la investigación es Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx incipiente y no está concluida, se han obtenido remociones hasta del 50 % del color con la ventaja de que la enzima puede ser recuperada. Con respecto al tratamiento mediante biofiltración con turba inoculada con Pleutorus ostreatus (fúngico), se probaron cuatro variantes de biofiltros para poder evaluar el efecto de la turba, del hongo y de su combinación. Un bifiltro fue sólo empacado con turba sin esterilizar, otro fue empacado con turba inoculada sin esterilización y dos más con las misma condiciones descritas sólo que esterilizados. se observa que de los cuatro reactores utilizados en el experimento el que mejor desempeño tuvo fue el reactor inoculado con el hongo Pleurotus ostreatus y sin esterilizar , mostrando que el procedimiento de esterilización del material de empaque si tuvo un efecto negativo; además de mostrar hasta el momento que la materia orgánica fue removida y disminuida por el proceso de adsorción, absorción de la turba y degradación debida a microorganismos adheridos al mismo material de empaque de los biofiltros. Para los procesos fisicoquímicos de oxidación avanzada las mejores condiciones fueron: Mezcla rápida a 200 rpm por 10 min; mezcla lenta a 20 rpm por 50 min, seguida de una sedimentación por 120 min. En promedio se emplean 470 mg/L de sulfato ferroso y 867 mg/L de peróxido de hidrógeno para obtener un color residual en el agua tratada de 543 UPtCo La remoción de color lograda en las diferentes pruebas está en un rango de 63.5 a 99.1%. Así, en promedio se emplean 430 mg/L de sulfato ferroso y 900 mg/L de peróxido de hidrógeno para obtener una DQO residual en el agua tratada de 1160 mg/L en promedio. La remoción de la DQO lograda está en un rango de 48 a 68 %.El obtener una remoción de alrededor del 60% en DQO indica que el reactivo Fenton rompe las estructuras de los colorantes y las oxida parcialmente. Para obtener una remoción u oxidación total de los compuestos que generan color. Es necesario un segundo tratamiento por lo que se probará en la continuación de este estudio el proceso acoplado fisicoquímico (Fenton) y biológico aerobio.(Lodos activados para permitir que el efluente obtenido mediante este tren cumpla con las regulaciones vigentes y que su descarga no afecte el sitio donde se descargue o eventualmente pueda ser reutilizado. Para esta segunda fase del proyecto se diseñó y construyó un prototipo de prueba que se probará con el tratamiento acoplado FQ-Biológico Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx - Objetivos: 1.1 Objetivo General Evaluar diferentes métodos de tratamiento utilizados para la remoción de colorantes utilizados en la industria textil: Métodos convencionales: Fisicoquímico (Oxidación avanzada por Fenton) Biológico (Sistema anaerobio – aerobio) Métodos no convencionales Biológico Fúngico-(Biofiltros empacados con turba e inoculados con P. ostreatus) Biológico enzimático (peroxidasas de soya obtenidas a partir de un residuo industrial) 1.2 Particulares Seleccionar un efluente industrial representativo. Determinar las condiciones óptimas de operación de los tratamientos convencionales: fisicoquímico (Fenton) y biológico acoplado(anaerobio-aerobio) Determinar la máxima concentración de colorante tratada en los procesos biológicos convencionales (Fisicoquímico y biológico acoplado). Evaluar los procesos de tratamiento convencional probados en cuanto a las condiciones de operación y eficiencia de remoción de color y materia orgánica. Proponer un tren de tratamiento que sea capaz de reducir el color y la carga orgánica de un efluente textil real. Desarrollar un prototipo piloto experimental como alternativa a los sistemas convencionales. Iniciar estudios con los procesos biológicos no- convencionales. Paseo Cuauhnáhuac 8532, Progreso, Jiutepec, Morelos,62550. México Tel: (777) 329 36 00 www.imta.gob.mx 2.- Antecedentes El agua es un recurso primordial para la actividad industrial, su utilización ha variado a lo largo del tiempo, disminuyendo su aprovechamiento local o puntual como fuente de energía primaria (molinos y turbinas), pero continúa siendo imprescindible para el desarrollo industrial usada como medio de reacción y disolvente o como regulador térmico en calderas y torres de refrigeración. La industria necesita agua en grandes cantidades, para sus procesos de producción, enfriamiento, calefacción, lavado, clasificación y traslado de materiales, etc. Las industrias de alimentos elaborados, bebidas y la mayoría de los sintéticos requieren agua de alta calidad para sus procesos de producción, pero también usan agua para la eliminación de sus desechos. La minería y la extracción de aceites contaminan el agua, pero la refinación y el chapeado de metales producen ácidos, álcalis y sales que son sumamente dañinos si se vierten en los ríos y lagos. Las fábricas de papel son industrias que requieren enormes cantidades de agua y sus desechos contienen fibras y productos químicos. Las plantas elaboradoras de alimentos y carne descargan desechos vegetales y animales que contaminan el agua. La industria química de síntesis de colorantes y pigmentos produce aguas coloridas y con compuestos tóxicos tanto orgánicos como inorgánicos. El sector industrial, ha tenido un crecimiento acelerado a partir de la década de los cuarentas con una distribución desigual en el territorio nacional que ha creado polos de concentración elevada de industrias, con los problemas consecuentes de migración de poblaciones hacia esas zonas que se han vuelto extremadamente pobladas, acumulándose los contaminantes ambientales e incrementándose el riesgo de accidentes químicos. El uso del agua en la industria en México, representa aproximadamente el 5% de la extracción del agua en el país. El 90% aproximadamente es abastecido por fuentes propias y el resto se abastece de tomas especiales para uso industrial, que proveen las redes municipales, (CNA 2011). Del total del consumo industrial, el 50% se utiliza para enfriamiento, el 35% en procesos; el 5% en calderas y en servicios el 10%. Casi el 80% del consumo de agua de este sector lo realizan sólo seis ramas industriales, a saber: azucarera, química, petróleo, celulosa y papel, textil y bebidas. Se estima que el agua de primer uso que realiza el sector industrial podría reducirse de un 40% a 80% si se extendieran (por ejemplo, en enfriamientos) las prácticas de reúso y se instalaran implementos ahorradores, (cuando económicamente sea conveniente para la industria aceptar el cambio). 2 La importancia del control de la contaminación del agua en los últimos años se ha incrementado debido al deterioro ambiental causado por el crecimiento urbano y la industrialización, haciendo que cada día cobren mayor importancia los residuos generados en los distintos procesos industriales. Esto ha creado la necesidad de tratar el agua para disminuir la concentración de contaminantes arrojados a ella. Para eliminarlos es necesario utilizar métodos que dependen en gran medida de la calidad de agua residual que se genera en cada procesos y que requiera tratarse asi como de la calidad del efluente que se desee obtener(Villegas-Rosas et al., 2003). El color es uno de los indicadores más obvios de la contaminación del agua, y la descarga de efluentes con alta concentración de colorantes sintéticos causa gran daño a los cuerpos receptores de agua (Nawar et al., 1989), por lo cual es necesario un tratamiento antes de ser vertidos. Los principales colorantes utilizados en el ámbito mundial en la industria textil, papelera, alimenticia, cosmética y farmacéutica son los de tipo azo de los que existen aproximadamente 3000 tipos (Bishop y Jiang, 1994). La industria textil tiene un alto consumo de agua potable y subterránea en sus procesos de teñido. El volumen y la composición de sus efluentes son unas de las más contaminantes en todos los sectores industriales (Fitzgerald et al., 2005) y tienen un gran impacto en los cuerpos receptores que son descargados, ya que contienen gran cantidad de contaminantes tóxicos (colorantes), agentes orgánicos disueltos, sales inorgánicas, alta temperatura en el agua, pH que van desde 5 a 10 unidades. (Salas, 2003). Algunos colorantes y subproductos son carcinógenos y mutágenos, deterioran estéticamente los cuerpos de agua e impactan la flora y la fauna. La utilización de colorantes textiles cada vez más resistentes provoca la generación de elevados volúmenes de efluentes fuertemente coloreados, constituidos por moléculas complejas que deben ser degradadas antes de su vertido. La producción de la industria de colorantes está relacionada con el crecimiento sobre todo de la industria textil. La producción de tejidos ha aumentado constantemente en los últimos años y se ha centrado en la producción de algodón y poliéster. Esto explica que la industria de los colorantes tienda a concentrar sus esfuerzos en la producción de colorantes para estos dos tipos de fibras. Actualmente el crecimiento del uso de los colorantes en nuevas tecnologías, como en las tintas de impresión, está suponiendo un impacto para el sector, puesto que aunque los volúmenes de producción sean pequeños respecto a los usos tradicionales, el valor es significativo por los altos precios de los productos. (Guía de Mejores Técnicas Disponibles en España del Sector de Química Fina Orgánica, 2006). Los colorantes que se emplean en estos procesos son de diversos tipos y pueden ser clasificados dependiendo de varios factores, tales como su composición química, clase de aplicación o uso final. Cada tipo de colorante presenta características físicas, químicas y biológicas diferentes, 3 que les atribuyen propiedades recalcitrantes y efectos tóxicos para el ambiente (Willmont et al., 1998). En un centro de teñido, casi el 50% del colorante que originalmente se encontraba en la solución colorante inicial para el teñido de la fibra se desechó después de la coloración de las fibras sintéticas. La generación de agua residual en una instalación de teñido normal se calcula entre 1 y 2 millones de galones al día. Incluyendo el teñido, la limpieza posterior y los procesos de enjuague, puede afirmarse que se producen entre 12 y 17 galones de agua residual por libra de producto en el caso del teñido disperso, mientras que la cifra más común para la coloración reactiva y directa se encuentra en el orden de 15 a 20 galones por libra. Los colorantes de tipo azo son los más consumidos en este sector. Aproximadamente corresponden al 70% de los colorantes empleados actualmente para teñir materiales textiles, de piel, cosméticos y alimentos. Estos colorantes son compuestos químicos caracterizados por la presencia de uno ó mas grupos azo (-N=N-). Se consideran compuestos xenobióticos recalcitrantes a los procesos biodegradativos, debido a su alta estabilidad a la luz y al ataque microbiano (Qayyum Husaui, 2006). Son resistentes a la biodegradación aerobia en procesos convencionales y bajo condiciones anaerobias se lleva a cabo la reducción del colorante originando subproductos conocidos como metabolitos (aminas aromáticas), algunas altamente carcinogénicas que presentan graves problemas de toxicidad ocasionando una severa contaminación de ríos y agua subterránea (Melgoza y Buitrón 2004; Moeller, 2005). Se estima que la cantidad de colorante que no se fija a las fibras puede variar entre el 2 y 50%, dependiendo del tipo que se use, los cuales son descargados en las aguas residuales de las plantas de tratamiento o directamente al ambiente (Moeller y Garzón 2000). Existen diferentes métodos físico-químicos y biológicos que pueden ser aplicados para remover colorantes de las aguas residuales. Cada método tiene sus limitaciones técnicas y económicas. Se ha reportado en la literatura que el uso de un solo proceso no es eficiente para la degradación del color y la mineralización de los compuestos que se forman, y el uso de un solo proceso biológico anaerobio o aerobio no es efectivo para la degradación o remoción del colorante (Supaka et al., 2004; Buitrón et al., 2003). Procesos tales como el de oxidación química, ósmosis inversa y adsorción, son altamente eficientes, pero los limitan algunas desventajas como son su elevado costo, aplicabilidad limitada, alto consumo de energía, producción de lodos y de subproductos tóxico Deza, 2007). En la actualidad se están desarrollando diferentes métodos de tratamiento para la remoción de compuestos recalcitrantes, cuando no pueden ser eliminados por un solo tratamiento físico, químico ó biológico; esto mediante el uso de sistemas acoplados: Biológicos (sistema anaerobio – aerobio); Químico-Biológicos (Oxidación avanzada seguida de filtros empacados);Químico4 Enzimáticos (Oxidación por métodos enzimáticos utilizando peroxidasas)y fúngico biológicos (métodos fúngicos y sistemas aerobios de biofiltración). Es por esto que se decidió iniciar esta investigación con miras a proponer con base en los estudios de laboratorio realizados probando las diferentes tecnologías un tren de tratamiento que sea el más adecuado desde un punto de vista operativo para aplicar en la industria textil que sea capáz de reducir el color y la carga orgánica utilizando un efluente de proceso textil real conteniendo colorantes del tipo azo. 3.- La industria textil en México En el siglo XX, esta industria evolucionó considerablemente. De realizarse como actividad artesanal pasó a constituirse en una industria tecnificada, desde la etapa de diseño hasta la comercialización. Durante este proceso de metamorfosis, la tecnología jugó un papel importante, además el diseño y las tendencias de la moda han sido los principales elementos que dictan la pauta en la fabricación de prendas de vestir. La industria mexicana del vestido tiene una gran tradición; su importancia se aprecia principalmente por su contribución al empleo y a la economía de muchas regiones del país. Con la firma del TLCAN esta industria incrementó las exportaciones de prendas de vestir al mercado estadounidense y nuestro país se ubicó en el primer lugar como proveedor de EUA durante 1997-2000. La producción de una prenda incluye el diseño, el corte, la confección, el armado y el acabado. Cada uno de estos procesos genera importantes fuentes de empleos, por ello se puede decir que la industria del vestido representa el 10.3% de la industria manufacturera y, a nivel nacional, genera el 2.7%. Hasta agosto de 2011, el empleo aumentó a 400,696 personas. (SE, 2012). Estos procesos productivos tienen un lugar importante en exportaciones de nuestro país, ya sea de materiales (telas, hilos, etc.), piezas que envían desde otro país para ensamblar en México o, también, como producto final. En el año 2010 la cadena textil-vestido mexicana ha generado 6,265.5 millones de dólares, equivalentes al 2.6% en exportaciones manufactureras, principalmente hacia Estados Unidos de Norteamérica y Canadá. De acuerdo con los datos de los censos económicos de 2010 reportados por INEGI, la industria textil-vestido contribuye con el 0.7% de la producción del PIB nacional y con el 4% del PIB manufacturero. Esta industria es muy importante para el mercado nacional. (SE, 2012) 5 3.1.-Colorantes utilizados en la industria textil en México La más elemental división de los colorantes es la que distingue entre colorantes naturales y artificiales. Los empleados actualmente en la industria textil son artificiales, en tan alto porcentaje que muy bien podría decirse que lo son en su totalidad. Sin embargo los colorantes naturales han sido tan importantes en la historia del vestido y la ornamentación que resulta imposible ignorarlos; la púrpura, la cochinilla, el índigo, el palo de Campeche, etc. Aparte de que las características de los colorantes artificiales son superiores a las de los naturales, éstos, además, resultan ahora mucho más caros de obtener. La lista de colores que actualmente pueden ser obtenidos en el laboratorio se hace poco menos que infinita. Por otro lado, la segunda cuestión en razón de importancia en la tintura del textil, la solidez, ha sido tan perfeccionada que en la vestimenta actual la vida del color es ya comparable a la propia vida del tejido, de la confección, de la prenda en definitiva. La luz solar sigue siendo enemiga vital del color; pero el otro gran combatiente, el lavado, ha dejado de serlo, porque los detergentes actuales ya no atacan el color artificial; las prendas no deslucen con el lavado. La mayoría de los colorantes textiles utilizados son de origen sintético, es decir, poseen una solubilidad alta en el agua, además de ser altamente resistentes a la acción de agentes químicos y poco biodegradables. Se calcula que alrededor del 60% de los colorantes para la industria textil son colorantes reactivos, es decir, que se caracterizan por crear una unión éter con la fibra, garantizando un color duradero en el tejido. (QUIMINET, 2012). Las moléculas de los colorantes están constituidas por dos grupos fundamentales: El grupo cromóforo, responsable de producir el color y auxocromóforo (Figura 3.1) el cual hace que las moléculas sean más solubles y den mayor afinidad hacia las fibras. (Gupta y Suhas 2009). Figura 3.1 Estructuras químicas con representación de grupos cromóforos y auxocromóforos 6 Los colorantes usados en la industria textil son de diversos tipos y pueden ser clasificados dependiendo de varios factores, tales como su estructura química, clase de aplicación o uso final. Cada tipo de colorante presenta características físicas, químicas y biológicas diferentes, que les atribuyen propiedades recalcitrantes y efectos tóxicos para el ambiente. 3.1.1.- Colorantes naturales El índigo es el colorante natural más utilizado en todos los tiempos, incluso actualmente, debido a su solidez; resiste bien a la luz, al lavado, a los álcalis y ácidos. Se utiliza en teñido textil como colorante a la tina. El índigo es el colorante que mayormente se utiliza para el teñido de los jeans y prendas vaqueras azules. Esta sustancia se extrae de plantas del género indigofera (que se dan en el Asia Sur oriental, cultivadas y empleado como tal sobre todo en la India, para el algodón), que lo contienen en forma de glucósido; éste se hidroliza Figura 3.2 Composición química del índigo por ácidos o por fermentos en glucosa e indoxilo, se oxida de forma natural por el oxígeno (fig. 3.2) del aire y se transforma en el colorante índigo o añil. Figura 3.3 Madeja de hilo de seda teñido con índigo natural. Buri Ram, Surín Tailandia. 2010 7 Una vez que se consiguió aislar esta sustancia, su producción química ha hecho que el índigo como colorante artificial sea más barato y abundante que el natural. 3.1.2 Colorantes artificiales Son los más importantes en la industria textil. Muchos de ellos proceden de aislar en laboratorio las sustancias correspondientes a los mismos colorantes en estado natural. A continuación se enlistan la clasificación de estos. 3.1.2.1 Colorantes ácidos Son los utilizados para tenir fibras protéicas en medio ácido. Su grupo cromóforo es aniónico. De ellos, los azóicos son los tintes amarillos, anaranjados, rojos, escarlatas, marinos sólidos, algunos verdeoscuros, y marrones (mezclas de varios azóicos). Figura 3.4 Colorantes azóicos De los colorantes ácidos, los antranoquinónicos son los azules de buena solidez a la luz y a tratamientos en húmedo. Corren peligro de volver a oxidarse con la humedad ambiental una vez teñidos. Los trifenilmetánicos son los violetas, azules y verdes de tonos muy brillantes y moderadamente sólidos a la luz, mejor a los tratamientos húmedos. Estos colorantes tienen su índice de solubilidad (en agua) y su índice de afinidad en relación inversa. Por otra parte, a mayor solubilidad, mayor igualación pero menor solidez ante agentes húmedos. 3.1.2.2.-Colorantes básicos Tiñen las fibras animales (lana, seda) de forma directa; pero de entre las naturales vegetales, solo el yute tiene afinidad por estos colorantes. Dentro de las fibras artificiales celulósicas indirectamente, mordentadas con tanino; sólo el rayón nitro-seda tiene afinidad por los colorantes básicos. 8 En la tintura de estas fibras para controlar el proceso de tintura con colorantes básicos se utilizan agentes catiónicos-aniónicos adicionales. Estos agentes son sales de bases orgánicas que fuerzan al grupo cromóforo a unirse al catión, resultando el anión incoloro. Esta reacción química da como resultando tres grupos de colorantes básicos nuevos: o Colorantes con carga positiva deslocalizada; derivados del di y trifenilmetano. o Colorantes con carga catiónica localizada; de tipo antraquinónico o azoico, que poseen elevada solidez a la luz y buena estabilidad al pH. o Colorantes con estructura heterocíclica, conteniendo nitrógeno cuaternario; estos son solubles en alcohol etílico; menos solubles en agua. 3.1.2.3.- Colorantes directos Se llaman así porque tiñen la fibra sin necesidad de un segundo producto que actúe como mordiente de ésta. Existen dos familias de colorantes directos: a) colorantes azoicos b) colorantes tiazólicos Los colorantes azóicos son derivados de las aminas del difenilo en donde N puede ser: -HN-NHarildiaminas, enlace simple de bencidínicos -CH=CH- etilbénicos -NH-O-S-CONH-NH-CO-NH- R puede ser: -H SO3Na -Cl -NO2 -OH -CH3 -OCH3 -OCH2-CONa Los colorantes tiazólicos se llaman así porque en su molécula contienen el anillo tiazólico. Estos colorantes son solamente amarillos, anaranjados y pardos 9 Las características de los colorantes artificiales directos son las siguientes: Generalmente son solubles en agua, aunque algunos precisan para ello la presencia de carbonato sódico. Su solubilidad aumenta con el número de grupos sulfónicos y disminuye al aumentar su peso molecular. En frío forman soluciones coloidales. Los colorantes directos resisten bien a los ácidos, aunque tienden a enrojecer. En presencia de agentes reductores rompen su molécula hacia derivados aminados. 3.1.2.4.- Colorantes a la tina Son colorantes que tienen entre sí diferente constitución química pero todos son insolubles en agua. Por su reducción en un medio alcalino se transforman en leucoderivados hidrosolubles. El proceso de reducción se fundamenta en la acción reductora del hidrógeno sobre el grupo carbonilo, transfiriéndolo al grupo alcohólico. Figura 3.5 Colorantes a la tina Una vez realizado el teñido, es fácilmente oxidable por el oxígeno del aire. Estos colorantes dan teñidos más brillantes que los antraquinónicos, pero menos sólidos ante la luz y el lavado 3.1.2.5.- Colorantes dispersos Estos colorantes son compuestos orgánicos no iónicos. Se aplican con un dispersante, porque son insolubles en agua, y se caracterizan fundamentalmente porque tienen un alto grado de dispersión. Se emplean para la tintura de rayón, acetatos y poliésteres 3.1.2.6.- Colorantes sulfurosos Se llaman sulfurosos porque en su molécula está presente el azufre, pero no como lo está en los colorantes directos, tiazólicos, etc., sino que aquí este azufre puede ser oxidado con facilidad. Por su aspecto, los colorantes sulfurosos son parecidos a los colorantes de tina y a los 10 sustantivos; tiñen las fibras directamente en estado reducido y se combinan con los colorantes básicos para dar una laca insoluble; la cantidad de colorante absorbido depende de su porcentaje en la solución, de la concentración de sal en el baño y de la temperatura. Lo mismo que los colorantes de tina, también son insolubles en agua pero solubles en medio alcalino y en presencia de sulfuro sódico como agente reductor. Son colorantes muy económicos pero sus matices son muy pobres. Figura 3.6 Colorantes sulfurosos La Tabla 3.1 presenta la clasificación de los colorantes de acuerdo a su grupo cromóforo y la Tabla 3.2 la clasificación de los colorantes de acuerdo a su forma de aplicación. Tabla 3.1 Clasificación de colorantes de acuerdo a su grupo cromóforo Familia Grupo cromóforo Descripción Azoicos Estos colorantes se caracterizan por tener un grupo funcional azo, consistente en un enlace doble –N=N–, unido a átomos de carbono. En cuanto a sus propiedades de color, aportan un rango de matices prácticamente completo y alta intensidad de color. Presentan buenas propiedades técnicas: solidez a la luz, al calor, al agua y a otros disolventes. Antraquinonas Los colorantes a base de antraquinonas y quinonas aromáticas policíclicas tienen gran importancia ya que colorantes ácidos con solidez a la luz, mordentes y dispersos corresponden a esta categoría 11 Familia Grupo cromóforo Indólicos Descripción El compuesto progenitor del grupo de colorantes indigoides, es el índigo, es un colorante de uso común desde tiempos prehistóricos. El índigo natural se obtiene de una planta, la indigofera. Puede reducirse por fermentación así como por medio de hidrosulfito de sodio, una vez reducido puede aplicarse a fibras celulósicas para después oxidarlo y obtener teñidos azules de gran brillantez. Estos colorantes están caracterizados por un grupo cromóforo altamente estabilizado por resonancia, son uno de los colorantes más intensos y brillantes que existen, pero generalmente exhiben poca solidez a la luz Trihalometanos (EPA 1996; O´ Neil et al., 1999; Robinson et al., 2001; Hunger, 2003; Husain 2006; Gupta y Suhas 2009) Tabla 3.2 Clasificación de colorantes de acuerdo a su forma de aplicación Clase Ácidos Solubilidad Producto químico principal Aplicaciones % de fijación Probables contaminantes Solubles en agua Tipo azo, antraquinona, trihalometano Nylon, lana, seda, acrílicos modificados, y también en cierta medida para el papel, cuero, impresión de chorro de tinta, los alimentos y cosméticos 80-93 Ácidos orgánicos, aminas aromáticas Papel, nylon, poliéster modificado, seda, lana y el algodón tanino mordentado 97-98 Ácidos orgánicos, aminas aromáticas Poliéster, en cierta medida nylon, celulosa, acetato de celulosa y fibras de acrílico 80-92 Sales, surfactantes, fosfatos, lubricantes, dispersantes Algodón, rayón, cuero y en cierta medida en nylon 70-95 Aminas aromáticas, sales, surfactantes Generalmente se utilizan para el algodón y otros materiales celulósicos, pero también se utiliza en menor medida en lana y nylon 60-90 Aminas aromáticas, sales, surfactantes Algodón, rayón, tienen un uso limitado con fibras de poliamida, seda, cuero, papel y madera 60-70 Básicos Solubles en agua Dispersos No iónicos insolubles en agua Directos Solubles en agua, aniónicos Reactivos Solubles en agua Sulfurados Solubles en agua Mordentes Tipo azo, antraquinona, oxazina, triarilmetano Contienen azoicos, antraquinona, nitro y grupo benzodifuranona Contienen poliazo, ftalocianinas y oxazinas Contienen grupos cromóforos, como azo, antraquinona, triarilmetano, ftalocianina No poseen una estructura determinada Aminas aromáticas, álcalis, agentes oxidantes y reductores Aminas aromáticas, sales orgánicas, Solubles en agua Azo y antraquinona Lana y seda 85-98 halogenados, metales pesados, color no fijado (EPA 1996; O Neil et al., 1999; Robinson et al., 2001; Hunger 2003; Husain 2006; Gupta y Suhas 2009) 12 3.2.- Características de las aguas residuales de la industria textil con colorantes El principal problema ambiental derivado del aporte de color a las aguas de los ríos y lagos se debe a la reducción de la transparencia y la disminución del oxígeno disuelto, debido a que altas cargas de color dificultan la función fotosintética de las plantas. Adicionalmente algunos problemas asociados a los efluentes textiles son debidos a la presencia de metales pesados ó azufre, que producen problemas ambientales debido a su naturaleza tóxica. Se ha comprobado que algunos colorantes de naturaleza azoica presentan un carácter cancerígeno potencial, y al menos 3000 colorantes azo comerciales han sido catalogados como cancerígenos (Guaratini y Zanoni, 2000). Su toxicidad radica en que pueden dar lugar a las aminas aromáticas de las cuales derivan, debido a procesos de oxidación, hidrólisis ó reducción del enlace azo. Algunas aminas aromáticas utilizadas en la fabricación de los tintes son carcinógenos reconocidos (Weisburger, 2002), Greenpeace, 2012. La exigencia actual de la industria textil radica en la búsqueda de colorantes con estabilidad química y fotolítica, por lo que se diseñan colorantes resistentes a la ruptura debida a la exposición a la luz, agua, jabones, lo cual hace más complicado se degradación. El alto consumo de agua generando volúmenes de agua residual que representa un 90-95% del agua utilizada en el proceso (Blánquez, 2005) y las elevadas pérdidas como consecuencia de la incompleta fijación de los colorantes a las fibras representando un porcentaje de 200 t/d de estos compuestos al medio ambiente (Guaratini y Zanoni, 2000; McMullan et al., 2001). Las operaciones que contribuyen con la mayor descarga de desechos líquidos son el lavado, la tintura, el estampado y el acabado. Las aguas residuales textiles son irregulares y variables en su composición ya que dependen de la unidad de proceso y la operación que se efectué. Las industrias textiles son contaminantes en términos de volumen y complejidad de sus efluentes ya que cada una de las actividades que realizan genera agua residual de características muy variables. Además las aguas residuales textiles se caracterizan por tener pH que varía de acuerdo al proceso, altos valores de DQO, DBO, altos niveles de color, turbiedad, una alta concentración de sólidos suspendidos y descargas a altas temperaturas. Valores típicos de DQO y DBO para industrias dedicadas al acabado textil son 1700 mg O2/L y 550 mg O2/L respectivamente. Las aguas residuales de teñido y de procesos de acabado de la industria textil con una demanda química de oxígeno que exceda 1600 mg/l y que tenga un color muy oscuro es considerada agua residual altamente contaminada y fuente significativa de contaminación. (Aristizábal et. al, 2007). La carga contaminante del desengomado está dada por sólidos suspendidos y disueltos, grasas y aceites. Ésta etapa contribuye aproximadamente en un 50% del total de sólidos suspendidos producidos por la planta. En el mercerizado también se emplea sosa cáustica causando los mismos efectos sobre la carga contaminante que el desengomado. 13 En la etapa de descrude se emplea hidróxido de sodio o sosa cáustica, que causa una elevada alcalinidad y color grisáceo en el agua residual (color que es justificado por las impurezas aun presentes en la tela), por lo general no es posible recuperar este agente químico por los altos costos que esto conlleva. El blanqueo es realizado con peróxido de hidrógeno que contribuye poco con la carga contaminante. El aporte a la carga contaminante de los procesos de teñido es muy significativo y depende del tipo de colorante utilizado en el teñido, por lo general se presentan bajas cantidades de sólidos suspendidos y valores elevados de DQO y DBO. En la Tabla 2.1 se presentan valores típicos de la carga contaminante causada por diferentes colorantes. Tabla 3.3 Carga contaminante que aportan los colorantes Colorante Reactivos Directos Sulfurosos Tinas Litros de agua por Kg de tela 74-210 14-53 24-212 8-160 DQO (ppm) 150-400 440-1200 4200-14100 250-3000 Rodriguez, Oscar y Roldan, Jhon Jairo. Alternativas para eltratamiento de aguas residuales en tintorerías textiles: Caso PANTEX S.A.Medellín, 1997 El estampado presenta elevada DQO y DBO, alto contenido de sólidos y los valores de pH se encuentran entre neutro y alcalino. En general las aguas residuales del proceso de teñido contiene fibras textiles, tintes reactivos hidrolizados que no se fijan en las fibras y que representan entre un 20% y 30% del tinte aplicado, estos residuos de tintes son los responsables de la coloración del agua y no pueden ser reciclados. Además contienen tintes auxiliares, sustancias orgánicas que tampoco son reciclables y que son los responsables del alto nivel de DBO y DQO de los efluentes, también contienen electrolitos principalmente carbonato de sodio y cloruro de sodio. Este tipo de efluentes alcanza pH entre 10 y 11 y temperaturas entre 50 y 70ºC. Los procesos de teñido son de los que aportan mayor carga contaminante de los procesos textiles debido a que causan coloración de las aguas y a los colorantes que contienen sustancias tóxicas y cancerígenas. (Azzi, 2006) Tal coloración tiene un impacto negativo sobre la fuente de agua receptora, porque interfiere con la transmisión de luz a través del agua impidiendo la fotosíntesis de las plantas acuáticas (Lemley, 1994; Mejia, 2003). Estas aguas cambian de color con frecuencia ya que los tintes varían según los requerimientos del consumidor. 3.3.- Regulación de descargas de aguas residuales de la industria textil En México la escasa cobertura de infraestructura de los sistemas de tratamiento presentan deficiencias en la remoción de contaminantes por la mezcla de sustancias toxicas aportadas por las industrias que limitan los procesos de remoción, y aunado a lo anterior los estándares de 14 calidad del agua impuestos a través de la NOM-001-SEMARNAT-1996 provoca que las descargas de diferentes giros industriales en la mayoría de los casos cumplan con los parámetros y los contaminantes específicos de cada giro no sean tomados en cuenta provocando que la incorporación de sustancias tóxicas deteriore el ambiente acuático y cause la perdida de flora y fauna, así como los límites de uso del cuerpo receptor (Saldaña et al., 2001). Países como EUA y Canadá cuentan con legislación ambiental segura, algunos países de Europa como Francia, Austria e Italia tienen valores límites para las descargas de efluentes coloreados. Sin embargo, debido a que estos países utilizan unidades diferentes para su estimación, hace imposible una comparación. En Francia, las unidades que utilizan para realizar su determinación son mg/L Pt-Co (Hessel, 2007). 4.- Colorantes del tipo azo El color es parte de la percepción visual que depende de un estímulo luminosos y del observador. Para que una sustancia sea considerada colorante, además de poseer color debe poder transferirlo al medio al cual se aplica. Debido a la facilidad de su síntesis y a su versatilidad son los más importantes, perteneciendo a este grupo casi la mitad de los colorantes sintéticos. Están caracterizados por la presencia de uno o más grupos “azo” en su molécula. La estructura química de este tipo de colorantes, se caracteriza por la presencia del grupo azo – N=N- como un ente cromóforo, asociados a grupos auxócromos de tipo amino o hidroxilo. En principio, cualquier amina aromática primaria es capaz de generar azo-compuestos por un proceso llamado de acoplamiento. Esta reacción similar a otras sustituciones electrofílicas aromáticas requiere de una especie positiva (un átomo de nitrógeno de la sal de diazonio) y un sustrato o acoplamiento, receptor de la especie positiva que debe estar activado por un grupo donador de electrones (que incrementa su densidad electrónica) y además poseer hidrógenos fácilmente sustituibles. El proceso consta de dos pasos fundamentales: Formación de la sal de diazonio por diazotación de la amina primaria: Acoplamiento de la sal de diazonio con el sustrato acoplante Cualquier sustituyente sobre el radical R que incremente la carga negativa (densidad electrónica) también favorecerá esta reacción. Entre los grupos atractores de electrones se encuentran: -COOR, -CO, -COOH, -CN, -NO2, -SO3H y entre los donadores: -NH2, -OH, -CH3, etc. El acoplamiento RH es generalmente un compuesto aromático, por ejemplo naftoles, naftilaminas, dimetilanilina, pero también se puede acoplar sales de diazonio con sistemas heterocíclicos conjugados como índoles, pirroles, pirazolonas o quinolonas. 15 Otra manera general de sintetizar colorantes azo es mediante el acoplamiento oxidativo de hidrazonas heterocíclicas utilizando con preferencia agua oxigenada en presencia de sales ferrosas, ferricianuro de potasio, persulfato de amonio, tetra-acetato de plomo, etc. Para homogenizar el medio se utilizan con solventes como alcoholes de bajo peso molecular, glicoles, dimetilformamida y otros. Debido a la complejidad de los nombres químicos, los colorantes azo son raramente referidos únicamente a la nomenclatura de la IUPAC o CAS. La literatura técnica ha adoptado ambas clasificaciones, por la constitución química y por el color. Todo colorante azo comercialmente es identificado por el sistema de índice de color (Colour Index). A cada colorante se le da un nombre genérico, por ejemplo:marrón directo, que brevemente da información sobre la aplicación y color. Además del nombre genérico, cinco dígitos se le destinan ambiguamente para identificar la estructura química del colorante. En el sistema de “Ïndice de Color”, los colorantes azo se proveen con los números desde 11,000 a 39,999 que corresponden a la clase química siguiente: Mono azo (11,000 – 19,999), Diazo (20,000 – 29,999), Triazo (30,000 – 34,999), Poliazo (35,000 – 36,999), Azoico (37,000-39,99) (Ollegard H. et al., 1998). 4.1.- Clasificación de los colorantes azo Los colorantes azo pueden subdividirse en dos grupos: los iónicos y no iónicos. Aunque el máximo de absorción está en el rango de luz UV-visible, las presiones de vapor disponibles son muy bajas, en el rango de 10-20 a 10-8 mmHg. La hidrólisis es, a excepción de colorantes reactivos, muy baja. Sin embargo, los dos grupos exponen diferencias importantes. En general, los colorantes azo iónicos son casi completamente o parcialmente disociados en solución acuosa. Los colorantes azo no iónicos, por otra parte, son únicos por su baja solubilidad (<100 mg/L). El coeficiente de partición, Kow, estimado para los colorantes iónicos son generalmente muy bajo, p. ej. 10-5 para el Naranja ácido 10*, y 100 para el Negro Directo 38*. Sin embargo, los no iónicos tienen coeficientes de partición muy altos (Kow), p. ejemplo, 3630 para el azul disperso 79*, y 11220 para el Amarillo Solvente 2. Las aminas aromáticas (metabolitos), que están entre las impurezas de los colorantes azo y los subproductos generados en la degradación de los colorantes, generalmente tienen propiedades físico químicas que varían dentro de los siguientes cuatro grupos: anilina, toluidina, benzidina y naftaleno. La solubilidad de los metabolitos varía en forma similar desde casi insoluble a muy soluble. Los máximos de absorción están generalmente en el rango de 240 a 300 nm; esto es abajo del rango de la región UV-visible. Las presiones de vapor están en el rango de 7.5* 10-7 a 0.32 mmHg (Ollegaard H. et al., 1998). Considerando el número de grupos azo presentes en la molécula se tiene mono- diazo, triazo compuestos y policondensados, y en cada clase hay representantes de los diferentes grupos tintóreos. Debido a la abundancia de los colorantes de esta familia identificarlos de acuerdo con su constitución química resultaría demasiado complejo, especialmente para los poliazo y por 16 ello el CI ha adoptado una notación adicional que informa acerca de su síntesis: en cuanto a la sal de diazonio, representada por la amina precursora, al sustrato y a las condiciones de reacción (ácida o básica); utilizando un sistema de flechas para indicar la secuencia de condensaciones. Para planificar la síntesis de los colorantes azo debe considerarse cuál sistema aromático debe ser el sustrato y cuál el que aporta el grupo diazonio. Como regla general se acepta que la porción aromática que contiene grupos atractores de electrones corresponde a la de la sal de diazonio y que los donadores de electrones se ubican sobre el sustrato acoplante. Los colorantes diazo “secundarios” se preparan en etapas de acoplamiento consecutivas. Están subdivididos según el CI en cuatro grupos, dependiendo de la naturaleza del acoplamiento azoico y el componente diazo. El término azoico se reserva en la clasificación tintórea, a los colorantes azo producidos sobre la fibra. Es por ello que para identificar este grupo químico, en ocasiones se usa indistintamente la denominación “colorante azo” o “azoico”. Los colorantes poliazoicos, en su mayoría sustantivos para fibras celulósicas, están divididos en grupos con el mismo criterio que para los bis-azoicos. Debido a la acumulación de grupos azo predominan los colores verdes, azules y negros en contraste con los monoazo y diazo que exhiben amarillos, naranjas y rojos. 4.2 .- Características de los colorantes azo Asimismo, según su estructura molecular y propiedades específicas pueden ser colorantes azo ácidos, básicos, dispersos, directos y reactivos. La aplicación de este tipo de colorantes es muy variada y depende del proceso de teñido o estampado, pero en la mayoría de los casos se requiere aplicar calor y un mordente. Los colorantes dispersos azo tienen muy baja solubilidad en agua y son apropiados para fibras hidrofóbicas. De los colorantes dispersos, los azo constituyen casi la mitad de la producción, siendo las antraquinonas el otro grupo químico importante de esta clasificación tintórea. Se los utiliza para poliésteres, acetato de celulosa y nylon, porque cubren bien los defectos causados por la tejedura no uniforme, conocido como efecto “barré” (barras o listas en los tejidos). Las estructuras químicas son derivadas de aminoazobenceno con grupos alquilo, CN, NO 2 o Cl, en posiciones para la función diazo; si hay grupos NO2, CN, en posición orto al diazo los colorantes son muy estables a la luz, gracias a la formación de quelatos internos. Los colorantes se liberan en el medio ambiente por medio de dispersiones o soluciones coloreadas en los efluentes industriales de las industrias de su síntesis y textil como las principales. En esta industria, en los procesos de teñido se estima que la cantidad de colorantes que no se fija a las fibras depende del tipo de colorante usado y puede variar del 2 al 50% los 17 cuales son descargados en las aguas residuales de las plantas de tratamiento o directamente al ambiente (Stolz ,2001; Moeller, et. al., 2000). Para evaluar los efectos nocivos que pueden causar los colorantes si son descargados en un cuerpo receptor hay que considerar entre otros los siguientes factores: Las concentraciones de los colorantes descargados en los efluentes industriales y el tipo de molécula descargada, la toxicidad a macro y microorganismos en el cuerpo de agua y su posible acumulación en las cadena alimenticias y en el ambiente (Leist, 1982). 18 5.- Tecnologías utilizadas para el tratamiento de aguas residuales de la industria textil con colorantes Se sabe que aproximadamente el 15% del total de la producción de colorantes es perdida en los efluentes de industrias de síntesis y procesamiento. Los colorantes de tipo azo son los más utilizados. Aproximadamente corresponden al 70% de los colorantes utilizados. La persistencia del color en las aguas residuales representa uno de los mayores problemas ambientales ya que estos son generalmente visibles a concentraciones aún por debajo de 1 mg/L. Aún cuando la normatividad mexicana no regula en la descarga el color que éstos producen, por protección a los cuerpos de agua y ecosistemas, es importante su eliminación debido a la toxicidad de sus moléculas y a los efectos estéticos que el color causa. La literatura reporta diferentes tecnologías para la remoción del color, entre las que se encuentran los procesos químicos (oxidación con cloro, ozono, etc.), los procesos físicos (adsorción con carbón activado, radiación UVA, electroquímica) y los de tipo biológico (sistemas anaerobios y aerobios de biomasa suspendida y fija entre otros). Los procesos biológicos son más económicos y amigables con el medio ambiente, mientras que los físico-químicos son menos complicados pero más costosos. Por lo cual la presente investigación pretende retomar las ventajas de los diferentes tipos de procesos para obtener un sistema de tratamiento optimizado que combine elementos físico-químicos y biológicos en forma acoplada. El tratamiento de aguas residuales de la industria de colorantes y textil es un problema ambiental al que se le ha dado mucha atención ya que muchos colorantes textiles son tóxicos y no son biodegradables, y en consecuencia son descargados a canales y ríos permaneciendo en el ambiente. Muchos de los colorantes que existen en el mercado son xenobióticos, por lo que con frecuencia se necesita más que un proceso biológico de tratamiento para su remoción total y los subproductos generados en la remoción de colorantes, conocidos como metabolitos (aminas aromáticas, algunas potencialmente carcinogénicas), presentan problemas de toxicidad, por lo que se hace indispensable la mineralización del colorante (Vandevivere C. et al., 1998). En general existen métodos físicos-químicos y biológicos para el tratamiento de colorantes azo, sin embargo, debido a la alta estabilidad de estos colorantes, su degradación no es fácil. Los procesos físicos y químicos son la floculación, membranas de filtración, coagulación electrocinética, destrucción electroquímica, intercambio iónico, oxidación química y diferentes técnicas de adsorción. Una revisión de las diversas tecnologías y técnica de tratamiento, y su eficiencia en la degradación de compuestos xenobióticos ha sido dada por Matsumoto et al., 1995. Sin embargo, Banat et al., 1996 y Pulgarin et al., 1999, concluyen que se necesitan más de 18 un proceso de tratamiento para la decoloración de un agua con colorantes recalcitrantes, los cuales probablemente involucran una combinación de diversos métodos. Pulgarin et al., 1999, indica que lo más viable es la combinación de un proceso físico-químico con un proceso biológico oxidativo. A pesar de que estos procesos físicos y químicos producen efluentes de buena calidad, en la mayoría de las ocasiones generan un alto costo mientras que el tratamiento biológico resulta más económico. (Quezada et al., 1999; Cruz et al., 1996; Kuppusamy,I.et. al.1996). En cuanto a la biodegradación de los colorantes del tipo azo, en años recientes se ha intensificado el estudio y las investigaciones sobre procesos biológicos y se ha llegado a demostrar que existen algunos microorganismos que son capaces de atacar el enlace azo de estas moléculas logrando la descomposición del grupo cromóforo y reduciendo o eliminando el color y bajo ciertas condiciones, también se ha demostrado en algunas ocasiones su total mineralización. Las principales procesos para la decoloración de este tipo de efluentes se puede dividir en 3, físicos, químicos y biológicos. En las Tablas 5.1, 5.2 y 5.3 se realiza una breve descripción de cada uno de los tratamientos empleados en la decoloración de efluentes de la industria textil así mismo las ventajas y desventajas que cada uno ellos presentan. 5.1.- Tratamientos biológicos Debido a las desventajas que presentan los tratamientos fisicoquímicos, se ha generado un gran interés por buscar otros procesos y condiciones de operación por medio de los cuales sea posible mineralizar los colorantes azo. Los procesos biológicos bajo diferentes condiciones de concentración de oxígeno como los procesos anaerobios, aerobios y la combinación de estos, pueden degradar ciertos colorantes (procesos biológicos convencionales). Asimismo, recientemente se ha dado importancia a la investigación sobre cierto tipo de procesos biológicos no- convencionales como son el uso de hongos del tipo de los Basidiomicetos y de las enzimas del tipo de las peroxidasas extraídas de ciertos productos naturales. 5.1.1.- Tratamiento biológico convencional El tratamiento biológico convencional para el tratamiento de aguas residuales municipales e industriales biodegradables hace uso de un consorcio microbiano cuya población mayoritaria es de bacterias heterótrofas o degradadoras de materia orgánica. Los colorantes azo son generalmente persistentes bajo condiciones aeróbicas y, en condiciones anaeróbicas, este tipo de colorantes sufren una reducción por acción de bacterias anaerobias produciendo aminas aromáticas, las cuales son recalcitrantes en los sistemas de tratamientos anaeróbicos y requieren condiciones aeróbicas para su degradación mediante un consorcio de bacterias cuyo aceptor final de electrones es el oxígeno molecular presente debido a las condiciones aeróbicas del sistema. 19 En este tipo de tratamiento de compuestos tóxicos, muchas veces se hace necesario la presencia de un co-sustrato. La reducción anaeróbica del grupo azo es no especifica, por lo que para el tratamiento de este tipo de moléculas se requiere entonces una etapa anaeróbica y luego una aeróbica para lograr en primera instancia el rompimiento del grupo azo, cromóforo y luego en una segunda etapa, la mineralización de las aminas producidas en la primera etapa. El grado de degradación de un colorante va a estar determinado por la estructura del mismo (Quezada, et al., 1999; Van der Zee, et al., 1999; Bishop, 1996, Kulla, 1981; Pagga & Brown 1986. 20 Tabla 5.1 Procesos físicos empleados en el tratamiento de efluentes de la industria textil Proceso Descripción Adsorción La eficacia del proceso de adsorción está influenciada por una gran variedad de parámetros, entre ellos la interacción entre el colorante y el soporte, superficie específica, tamaño de la partícula, temperatura, pH o tiempo de contacto. La eficacia del método depende en gran medida del tipo de soporte elegido. Se emplean tanto soportes inorgánicos como orgánicos. Los primeros tienen una gran estabilidad mecánica y química, alta superficie específica y alta resistencia a la degradación microbiana. Los soportes orgánicos se generan a partir de fuentes renovables o son residuos industriales. Coagulación floculación Membranas de filtración Ventajas Desventajas Fuente Los procesos de adsorción generan efluentes de alta calidad. Aplicable a diferentes colorantes (ácidos, básicos, reactivos). Posibilidad de reutilización del agua dentro del proceso. Capacidad de tratamiento del orden de cientos de m3/d. Son procesos lentos; no selectivos, de manera que hay una competición entre las moléculas del colorante y otros compuestos presentes en el efluente; no destructivos, generándose un residuo que debe ser eliminado. La desorción es un proceso muy difícil y costoso. Los adsorbentes suelen ser caros y en ocasiones requieren un proceso de activación previo Hai et al., 2007 Allegre et al., 2004 Forgacs et al., 2004 Rai et al., 2005 Gulnaz et al., 2006 Este proceso se basa en la adición de polielectrolitos ó floculantes inorgánicos (sales de hierro o aluminio), que forman flóculos con las moléculas de colorante facilitando su eliminación por sedimentación. Este proceso es eficiente al tener altos porcentajes de remoción de color. El equilibrio del sistema se alcanza en tiempos cortos de 2-4 horas. Los métodos de tratamiento basados en el empleo de membranas permiten una separación efectiva de las moléculas de colorante y otros compuestos de tamaño mayor al del poro de la membrana seleccionada. Los métodos, tales como microfiltración, ultrafiltración, nanofiltración, ósmosis inversa y la adsorción, son altamente eficientes. Aplicable a un número amplio de colorantes. Resulta factible con la combinación de procesos biológicos y de oxidación avanzada. La fracción de rechazo de la membrana puede ser incinerada favoreciéndole balance energético del proceso 20 El proceso genera lodos que deben ser eliminados. Los mejores rendimientos se logran al aplicar un exceso de coagulante, que aumenta la concentración de contaminante en el efluente. Este proceso no es eficiente para colorantes altamente solubles y el resultado con colorantes azoicos, ácidos, reactivos generalmente no son muy buenos. Costo elevado. Altos costos energéticos del tren de tratamiento. Generación de lodos tóxicos. Taponamiento de las membranas. Adsorción del colorante sobre la membrana Lee et al., 2006 Mishra y Bajpai, 2006 Yue et al., 2008 Shi et al., 2007 Wang et al., 2006a Zhou et al,. 2008 Hai et al., 2007 Rai et al., 2005 Hai et al., 2007 Zhang et al., 2009 Gomes et al., 2005 Tabla 5.2 Procesos químicos empleados en el tratamiento de efluentes de la industria textil Proceso Descripción Ventajas Oxidación química La oxidación química emplea agentes oxidantes como el ozono (O3), peróxido de hidrógeno (H2O2), permanganato (MnO4), Cloro y Reactivo Fenton, para cambiar la composición química de un compuesto o grupo de compuestos Tiempos de reacción bajos en min. Posibilidad de combinación con procesos de oxidación avanzada. Aprovechamiento de las sales presentes en el influente. Puede ser utilizado como alternativa de pretratamiento económica ozonización Las técnicas de ozonización consisten en la destrucción de compuestos con base a la elevada capacidad oxidativa del ozono. La reacción de oxidación es rápida, se pueden tratar altos caudales, no se generan residuos ni lodos y se obtiene un efluente incoloro y con baja DQO, de manera que es apto para su vertido al medio ambiente Algunos autores sugieren que este proceso puede ser utilizado para el reuso del agua ya que puede llegar a remover el color en su totalidad y la DQO hasta cierto punto, incluso en condiciones críticas como el teñido con tonos claros. Corto tiempo de vida aproximadamente de 20 min, lo cual repercute fuertemente en el coste del proceso. Los compuestos generados tienen mayor carácter tóxico que los colorantes de partida. Soares et al., 2006 Wu et al., 2008b Sundrarajan et al., 2007 Foto-Fenton El reactivo Fenton es una combinación de H2O2 y sales de Fe (II). El ion ferroso se oxida a férrico mientras el H2O2 produce iones hidróxido y radicales hidroxilo. Estos últimos oxidan al colorante y el compuesto formado precipita con el ion férrico y compuestos orgánicos. Es eficiente en la decoloración de colorantes solubles como insolubles. Tiempo de residencia cortos. Formación de lodo mínima. Aplicación exitosa en procesos a escala piloto y semi-indiustrial. Generación de lodos debida a la floculación de los reactivos con el colorante. Elevados costos de los reactivos Meric et al., 2003 Cheng, 2004 Pignatello et al., 2006 Papadopoulos et al., 2007 21 Desventajas Fuente Generación de efluentes más tóxicos. Costos elevados de materias primas. Metcalf y Eddy, 2003. Aleboyeh et al., 2009 Li et al., 2009 Tabla 5.3 Procesos biológicos convencionales empleados en el tratamiento de efluentes de la industria textil Proceso Descripción Aerobios Pocos estudios han reportado que los colorantes azo pueden ser utilizados por las bacterias aerobias como fuente de carbono y energía. Por lo general, los tratamientos aerobios basados en consorcios de bacterias en sistemas convencionales no son capaces de degradar colorantes procedentes de efluentes textiles Sin embargo se ha conseguido aislar cepas de bacterias que son capaces de degradar algunos colorantes. Anaerobios Este proceso ha sido empleando en gran medida para el tratamiento de colorantes ya que ha demostrado una gran eficiencia de decoloración. La decoloración de compuestos azo mediante este proceso no es considerada especifica debido a que diversas cepas pueden romper el enlace azo de manera eficiente. Desde sus investigaciones en 1970 se han reportado trabajos con altas eficiencias de decoloración. Es importante destacar que el tipo de reactor, el tiempo de retención hidráulica, el origen y la estrategia de aclimatación del inóculo, la presencia de mediadores redox, así como el tipo y la concentración de co-sustrato juegan un papel importante en la eficiencia de decoloración. Ventajas Económicos y con una infraestructura disponible en algunos casos. Capacidad de tratamiento del orden de m3/d. Impacto ambiental bajo. Posibilidad de aplicación de mediadores redox para mejorar el porcentaje como la velocidad de decoloración. Factibilidad de bio-aumentación de los cultivos. 22 Desventajas El mecanismo primario de remoción es la adsorción sobre la pared celular. La reducción de la DQO no está correlacionada con la decoloración del efluente. Altos tiempos de retención hidráulica. Inhibición por compuestos recalcitrantes Generación de subproductos tóxicos. Requerimiento de cepas especificas. Bajas remociones de materia orgánica expresada como DQO. Probable efecto recalcitrante de los auxiliares del proceso de tinción. Largos periodos de aclimatación. Los colorantes y otros compuestos refractarios no se mineralizan, Los micronutrientes presentes en las aguas residuales como N y P no se remueven mediante este sistema Los sulfatos dan lugar a sulfuros. Fuente Robinson et al., 2001 McMullan et al., 2001 Buitrón et al., 2004 Stolz, 2001 Tan, 2001 Pandey et al., 2007 Delee et al.,1998 Forgacs et al., 2004 Rai et al., 2005 van der Zee, 2005 Rai et al., 2005 Razo Flores et al., 1996 Proceso Descripción Ventajas Desventajas Fuente Acoplados Cuando se conocen las bondades, capacidades y limitaciones de diferentes tipos de tratamientos, físicos, químicos y biológicos, es conveniente utilizar las ventajas encontradas en cada uno de ellos y combinarlas en tratamientos que se denominan acoplados. Los tratamientos acoplados, ya sea combinando procesos fisicoquímicos y biológicos o sólo biológicos (anaerobio-aerobios) son una buena alternativa para el tratamiento de estos efluentes. Mineralización completa que a menudo se logra gracias a la acción sinérgica de diferentes organismos. la reducción del enlace azo se puede lograr en las condiciones de reducción en biorreactores anaeróbicos y las resultantes aminas aromáticas incoloras puede ser mineralizada en condiciones aeróbicas Tiempos elevados de residencias en fase anaerobia. Requerimientos de cepas especificas para degradar colorantes específicos. Uso de co-sustratos. Persistencia de las aminas aromáticas. Cruz et al., 1996 Moeller y Garzón, 2006 Melgoza, 2004. López Ayala 2004. Stolz, 2001. Buitrón et al., 2004 van der Zee,2005 23 5.1.2 Tratamiento biológico no convencional 5.1.2.1.- Tratamiento fúngico Como ya se ha mencionado, en últimas fechas se ha dado importancia al grupo de los hongos Basidiomicetos, ya que se determinó que ciertas enzimas del tipo oxidasas producidas por estos organismos son capaces de oxidar moléculas recalcitrantes, entre ellas las moléculas de colorantes. Bumpus y Brock (1998) determinaron que la lignino-peroxidasa lleva a cabo la Ndes-metilación del cristal violeta. Este, junto con otros colorantes del tipo del trifenilmetano, como la benzen-amina, rojo cresol, azul de bromofenol, violeta de etilo, verde de malaquita y verde brillante, son biodegradados en cultivos de Phanerochaeta chrysosporium bajo condiciones de limitación de nitrógeno. Colorantes del tipo azo: naranja II, tropaeolin O, rojo congo y un colorante heterocíclico azure B, también fueron decolorados por cultivos de P. chrysosporium. Pasti-Grigsby et al. (1992), compararon la capacidad de decoloración en cultivos de diferentes especies de actinomicetos (Streptomyces spp.) y cultivos en condiciones de limitación de nitrógeno de P. chrysosoporium con 22 colorantes tipo azo. Demostraron que los estreptomicetos tenían la capacidad de decolorar aquellos colorantes que también eran oxidados por la Mn (II) peroxidasa producida por P. chrysosoporium. a) Biodegradación de colorantes tipo azo Hasta 1981 se había reportado que los colorantes no se degradaban por medio de procesos aeróbicos. Sin embargo, Kulla (1981) menciona que con un proceso adecuado de aclimatación, la degradación aerobia resulta factible. Los tratamientos aerobios pueden degradar muchos colorantes azo, como por ejemplo el Anaranjado ácido 7 (AA7), Anaranjado ácido 8 (AA8), Anaranjado 24, Amarillo ácido 151 (AA151), Rojo ácido 18 (RA18) y otros. Sin embargo, únicamente los colorantes AA7 y AA8 fueron mineralizados (formación de CO 2 y agua) bajo condiciones aerobias (Jian y Bishop, 1994). b) Experimentos de la degradación de colorantes por Pleurotus ostreatus(P.O.)y otros géneros fúngicos Los hongos también han sido utilizados para la inoculación de biofiltros, los cuales proporcionan varias ventajas en comparación con los biofiltros inoculados con bacterias, entre ellas una mayor resistencia a la acidificación y una mayor superficie de contacto. Los primeros reportes de degradación aerobia de colorantes azo mediante hongos blancos de la putrefacción apareció en 1990, cuando Crippset al., (1990) demostraron que una limitante de nutrientes en los cultivos de Phanerochaete chrysosporium daba como resultado la decoloración del colorante azo Naranja Ácido 7. En (1992) Pasti- Grigsby realizó un ensayo en donde probó la decoloración de 22 colorantes azo por S. chromofus y P. chrysosporium. En tal estudio obtuvo que P. chrysosporium es viable para decolorar 19 colorantes tipo azo. Encontró que el colorante 23 amarillo ácido 9 puede ser degradado en un rango de 85 al 99% a concentraciones de 150ppm. Esto ha sido comprobado no solamente con P. chrysosporium sino que también con otros varios hongos principalmente del género de la podredumbre blanca (Geotrichumcandidum, Tremetesversicolor, Bjerkandera adusta, Penicilliumsp., Pleurotusostreatus, Pycnoporuscinnabarinus, y Pyriculariaoryzea) que son capaces de decolorar soluciones de colorantes azo con estructuras químicas más complejas. Estudios más recientemente han demostrado que enzimas excretadas por Grifola frondosa son capaces de decolorar, colorantes azo como el Azul brillante de remazol R y el azul de bromofenol (Nitheranont et al., 2011). Los hongos de la podredumbre blanca (como lo son Pleurotusostreatus y Phanerochaetechrysosporium) han sido utilizados ampliamente para la degradación de muchos contaminantes e incluso los más complejos; esta capacidad de degradación de xenobióticos es ampliamente relacionada con la actividad ligninolítica y las enzimas que segregan estos hongos. El hongo Pleurotus ostreatus posee la capacidad de degradar grandes polímeros (lignina y celulosa) que constituyen el substrato vegetal, así como contaminantes ambientales mediante la secreción de un complejo enzimático. La efectividad de degradación depende en gran medida de las oxidoreductasas extracelulares y los metabolitos secundarios de bajo peso molecular. Tres diferentes familias enzimáticas han sido caracterizadas en este género: Manganeso peroxidada, Versátil peroxidada, y Lacasa. Gracias a la presencia de todas estas enzimas, Pleurotus ostreatus ha sido usado en biorremedición de sustancias toxicas (Cohen et al., 2002). Rodríguez et al. (1999) hicieron comparaciones entre 15 diferentes cepas de hongo para evaluar su capacidad de decoloración sobre algunos colorantes. Entre los géneros estudiados se encontraba Phanerochaete, Pleurotus y Trametes. Siendo estos dos últimos los que más altos valores de decoloración presentaron. En este estudio se identificó a la lacasa como la enzima responsable de dicha decoloración. La utilización de hongos del género Pleurotus para la degradación de xenobióticos, en este caso el colorante (Buitron,1996), se basa en la inespecificidad del sistema degradativo desarrollado por estos hongos para despolimerizar y mineralizar la lignina, polímero aromático estructuralmente relacionados con muchos compuestos que causan problemas de contaminación al ambiente; esta capacidad de Pleurotus y otros hongos se debe a la presencia de enzimas extracelulares como la Manganeso- Peroxidasa (MnP), y la lacasa (Renhammar y Malstrom,1981). Moeller y Garzón (2003) realizaron una comparación entre 3 diferentes tipos de hongos basidiomicetos: Pleutorus ostreatus, Phanerochaete chrysosporium y Colorius versicolor. Los resultados demostraron que Pleurotus ostreatus tiene un mayor porcentaje de remoción de color en comparación con los otros dos, por lo que se utilizó como inóculo en reactores empacados con turba. Dávila (2005) reportó que Pleutorus ostreatus y Phanerochaete 24 Chrysosporium son capaces de decolorar entre un 60 y 90% al naranja ácido 24 (colorante azo) en medio de cultivo líquido. También reportó que reactores empacados con turba funcionan de manera óptima al servir como soporte al micelio de hongos ligninolíticos, representar una fuente alterna de nutrientes y presentar procesos de sorción de colorantes. También Dellamatrice et al., (2005) en su investigación sobre decoloración de un efluente municipal que contenía aguas domésticas y de origen textil reportó que P. ostreatus disminuye la toxicidad de sus efluentes. Realizaron ensayos con P. ostreatus estéril y sin esterilizar. En los cuales observaron que Pleurotus ostreatus (P.O.) disminuye la toxicidad por un proceso diferente de la adsorción. La figura 5.1 presenta una imagen de Pleurotus ostreatus. Figura 5.1 Pleurotus ostreatus Rodríguez (2006) realizó un estudio para la selección de cepas de P.ostreatus con potencial para el tratamiento de aguas coloreadas. Con este objetivo realizó una estrategia de selección basada en parámetros como el índice de crecimiento a temperatura ambiente, en medios colorantes y residuos coloreados. Además ensayó la decoloración de los residuos líquidos de destilería (vinaza) y del cultivo de setas comestibles (extracto líquido de pulpa de café), mediante el cultivo sumergido de este hongo. En ambos casos la remoción del color fue del 50% con las cepas 3022 y 3024. También en el (2006) Gómez demostró que los complejos enzimáticos ligninolíticos presentes en P. ostreatus tienen potencial aplicación en la degradación de residuos xenobióticos. En su estudio la decoloración del Azul Brillante Ramazol R con P. ostreatus fue monitoreada espectrofotométricamente a 592nm. En el estudio obtuvo que a concentraciones de 1 mMH 2O2 y pH 4 fueron las mejores condiciones para la decoloración del Azul Brillante Ramazol R. Alatorre (2007) menciona en su trabajo sobre diseño de reactores que el reactor con una relación geométrica 6:1 (altura: diámetro) posee mejor desempeño en la remoción de color y un mejor funcionamiento hidráulico ya que presenta una menor cantidad de zonas muertas. También argumenta que el tiempo de retención hidráulico ideal para la remoción de color se encuentra entre 12 y 24 horas, tiempo en el que se remueven valores arriba del 50% del color. Además comprobó en su trabajo la viabilidad de Pleurotus ostreatus dentro del sistema para 25 decolorar y las propiedades físicas de la turba tal como absorción, absorción y decoloración ayudan a la remoción de contaminantes. Faroco et al., (2009) demostraron en su trabajo sobre bioremediación de aguas residuales con colorantes industriales que P. ostreatus es capaz de decolorar el 40% y el 60% de colorantes ácidos en agua residual. En el 2009 Garzón en su trabajo reportó que el tratamiento realizado con P. ostreatus fue el más efectivo en la remoción del colorante antraquinoi de Azul disperso 3, el cual presentó un porcentaje de remoción de 62,39%. Teixteira (2010) reportó que las lacasas producidas por Pleurotus ostreatus son eficientes para remover concentraciones de 240ppm Drimaren Blue X-3LR y Drimaren Blue X-BLN en un 96.99 y 68.02%. En el mismo año Papinutti y Forchiassin (2010) en su investigación de decoloración con residuos sólidos provenientes de la producción de Pleurotus ostreatus, encontraron que las enzimas manganeso peroxidada y lacasa eran capaces de decolorar el 100% del azure B (colorante heterocíclico) y carmín índigo (colorante índigoide). La concentración de decoloracion fue 0.4 g/l de colorante y en un rango de temp C. Landolo (2011) realizó un estudio para la decoloración de aguas residuales. Mediante una fermentación en un reactor de lecho fijo con P. ostreatus colonizado en residuos de manzana. En su ensayo obtuvo un 50% de decoloración. Muchos estudios muestran que las enzimas ligninolíticas de los hongos de la pudrición blanca como P. ostreatus tienen la habilidad de degradar compuestos recalcitrantes y que son viables para la decoloración de varias clases de colorantes industriales (Robinson et al., 2001). Garzón (2003) realizó una investigación sobre la remoción de contaminantes a través de la biofiltración sobre turba de 3 diferentes tipos de aguas residual: Agua residual de una granja porcícola, agua con colorante naranja ácido 24 y agua residual de un complejo petroquímico. La remoción de DQO para el influente de colorante y granja porcícola fue mayor del 90%. En la tabla 5.4 se presentan algunos procesos no convencionales con algunas de las tecnologías descritas anteriormente. 26 Tabla 5.4 Algunos procesos no convencionales utilizados para el tratamiento de aguas residuales de la industria textil (Casos de estudio sobre las tecnologías usadas para la remoción de colorantes por P. ostratus) Título Remoción de materia orgánica y decoloración Descripción Desarrollo de tecnologías no convencionales para el tratamiento de efluentes de la fabricación de colorantes tipo azo. Con P. ostreatus y P. chrysosporium se obtuvo una decoloración de 12.5% Y con C. versicolor19.2% Moeller y Garzón, 2003. Decoloración de efluentes y lodos urbanos por Pleurotussajor-caja y Pleurotusostreatus. Reportaron que: P. ostreatus no produce una decoloración de lodos y efluente. P. ostreatus reduce el contenido de carbono en lodos. P. ostreatus disminuye la toxicidad de los efluentes por medio de mecanismos diferentes de la adsorción. Pleurotus sajor-cajuF2 y F6 son viables para la decoloración de lodos. Las 3 cepas producen grandes cantidades de lacasa y manganeso peroxidasa en presencia de lodos. La decoloración del azul brillante remazol R por el extracto enzimático fue del 100% a una concentración de color de 0.2 % (V/V) a un pH de 4. Realizaron una comparación entre P.ostreatus, P. chrysosporiumy C. versicolor. Donde midieron la remoción de color. P. ostreatus demostró mayor remoción de color (colorante ácido 24 a una concentración de 250 mg/l) y lo utilizaron en reactores empacados con turba. En su investigación sobre decoloración de un efluente municipal que contenía aguas domésticas y de origen textil utilizaron 3 cepas de Pleurotus sajor-cajuF2 y F6 y Pleurotusostreatus. Realizaron ensayos con P. ostreatus estéril y sin esterilizar en los cuales evaluaron espectrofotométricamente la decoloración y con Hydraattenuata. Además hicieron ensayos de actividad enzimática para lacasas y manganeso peroxidada. En su trabajo ellos obtuvieron un extracto enzimático y midieron la actividad enzimática de la peroxidada y lacasa. Además determinaron la concentración óptima de peróxido de hidrógeno y pH en donde trabajan mejor las enzimas. En su estudio la decoloración del Azul Brillante Ramazol R con P. ostreatus fue monitoreada espectrofotométricamente a 592nm Evaluaron la capacidad de decoloración de P. ostreatus y Phanerochaete chrysosporium en aguas residuales con colorantes de la industria. Realizaron ensayos enzimáticos donde midieron la actividad enzimática la lacasa, manganeso peroxidasa, ligninoperoxidasa. La decoloración fue evaluada espectrofotométricamente Este estudio comparó la acción de una lacasa comercial con un extracto enzimático de Pleurotus ostreatus para la decoloración de Drimaren azul X-3LR (DMBLR), Drimaren azul X-BLN (DMBBLN), DrimarenRubinol X-3LR (DMR), y Drimaren azul CR (rbbr). La remoción del color y la actividad enzimática fueron evaluadas espectrofotométricamente. Realizaron un estudio para la decoloración de aguas residuales. Mediante una fermentación en un reactor de lecho fijo con P. ostreatus colonizado en residuos de manzana. La decoloración se evalúo por la diferencia del espectro de absorción. Gómez y Matheus 2006. Biodegradación del Azul Brillante Remazol R por un complejo enzimático producido por Pleurotusostreatus. Bio-remediación de aguas residuales coloreadas de la industria por hongos de la podredumbre blanca Phanerochaete chrysosporiumyPleurotusostreatus y sus enzimas. P. ostreatus es capaz de decolorar el 40% y el 60% de colorantes ácidos en agua residual a una concentración de 0.10g/l de colorante. Extracción y aplicación de las lacasas de setas Shimeji (Pleurotus ostreatus) para la decoloración de residuos de los colorantes reactivos y un estudio comparativo con lacasa comercial de Aspergillus oryzae. P. ostreatus es capaz de remover concentraciones de 240ppm Drimaren Blue X-3LR y Drimaren Blue X-BLN en un 96.99 y 68.02%. Fermentación fúngica de estado sólido de desechos agroindustriales para la decoloración de aguas residuales ácidas en un reactor de lecho fijo. En su ensayo obtuvo un 50% de decoloración a una concentración de color de 100mg/l 27 Fuente Dellamatrice et al., (2005). Faroco et al., 2009 Texteira et al., 2010. Landolo et al., 2011. c) Utilización de Pleutorus ostreatus para inóculo de biofiltros con turba. Los hongos ligninolíticos, denominados hongos de la pudrición blanca de la madera, comprenden un grupo de organismos cuya característica es su eficiencia en mineralizar eficientemente la lignina. Estos organismos secretan varias enzimas extracelulares que son esenciales para la transformación inicial de la lignina y que en conjunto logran su mineralización. El mecanismo del sistema degradador de la lignina está basado en la producción de radicales libres. Este mecanismo permite que estas enzimas sean catalíticamente activas sobre una gran diversidad de sustratos orgánicos. El mecanismo enzimático se da por la acción de oxidasas y peroxidasas, como estas enzimas no presentan especificidad alta, pueden tener actividad sobre la estructura de diferentes sustratos fenólicos y azo (Robison et al., 2001). Pleurotus ostreatus es responsable del reciclaje del carbono proveniente de la lignina, presenta enzimas poco específicas con un uso potencial en la transformación de compuestos contaminantes y xenobióticos. Se ha reportado que los complejos enzimáticos producidos por Pleurotus ostreatus pueden decolorar azul brillante de remazol en porcentajes altos en un rango de pH de 4 a 5 (Gomez et al., 2006). Las razones por las que es más viable remover color del agua residual proveniente de la industria utilizando un reactor empacado con una cama de turba son: Las plantas de tratamiento de aguas residuales convencionales, tienen baja eficiencia de remoción para colorantes, lo cual conduce a aguas coloreadas en las fuentes receptoras de los efluentes de la industria de colorantes y textil. Como consecuencia se han establecido nuevas restricciones para las descargas de efluentes coloreados (Vandevivere et al., 1998) Las características de esta tecnología (simplicidad, eficiencia y economía) hacen de ella una bioalternativa adaptada al contexto socio-económico de un buen número de países ya que reduce los costos de inversión, operación y mantenimiento asociados a los sistemas convencionales de tratamiento de aguas residuales (Buelna, 1994) 5.1.2.2. – Tratamiento con enzimas del tipo de las peroxidasas Hasta la fecha, la mayoría de las investigaciones de biodegradación o degradación enzimática de colorantes, se ha centrado en el estudio de colorantes tipo azo y sus variedades. En ocasiones, se ha concluido que es más factible el sintetizar colorantes con estructuras químicas que se adapten a las características de los sistemas biológicos o a las propiedades de las enzimas ya conocidas, que el explorar y localizar un sistema capaz de llevar a cabo la degradación de la mayor variedad de colorantes sintéticos ya existentes. (Moeller-Chávez y Garzón-Zúñiga, 2003). 28 En los últimos años se han realizado estudios de métodos enzimáticos para la remoción de compuestos recalcitrantes, cuando no pueden ser eliminados por tratamientos biológicos o físicos, esto mediante el uso de peroxidasas y peróxido de hidrógeno (Villalobos y Buchanan 2002, Villegas et al., 2003), ya que presentan ventajas por ser altamente selectivas (Aitken, 1993), son menos probables a que se inhiban por sustancias que pueden ser tóxicas para los organismos vivos y su costo podría llegar a ser inferior a la de otros métodos. Por otra parte, requiere bajos tiempos de retención con respecto a otros tratamientos (Siddiqueet al., 1993). A diferencia de los tratamientos biológicos las enzimas son aplicables a una extensa gama de compuestos; actúan en presencia de sustancias tóxicas para los microorganismos; poseen un amplio rango de acción de pH y temperatura; no necesitan aclimatación y no generan biomasa y, necesitan procesos de control más simples (Wagner y Nicell, 2002). En comparación con los tratamientos físicos y químicos, su funcionamiento no es corrosivo y reduce el consumo de compuestos oxidantes. Las enzimas que han presentado mayor utilidad en el tratamiento de compuestos recalcitrantes y de efluentes coloreados son: Peroxidasa, Lignina Peroxidasa, Manganeso Peroxidasa, Lacasa y Azoreductasa (Husain, 2006). En la Tabla 5.5 se presentan una lista de enzimas y su principal aplicación en el tratamiento de residuos orgánicos. Tabla 5.5 Enzimas y su principal aplicación en el tratamiento de residuos orgánicos Enzimas Azoreductasa Pseudomona ssp. Cloro-peroxidasa Caldariomyces fumago Cyanidasa Alcaligenes denitrificans Aplicación Degradación de colorantes Oxidación de compuestos fenólicos Descomposición de la cyanida Lacasa Trametes versicolor Soya Fenoles, aminas aromáticas, colorantes sintéticos Lignina peroxidasa Phanerochaete chrysosporium Fenoles, aminas aromáticas, colorantes sintéticos Bacterias Phanerochaete chrysosporium Basidiomycetes Raices de rábano, tomate, hongos blancos, soya. Pleurotus ostreatus Ipomea palmata Saccharumspontaneum Coprinuscinereus Oxidación de compuestos aromáticos y fenoles, colorantes azo Manganeso peroxidasa Peroxidasa Fuente Oxidación de compuestos aromáticos, fenoles y sus derivados, colorantes sintéticos, colorantes reactivos 29 Referencia Husain, 2006 Aitkenet al., 1993. Basheeret al., 1992. Duran y Esposito 2000; Duran et al., 2002;Christian et al., 2005; Husain 2006 Christian, 2005; Husain, 2006, Yuet al., 2006; Park et al., 2006; Kalmeet al., 2007; Park et al., 2007. Duran et al., 2002; Christian et al., 2005; Eibeset al., 2005; Husain, 2006; Babarovaet al., 2006. Shaffiquet al., 2002; Gudeljet al., 2002; Mohan, 2005; Akhtaret al., 2005a, 2005b; Husain 2006; Kulshretha y Husain 2007; Matto y Husain, 2007. a) Peroxidasas Las peroxidasas (EC 1.11.1.7) son oxidorreductasas que se encuentran distribuidas en el reino vegetal, los tejidos animales y microorganismos. Catalizan la oxidación de un amplio número de sustratos orgánicos e inorgánicos, utilizando la capacidad oxidante del peróxido de hidrógeno. De entre ellas la extraída de la raíz del rábano picante (HRP) es la más usada. Las enzimas peroxidasas se emplean como biocatalizadores para la generación de productos de interés biotecnológico e industrial como resinas fenólicas, adhesivos, antioxidantes, antiestáticos y protectores de radiación magnética, colorantes alimentarios y componentes bioactivos de detergentes (Rodríguez et al., 2002). Algunos autores han mostrado que la destrucción oxidativa de compuestos coloreados es estimulada significativamente por enzimas (Bhunia et al., 2002) y puede ser de interés práctico para la decoloración de colorantes sintéticos. Recientemente, Bhunia et al., 2002 muestra una efectiva degradación y precipitación de importantes colorantes azo de la industria textil mediante el empleo de la HRP. Una enzima purificada producida por Geotrichum candidum Dec1 fue utilizada en la decoloración de 21 colorantes principalmente de antraquinona, de los cuales 9 fueron decolorados por esta peroxidasa (Kim y Shoda, 1999). Shaffiqu 2002 estudio la degradación de colorantes textiles mediante enzimas (peroxidasas) extraídas de la planta Iponemapalmatay Saccharumspontaneum las cuales utilizó como fuente alternativa a la peroxidasa del rabano picante. Ocho colorantes empleados en la industria textil fueron estudiados en un rango de concentración de 25 a 200 mg/L. Las enzimas fueron purificadas y se emplearon en la decoloración de los colorantes, obteniendo eficiencias de decoloración mayores del 80%. En la Tabla 5.6 se muestran algunos trabajos realizados con las peroxidasas de mayor aplicación así como los colorantes evaluados y los porcentajes de remoción alcanzados. Tabla 5.6 Trabajos realizados con peroxidasas de mayor aplicación. Enzima Peroxidasa HRP MnP LiP Lacasa Colorante % de remoción Negro Directo Cibacron Solofenil Negro Acido 10 Amarillo directo 12 IndigoCarmine Negro acido 52 Naranja II RBBR Azul brillante Naranja disperso 3 Efluente textil 93% 97% 96% 85% 91% 93% 90% 90-95% 75 % 83% 89% 87% 30 Referencia Calderón et al., 2003 Mohanet al., 2005 Maddhinniet al., 2006 Rodríguez-Cuotoet al., 2002 Mielgo et al., 2003 Feijo Costa G. et al., 2003 Ollikkaet al., 1993 Verma y Madamwar, 2002 Zhaoet al., 2006 Campos et al., 2001 Rojo Directo 28 Azul Astrazone 91% 90% Claus et al., 2002 Yesiladaet al., 2003 Mecanismo de reacción: Las peroxidasas oxidan una amplia variedad de sustratos, siguiendo un mecanismo bi-sustrato ordenado, donde participan dos sustratos y se obtienen dos productos. Las peroxidasas catalizan reacciones de peroxidación, como se muestra en la Figura 5.2 Figura 5.2 Mecanismo de reacción general de las peroxidasas (Welinder, 1992). La reacción enzimática general es la siguiente: H2O2 + AH2 → 2(∙AH) + H2O Los radicales libres formados durante el ciclo catalítico se unen formando cadenas de polímeros con baja solubilidad y que tienden a precipitar en la solución. En la Tabla 5.7 se presentan algunos de los factores que influyen en la actividad catalítica de las enzimas. 31 Tabla 5.7 Factores que influyen en la capacidad catalítica de las enzimas. pH Temperatura Otros factores Se ha demostrado que no hay coincidencia en el pH óptimo de las peroxidasas de diversas fuentes vegetales cuando se emplea el guayacol como donador de hidrógeno. Sin embargo, la mayoría de las peroxidasas son activas en un rango de pH relativamente amplio (3-12), lo que puede deberse a la presencia de diferentes isoenzimas las cuales tienen cada una un pH óptimo para realizar su función catalítica La complejidad de la inactivación de las peroxidasas es debida a la presencia de diferentes especies isoenzimáticas, por ejemplo la peroxidasa del maíz consta de fracciones resistentes y lábiles al calor, donde el 5% de la actividad total pertenece a la fracción resistente al calor la que requiere un tratamiento adicional para ser inactivada. Estudios demuestran que las peroxidasas de varios vegetales contienen isoformas resistentes y sensibles al calor. La peroxidasa es una de las enzimas más termoestables de las plantas y bajo ciertas condiciones de tratamiento con calor puede retener la actividad durante el almacenaje. Investigaciones muestran que al estudiar la peroxidasa de coliflor determinaron que la temperatura óptima era de 40oC y que la actividad disminuía drásticamente a temperaturas superiores hasta llegar al 50% a 48oC y aproximadamente 0% a 60oC, por lo que llegaron a la conclusión de que la enzima de la coliflor es termolábil. Se han realizado investigaciones de la influencia de los metales pesados sobre la actividad enzimática de la papa alcachofa de Jerusalén (HelianthustuberosusL.). Evaluando el efecto in vitro de metales pesados como: hierro (Fe2+ y Fe3+), cobalto (Co2+), estroncio (Sr2+), zinc (Zn2+), mercurio (Hg2+), níquel (Ni2+), aluminio (Al2+) y plomo (Pb2+), determinando que ciertas concentraciones de dichos metales inhiben la actividad peroxidásica hasta en un 50 % (Lee et al., 1984; Shaffiquet al., 2002; Güngör, 2008; Mohsina y Khalil, 2009) Las fuentes principales de obtención de las peroxidasas son muy diversas. Se encuentra distribuidas en animales (ratas, conejos, cerdos), plantas superiores (rábano picante, mango, arroz, soya, piña, pera, papa, tabaco, maíz, maní, caña de azúcar, tomate, remolacha, nabo), levaduras, hongos y bacterias. En los mamíferos se halla principalmente en leucocitos, hígado, útero, leche y tiroides; por tanto la enzima puede ser aislada de muy diferentes fuentes. Las especies vegetales más ricas en peroxidasas son las higueras y el rábano picante, las enzimas con actividad peroxidasa se encuentran principalmente en la savia y raíz (Shaffiqu, 2002). Las principales fuentes portadoras de enzimas son los hongos y raíces de rábano, actualmente se está prestando más atención a la extracción de enzimas de plantas, vegetales y leguminosas entre las cuales destaca la soya. La soya es una planta oleaginosa de mayor importancia a nivel mundial por su gran cantidad de usos, derivado de su alto contenido de proteína y energía (Figura 5.3). En promedio, el grano seco contiene 20% de aceite y 40% de proteína (Luna, 2007). Figura 5.3. Variedades de soya producida en México 32 En el año 2009 en México se produjeron 153,000 toneladas de soya. El 87% de la producción se concentró en los estados de Tamaulipas (58%), Chiapas (16%) y San Luis Potosí (13%). En el país hay una gran variedad de especies de soya que se cultivan, pero son las variedades de Tapachula 86 y UFV-1 las que más se producen ocupando un 60% en los cultivos, debido a que poseen mayor capacidad de rendimiento y estabilidad (SAGARPA, 2009). Debido al empleo de la soya como alimento para ganado y actualmente su potencial uso para el consumo humano, su industrialización ha ido en aumento, generando grandes cantidades de residuo industrial llamado okara, el cual se cree puede ser una fuente potencial para la obtención de enzimas (peroxidasas) las cuales pueden aplicarse en el tratamiento de aguas residuales de efluentes textiles. 5.2 – Tratamientos fisicoquímicos: Procesos avanzados de oxidación Como ya antes se mencionó, los efluentes de la industria textil y de la industria de colorantes son uno de los principales contaminantes de agua ya que se encuentran altamente coloreados y con grandes cantidades de químicos los cuales son utilizados en sus procesos de producción. Descargas directas de estos efluentes proporcionan color intenso y toxicidad en los ambientes acuáticos, causando serios problemas ambientales (Wang, 2008). Los colorantes azo son caracterizados por tener un grupo funcional azo el cual consiste en un doble enlace de nitrógeno unido a átomos de carbono, estos son los colorantes más usados por la industria textil. Los colorantes azo son usualmente los contaminantes más problemáticos en los efluentes de la industria textil debido a que no se fijan en su totalidad a las fibras y el resto termina en los cuerpos receptores (Park y Choi, 2003). Existen varias tecnologías disponibles para el tratamiento de efluentes con colorantes, entre las que se tienen algunos métodos físico-químicos como adsorción, coagulación-floculación, oxidación avanzada y filtración en membranas. Estos métodos, pueden llegar a ser muy efectivos, aunque son complejos y de difícil aplicación a gran escala; sin embargo, el desarrollo de tecnologías avanzadas de oxidación han facilitado su conocimiento e implementación, sobre las aplicaciones en la degradación de un sinnúmero de contaminantes ambientales tales como plaguicidas, colorantes, residuos de laboratorios, entre otros (Arroyave, 2008). Los procesos de oxidación avanzada aparecieron como una opción de tratamiento particularmente en los casos donde los contaminantes son difíciles de remover. Recientemente, los procesos de oxidación avanzada (PAO), los cuales están basados en la generación radicales hidroxilos altamente reactivos como oxidante primario, han sido desarrollados para que reaccionen con el contaminante y lo transforman en compuestos inocuos al ambiente (Neamtu et al., 2004). Estos se basan en procesos fisicoquímicos capaces de producir cambios profundos en la estructura química de los contaminantes, ya que involucran la generación y uso de especies transitorias con elevado poder reductor, 33 fundamentalmente el radical hidroxilo (HO•). Este radical se genera por medios fotoquímicos o por otras formas de energía y posee una alta eficacia en la oxidación de materia orgánica. Además de estos tratamientos, el proceso de oxidación de Fenton es un método muy prometedor de tratamiento debido a su alto poder de oxidación, cinéticas de oxidación rápidas, relativamente de bajo costo y fácil operación (Sun et al., 2007a, b). En la 5.8 se muestra un listado de las principales Tecnologías Avanzadas de Oxidación, TAO's y posteriormente se realizará una breve descripción de cada una de ellas, así como las principales reacciones que tienen lugar en la generación de radicales hidroxilo y otros agentes reductores. Tabla 5.8 Tecnologías avanzadas de oxidación (TAO) Procesos no fotoquímicos Ozonización en medio alcalino (O3/OH-) Procesos fotoquímicos Fotólisis del agua en el ultravioleta de vacío (UVV) UV/peróxido de hidrógeno Ozonización con peróxido de hidrógeno (O3/H2O2) Procesos Fenton (Fe2+/H2O2) Oxidación electroquímica Radiólisis g y tratamiento con haces de electrones Plasma no térmico Descarga electrohidráulica - Ultrasonido Oxidación en agua sub/y supercrítica UV/O3 Foto-Fenton Ferrioxalato y otros complejos de Fe(III) UV/peryodato Fotocatálisis heterogénea 5.2.1.- Procesos no fotoquímicos a) Ozonización en medio alcalino El ozono puede reaccionar de forma directa con un sustrato orgánico a través de una reacción lenta y selectiva (primera ecuación) o de una reacción radical favorecida en medio alcalino, rápida y no selectiva (ecuación 2): O3 + S → Sox ; k = 1 – 100 M-1 s-1 2 O3 + H2O → 2 HO• + 2 O2 + HO2•; k = 108 – 1010 M-1 s-1 b) Ozonización con peróxido de hidrógeno La ozonización transforma los contaminantes en compuestos más simples, más refractarios al reactivo. Se logra una mejora agregando agua oxigenada (peróxido de hidrógeno, H2O2), que es un ácido débil, un poderoso oxidante y un compuesto inestable: 34 O3 + H2O2 → HO• + O2 + HO2•; siendo: H2O2 = HO2- + H+ y HO2• = O2•- + H+; por tanto la reacción en cadena es: HO2- + O3 → O3- + HO2•; k = 2,8 * 106 M-1 s-1 O2•- + O3 → O3- + O2; k = 1,6 * 109 M-1 s-1 O3- + H+ → HO3 + O2; k = 5,2 * 1010 M-1 s-1 HO3 → HO• + O2; k = 1,1 * 105 s-1 O3 + HO• → O2 + HO2•; k = 1,1 * 105 s-1 O3 + HO2• → 2 O2 + HO• c) Reactivo de Fenton La combinación de Fe2+ y H2O2 va a generar radicales HO•, que a su vez van a reaccionar a continuación por dos vías: la oxidación de Fe (II) (reacción improductiva) y el ataque a la materia orgánica: Fe2+ + H2O2 → Fe3+ + HO- + HO•; k = 76 M-1 s-1 Fe (II) + HO• → Fe (III) + HORH + HO• + H2O → ROH + H3O+ → productos oxidados Más adelante se realizará una descripción más detallada de este proceso. d) Oxidación electroquímica La aplicación de una corriente eléctrica (2 – 20 A) entre dos electrodos en agua produce reacciones químicas primarias que van a generar HO•, que oxidará la materia orgánica: H2O → HO• + H+ + e-; oxidación anódica O2 + 2 H+ + 2 e- → H2O2; reacción catódica e) Radiólisis tratamiento con haces de electrones 35 Estos procesos se basan en la generación de electrones altamente reactivos, iones radicales y radicales neutros por exposición de las aguas a tratar a haces de partículas másicas u ondas electromagnéticas de alta energía. Se pueden usar rayos γ, rayos X o aceleradores de haz de electrones como los de tipo Van-de-Graaf o los lineales. Cuando el haz de electrones penetra en el agua, los electrones pierden energía por colisiones no elásticas con las moléculas de H2O, y se generan especies reactivas: H2O → e-aq + H• + HO• + H2 + H2O2 + H+ f) Plasma no térmico El plasma es considerado el cuarto estado de la materia que contiene iones y electrones libres (gas eléctrico). El plasma puede generarse, en forma no térmica, por una descarga eléctrica o bombardeo de un gas con un haz de electrones de alta energía; la energía de los electrones en el plasma es de unos 10 eV, lo que equivale a temperaturas elevadas. Estos plasmas son buenas fuentes de especies reactivas altamente reductoras y oxidantes, como O (3P), HO•, N, H, NH, CH, O3. g) Descarga electrohidraúlica - ultrasonido Esta tecnología usa ultrasonido de alta potencia (de 15 kHz hasta 1 MHz), y se aprovecha la cavitación electrohidráulica, es decir, el crecimiento y colapsado cíclico de burbujas de gas. El gas implota y se alcanzan temperaturas y presiones locales muy altas (4.000-10.000 K y 1.00010.000 bares en el centro de las burbujas colapsadas). La degradación de materia orgánica ocurre a través de reacciones con los radicales generados por la reacción térmica, o por las reacciones en presencia de oxígeno: H2O → H• + HO• O2 → 2 O• H• + O2 → HO2• H• + O2 → HO• + O• h) Oxidación en agua sub/ y supercrítica El proceso que opera en condiciones subcríticas es llamado también oxidación en aire húmedo; se trabaja a presiones entre 10-220 bars y temperaturas entre 150-370 °C. El mecanismo involucra la carbonización primaria de los sustratos orgánicos y su posterior reacción con los HO• producidos en la transformación catalítica del O2 disuelto en la superficie del centro carbonoso. El nitrógeno, los halógenos y el azufre son también mineralizados: 36 O2 → H2O2 → O2 + HO2• HO• + C → CO2 + H2O N → NH3, NO3-, N elemental X→X S → SO42C + HO• → ácidos orgánicos de bajo peso molecular La oxidación con agua supercrítica usa agua en condiciones de presión y temperatura superiores que las del punto crítico, entre 450 y 700 °C y presiones cercanas a los 25 MPa. En estado supercrítico, el agua se comporta como un fluido cuya viscosidad, densidad y constante dieléctrica son relativamente bajas. En condiciones supercríticas, disminuye el número de uniones puente hidrógeno, aumenta la solubilidad de los compuestos orgánicos y gases y disminuye la solubilidad de los electrolitos. Por ello, este método posee características que lo llevan a ser un excepcional sistema de tratamiento, con una eficiencia de oxidación mayor que 99,99 % en tiempos de contacto muy breves (5-60 segundos), que no requiere ningún tratamiento adicional de los productos gaseosos. Debido a la alta solubilidad del O 2 en el agua supercrítica, no existen problemas de transferencia de masa. Como además la tensión superficial es nula, el O2 penetra en los poros más pequeños y puede oxidar cualquier sustancia orgánica. 5.2.2.- Procesos fotoquímicos a) Fotólisis del agua en el ultravioleta de vacío (UVV) Se utiliza radiación con una longitud de onda menor a la UV-C (menores a 190 nm) que producen la degradación de la materia orgánica en fases condensadas o gaseosas o la fotólisis del agua, que produce radicales hidroxilo, átomos de hidrógeno y electrones acuosos: H2O + hν → HO• + H• H2O + hν → HO• + H+ + e-aq A partir de los radicales primarios se generan rápidamente HO2• y O2•-: O2 + H• → HO2•; k = 1 * 1010 M-1 s-1 O2 + e-aq → O2•-; k = 2 * 1010 M-1 s-1 37 b) UV/peróxido de hidrógeno La fotólisis del peróxido de hidrógeno (H2O2) se realiza utilizando lámparas de vapor de mercurio de media o baja presión: H2O2 + hν → 2 HO• En exceso de peróxido y con altas concentraciones de HO• tienen lugar reacciones competitivas que producen un efecto inhibitorio para la degradación. Los HO• son susceptibles de recombinarse o de reaccionar de acuerdo con el siguiente esquema: HO• + H2O2 → HO2• + H2O HO2• + H2O2 → HO• + H2O + O2 2 HO2• → H2O2 + O2 HO2• + HO• → H2O + O2 c) UV/O3 Combinación de los métodos UV/H2O2 y O3/H2O2: O3 + hν + H2O → H2O2 + O2 H2O2 + hν → 2 HO• O3 + H2O2 → HO• + O2 + HO2• d) Foto-Fenton La reacción de Fenton aumenta su eficacia por irradiación luminosa debido a varios factores, entre ellos la reacción adicional: Fe (III) (OH)2+ + hν → Fe(II) + HO• e) Ferrioxalato y otros complejos de Fe (III) En presencia de ligandos orgánicos, como por ejemplo ácidos carboxílicos, el Fe (III) puede formar complejos estables o pares iónicos asociados que exhiben bandas de transferencia de carga del ligando al metal en el espectro UV-visible. Son fotoquímicamente activos y generan Fe (II) por irradiación: Fe (III) (O2CR)2+ + hν → Fe(II) + CO2 + R• 38 La fotólisis del trisoxalatoferrato (III) (ferrioxalato) se aprovecha para la medición de intensidades de luz, y constituye el actinómetro químico más utilizado: [Fe (C2O4)3]3- + hν → [Fe (C2O4)2]2- + C2O4•C2O4•- + [Fe (C2O4)3]3- → [Fe (C2O4)2]2- + C2O42- + 2 CO2 C2O4•- + O2 → O2•- + 2 CO2 f) UV/peryodato El ácido peryódico (H5IO6) y el ion peryodato (IO4-) son oxidantes fuertes: H5IO6 + H+ + 2 e- → IO3- + 3 H2O; E° = + 1.6 V La irradiación de soluciones de peryodato con luz UV corta genera radicales (IO3•, HO•, IO4•) y otras especies oxidantes (IO3-, O3). El ataque a contaminantes orgánicos se vuelve así menos selectivo pero más eficiente. El mecanismo es complejo como se muestra en la figura 5.4 Figura 5.4. Mecanismo de oxidaciónUV/peryodato 39 g) Fotocatálisis heterogénea Se basa en la absorción de energía radiante (visible o UV) por un fotocatalizador heterogéneo, que normalmente es un semiconductor sólido. Las reacciones de destrucción de los contaminantes tienen lugar en la región interfacial entre el catalizador y la solución como se muestra en la siguiente ilustración. Figura 5.5 Mecanismo de oxidación fotocatálisis heterogénea 5.2.3.- Proceso de oxidación de Fenton El proceso de oxidación de Fenton es un método de oxidación catalítico homogéneo que usa una mezcla de iones de Fe2+ y peróxido de hidrógeno en un medio ácido. Este es conocido por ser muy efectivo en la remoción de compuestos contaminantes en el agua. La principal ventaja es la completa destrucción de los contaminantes en compuestos más simples y logra la decoloración de efluentes coloreados con bajos tiempos de reacción. Esta reacción se realiza sin la presencia de radiación ultravioleta, pero, recientemente se ha demostrado que su poder oxidante puede ser incrementado significativamente, empleando radiación ultravioleta ó ultravioleta/visible (reacción de Fotofenton). El mecanismo que describe la reacción de Fenton principalmente incluye las siguientes reacciones (Neyens y Baeyens 2003). Fe2+ + H2O2 Fe3+ + OH.+ OH- El ion ferroso inicia y cataliza la descomposición del peróxido de hidrógeno, resultando la generación de radicales hidroxilos. Los radicales hidroxilos pueden rápidamente y no selectivamente reaccionar con un amplio rango de contaminantes orgánicos para mineralizarlos hasta CO2, H2O y productos inorgánicos (Sun et al. 2009). El ion ferroso es generado lentamente 40 entre la formación del ion férrico y el peróxido de hidrógeno, como se indica en las siguientes reacciones: Fe3+ + H2O2 Fe- OOH2+ Fe3+ + HO2 Fe- OOH2+ H+ HO2 + Fe2+ Fe2+ + O2 + H+ Consecuentemente, la tasa de oxidación de compuestos orgánicos es rápida cuando grandes cantidades del ion ferroso están presentes porque grandes cantidades de radicales hidroxilo se producen. El proceso de oxidación de Fenton tiene doble ventaja, la oxidación y la coagulación así reduciendo contenido de color como a su vez la DQO de las aguas residuales (Kuo, 2000). Existen muchos estudios dedicados a los procesos de Fenton para el tratamiento de aguas residuales de la industria textil en la Tabla 5.9 se muestran algunos trabajos realizados: Tabla 5.9. Trabajos realizados utilizando el proceso de Fenton para la oxidación de colorantes Tipo de colorante Agua real mg/L Rojo directo 28 10 130 250 Rojo ácido 18 100 Tartrazina 100 Violeta cristal 1.2x10 mol/L Azul reactivo 221 Amarillo 145 86 25 -4 Reactivos FeSO4 7 H2O H2O2 H2SO4 NaOH Virutas de acero H2O2 H2SO4 NaOH 3+ Fe H2O2 H2SO4 NaOH FeSO4 7 H2O H2O2 H2SO4 NaOH FeSO4 7 H2O H2O2 HCL NaOH Tiempo % Remoción Condiciones 15 minutos 100 pH=3 150 rpm T (23-25°C) pH Absorbancia COT Filiz, et al., 2008 120 h 88.7 pH=2.5 T= 25°C pH Absorbancia DQO Barbusiński, 2004 2h 99.3 pH=3 T (20-25°C) pH Absorbancia Arroyave, 2008 Wu, et al., 2010 Kabdasli, et al., 2007 Parámetros 30 minutos 87 T (20-50°C) Absorbancia Temperatura H2O2 2+ Fe 90 minutos 96 pH=3 T (20-25°C) pH Absorbancia DQO 41 Bibliografía 6.- Metodología 6.1.- Selección y Caracterización de las aguas residuales Las características del agua de la industria textil que contiene colorantes son muy variadas y dependen del tipo de fibra y prenda utilizada, del tipo de colorantes utilizados y de los acondicionadores utilizados y sus características fisicoquímicas varían en cada lote de producción. Como fuente de las aguas residuales se consideraron varias fuentes: Preparación de efluentes sintéticos con diferentes colorantes del tipo azo: Naranja ácido 24, Azul negro directo, Rojo Congo y negro Terasil Una industria Lavadora de Mezclilla en Santa Ana Xamimilulco, Puebla Textiles Gütermann, empresa ubicada en CIVAC, Morelos que se dedica a la fabricación de hilos 6.1.1. Aguas residuales de la Empresa Gutterman Las aguas residuales que se seleccionaron fueron de la empresa Gütermann, que utiliza colorantes del tipo azo. Se seleccionó esta empresa por la facilidad de su ubicación ya que está situada en la Ciudad Industrial del Valle de Cuernavaca, CIVAC, por su cercanía con el IMTA y sus instalaciones experimentales donde se realizó la investigación, además por la apertura y buena disposición de la empresa por brindar la información de sus procesos y materias primas, así como suministro de aguas residuales reales de sus procesos de producción y suministro de colorantes azo para la preparación de los efluentes sintéticos. Se hizo inicialmente la caracterización del efluente final, que es una mezcla de todas las aguas residuales de sus procesos y el cual tenía mucha variabilidad por lo que se decidió utilizar la descarga de una de las tinas. El efluente final contiene las descargas de todos los procesos productivos y los lavados. El agua residual se transportaba en tambos de 200L hasta el laboratorio del IMTA y se tomaban muestras cada vez que se realizaba la carga a cada uno de los experimentos El efluente de la tina de teñido es más controlable y la industria proporcionó la información sobre los colorantes y aditivos usados para cada lote de teñido. El efluente sale a una temperatura mayor de 70°C, por lo cual había que esperar hasta que se enfriara para tomar la muestra y transportarlo. Los análisis físico-químicos realizados fueron los siguientes: pH, 43 conductividad, SDT, DQO, N (NH3, NO3, NO2, PT, Color Pt-Co y Concentración de colorante cuando procediera según el experimento. Las frecuencias de muestreo se describen en la metodología de las pruebas de tratabilidad de cada uno de los procesos probados. 6.1.2.- Aguas residuales de la Empresa lavadora de mezclillas La caracterización del efluente real se realizó en la zona de Santa Ana Xalmimilulco Puebla. Ya que esta población se caracteriza por tener un sector productivo de microempresas familiares para lavado de mezclilla, debido a estas actividades se ha generado un problema local, ya que ha sido afectado en gran manera al rio Xochiac. Debido a las características heterogéneas que presentan estos efluentes se realizó un muestreo compuesto durante una jornada de trabajo analizando los parámetros de la NOM 001. La lavandería cuenta con 3 procesos de teñido y solo tiene un canal de descarga donde se unen todos los efluentes del proceso los cuales llegan a una planta de tratamiento de coagulación floculación la cual no opera debido a la falta de conocimientos técnicos por lo cual es efluente del proceso es descargado sin ningún tratamiento previo. El muestreo se realizó en un día laboral de 7 am a 2 pm. En este día se tiñeron más 1000 pantalones de mezclilla tono azul directo. 6.2.- Pruebas de tratabilidad 6.2.1.- Tratamiento biológico convencional: Proceso acoplado Anaerobio- Aerobio Como ya se mencionó, como modelo para este estudio se utilizó agua residual de la industria textil Gütermann (Jiutepec, Mor.), inicialmente el efluente final de la industria y después la descarga de una de las tinas. El sistema experimental consistió de dos reactores conectados en serie, primero el agua residual pasaba por un reactor anaerobio con lecho de lodo granular (reactor UASB) y después se introducía a un reactor de lodos activados (LA) con su sedimentador secundario. 6.2.1.1.- Sistema experimental El reactor experimental UASB se ilustra en la Figura 6. 1. Está elaborado de acrílico y tiene una forma cilíndrica con un diámetro interno de 15 cm y una altura total de 146 cm. La altura del lecho granular es de 50 cm y la de la zona del agua es también de 50 cm. En la parte inferior hay un falso fondo formado por un disco perforado el cual soporta el lecho de granos y está ubicado a 14 cm desde el fondo. El influente se introduce en la parte inferior del reactor a unos 3 cm desde el fondo. La salida del efluente está ubicado a una altura de 114 cm desde el fondo. En la parte superior del reactor está introducido un separador sólido-líquido-gas. El reactor UASB 44 cuenta con dos bombas peristálticas Masterflex de control variable, una para alimentar el agua residual al reactor y la otra para recircular una parte del efluente. La salida de la línea de recirculación se encuentra a 88 cm desde el fondo. El agua recirculada se introduce en la parte inferior del rector a 3 cm desde el fondo por un orificio contrario al del influente. De esta manera en la zona debajo del lecho ambos flujos se mezclan antes de entrar de manera ascendente al lecho de granos anaerobios. El agua residual utilizada como modelo para este estudio se transporta desde la industria textil Gütermann (Jiutepec, Mor.)hasta el laboratorio del IMTA en tambos de 200 L. El agua se almacena en un cuarto frio. Periódicamente se extrae un volumen de 100 L de agua residual el cual se deposita en un tanque al lado del sistema experimental y desde allí se bombea al reactor UASB. El efluente del UASB se recolecta en un recipiente de 100 L y de allí es transferido al reactor aerobio de lodos activados. En la parte superior del reactor UASB se instaló un sistema para la medición del biogás (metodología del desplazamiento). El volumen del reactor es de 25.8 L, el volumen de operación (lodo y agua) es de 17.7 L y el volumen del lecho es de 8.8 L. En la Figura 6.2 se presenta el esquema y las dimensiones del reactor lodos activados (LA). El agua efluente del UASB se introduce por bombeo. Mediante un compresor se suministra aire el cual se dispersa dentro de la zona aerobia mediante difusores de piedra porosa. Un bafle separa la zona aerobia del sedimentador. El bafle es movible y mediante su posición vertical se puede variar la recirculación del lodo sedimentado al reactor aerobio. El efluente del sedimentador sale mediante un dispositivo rectangular con paredes-vertedores ubicado en la parte superior del sedimentador. El ancho del reactor es de 21.4 cm. El volumen de operación de la zona aerobia LA es de 18.4 L. El volumen del sedimentador es 10.4 L. 45 Biogás Separador sólido-líquidogas 32 Efluente 26 Agua 50 24 146 50 14 Re cir cu la ci ón Lecho de lodos 114 64 Influent e 15 Figura 6.1 Esquema y dimensiones del reactor UASB. 46 Influent e 16.0 18.6 29.2 18.5 15.9 34.5 5.3 Aire Efluente 4.4 42.2 5. 9.1 1 Figura 6.2 Esquema y dimensiones del reactor LA. 6.2.1.2.- Procedimiento experimental El reactor experimental UASB se inoculó con biomasa granular anaerobia obtenida del reactor UASB de la industria UNIPAK S.A de C.V. localizada en Cuernavaca, Morelos. La caracterización inicial del lodo granular indicó que las concentraciones de ST y SV fueron de 186,331 y 136,443 mg.L-1 respectivamente. Durante la primera etapa del experimento se trabajó con el agua residual efluente final de la industria cuya DQO fue de 2,446±592 mg/L en promedio. El influente fue de 26.5 ml.min -1 equivalente a 38.1 L d-1. La carga orgánica volumétrica (COV) se calculó de 5.3kg DQO m-3 d-1 y el TRH de 11.1 h. La carga se seleccionó por debajo de los valores típicos para los reactores UASB (de 10-30 kg DQO m-3 d-1) para crear mejores condiciones para la aclimatación de la biomasa al sustrato del agua residual de la industria textil. Debido al bajo caudal de agua, la velocidad ascendente del flujo de agua en el reactor fue de 0.09m/h, muy por debajo de los valores típicos de 1.0-1.5 m/h. Para mejorar las condiciones hidrodinámicas en el reactor, se decidió implementar una recirculación del efluente de 100% con lo cual se aumentó la velocidad ascendente en el reactor a 0.18 m/h. Durante la segunda etapa del experimentó el reactor UASB se alimentó con el agua residual descargada directamente de la tina de teñido en la industria. La DQO promedio fue de 7,739±3,180 mg/L, casi tres veces mayor que la DQO del efluente final de la industria textil. Para 47 evitar un incremento grande de la carga orgánica al UASB se disminuyó el caudal a 16.2 ml.min -1 o 23.3 L d-1, el más bajo que se puede lograr con la bomba peristáltica instalada. La disminución del caudal permitió lograr un TRH de 18.2 h, mayor que el obtenido en la primera etapa. La velocidad ascendente considerando solo el Q del influente fue de 0.055 m/h y con la recirculación aumentó a 0.11 m/h. Debido a la alta DQO la carga orgánica aumentó casi dos veces obteniéndose en promedio una COV de 10.2 kg DQO m-3 d-1. Tabla 6.1 Parámetros de operación del reactor UASB. Parámetros -3 COV, kg DQO m d TRH, h Q, L d -1 -1 Etapa 1 Etapa 2 5.3 10.2 11.1 18.2 38.1 23.3 El día 66 desde el arranque del reactor UASB, cuando ya se había empezado la alimentación con el agua residual proveniente de la tina de teñido de la industria textil, se inoculó el reactor aerobio LA con biomasa de un reactor real de LA y empezó su alimentación con el efluente del UASB. Las concentraciones de SSTLM y de SSVLM fueron de 2,970 y 1,460 mg/L respectivamente. El caudal del influente al reactor aerobio LA se ajustó a 16.2 ml.min -1 o 23.3 L d-1, con lo cual se obtuvo un TRH de 14.0 h. La carga orgánica volumétrica dependía de la DQO del efluente del UASB y la carga orgánica másica dependía y de la concentración de los SSVLM. 6.2.1.3.- Muestreo y análisis físico-químicos El seguimiento de los procesos en los reactores anaerobio UASB y aerobio de lodos activados, LA se realizaba determinando dos veces por semana en muestras del influente al UASB, efluente del UASB y efluente del LA los siguientes parámetros: DQO, NT, N-NH4, N-NO2, N-NO3, P-PO4, SST y SSV. Los análisis se realizaron de acuerdo con los métodos recomendados por el Standard Methods for the Examination of Water and Wastewater (APHA, 1999) y para el caso de nitrógeno y fósforo los métodos espectrofotométricos de HACH. En los mismos puntos de muestreo se determinaban diariamente pH, Conductividad, SDT y temperatura usando equipo para determinaciones potenciométricas. 6.2.2.- Tratamiento biológico no- convencional 6.2.2.1.- Tratamiento fúngico En esta investigación se consideró el utilizar el hongo Basidiomiceto Pleutorus ostreatus por su alto contenido en enzimas del tipo de las lacasas y las peroxidasas inoculando la cepa de P. ostreatus en turba para su propagación y proliferación. 48 a) Sistema experimental El sistema experimental estuvo constituido por 4 biofiltros separados uno del otro. De los cuales dos de ellos fueron empacados únicamente con turba (blanco y su réplica). Los otros dos fueron empacados con turba e inoculados con P. ostreatus (tabla 6.2). Los biofiltros se evaluaron bajo dos condiciones diferentes de operación (2 cargas orgánicas diferentes). El reactor contó con una salida en la parte inferior y la entrada en la parte superior. La parte inferior del reactor contó con una cama de grava fina para evitar que el medio de soporte obstruya la manguera de efluente. Los modelos fueron a escala laboratorio y se ilustran en la figura 6.3. El sistema experimental propuesto se basa en los estudios realizados por Moeller et al (2003) y Dávila (2005). Figura 6.3 -Biofiltros empacados. 49 Tabla 6.2. Características del material de empaque de los biofiltros Biofiltro 1 2 3 4 Características del empaque Empacado con turba sin esterilizar. Empacado con turba estéril e inoculado con P.ostreatus Empacado con turba estéril. Empacado con turba sin esterilizar e inoculado con P. ostreatus b) Agua residual a tratar El agua a tratar provino de la industria productora de hilos Gutterman, donde utilizan en sus procesos de teñido colorantes azo, que son objeto de estudio de este trabajo. Este efluente presenta una problemática especial con los colorantes ya que, después del proceso de elaboración de sus productos, su efluente presenta una concentración elevada de DQO (8000mg/L) y de concentración de colorante (566mg/L). El efluente a tratar se tomó de una de las tinas de tintura de hilos, el colorante empleado es el Negro Terasil SRL cuya estructura química se muestra en la figura 6.4 y la figura 6.5 muestra un lote de hilos teñido con el mismo colorante. Debido a las altas concentraciones de este efluente y su toxicidad, se trabajó con los siguientes factores de dilución (FD) 10, y 37. La caracterización de esta agua diluida se muestra en la tabla 6.3. Figura 6.4 -Estructura del colorante Negro Terasil SRL ( http://www.lookchem.com/). 50 Figura 6.5 Hilos después del proceso de teñido con el colorante negro terasil. Tabla 6.3. Características de los influentes utilizados para la alimentación de los biofiltros DQO (mg/L) Influente 1 (FD. 10) 841 Influente 2 (FD. 37) 217.7 Color aparente (Upt/Co) 2130 233 Color verdadero (Upt/Co) 1780 79.3 Concentración de color(mg/L 56.6 13.55 SDT (g/L) 0.33 0.12 pH 5.23 8.3 Temperatura (˚C) 23.7 23.7 Fosforo total (mg/L) 8.6 4.5 Parámetro c) Caracterización del efluente textil La caracterización de este efluente textil se determinó en función de los siguientes parámetros: pH, sólidos disueltos totales (SDT), concentración de color (espectrofotométricamente), demanda química de oxígeno (DQO), nitrógeno amoniacal (N-NH4) y nitrógeno total (NT) (Tabla 6.4). d) Obtención de la cepa de Pleurotus ostreatus La cepa de P.ostreatus se obtuvo de Herbario Micológico de Morelos (HEMIM) del centro de investigaciones Biológicas (CIB) de la Universidad Autónoma del estado de Morelos. 51 e) Siembra, cultivo, y conservación P. ostreatus Ya obtenidas las cepas se procedió a la verificación de la viabilidad del hongo. Para lo cual se realizó un aislamiento vegetativo: Se tomó un fragmento de aproximadamente de 2 a 3 mm del cuerpo fructífero y se colocó con la ayuda de unas pinzas de disección en cajas con medio previamente esterilizado (agar de extrac C por 4 días hasta que se observó el micelio. Tabla 6.4. Características de los influentes utilizados. Parámetro VALOR(mg/L) DQO(mg O2/L) 8401 SDT 0.9 pH 5.23 T (˚C) 23.7 N-NO3 15 N-NO2 45 Color aparente (Upt-Co) Color verdadero (Upt-Co) N-TOTAL 21300 17800 275 PT 10 N-NH3 97 f) Reproducción masiva de P. ostreatus Una vez que el micelio cubrió toda la caja se utilizó para su propagación. En esta etapa P. ostreatus creció en medio líquido. La metodología para la reproducción masiva de P. ostreatus se basa en la metodología utilizada por Dávila (2005) que consiste en: Cuadricular con un bisturí el micelio contenido en la caja Petri en porciones de 1 cm2. Estas porciones se colocaron en matraces de 250 ml con caldo fungal y se incubaron a 70 rpm a 30 ˚C por 6 días en obscuridad. Obtenida la biomasa suficiente de P. ostreatus se inoculó dos reactores. g) Acondicionamiento del material de empaque Para el acondicionamiento de la turba (turba comercial) se cribó utilizando un tamiz con el fin de remover impurezas. Posteriormente y para cada caso particular la turba se esterilizó u omitió. Después la turba se humedeció hasta aproximadamente un 60% de humedad. Una buena aproximación para este contenido de humedad es cuando al exprimir el material con la mano escurren unas cuantas gotas de agua (Garzón- Zuñiga et al., 2003). h) Reactores Se construyeron y montaron 4 reactores de acrílico con dimensiones de 10 cm de diámetro, 60 cm de altura y una capacidad de 4712. 4 cm3.El diseño se basó en los trabajos realizados por Garzón- Zúñiga (2001), el cual consistió en una torre donde se encuentra mezclado el medio de 52 soporte con el micelio lo que abarca un 70% de la torre. El reactor contó en la parte superior con una entrada del influente, en la parte inferior del reactor con una cama de grava fina para evitar que el medio de soporte colmate la salida del efluente. Los reactores se alimentaron con agua real a una carga orgánica volumétrica de (607.17 y posteriormente 161.7 mg/L d), con un tiempo de retención hidráulico de 0.85 días (20.47 hr) a un flujo de 2.43 ml/min (3. 5 L/día), el TRH se calculó de acuerdo a metodologías dadas por Garzón-Zúñiga et al., (2003), donde por medio del cálculo de los espacios porosos del medio de soporte se obtiene el TRH. i) Montaje del biofiltro empacado con turba estéril inoculado con P.ostreatus. Se drenó el micelio y se preparó en proporciones adecuadas para el reactor. El reactor se desinfectó con luz UV. La turba se esterilizó y posteriormente se humedeció con agua esterilizada hasta obtener un 60% de humedad. Se empaquetaron los reactores y se inocularon con el micelio obtenido en el medio líquido, de tal manera que el micelio quedó distribuido en forma abundante y homogénea en todo el reactor. j) Montaje del biofiltro empacado con turba sin esterilizar inoculado con P.ostreatus. Se drenó el micelio y se preparó en proporciones adecuadas para el reactor. La turba se humedeció con agua esterilizada hasta obtener un 60% de humedad. Se empaquetaron los reactores y se inocularon con el micelio obtenido en el medio líquido, de tal manera que el micelio quedó distribuido en forma abundante y homogénea en todo el reactor. k) Montaje del biofiltro empacado con turba estéril La turba se esterilizo y humedeció con agua esterilizada hasta obtener un 60% de humedad y con ella se empacaron los reactores. El reactor se desinfectó con luz UV. l) Montaje del biofiltro empacado con turba sin esterilizar La turba se humedeció con agua esterilizada hasta obtener un 60% de humedad y con ella se empaquetaron los reactores. m) Evaluación del desempeño de los biofiltros Para el seguimiento, control y evaluación del desempeño del sistema experimental se midieron los siguientes parámetros: pH, Temperatura, Color aparente, Color verdadero y DQO. Estos parámetros fueron monitoreados con las frecuencias mencionadas en la tabla 6.5. y con los métodos señalados en la tabla 6.6. 53 Tabla 6.5. Parámetros de medición, puntos y frecuencia de muestreo para los biofiltros. PARÁMETRO PUNTOS DE MUESTREO INFLUENTE EFLUENTE X X FRECUENCIA DQO COLOR APARENTE COLOR VERDADERO 3 Veces por semana CONCENTRACIÓN DE COLOR pH TEMPERATURA 3 Veces por semana X X X X X X X X X X Tabla 6.6. Parámetros analizados y sus técnicas de análisis. PARÁMETRO TÉCNICA ANALÍTICA DQO COLOR Método estándar HACH Método estándar HACH CONCENTRACIÓN DE COLOR Espectrofotometría HACH pH TEMPERATURA Medición directa con potenciómetro de acuerdo a la NMX-AA-008 Medición directa con termómetro de acuerdo a la NMX-AA-007 También se midió esporádicamente la toxicidad y la actividad enzimática, para lo cual se utilizaron las siguientes técnicas. n) Evaluación de actividad enzimática La evaluación de la actividad enzimática se realizó por separado para cada enzima. Se tomó una muestra de cada uno de los reactores para la evaluación de la actividad enzimática de la Manganeso Peroxidasa, posteriormente se tomó una muestra de cada reactor y se evaluó la actividad de la Lacasa y se tomó otras muestras para la medir la actividad enzimática de la Versátil Peroxidasa. o) Evaluación de toxicidad Para la evaluación de la toxicidad se realizaron diluciones de las muestras (efluente e influente) a las cuales se expone una población de la bacteria luminiscente marina (Photobacterium phosphoreum o Vibrio fisheri). En caso de existir agentes tóxicos en las muestras, las bacterias cambiarán la emisión de su luminosidad, de manera decreciente al incremento del tóxico. Para este análisis se utilizó el equipo Microtox donde por medio de un sensor se medirá el cambio de luminosidad. Dicho procedimiento se realizó de acuerdo al método aprobado por SECOFI NMXAA-112-1995. 54 6.2.2.2.- Tratamiento enzimático Como producto para la extracción de las peroxidasas se trabajo con el residuo del procesamiento del frijol de soya para la elaboración de bebidas de soya por ser un producto de desecho que se considera que contiene aun un alto contenido de estas enzimas. La hipótesis de trabajo en esta etapa fue que mediante las peroxidasas obtenidas a partir de un residuo industrial del procesamiento del frijol de soya es posible decolorar efluentes del proceso de teñido de la industria textil que emplean colorantes tipo azo. Esta investigación está en sus inicios ya que no existe a la fecha literatura reportada de su utilización para este propósito. El objetivo inicial es el evaluar la capacidad catalítica de la enzima peroxidasa (obtenida a partir de un residuo industrial del procesamiento del frijol de soya) en la decoloración de efluentes de la industria textil que emplean colorantes azo. Y el objetivo específico el implementar una técnica para la obtención de extracto crudo y su purificación parcial con actividad enzimática. Asimismo determinar el modelo cinético para el tratamiento enzimático de un efluente sintético y uno real a) Obtención del extracto de soya En la actualidad los estudios realizados para la decoloración de efluentes textiles utilizando enzimas han demostrado ser un tratamiento eficiente. Las principales fuentes de obtención se centran principalmente en la raíz del rábano picante, hongos, soya y vegetales de consumo tales como: chayote, rábanos, papas etc. En este trabajo se pretende utilizar un residuo industrial, generado en el proceso de elaboración del jugo (ADES) hecho a base de soya, el cual es proporcionado por UNILEVER, utilizándolo como única fuente obtención de peroxidasas. Para obtener el extracto crudo se utilizan diversas técnicas optimizando los procesos para la obtención de la mayor cantidad de enzima con alta actividad de peroxidasas, evaluando diferentes condiciones de operación como, pH, temperatura, tiempo de homogenización, buffers. b) Purificación parcial de peroxidasas Existe una gama diversa de procesos para la purificación de enzimas tales como: precipitación con sulfato de aluminio, cromatografía en filtración de gel, cromatografía de intercambio aniónico. Considerando las propiedades físicas y características de la enzima de interés en este trabajo se realizará la purificación parcial mediante cromatografía de intercambio aniónico, en una columna de 142.35 mL de volumen total, utilizando como intercambiador Dietilaminoetil celulosa (DE53) de acuerdo a Jakoby, 1971 y Zia 2002. c) Valoración de la proteína total y determinación de actividad enzimática El seguimiento de la obtención del extracto crudo y la purificación parcial de la enzima se monitoreará mediante la determinación de proteínas totales y actividad enzimática empleando las siguientes técnicas: 55 Proteínas Para la medida de la proteína total se empleará el método Bradford (Bradford, 1976) en el cual se utiliza el reactivo Bio-Rad ProteinAssay (BIO-RAD laboratorios GmbH). El método está basado en el cambio de absorbancia a 595 nm de una disolución ácida de azul brillante de Comassie G250 al quedar este colorante unido a las proteínas. Se empleará albúmina de suero bovino (Sigma Chemical CO, St Louis) como patrón de proteína. Actividad enzimática La actividad enzimática (AE) se define como la cantidad de enzima que convierte 1 mol de peróxido de hidrógeno por minuto a pH 7,4 y 25 °C. La actividad de la peroxidasa se determina generalmente por métodos espectrofotométricos, que emplean diferentes combinaciones de tampones y sustratos, variando las condiciones de ensayo en cuanto a temperatura, volumen, concentraciones y pH. En este trabajo se utilizarán 2 técnicas para su determinación empleando como sustrato primario peróxido de hidrogeno y Guayacol (Pütter, 1974). Y 4-aminoantipirina (Bhuniaet al., 2002). d) Caracterización de agua residual de la industria textil Se realizaron 2 muestreos compuestos analizando los parámetros de la NOM 001-SEMARNAT1996 incluyendo color (Pt-Co), colorante (mg/L) y DQO (mg/L) para la caracterización de los efluentes industriales: Uno se realizó en la zona de Santa Ana Xamimilulco Puebla, a una lavandería de mezclilla en donde utilizan principalmente colorantes azo . El segundo muestreo se realizó en la empresa Gutermann, industria ubicada en la zona industrial de Civac, donde realizan la fabricación y teñido de hilos. Es importante mencionar que se contaron con las recetas de cada una de las mezclas utilizadas en los procesos de teñido así como las materias primas que utilizan en cada industria, esto con el objetivo de preparar el agua sintética en el laboratorio en condiciones controladas. Los muestreos se realizaron una sola vez y las industrias proporcionaron suficiente muestra de sus efluentes para realizar los estudios correspondientes. Así mismo para cada uno de las pruebas subsecuentes de tratabilidad se continuó con la toma y recolección semanal de muestras en la empresa Gutterman. e) Cinéticas experimentales con agua artificialmente contaminada y efluente real Las cinéticas experimentales se llevaron a cabo en reactores en discontinuo con un volumen total de 100 mL de capacidad con 50 mL de solución de estudio. El agua residual sintética estará constituida por la receta proporcionada por la lavandería de mezclilla y la fábrica de hilos (Tabla 6.7). El efluente real estudiado será proporcionado por cada una de las industrias, el cual será caracterizado previamente. 56 Tabla 6.7. Aditivos utilizados en la preparación de mezclas para teñido de hilos Aditivo Concentraciones para 3.5 kilos de hilos 105 g 35 g 17.5 g 60 g 350 g Colorantes Sulfato de amonio Albaflow FFA Diadavin Lubricante La reacción se inicia al añadir H2O2, que se bombea en continuo mediante una bomba peristáltica de velocidad variable Masterflex®C/L® Cole-Parmer. Se evaluaron diferentes caudales de adición de H2O2 para obtener las velocidades de adición óptimos para el tratamiento. En las cinéticas se estudiaron los diversos factores que influyen en la decoloración de los efluentes, con el objetivo de encontrar los parámetros óptimos de operación, evaluando los parámetros indicados en la Tabla 6.8 a una temperatura constante de 25°C. Tabla 6.8. Parámetros a evaluar en la degradación enzimática de agua artificialmente contaminada y efluente real. Colorantes utilizados en las industrias (Para cinéticas experimentales con agua sintética) H202 Extracto parcialmente purificado Temperatura pH 10, 20, 30, 40 y 50 mg/L 12.5 - 40 mM 50 - 200 U/L 25 ± 5 2a9 En todas las pruebas se realizó un seguimiento de la concentración del colorante evaluado mediante espectrofotometría, y actividad enzimática, con el objetivo de observar la posible inhibición. Para excluir la posibilidad de que la decoloración fuese debida a un proceso distinto a la reacción enzimática, se realizó un control con peroxidasa de soya inactivada térmicamente. f) Métodos analíticos Cuantificación de color (Pt-Co) y colorante en mg/L presente en el influente y efluente mediante espectrofotometría. Determinación de parámetros de campo, pH, conductividad, temperatura. Determinación de subproductos de degradación por HPLC para el seguimiento de la degradación del colorante y la cuantificación de subproductos generados en el tratamiento enzimático. Las cuales se llevaron a cabo mediante cromatografía de líquidos en un equipo Hewlett-Packard (Series 1100), equipado 57 con un detector de arreglo de diodos con una columna de fase reversa Zorbax Eclipse XDB C-18, 5 μm, 4.6 mm X 250 mm. Se utilizaron 25 L de muestra. g) Determinación del modelo cinético para la degradación de agua sintética y efluentes textiles Se aplicó el método de las velocidades iniciales en pruebas en discontinuo, en los que se variaron las concentraciones iniciales de sustrato y las velocidades de adición de H2O2. Trabajando con concentraciones de sustrato hasta valores de 50 mg/L para cinéticas con agua sintética, con el objetivo de determinar si el sustrato tiene carácter inhibitorio sobre la cinética de la degradación. 6.2.3.- Tratamiento Fisicoquímico: Oxidación Avanzada (Pruebas de Fenton) a) Se preparó una solución de sulfato ferroso de 10,000 mg/L y peróxido de hidrógeno al 50%. b) Se preparó una mezcla de agua con tres colorantes en concentraciones iguales que van de 10 a 100 mg/L, como se muestra en la ¡Error! No se encuentra el origen de la referencia. 6.9 . Tabla 6.9. Concentraciones de preparación. Jarra 1 2 3 4 5 6 Colorante 1 (mg/L) 10 20 40 60 80 100 Colorante 2 (mg/L) 10 20 40 60 80 100 Colorante 3 (mg/L) 10 20 40 60 80 100 Mezcla (mg/L) 30 60 120 180 240 300 Las pruebas se realizaron en un equipo de prueba de jarras, con vasos de precipitado con capacidad de un litro. c) Determinar al agua con la mezcla de colorantes la demanda química de oxígeno (DQO), pH, conductividad eléctrica y color. d) Ajustar el pH de cada jarra a 3, con una solución de ácido sulfúrico 1 N. e) Realizar las siguientes pruebas para determinar condiciones de: - Dosis de sulfato ferroso y peróxido de hidrógeno. - Reacción con agitación de 100 a 200 rpm, con tiempos de 10 a 60 min. - Sedimentación con tiempos de 30 a 120 min. 58 f) Probar y/o validar las condiciones obtenidas con un agua residual de una textilera. g) Obtener las concentraciones de sulfato ferroso y de peróxido de hidrógeno, de tal manera que pueda establecer un intervalo amplio de remoción de color y DQO. 59 7.- Resultados 7.1.- Caracterización de las aguas residuales 7.1.1. Preparación de aguas residuales sintéticas y colorantes utilizados para las pruebas de tratabilidad fisicoquímicas. Los siguientes colorantes fueron empleados para simular un agua residual proveniente de la industria textilera. a) Naranja ácido 24. Clasificación: Diazo. Usos: Se emplea para colorear lana, nylon y cuero. Es soluble en agua y etanol. Estructura química: b) Azul negro directo Clasificación: Diazo Usos: Se utiliza en el teñido de algodón, mezclillas y en el teñido del papel. Estructura química c) Rojo congo Clasificación: Diazo Usos: Tiene una gran afinidad aparentemente, por las fibras de celulosa. Sin embargo, el uso de rojo congo en la industria de la celulosa (algodón textil, pulpa de árbol y papel) ha desaparecido, en parte por su tendencia a cambiar de color una vez que se toca con los dedos manchados de sudor, al correr, y por su toxicidad. En bioquímica e histología, el rojo congo se usa para teñir preparaciones microscópicas, especialmente en tinciones para el citoplasma y los eritrocitos. Estructura química Se hicieron mezclas a partes iguales utilizando éstos tres colorantes con concentraciones de 50 a 300 mg/L. Su caracterización se muestra en la Tabla 7.1. 59 Tabla 7.1. Características del agua residual sintética Colorante mg/L 50 100 150 200 250 300 Color (UPtCo) 847 1692 2650 3667 4242 5208 Solución inicial DQO Conductividad (mg/L) (µS/cm) 35.2 478 50.2 539 69.8 599 93.1 693 98.1 771 122.0 835 pH 7.00 7.14 7.19 7.31 7.42 7.52 Caracterización del efluente general de la lavandería de Santa Ana Xalmimilulco Tabla 7.2 Aguas residuales de la empresa lavadora de mezclillas. 60 Tabla 7.2 b Aguas residuales de la Empresa Gütterman 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Prom pH Conductividad Color (µS/cm) (Pt Co) DQO (mg/L) 6.26 4.79 5.46 6.20 6.77 5.94 6.70 7.19 4.38 5.84 5.70 4.02 6.26 5.28 7.15 5.86 750 1140 1970 1670 1100 1630 2660 2350 1680 1610 1400 2020 1400 1070 1300 1517 1395 1890 2896 2295 2263 3972 2654 2013 4405 2999 2653 2434 2808 3852 2967 2766 1548 1917 2108 1605 1472 5882 3400 3173 8415 5358 2123 3767 4358 3247 5416 3586 7.2.- Pruebas de tratabilidad 7.2.1.- Tratamiento biológico convencional: Procesos acoplado anaerobio-aerobio Durante la primera etapa del experimento para la alimentación del reactor anaerobio UASB se usó el agua residual efluente final de la industria textil Gütermann que contiene las descargas de todos los procesos productivos y los lavados. El agua residual se transportaba en tambos de 200L hasta el laboratorio del IMTA y se tomaban muestras cada vez que se realizaba la carga y transportación del agua. A partir del 11 de octubre de 2012 se empezó a cargar y transportar solo el efluente de la tina de teñido. El efluente sale a una temperatura mayor de 70°C, por lo cual se esperaba hasta que se enfríe para tomar la muestra y transportarlo. Los resultados de los análisis físico-químicos se presentan en la Tabla 7.3. En la muestras se determinaba el parámetro de alcalinidad. Los valores obtenidos variaron entre cero y 8 mg CaCO3/L. Como se puede observar en la Tabla 7.3 el pH del efluente final de la industria varió entre 4.7 y 6.9 y del efluente de la tina varió entre 3.7 y 4.9. Es por esto que el agua residual se neutralizaba con NaOH antes de introducirla al UASB. 61 Tabla 7.3. Características de las aguas residuales utilizadas en el estudio. No. De Punto de muestre muestreo o 1 Efluente Gütermann 2 Efluente Gütermann 3 Efluente Gütermann 4 Efluente Gütermann 5 Efluente Gütermann 6 Efluente Gütermann 7 Efluente Gütermann 8 Efluente Gütermann 9 Efluente Tina 10 Efluente Tina 11 Efluente Tina 12 Efluente Tina 13 Efluente Tina 14 Efluente Tina 15 Efluente Tina pH Conduc tividad, µS·cm-1 SDT, DQO, mg·L-1 mg·L-1 N-NH4, N-NO3, N-NO2, PT, mg·L-1 mg·L-1 mg·L-1 mg·L-1 6.16 830 490 2,745 48 8.9 10 20 6.09 850 416 2,228 30 3.2 3 50 6.62 1,230 609 1,832 65 1.4 70 30 4.69 1,432 709 2,312 84 1.1 113 5 6.67 1,150 840 2,790 114 0.0 123 270 6.54 1,230 740 3,118 129 9.9 11 35 6.88 1,210 620 3,898 98 1.0 70 0.0 6.87 1,030 510 2,282 60 4.0 52 35 4.45 3,880 2,010 7,881 388 15 450 10 4.66 3,900 2,030 10,871 276 90 300 25 4.94 1,518 756 3,635 160 40 100 40 4.68 2,890 1,476 7,128 271 0 105 155 4.88 3,130 1,603 9,426 420 0 56 165 4.21 4,070 2,110 9,200 615 0 37 140 3.67 3,470 457 8,167 84 0.5 5 0.0 62 La conductividad y la concentración de SDT en el efluente de la tina fueron 2.4 veces mayores comparadas con las del efluente final de la industria. El promedio de los SDT en la tina fue de 1,492±654 mg/L y en el efluente final fue de 616±142 mg/L. El promedio de la DQO en la tina fue tres veces mayor que en el efluente final. La DQO promedio en la tina se determinó de 8,044±2,293 mg/L y en el efluente final fue de 2,651±644 mg/L. El promedio del N-NH4 en la tina fue cuatro veces mayor que en el efluente final. La concentración promedio del N-NH4 en la tina se determinó de 316±177 mg/L y en el efluente final fue de 78±34 mg/L. El nitrógeno en ambas aguas residuales es suficiente para el desarrollo normal de las bacterias anaerobias. Tanto en el efluente de la tina como en el efluente final de la industria se determinó presencia de nitritos y nitratos. La concentración promedio del N-NO2 en la tina se determinó de 150±163 mg/L y en el efluente final fue de 56±46 mg/L. La concentración de los nitritos en el efluente de la tina es 2.7 veces mayor que la en el efluente final de la industria. La concentración promedio del N-NO3 en la tina se determinó de 21±34 mg/L y en el efluente final fue de 3.7±3.8 mg/L. La concentración de los nitratos en el efluente de la tina es 5.6 veces mayor que la en el efluente final de la industria. En ambos efluentes, de la tina y el final de la industria, se determinó Ptotal. La concentración promedio del PT en la tina se determinó de 76±73 mg/L y en el efluente final fue de 55±88 mg/L. La concentración del PT en el efluente de la tina es solo 1.4 veces mayor que la en el efluente final de la industria. El fósforo en ambas aguas residuales es suficiente para el desarrollo normal de las bacterias anaerobias. 7.2.1.1.-Seguimiento del proceso en el reactor UASB y LA a) Remoción de DQO Como ya se mencionó en la metodología, el reactor experimental UASB se inoculó con biomasa granular obtenida del reactor UASB de la industria UNIPAK S.A de C.V. localizada en Cuernavaca, Morelos. La caracterización inicial del lodo granular indicó que las concentraciones de ST y SV fueron de 186,331 y 136,443 mg.L-1 respectivamente. En la Figura 7.1 se presenta la variación de la DQO en el influente al reactor anaerobio UASB, en el efluente de este reactor que es el que ingresa después al reactor aerobio de lodos activados, LA y en el efluente del reactor aerobio, LA. En la Figura 7.2 se presentan las remociones de DQO y en la Figura 7.3 se ilustra la variación de la carga orgánica volumétrica en ambos reactores UASB y LA. 63 Durante la primera etapa del experimento se trabajó con el agua residual efluente final de la industria cuya DQO fue de 2,446±592 mg/L en promedio. Se observa que el valor de la DQO es muy similar al mencionado anteriormente promedio de DQO obtenido con base en los muestreos del efluente final de la industria. Durante los 46 días de la primera etapa la remoción de la DQO en el UASB presentó variaciones entre 20 y 67% con una tendencia de incremento. Prácticamente no hubo formación de biogás pero la decoloración del agua lograda en el reactor era evidente. El valor promedio de la DQO en el efluente fue de 1,425±465 mg/L. En resumen aplicando una carga orgánica de 5.3 kg DQO.m-3.d-1 y con un TRH de 11.1 h en el reactor UASB se alcanzó una remoción de 67% después de 46 días de operación. 18000 DQO, mg·L-1 16000 Etapa 1 14000 12000 Etapa 2 10000 8000 6000 4000 2000 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días Influente UASB Efluente UASB Efluente LA Figura 7.1 Variación de los valores de la DQO 64 80% Remoción de DQO 70% Etapa 1 60% Etapa 2 50% 40% 30% 20% 10% 0% 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Remocion de DQO en UASB Tiempo, días Remoción de DQO en LA Remoción total de DQO Figura 7.2 Remociones de DQO 40 COV, kg DQO.m-3.d-1 35 Etapa 1 30 Etapa 2 25 20 15 10 5 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días COV UASB COV LA Figura 7.3 Variaciones de las cargas orgánicas volumétricas en los reactores UASB y LA. 65 Durante la segunda etapa del experimento, la cual empezó el día 52 desde el arranque, el reactor UASB se alimentó con el agua residual descargada directamente de la tina de teñido en la industria. La DQO promedio fue de 7,739±3,180 mg/L, casi tres veces mayor que la DQO del efluente final de la industria textil. Desde el día 52 hasta el día 64 se operó con el mismo caudal de influente que se había aplicado en la Etapa 1. Durante estos días la DQO del agua fue muy elevada, entre 7,691 y 15,669 mg/L, esto provocó un incremento muy grande de la carga orgánica, la cual subió a valores entre 16 y 34 kg DQO.m-3.d-1. Estos valores son típicos para reactores UASB, pero el incremento de la carga fue muy grande y esto provocó inhibición del proceso, la remoción de la DQO fue entre 0 y 10% y no hubo ninguna decoloración del agua la cual tenía un color negro intenso. Para superar la inhibición del proceso se disminuyó el caudal a 16.2 ml.min-1 o 23.3 L d-1, el más bajo que se puede lograr con la bomba peristáltica instalada. La disminución del caudal permitió lograr un TRH de 18.2 h, mayor que el obtenido en la primera etapa. En la Figura 7.1 se observa que a partir del día 66 desde el arranque la DQO en el efluente de la tina disminuyó a 9,853 mg/l y después los valores se mantuvieron entre 4,902 y 8,371 mg/L. Así la COV se redujo y durante los días 73-103 fue de 8.3 ±1.8 kg DQO m-3 d-1. La remoción promedio de DQO durante este tiempo (1 mes de operación en las nuevas condiciones) fue de 16±5% con tendencia de incremento. La DQO promedio en el efluente correspondiente a este período fue de 5,134±1,003 mg/L. El día 66 desde el arranque del reactor UASB, cuando ya se había empezado la alimentación con el agua residual proveniente de la tina de teñido de la industria textil, se inoculó el reactor aerobio de LA con biomasa de un reactor real de LA y empezó su alimentación con el efluente del UASB. Las concentraciones de SSTLM y de SSVLM fueron de 2,970 y 1,460 mg/L respectivamente. El caudal del influente al reactor aerobio LA se ajustó a 16.2 ml.min-1 o 23.3 L d-1, con lo cual se obtuvo un TRH de 14.0 h. La carga orgánica volumétrica dependía de la DQO del efluente del UASB y la carga orgánica másica dependía y de la concentración de los SSVLM. La variación de la COV en LA se puede observar en la Figura 7.3. El promedio de COV en el período día 73-103 fue de 6.51±1.27 kgDQO.m-3.d-1. Al empezar la alimentación del reactor LA, el día 66 desde el arranque del reactor UASB, se determinó una remoción muy baja de DQO, de solo 3%, se manifestaron fenómenos de intoxicación de la biomasa, flotación y formación intensa de espuma. Esto produjo una disminución de la concentración de los SSVLM que el día 72 se determinaron de 660 mg/L, casi la mitad de la biomasa se perdió. Esto provocó incremento de la carga orgánica másica F/M, de 7.7 a 9.9 kg DQO.kg SSV -1.d-1 durante los días 66-72. Sin embargo, a partir de este día disminuyó el efecto de flotación de biomasa y empezó a aumentar la remoción en el reactor LA. La biomasa no crecía y en los siguientes días se mantuvo entre 660 y 880 mgSSVLM/L. En el período días 73-103 la F/M varió entre 6 y 10kg DQO.kg SSV-1.d-1.La remoción promedio de la DQO en el reactor LA durante estos 30 días de operación fue de 14.9±7.7% y la DQO promedio en el efluente del LA fue de 66 4,346±757 mg/L. El promedio de la remoción global de la DQO durante estos 30 días de operación fue de 28.7±7.3% con una tendencia de incremento. Se necesita seguir el proceso de aclimatación y estabilización del proceso en ambos reactores. b) Remoción de SST y SSV En las Figuras 7.4 y 7.5 se presentan las variaciones de los SST y SSV en el influente al reactor anaerobio UASB, en el efluente de este reactor y en el efluente del reactor aerobio LA. En la Figura 7.6 se presentan las remociones de SST y SSV en el reactor UASB y en la Figura 7.7 se presentan las remociones de sólidos en el reactor LA. Durante la primera etapa el reactor UASB se alimentaba con agua del efluente final de la industria y como se observa en las Figuras 7.4 y 7. 5 las concentraciones de los SST y SSV en esta agua eran muy bajos con promedios de 60±16 mg/L y 46±11 mg/L respectivamente. Las remociones de estos sólidos eran muy bajos, con promedios de 21±12% y 30±26% respectivamente. Durante la segunda etapa se alimentó agua residual de la tina de teñido y esta tenía muchos SST y SSV, promedio de SST y SSV de 365±87 y 178±62 mg/L respectivamente. Los SSV representan un 49% de los SST, es decir hay muchas partículas finas inorgánicas en los sólidos suspendidos. Como se puede observar en la Figura 7. 6, las remociones de sólidos suspendidos en el UASB aumentaron. Las remociones promedio de SST y SSV durante la segunda etapa fueron de 84±9% y 75±11% respectivamente. Los sólidos removidos quedan retenidos en el lecho y la fracción orgánica se puede degradar lentamente, la otra fracción la inorgánica queda en el lecho. Durante la segunda etapa las concentraciones promedio de los SST y SSV en el efluente del UASB fueron de 54±18 mg/L y de 44±20 mg/L respectivamente. Esta agua fue influente al reactor LA donde la remoción de SST y SSV fue baja, de 20±20% y 36±27% respectivamente. En la Figura 7.4 se puede observar la tendencia de incremento de la remoción a través del tiempo. Los promedios de SST y SSV en el efluente de LA fueron de 41±2 mg/L y 24±5 mg/L respectivamente. 67 600 500 SST, mg·L-1 400 300 200 100 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 Tiempo, días Influente UASB Efluente UASB Efluente LA Figura 7.4 Variación de las concentraciones de SST 300 250 SSV, mg·L-1 200 150 100 50 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 Tiempo, días Influente UASB Efluente UASB Efluente LA Figura 7.5 Variación de las concentraciones de SSV 68 100 90 80 Remoción, % 70 60 50 40 30 20 10 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 Tiempo, días Remoción de SST en UASB Remoción de SSV en UASB Figura 7.6 Remociones de SST y SSV en el reactor UASB 80 70 60 Remoción, % 50 40 30 20 10 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 Tiempo, días Remoción de SST en LA Remoción de SSV en LA Figura 7.7 Remociones de SST y SSV en el reactor LA. 69 d) Cantidad de biomasa en el reactor de LA La cantidad de biomasa en el reactor LA se midió con los parámetros SSTLM y SSVLM. La variación de estos parámetros se presenta en la Figura 7.8. El día 66 desde el arranque del reactor UASB, cuando ya se había empezado la alimentación con el agua residual proveniente de la tina de teñido de la industria textil, se inoculó el reactor aerobio LA con biomasa de un reactor real de LA y empezó su alimentación con el efluente del UASB. Las concentraciones de SSTLM y de SSVLM fueron de 2,970 y 1,460 mg/L respectivamente. Este día y los 2-3 días posteriores se manifestaron fenómenos de intoxicación de la biomasa, flotación y formación intensa de espuma. Esto produjo una disminución de la concentración de los SSVLM que el día 72 se determinaron de 660 mg/L, casi la mitad de la biomasa se perdió. A partir de este día disminuyó el efecto de flotación de biomasa pero no hubo crecimiento significativo ya que en los siguientes días la concentración de SSVLM se mantuvo entre 660 y 880 mg/L. 3200 2800 SSTLM y SSVLM, mg·L-1 2400 2000 1600 1200 800 400 0 60 65 70 75 80 85 90 95 100 Tiempo, días SSTLM SSVLM Figura 7.8 Variación de las concentraciones de SSTLM y SSVLM en el reactor LA. e) Seguimiento de las concentraciones de las diferentes formas de nitrógeno En las Figuras 7.9 y 7.10 se presenta la variación del N-NH4 en el influente al reactor anaerobio UASB, en el efluente de este reactor (influente al reactor aerobio de LA) y en el efluente del reactor aerobio LA. En la Figura 7.11 se presentan las remociones del N-NH4 en el UASB, en LA y la global en los dos reactores. Durante la primera etapa, cuando el reactor UASB se alimentaba con el efluente final de la industria, el promedio de la concentración del N-NH4 en el influente fue de 98±27 mg/L, en un 70 25% mayor que el determinado con base en los resultados de los muestreos realizados en la industria. El promedio en el efluente fue de 92±19 mg/L, es decir en el reactor UASB hubo una remoción promedio de N-NH4de solo 4%, lo cual es normal para un proceso anaerobio en el cual el N-NH4 se puede remover solo por el consumo para el crecimiento de las bacterias y en muy pequeñas cantidades. La variación de la remoción fue muy grande y en seis ocasiones (día 4, 9, 11, 37, 39 y 43 desde el arranque) se obtuvieron valores de remoción negativos, es decir la concentración del N-NH4 en el efluente en estos casos era mayor que la en el influente. En la Figura7 se presentan solo los valores positivos de la remoción del N-NH4. Considerando la cantidad de DQO removida durante la primera etapa, una remoción de hasta un 23% se puede atribuir a bioasimilación. Durante la segunda etapa el reactor UASB se alimentaba con el agua de la tina. El promedio de la concentración del N-NH4 en el influente fue de 583±367 mg/L, casi 1.8 veces mayor que el determinado con base en los resultados de los muestreos realizados en la industria. Esta diferencia se atribuye a la alimentación de una cantidad de agua residual que tenía una concentración de N-NH4 muy elevada, más de 1,000 mg/L, la cual se tomó y transportó en un día en el cual no se realizó muestreo en la industria. El promedio en el efluente fue de 558±318 mg/L, la remoción promedio fue de un 4% y considerando la cantidad de DQO removida durante la segunda etapa, esta remoción se puede atribuir básicamente a la bioasimilación. Igual que durante la primera etapa en la segunda parte del estudio la variación de la remoción fue grande y en cinco ocasiones (día 73, 75, 85, 94 y96 desde el arranque) se obtuvieron valores de remoción negativos, es decir la concentración del N-NH4 en el efluente en estos casos era mayor que la en el influente. El día 66 desde el arranque del UASB se arrancó el reactor aerobio de LA alimentándolo con el efluente del UASB. En este reactor se espera que las aminas formadas durante la transformación anaerobia se degraden y en este proceso se libera N-NH4. Como se puede observar en la Figura 7.10, el incremento del N-NH4 se observa solo en cuatro de los 10 muestreos realizados, en el resto de los casos (Figura 7.11) se determinaron remociones entre 5 y 23%.El promedio de la concentración del N-NH4 en el influente al LA fue de 558±318 mg/L. El promedio en el efluente fue mayor, de 572±298 mg/L. Durante los muestreos en la industria se determinaron nitritos y nitratos en las descargas del agua residual, tanto en el efluente final de la industria, como en la descarga de la tina de teñido. En las Figuras 7.12 y 7.13 se presentan las concentraciones de los nitritos y de los nitratos determinados en el influente al reactor anaerobio UASB, en el efluente de este reactor y en el efluente del reactor aerobio LA. Durante la primera etapa el promedio de los N-NO3 en el influente al UASB fue de 3.9±0.6 mg/L, similar al determinado con base en los resultados de los muestreos realizados en la industria. En el reactor UASB los nitratos se reducen y en el efluente prácticamente no había nitratos, en algunos muestreos se determinaban concentraciones de 1, 71 mg/L, por lo cual se calculó un promedio para la primera etapa de 0.3 mg/L. El promedio de los nitritos en el influente fue de 54±22 mg/L. Los nitritos también se reducen en el reactor anaerobio pero se observó que la reducción no fue completa y el promedio de la concentración de N-NO2 en el efluente fue de 19±9 mg/L, es decir se redujeron en promedio el 71% de los nitritos presentes en el agua residual. Durante la segunda etapa los análisis de nitratos en el influente al reactor UASB indicaron ausencia de nitratos, solo los días 52 y 58 se determinaron 5 y 3 mg/L respectivamente, los cuales se redujeron en el reactor UASB. En los primeros tres de los seis muestreos del agua residual de la tina realizados en la planta se determinaron nitratos y en el resto de los muestreos no había, lo cual se refleja en el seguimiento de los nitratos en el influente del sistema experimental. El promedio de los nitritos en el influente al UASB fue de 21±4 mg/L, pero los análisis indicaron presencia de nitritos solo los días 52, 58 y 64, después ya no había nitritos. Los muestreos en la planta indicaban presencia de nitritos en el intervalo entre 5 hasta 450 mg/L. Esta diferencia se puede atribuir en una rápida reducción de los nitritos en el agua durante el transporte del agua hasta las instalaciones del IMTA. En los días cuando sí se determinaron nitritos en el influente al UASB, estos se redujeron en el proceso anaerobio. Después del día 66 hasta el día 103 no se encontraron nitritos y nitratos en el influente y efluente del UASB. Tampoco aparecieron nitritos y nitratos en el efluente del reactor aerobio. Esto puede indicar que la degradación de las aminas hasta el momento llega solo hasta la liberación de N-NH4 y todavía no hay nitrificación en el reactor LA. 1400 Concentración del N-NH4, mg L-1 1200 1000 800 600 400 200 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días Influente UASB Efluente UASB Figura 7.9 Variación de las concentraciones del N-NH4 en el influente y efluente del reactor UASB 72 1400 Concentración del N-NH4, mg L-1 1200 1000 800 600 400 200 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días Influente LA Efluente LA Figura 7.10 Variación de las concentraciones del N-NH4 en el influente y efluente del reactor LA. 40% Remoción de N-NH4, % 35% 30% 25% 20% 15% 10% 5% 0% 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días UASB LA Global en el sistema Figura 7.11 Remoción del N-NH4 en los dos reactores UASB y LA. 73 160 140 Concentración NO2, mg·L-1 120 100 80 60 40 20 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 110 Tiempo, días Influente Efluente anaerobio Efluente aerobio Figura 7.12 Variación de las concentraciones de los nitritos 9 8 Concentración NO3, mg·L-1 7 6 5 4 3 2 1 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días Influente Efluente anaerobio Efluente aerobio Figura 7.13 Variación de las concentraciones de los nitratos 74 f) Remoción de fósforo total En la Figura 7.14 se presenta la variación del fósforo total (PT) en el influente al reactor anaerobio UASB, en el efluente de este reactor y en el efluente del reactor aerobio LA. En la Figura 7.15 se presentan las remociones del fósforo en el UASB, en LA y la global en los dos reactores. Durante la primera etapa, cuando el reactor UASB se alimentaba con el efluente final de la industria, el promedio de la concentración del PT en el influente fue de 68±53 mg/L, muy similar al determinado con base en los resultados de los muestreos realizados en la industria. El promedio en el efluente fue de 38±34 mg/L, alrededor de 44% de remoción con grandes variaciones, obteniéndose en tres ocasiones (día 4, 9 y 16 desde el arranque) valores de remoción negativos, es decir la concentración del PT en el efluente era mayor que en el influente. En la Figura12se observa que la remoción del PT aumentaba a través del tiempo, alcanzando una remoción de hasta 87%el día 35 desde el arranque pero las variaciones eran grandes de casi 20% entre una u otra determinación. En el último día de este período se determinó otra vez una remoción baja, de solo 19%. Una remoción del fósforo de 15% se puede atribuir a bioasimilación, las remociones mayores de esta se pueden atribuir a precipitación y acumulación dentro del lecho. El fósforo acumulado probablemente se solubiliza y libera periódicamente lo cual puede explicar las variaciones tan grandes de las remociones. Durante la segunda etapa el reactor UASB se alimentaba con el agua de la tina. El promedio de la concentración del PT en el influente fue de 58±44 mg/L, en un 40% menor que el determinado con base en los resultados de los muestreos realizados en la industria. El promedio en el efluente fue de 59±33 mg/L, es decir en promedio no hubo remoción de PT en esta etapa. En la Figura12se observan solo tres resultados que muestran remoción de PT, en el resto de los muestreos se determinaba una remoción nula o se obtenían valores negativos. El día 66 desde el arranque del UASB se arrancó el reactor LA alimentándolo con el efluente del UASB. Casi 20 días después del arranque del reactor LA por primera vez se observó una remoción del PT en este.El promedio de la concentración del PT en el influente al LA fue de 59±33 mg/L. El promedio en el efluente fue de 49±28 mg/L, representando esto una remoción promedio para la segunda etapa de solo 16%. 75 200 180 Concentración PT, mg·L-1 160 140 120 100 80 60 40 20 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días Influente Efluente anaerobio Efluente aerobio Figura 7.14 Variación de las concentraciones del PT 100% 90% Remoción de PT, % 80% 70% 60% 50% 40% 30% 20% 10% 0% 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100 105 Tiempo, días UASB LA Global en el sistema Figura 7.15 Remoción del PT en los dos reactores UASB y LA. 76 Conclusiones El reactor anaerobio tipo UASB puede ser utilizado como primera etapa del tratamiento biológico del efluente general de la industria textil que tiene una DQO promedio de 2,446±592 mg/L. Aplicando una carga orgánica de 5.3 kg DQO.m-3.d-1 y con un TRH de 11.1 h en el reactor UASB se alcanzó una remoción de 67% después de 46 días de operación. Las concentraciones de SST y SSV en el efluente general de la industria son bajas, con promedios de 60±16 mg/L y 46±11 mg/L respectivamente. Las remociones de estos sólidos en el UASB son de 21±12% y 30±26% respectivamente. La concentración promedio del N-NH4 en el influente al UASB mientras se operaba con el agua residual del efluente general de la industria fue de 98±27 mg/L. Como es de esperarse en el reactor anaerobio no hubo una remoción significativa del N-NH4. La remoción promedio fue de solo 4% y considerando la cantidad de DQO removida durante la primera etapa, esta remoción se puede atribuir a bioasimilación. Durante los muestreos en la industria se determinaron nitritos y nitratos en las descargas del agua residual, tanto en el efluente final de la industria, como en la descarga de la tina de teñido. El promedio de la concentración de N-NO3 en el influente al UASB mientras este se operó con el efluente general de la industria fue de 3.9±0.6 mg/L. En el reactor UASB los nitratos se reducen y en el efluente prácticamente no hay nitratos. La concentración promedio de los nitritos en el influente al UASB fue de 54±22 mg/L. Los nitritos también se reducen en el reactor anaerobio pero se observó que la reducción no fue completa, se redujeron en promedio el 71% de los nitritos presentes en el agua residual. La concentración promedio del fósforo total en el influente al UASB mientras se operaba con el agua residual del efluente general de la industria fue de 68±53 mg/L. La remoción promedio fue de 44% con variaciones muy grandes. Una remoción del fósforo de 15% se puede atribuir a bioasimilación, las remociones mayores de esta se pueden atribuir a precipitación y acumulación dentro del lecho. El fósforo acumulado probablemente se solubiliza y libera periódicamente lo cual puede explicar las variaciones tan grandes de las remociones. El agua residual descargada directamente de la tina de teñido en la industria tiene una DQO promedio de 7,739±3,180 mg/L, casi tres veces mayor que la DQO del efluente general de la industria textil. Esta agua residual es fuertemente inhibitoria para la biomasa granular del reactor UASB. Operando el reactor con una carga orgánica de 8.3 ±1.8 kg DQO m-3 d-1 y con un TRH de 18.2 h durante más de un mes se obtuvo una remoción promedio de DQO de solo 16±5% con tendencia de incremento. 77 Las concentraciones de SST y SSV en el efluente de la tina son de 365±87 y 178±62 mg/L respectivamente. Los SSV representan un 49% de los SST, es decir hay muchas partículas finas inorgánicas en los sólidos suspendidos. Las remociones de SST y SSV logradas en el UASB son de 84±9% y 75±11% respectivamente. Los sólidos removidos quedan retenidos en el lecho y la fracción orgánica se puede degradar lentamente, la otra fracción la inorgánica queda en el lecho. La concentración promedio del N-NH4 en el influente al UASB, mientas este se operaba con agua de la tina de teñido, fue de 583±367 mg/L. La remoción promedio de 4%, se atribuye igual que en el caso anterior, a bioasimilación. En el influente al UASB, mientras se operaba con el agua residual de la tina, no se había nitratos. Nitritos se encontraron solo durante los primeros 12 días y después ya no. En los días cuando sí se determinaron nitritos en el influente al UASB, estos se redujeron en el proceso anaerobio. La concentración promedio del fósforo total en el influente al UASB, mientas este se operaba con agua de la tina de teñido, fue de 58±44 mg/L. El promedio en el efluente fue de 59±33 mg/L, es decir en promedio no hubo remoción de fósforo. El reactor de lodos activados usado como segunda etapa del tratamiento biológico del agua residual de la tina de teñido de la industria textil, operado con una carga orgánica volumétrica de 6.51±1.27 kgDQO.m-3.d-1y un TRH de 14.0 h, permitió obtener una remoción promedio de14.9±7.7%. La aclimatación de la biomasa al sustrato presente en el agua residual efluente del UASB es difícil, con problemas de intoxicación de la biomasa e inhibición de la degradación de la materia orgánica y del crecimiento de la biomasa, sin embargo, fue posible superar la intoxicación en unos 10 días, pero la remoción aumenta muy lentamente. El promedio de la remoción global de la DQO (en los dos reactores) durante los últimos 30 días de operación fue de 28.7±7.3% con una tendencia de incremento. Se necesita seguir el proceso de aclimatación y estabilización del proceso en ambos reactores. Las remociones de SST y SSV en el reactor lodos activados son de 20±20% y 36±27% respectivamente, obteniéndose en el efluente concentraciones de SST y SSV de 41±2 mg/L y 24±5 mg/L respectivamente. El promedio de la concentración del N-NH4 en el influente al LA fue de 558±318 mg/L. El promedio en el efluente fue mayor, de 572±298 mg/L. En este reactor se espera que las aminas formadas durante la transformación anaerobia se degraden y en este proceso se libera N-NH4. En el efluente del reactor aerobio no se encontraron nitritos y nitratos. Esto puede indicar que la degradación de las aminas llega solo hasta la liberación de N-NH4 y todavía no hay nitrificación en el reactor LA. 78 El promedio de la concentración del fósforo total en el influente al LA fue de 59±33 mg/L. El promedio en el efluente fue de 49±28 mg/L, representando esto una remoción promedio de 16%. 79 7.2.2.- Tratamiento biológico no- convencional 7.2.2.1.- Tratamiento fúngico Color aparente Los estudios sobre color, fueron analizados en sus 2 modalidades (aparente y verdadero) como se muestran en las gráficas siguientes. En la figura 7.16 y 7.17, se observó el comportamiento de los datos de los 4 reactores para las dos cargas orgánicas de operación. El reactor 2 fue el único que muestra picos sobre el color del influente, los demás están por debajo del influente. El reactor 4 (figura 7.16), mostró una disminución gradual del color aparente a diferencia del reactor 1 que se mantiene inestable. Por lo que se puede intuir que el P.O. tuvo un efecto para la disminución de color. El reactor 2 mostró una disminución de color aparente pero muy inestable. En comparación, el reactor 3 mantuvo un comportamiento más estable (figura 7.17). Las remociones de los reactores se muestran en la tabla 7.4, mostrando mejores remociones promedio el reactor 4, debido posiblemente al trabajo en conjunto de P.O., bacterias y procesos físicos. Figura 7.16 Comportamiento del color aparente en los efluentes de los reactores 1 y 4 con respecto al influente 79 Figura 7.17 Comportamiento de color aparente en los efluentes de los reactores 2 y 3 con respecto al influente Tabla 7.4 Remoción de color aparente Reactor 1 2 3 4 Remoción de color aparente Carga 1 (%) Carga 2 (%) 25 42 10 31 13 30 14 61 Color verdadero En el caso del color verdadero, como lo muestra la figura 7.18 y 7.19, donde se condensan los datos de los 4 reactores respecto al influente. Se observó para la primera carga (607.17 mg/L d) una disminución en el color verdadero en todos los reactores, con algunas alzas repentinas. En la segunda carga (161.7 mg/L d) el comportamiento general del color verdadero en los cuatro reactores tiende a bajar. En la figura 7.18 se comparó el reactor con turba sin esterilizar (R1) y el reactor 4 inoculado con Po con turba sin esterilizar (R4). En esta gráfica se mostró que el reactor 1 tuvo mejor desempeño que el reactor 4 con la primera carga. Pero para la segunda carga este 80 comportamiento cambio totalmente, mostrando el reactor 4 mejores resultados. Los porcentajes de remoción para los reactores se muestran en la tabla 7.5. Figura 7.18 Comportamiento del color verdadero en los efluentes de los reactores 1 y 4 con respecto al influente Figura 7.19 Comportamiento del color verdadero en los efluentes de los reactores 2 y 3 con respecto al influente 81 Tabla 7.5 Remoción de color verdadero Reactor 1 2 3 4 Remoción de color verdadero Carga 1 (%) Carga 2 (%) 18 43 10 50 10 27 11 80 Concentración de color Las gráficas siguientes muestran el comportamiento de la concentración de colorante en el influente como en los efluentes. En la gráficas 9.15 y 9.16, se observó que el reactor 2, 3 y 4 tienen un comportamiento similar para la primera carga, sin embargo el reactor 1 sobresale, mostrando valores bajos de concentración de colorante en su efluente. Para la segunda carga (161mg/L d), los reactores 1, 2 y 4 mostraron el mismo comportamiento, excepto el reactor 3, mostrando concentraciones de colorante más altas en su efluente. Al realizar una comparación entre el reactor 4 y el reactor 1. Se observó que el reactor 1 en la primera etapa tuvo mejores resultados, ya que la concentración de colorante en su efluente fue baja. A diferencia, el reactor 4 mostró mayores concentraciones de colorante. El comportamiento de los reactores para la segunda carga cambio, mostrando el reactor 1 remoción de concentración de colorante de 43% y el reactor 4 de 60% (tabla 7.6). Esto se observó claramente en la figura 7.20, con la disminución de la concentración de colorante. En la figura 7.21 para los reactores 2 y 3 observamos un comportamiento similar en la concentración de color para el tratamiento con la primera carga. Los reactores 2 y 3 con esta carga mostraron remociones de 13 %y 12%. Del día 31 de operación donde se operó con una carga de 161mg/L d, observamos mejores resultados con el reactor 2. En promedio el reactor 2 obtuvo una remoción del 48% y el reactor 3 una remoción de 12%. En la figura 7.21 podemos se observó claramente el comportamiento de disminución de la concentración de colorante en el efluente reactor 2. 82 Figura 7.20 Comportamiento de la concentración de color en los efluentes de los reactores 1 y 4 con respecto al influente Figura 7.21 Comportamiento de la concentración de color en los efluentes de los reactores 2 y 3 con respecto al influente 83 Tabla 7.6 Remoción de color Reactor 1 2 3 4 Remoción de concentración de color Carga 1 (%) Carga 2 (%) 24 43 13 48 12 12 13 60 Demanda química de oxígeno En cuanto a los resultados de DQO para la primera carga orgánica volumétrica (607.17mg/L d) se observó un decremento en la DQO de salida en todos los reactores (figura 7.22 y 7.23). En la figura 7.22, donde se comparó el reactor 1 y 4 para la primera carga, observamos que el reactor 4 muestra DQO más alta que el reactor 1. Esto debido a que el P. ostreatus tiene un aporte de materia orgánica al medio, ya sea por desprendimiento de micelio o por las enzimas excretadas. También para el reactor 4 en el día 23 observamos muerte del hongo. Por lo cual decidimos bajar la carga orgánica a 161.7mg/L d. Con esta nueva carga observamos los primeros días un incremento en la DQO y posteriormente una estabilización. Las DQO obtenidas son bajas en comparación del influente y ligeramente más altas que el efluente del reactor 1. Los porcentajes de remoción en promedio para estos dos reactores se muestran en la tabla 7.7. La figura 7.23, que comparó el reactor 2 y 3 para la primera carga, observamos que el reactor 2 muestra variabilidad en DQO al igual que el reactor 3. También para el reactor 2 en el día 23 observamos muerte del hongo. Por lo cual decidimos bajar la carga orgánica a 161.7mg/L d. Con esta nueva carga observamos los primeros días un incremento en la DQO. Esto debido a que P. ostreatus tiene un aporte de materia orgánica al medio, ya sea por desprendimiento de micelio o por las enzimas excretadas Las DQO obtenidas son muy altas en comparación del influente y el efluente del reactor 3. Los porcentajes de remoción en promedio para estos dos reactores se muestran en la tabla 7.7. Mostrando mejores remociones el reactor sin inocular y que pasó por un proceso de esterilización. De los cuatro reactores el que mejor desempeño tuvo hasta el momento es el reactor 1, mostrando que el procedimiento de esterilización del material de empaque si tuvo un efecto negativo. Además de mostrar hasta el momento que la materia orgánica fue removida y disminuida por el proceso de adsorción, absorción de la turba y degradación debida a microorganismos adheridos a la turba. 84 Figura 7.22 Comportamiento de la demanda química de oxígeno en el reactor con turba sin esterilizar (R1) y el reactor con turba sin esterilizar inoculado con P.O. (R4) Figura 7.23 Comportamiento de la demanda química de oxígeno en el reactor con turba que pasó por un proceso de esterilización (R3) y el reactor con turba estéril inoculado con P.O. (R2) 85 Tabla 7.7. Remoción de materia orgánica Reactor 1 2 3 4 Remoción de DQO Carga 1 (%) Carga 2 (%) 52 30 29 0 30 33 41 8 7.2.2.2 Tratamiento enzimático Cinéticas en función de la concentración de colorante Se realizaron pruebas de degradación a distintas concentraciones iníciales del colorante con el fin de observar el efecto de la concentración de sustrato en la cinética de degradación. Se trabajó con las mismas concentraciones iníciales de EPP en todas las pruebas, y se siguió la concentración del colorante durante 6 h, a intervalos de 1 h. Los perfiles de decoloración para las concentraciones iníciales de 10-20-30 y 40 mg/L se muestran en la Figura 7.24. Figura 7.24 Decoloración del colorante AND en pruebas en discontinuo a diferentes concentraciones iniciales: ( ) 10 mg/L; ( ) 20 mg/L; ( ) 30 mg/L; () 40 mg/L. Aplicando el método de las velocidades iníciales, se consideraron las pendientes de degradación de cada ensayo en el intervalo de tiempo tal que los pares de puntos proporcionaran una cinética de primer orden con respecto al sustrato. Para determinar ese intervalo se realizó una representación de ln(S/S0) frente al tiempo y se calculó la constante cinética k de cada ensayo 86 como la pendiente de los puntos que constituyen una recta. Los valores de dichas constantes y las velocidades de reacción calculadas a partir de las mismas se representan en la Tabla 7.8. Tabla 7.8. Parámetros cinéticos de la degradación del colorante AND a diferentes concentraciones iniciales Como se puede observar en la Tabla 7.8, las mayores velocidades de degradación se obtuvieron en el intervalo entre 20 y 30 mg/L de colorante AND. A partir de esta concentración la velocidad de reacción disminuye, lo cual indica un posible comportamiento cinético de inhibición por sustrato. Se realizó un ajuste de estos datos al modelo de Haldane (Ecuación 2), cuya linealización se representa en la Ecuación 3 y Figura 7.25. 87 Figura 7.25 Linealización de los datos experimentales de velocidades de degradación del colorante AND mediante un modelo de inhibición por substrato Para valores elevados de S, el primer término del segundo miembro de la Ecuación 3 pierde importancia, por lo que resulta una expresión lineal de S. Por el contrario, para valores pequeños de S, es el tercer término del segundo miembro de la Ecuación 3 es el que resulta menos significativo. De ahí que las linealizaciones sean efectivas para el cálculo de K I en el primer caso y KM en el segundo. Las constantes cinéticas obtenidas rm, KM y KI se representan en la Tabla 7.9. Tabla 7.9. Parámetros cinéticos del modelo de inhibición por substrato El valor de la constante de inhibición es muy pequeño, lo que indica que la inhibición sólo se produce cuando las concentraciones del colorante AND son elevadas. Por otro lado, la disminución en la velocidad de reacción no es demasiado alta incluso para concentraciones del orden de 30 mg/L, como se puede observar en la Figura 7.26, en la que se corrobora el ajuste del modelo cinético a los datos experimentales. 88 Figura 7.26 Comprobación del modelo cinético de inhibición por substrato ( experimentales: (--) modelo cinético. ) datos La obtención de un modelo cinético que ajuste los datos experimentales es de gran utilidad para el diseño de un reactor en continuo y su escalado. En primer lugar, el modelo ofrece información acerca del tipo de reactor más adecuado para el proceso. En el caso de un proceso de inhibición por substrato, un reactor de mezcla completa minimiza la posible ralentización que pueda surgir debida a la presencia de altas concentraciones de sustrato. La disponibilidad de un modelo cinético resulta de gran utilidad para el diseño de reactores, aunque es necesario estudiar la aplicabilidad de la ecuación obtenida a otras configuraciones de reactores (Bódalo et al., 2001a; Cantarella et al., 2004). Por último, el modelo permite realizar simulaciones que describan el comportamiento del reactor en estados no estacionarios y la respuesta del sistema a cambios en las condiciones de trabajo similares a los que puedan tener lugar en un proceso real (Bódalo et al., 2001b). Cinética en función de la concentración de colorante AND y H2O2 El H2O2 es sustrato de la reacción enzimática de oxidación de la forma P nativa a P I, de manera que puede ser considerado, junto con el colorante AND, en el modelo cinético del proceso de degradación. Sin embargo se debe tener en cuenta que el H2O2 tiene una doble función en la reacción enzimática. Por una parte, como sustrato de la primera reacción del ciclo catalítico, un aumento en la concentración de H2O2 debería favorecer la cinética de la degradación enzimática. Pero por otra parte, el H2O2 actúa sobre la forma P II dando lugar a una forma P III inactiva (Timofeevski et al., 1998), con lo cual una excesiva concentración de H2O2 puede provocar una elevada pérdida de actividad enzimática. Con el objetivo de determinar la relación entre la cinética de la reacción y la pérdida de actividad, se estudiaron diversas estrategias de adición de H2O2 al medio de reacción (Mielgo et al., 2003) y se concluyó que un bombeo en continuo permite adecuar la 89 adición de H2O2 al consumo que tiene lugar en el reactor, de manera que la concentración puntual sea prácticamente nula y la desactivación enzimática sea mínima. Con el objetivo de obtener un modelo cinético en función de las concentraciones del colorante AND y de H2O2, se planteó realizar pruebas de degradación en discontinuo a diferentes concentraciones iníciales de ambos sustratos, y realizar un seguimiento de las cinéticas de desaparición de los mismos, aplicando el método de las velocidades iníciales para determinar los parámetros cinéticos. Sin embargo, se ha de considerar que la operación en continuo persigue una estrategia de adición de H2O2 tal que las concentraciones puntuales en el reactor sean prácticamente nulas. Moreira et al., (2001) midieron la concentración de H2O2 en las pruebas en discontinuo mediante un electrodo de epoxi-grafito y obtuvieron que el consumo de H2O2 es del orden de 0,17 μmol H2O2 por unidad enzimática y min. Para evitar la desactivación, la adición de H 2O2 en el reactor en continuo estará dentro de un rango que no debería superar este valor, que equivale a unos 8 μmol/L-min H2O2 para las condiciones de trabajo. Con esta velocidad de adición la concentración puntual de H2O2 debería ser prácticamente nula. Por este motivo, el modelo cinético no puede ser una función de la concentración de H 2O2, sino de la velocidad de adición del mismo, que presenta una relación directa con la cinética de degradación. En función de lo indicado, el modelo cinético propuesto supone un modelo físico con respecto a la concentración deI colorante AND y un modelo empírico con respecto a la velocidad de adición de H2O2. Se realizaron pruebas de degradación enzimática del colorante AND en discontinuo a diferentes concentraciones iniciales de colorante de (10-20-30-40 mg/L) y diferentes velocidades de adición de H2O2 (1.25, 8 y 12.5 μmol/L-min) en un medio conteniendo EPP en las concentraciones presentadas en el capítulo de Materiales y métodos. Se siguió la concentración del colorante durante 6 h, a intervalos de 1 h hasta la finalización de los experimentos. Los resultados se muestran en las Figuras 7.27. 90 Figura 7.27 decoloración del colorante AND en pruebas a diferentes velocidades de adición de H2O2: ( ) 1.25 µmol/L-min; ( ) 8 µmol/L-min; () 12.5 µmol/L-min y diferentes concentraciones de colorante: (a) 40 mg/L; (b) 30 mg/L; (c) 20 mg/L; (d) 10 mg/L En la mayoría de las condiciones aplicadas se alcanzó una decoloración superior al 90% tras 6 h de reacción. Para una concentración del colorante AND de 40 mg/L fue necesaria una mayor cantidad de H2O2 para lograr una decoloración entorno a ese valor. Sin embargo, una adición de 1.25 μmol/L-min no fue suficiente para degradar el 90% del colorante aun cuando la concentración inicial de este fue de 10 mg/L. En la Tabla 7.10 se presentan los valores de las velocidades iníciales para cada uno de las pruebas realizadas. Para trabajar con concentraciones de sustrato iguales o inferiores a 40 mg/L, y tal como se ha visto en el apartado anterior, cabe esperar fenómenos de inhibición por sustrato (colorante AND). Sólo en el caso de una adición de H2O2 elevada, de 12.5 μmol/L-min se pudo observar cierta inhibición a concentraciones de 40 mg/L de colorante AND, debida probablemente a una inhibición parcial de la enzima. Por otra parte, se observa que existe una relación entre las velocidades cinéticas y la velocidad de adición de H2O2. Tabla 7.10. Velocidades de degradación del colorante AND a diferentes concentraciones de colorante y diferentes velocidades de adición de H2O2 91 En las condiciones de operación, el término de inhibición de la ecuación de Haldane determinado anteriormente no sería significativo con respecto al resto de los términos de la ecuación. Se consideró por ello el modelo más sencillo de Michaelis-Menten con respecto a la concentración del colorante, y una función lineal con respecto a la velocidad de adición de H 2O2, como se presenta en la Ecuación 4. donde KH2O2 es la constante de la función de la adición de H2O2 y QH2O2 es la velocidad de adición de H2O2. Si bien la constante cinética rm ya no tiene el significado de velocidad máxima, se seguirá manteniendo esta nomenclatura. Para una velocidad de adición de H 2O2 constante, se puede considerar una velocidad máxima rm’ para cada uno de los valores de velocidad de adición, de manera que la Ecuación 4 se puede transformar en la Ecuación 5, en donde el término de la velocidad máxima aparente resulta una función lineal de la velocidad de adición de H2O2, para valores de este, iguales o inferiores a 12.5 μmol/L∙min. Los valores de rm’ y KM para cada valor de velocidad de adición se expresan en la Tabla 7.11. Tabla 7.11. Parámetros cinéticos de la degradación del colorante AND a diferentes velocidades de adición de H2O2. Considerando un valor medio de KM, que no debe variar con la velocidad de adición de H2O2, se obtiene una regresión lineal entre el valor de la velocidad máxima aparente r m’ y la velocidad de adición de H2O2, determinándose los parámetros cinéticos de la Ecuación 4, que se muestran en la Tabla 7.12. 92 Tabla 7.12. Parámetros del modelo cinético en función de la concentración del colorante AND y la adición de H2O2. A partir de estos parámetros cinéticos se puede comprobar cómo el modelo propuesto ajusta los datos experimentales, para cada una de las velocidades de adición de H2O2 de trabajo (Figura 7.28). El error entre los datos experimentales y los propuestos por el modelo es menor del 5% en la mayoría de los casos, lo que indica que el tipo de modelo aplicado y los valores de las constantes cinéticas obtenidos son adecuados para describir el sistema de reacción. Figura 7.28 Comprobación del modelo cinético en función de la concentración del colorante AND y la velocidad de adición de H2O2: ( ) 1.25 µmol/L.min; ( ) 8 µmol/L.min; () 12.5 µmol/L.min; (--) datos simulados por el modelo cinético Conclusiones La oxidación enzimática del colorante AND mediante la enzima Peroxidasa constituye un método muy efectivo para su degradación. Las condiciones en las cuales la oxidación es más rápida y la actividad enzimática se ve menos afectada. El crudo enzimático es el factor más costoso del proceso. Por ello, para determinar el valor de actividad enzimática más adecuado se consideraron parámetros económicos. Por encima de 150-200 U/L de Peroxidasa no se 93 apreciaron grandes cambios en cuanto a la cinética del proceso. Por ello, se consideró ese rango como el más adecuado para los procesos de degradación. Para facilitar la obtención y posterior aplicación de las ecuaciones cinéticas asumieron una serie de consideraciones: el proceso es isotérmico, el volumen reacción es constante y el reactor está perfectamente agitado. A partir de estas suposiciones se aplicó el método diferencial de velocidades iníciales, en el que se consideró la pendiente inicial de degradación del colorante AND para cada concentración inicial de colorante. Se podría considerar un método diferencial que tomase todos los pares de puntos de concentración frente a tiempo para realizar el cálculo de los parámetros cinéticos, de forma que ganasen más peso aquellos puntos obtenidos a concentraciones bajas de colorante, por ser los más abundantes. El modelo propuesto para la degradación del colorante AND es un modelo semiempírico, que resulta de la combinación del modelo de Michaelis-Menten con respecto a la concentración del colorante y un modelo matemático con respecto a la velocidad de adición de H 2O2. Concentraciones elevadas de colorante producen un efecto inhibitorio en la reacción enzimática, de manera que la velocidad de reacción disminuye, aunque muy levemente. El modelo es útil para determinar la concentración de colorante que aporta una cinética más elevada, que está entorno a 40, 50 mg/L. Sin embargo a medida que la concentración inicial aumenta, el porcentaje de decoloración alcanzado es menor, lo que implica que tras la reacción puede permanecer en el medio una concentración elevada del colorante. La concentración del AND se ha de seleccionar teniendo en cuenta ambos factores, cinética y decoloración, con el objetivo de alcanzar una decoloración adecuada en un tiempo reducido. El efecto del H2O2 en la ecuación cinética resulta ejercer una dependencia lineal con respecto, no a su concentración puntual (que es prácticamente nula), sino a su velocidad de adición. El modelo indica que a medida que aumenta la velocidad de adición de H 2O2 (hasta 12.5 μmol/L∙min) la degradación de tinte tiene lugar a mayor velocidad. Para velocidades más altas de adición de H2O2 deberá considerarse el aspecto de desactivación de la Peroxidasa debido a concentraciones elevadas de H2O2. La determinación del caudal óptimo de H2O2 ha de resultar un factor entre la velocidad de la degradación y la desactivación enzimática. En conclusión, el modelo cinético propuesto es una herramienta útil para conocer la cinética del proceso, ya que por medio de ella se puede estudiar cómo los diversos parámetros (concentración del colorante AND, velocidad de adición de H2O2) afectan a la velocidad de degradación del colorante, y permite decidir cuáles son las condiciones que favorecen una cinética más rápida. 94 7.2.3. - Tratamiento Fisicoquímico: Procesos avanzados de oxidación (procesos Fenton) Los efluentes de la industria textil y de la industria de colorantes son uno de los principales contaminantes de agua ya que se encuentran altamente coloreados y con grandes cantidades de químicos los cuales son utilizados en sus procesos de producción. Los colorantes azo son usualmente los contaminantes más problemáticos en los efluentes de la industria textil debido a que no se fijan en su totalidad a las fibras y el resto termina en los cuerpos receptores (Park y Choi, 2003). Los procesos de oxidación avanzada aparecieron como una opción de tratamiento particularmente en los casos donde los contaminantes son difíciles de remover. Se presentan a continuación las pruebas realizadas para la obtención de las condiciones de operación para el proceso de oxidación avanzado de los efluentes de la industria textil (agua residual industrial real) utilizando el Proceso de Fenton. La combinación de Fe2+ y H2O2 va a generar radicales HO•, que a su vez van a reaccionar a continuación por dos vías: la oxidación de Fe (II) (reacción improductiva) y el ataque a la materia orgánica como se explica en el inciso 5.2.1.c) a) Prueba No. 1 La prueba se realizó en un equipo de jarras y las condiciones fueron: Agitación 150 rpm por 10 min, 100 rpm por 20 min y sedimentación por 30 min., con ajuste a pH 3. Las características iniciales y finales del agua de prueba se presentan en la 7.13 y en la ¡Error! No se encuentra el origen de la referencia.7.14. Tabla 7.13. Características del agua de la prueba 1ª H2O2 mg/L 560 760 960 1160 1360 1560 FeSO4 mg/L 120 170 220 270 320 370 Color (UPtCo) Inicial Final 926 75.33 1767 101.67 3508 74.00 4583 90.33 4967 78.33 6042 110.33 mg/L 50 100 150 200 250 300 Remoción (%) 91.87 94.25 97.89 98.03 98.42 98.17 Tabla 7.14. Características del agua de la prueba 1b H2O2 mg/L FeSO4 mg/L Color (UPtCo) mg/L Inicial Final Remoción % 560 960 120 220 50 150 51.33 86.33 94.46 97.54 926 3508 105 1360 320 250 4967 136.67 97.25 Con las condiciones antes descritas se obtienen remociones de color superiores al 90% de color. Si el color inicial del agua aumenta será necesario incrementar las dosis de los reactivos hasta en un 300% para mantener una remoción superior al 90%. En este caso la relación empleada de sulfato y peróxido fue de 1:4. b) Prueba No.2 La prueba se realizó en un equipo de jarras y las condiciones fueron: Agitación 175 rpm por 30 min y sedimentación por 120 min., con ajuste a pH 3. Las características iniciales y finales del agua de prueba se presentan en la 7.15 y en la ¡Error! No se encuentra el origen de la referencia.7.16. Tabla 7.15. Características del agua de la prueba No.2 H2O2 mg/L FeSO4 mg/L Solución inicial Color mg/L (UPtCo) DQO (mg/L) Conductividad pH (µS/cm) 560 120 50 847 35.2 478 7.00 750 165 100 1692 50.2 539 7.14 930 200 150 2650 69.8 599 7.19 1100 240 200 3667 93.1 693 7.31 1240 260 250 4242 98.1 771 7.42 1320 280 300 5208 122.0 835 7.52 Tabla 7.16. Características finales del agua de la prueba No.2 14.00 Conductividad pH (µS/cm) 1033 2.85 Color DQO (UPtCo) (mg/L) 112.67 34.9 Remoción Color (%) 86.06 Remoción DQO (%) 0.85 11.33 1199 2.85 102.33 24.1 94.73 51.99 15.00 1385 2.84 118.33 22.4 95.49 67.91 17.00 1508 2.83 147.67 36.6 95.20 60.69 17.67 1547 2.86 176.67 31.6 95.83 67.79 24.33 1734 2.84 249.00 15.3 95.59 87.46 SST (mg/L) 106 Con las condiciones antes descritas se obtienen remociones de color que están entre un 86 y un 95% de color, y de DQO del 1 al 87%. Además, se mantuvo la relación empleada de sulfato y peróxido que fue de 1:4. En este caso como se puede observar las remociones disminuyeron, al obtenerse valores finales de color en el agua superiores a los 100 UPtCo. c) Prueba No. 3. La prueba se realizó en un equipo de jarras y las condiciones fueron: Agitación 200 rpm por 15 min y sedimentación por 120 min. Con ajuste a pH 3. Las características iniciales y finales del agua de prueba se presentan en la ¡Error! No se encuentra el origen de la referencia.7.17 y en la ¡Error! No se encuentra el origen de la referencia.7.18. Tabla 7.17. Características del agua de la prueba No. 3 H2O2 mg/L 560 FeSO4 mg/L 120 Colorante (mg/L) Solución inicial DQO Conductividad Color (UPtCo) (mg/L) (µS/cm) 50 808 49.9 475 7.60 750 165 100 1942 67.3 529 7.60 930 200 150 2625 74 636 7.50 1100 240 200 3075 138.8 724 7.60 1240 260 250 4233 113.9 808 7.70 1320 280 300 5650 142.1 882 7.70 pH Tabla 7.18. Características finales del agua de la prueba No. 3 SST (mg/L) Cond (µS/cm) pH Color (UPtCo) DQO (mg/L) Remoción Color (%) Remoción DQO (%) 10.00 1185 3.2 122.67 15.3 84.82 69.34 28.67 1378 3.1 274.67 20.8 85.86 69.09 22.67 1484 3.0 204.33 34.1 92.22 53.92 31.00 1666 3.0 294.00 50.7 90.44 63.47 30.33 1769 3.0 300.33 40.7 92.91 64.27 33.00 1839 2.9 281.33 46.5 95.02 67.28 107 Estas condiciones descritas propician remociones de color que están entre un 84 y un 95% y de DQO del 53 al 69%, con una conductividad que se incrementa en un poco más del 200%. Además, se mantuvo la relación empleada de sulfato y peróxido que fue de 1:4. En este caso como se puede observar las remociones disminuyeron también con estas condiciones, al obtenerse valores finales de color en el agua superiores a los 100 UPtCo y que llegan hasta las 300 unidades. d) Prueba No. 4 La prueba se realizó en un equipo de jarras y las condiciones fueron: Agitación 200 rpm por 30 min y sedimentación por 120 min. Con ajuste a pH 3. Las características iniciales y finales del agua de prueba se presentan en la 7.19 y en ¡Error! No se encuentra el origen de la referencia.7.20. Tabla 7.19. Características del agua de la prueba No.4 Solución inicial DQO Conductividad Color (UPtCo) (mg/L) (µS/cm) H2O2 mg/L 560 FeSO4 mg/L 120 Colorante (mg/L) 50 918 55.7 323 6.98 750 165 100 1643 85.6 492 7.09 930 200 150 2293 95.4 6154 7.22 1100 240 200 3450 107 702 7.27 1240 260 250 4333 133 796 7.40 1320 280 300 4918 140 869 7.47 pH Tabla 7.20. Características finales del agua de la prueba No. 4 SST (mg/L) Conductividad (µS/cm) pH Color (UPtCo) DQO (mg/L) Remoción Color (%) Remoción DQO (%) 5.00 1183 2.86 60.34 15.3 92.53 72.53 17.33 1385 2.76 155.67 22.4 91.98 73.83 14.67 1558 2.83 139.67 15.3 94.68 83.96 16.33 1677 2.84 178.67 15.3 94.19 85.70 19.67 1794 2.85 226.67 15.3 94.65 88.50 19.67 1846 2.87 217.00 24.9 96.16 82.21 108 Bajo estas condiciones de operación las remociones de unidades de color están entre un 92 y un 96% y de DQO del 72 al 82%, con una conductividad que nuevamente se incrementa en un poco más del 200%. También, se mantuvo la relación empleada de sulfato y peróxido que fue de 1:4. Estas nuevas condiciones mejoraron las remociones de color y materia orgánica, como DQO, aunque los valores de color residual en su mayoría están entre 150 y 230 UPtCo. Sin embargo, se observa que los flóculos formados son muy pequeños y quedan muchos sólidos suspendidos. e) Prueba No. 5 Para incrementar el tamaño de los flóculos y disminuir los sólidos suspendidos se propusieron nuevas condiciones de operación: Agitación 200 rpm por 10 min, 20 rpm por 50 min., y sedimentación por 2, 4, 5 y 6 horas, con ajuste a pH 3. La prueba se realizó en un equipo de jarras. Las características iniciales se presentan en la ¡Error! No se encuentra el origen de la referencia. y las finales del agua de prueba se presentan de la 7.22 a la ¡Error! No se encuentra el origen de la referencia.7.25. Tabla 7.21. Características del agua de la prueba No. 5 H2O2 mg/L FeSO4 mg/L Fe mg/L Color (UPtCo) Solución inicial DQO Conductividad pH (mg/L) (µS/cm) 450 650 1150 1600 2150 45 70 130 200 280 9.00 14.10 26.18 40.28 56.40 1183 2216 4416 5775 10066 46 76.5 151 245 224 250 250 300 350 400 7.05 7.14 7.19 7.17 7.30 3000 380 66.54 10675 390 440 7.43 Tabla 7.22. Características finales del agua de la prueba No.5 (2h de sedimentación) Fe (mg/L) 8.00 12.20 14.00 23.00 29.60 Conductividad (µS/cm) 3100 3000 2900 2800 2700 44.2 2600 2.87 2.77 2.81 2.81 2.68 Color (UPtCo) 31 57 245 468 1260 DQO (mg/L) 26.1 26.1 33.5 61.2 40.3 Remoción Color (%) 97.38 97.43 94.45 91.90 87.48 Remoción DQO (%) 43.26 65.88 77.81 75.02 82.01 2.64 1285 118.0 87.96 69.74 pH 109 Al analizar el agua con dos horas de sedimentación los resultados muestran que las remociones de color están entre un 87 y un 97% de color, y de DQO del 43 al 82%, con una conductividad que se ha incrementado en algunos casos hasta en un 1000%. La relación de sulfato y peróxido también se incrementó en una relación de 1:10. Estas nuevas condiciones muestran que conforme el color del agua de prueba va en aumento las remociones de color disminuyen y caso contrario para la DQO, en donde su remoción aumenta. También se observa que los sólidos suspendidos aumentan. Tabla 7.23. Características finales del agua de la prueba No.5 (4h sedimentación) Fe (mg/L) 7.40 12.20 12.20 20.00 25.8 Conductividad (µS/cm) 440 550 660 830 940 37.6 1100 3.04 2.93 2.86 2.77 2.74 Color (UPtCo) 25 28 92 222 340 DQO (mg/L) 15.3 18 22.9 21.2 15.3 Remoción Color (%) 97.89 98.74 97.92 96.16 96.62 Remoción DQO (%) 66.74 76.47 84.83 91.35 93.17 2.69 508 31 95.24 92.05 pH Los resultados con cuatro horas de sedimentación muestran que las remociones de color están entre un 95 y un 98% de color, y de DQO del 66 al 93%, con una conductividad que disminuyó. Tabla 7.24. Características finales del agua de la prueba No.5 (5h sedimentación) Fe (mg/L) Conductividad (µS/cm) pH Color (UPtCo) DQO (mg/L) Remoción Color (%) Remoción DQO (%) 6.60 12.20 12.60 19.80 25.8 450 550 660 820 930 2.89 2.79 2.74 2.67 2.65 59 25 54 139 204 15.3 15.3 15.3 27.8 52.2 95.01 98.87 98.78 97.59 97.97 66.74 80.00 89.87 88.65 76.70 16.6 1100 2.60 323 16.3 96.97 95.82 Los resultados a cinco horas de sedimentación muestran que las remociones de color se mantiene entre un 95 y un 98%, y de DQO mejora un poco al estar entre un 66 al 95%. La conductividad se mantiene. Tabla 7.25. Características finales del agua de la prueba No. 5(6h sedimentación) Fe (mg/L) Conductividad (µS/cm) pH Color (UPtCo) 110 DQO (mg/L) Remoción Color % Remoción DQO% 6.60 12.20 12.20 19.80 25.8 480 550 670 840 940 2.86 2.81 2.78 2.71 2.70 15.3 15.3 29.4 23.7 15.3 106 31 54 107 157 91.04 98.60 98.78 98.15 98.44 66.74 80.00 80.53 90.33 93.17 37.4 1130 2.64 40.0 270 97.47 89.74 Después de seis horas de sedimentación los resultados muestran que las remociones de color mejoran en algunos casos, sin embargo, la remoción de DQO disminuyó en algunas jarras de prueba. La conductividad se mantiene. Los resultados de esta prueba indican que no es necesario llevar la prueba hasta más de dos horas de sedimentación, debido a que si se escala a condiciones reales se tendría que construir una unidad muy grande. f) Prueba No.6 La prueba se realizó en un equipo de jarras y las condiciones fueron: Agitación 200 rpm por 10 min, 20 rpm por 50 min., sedimentación por 120 min., y filtración, con la finalidad de poder eliminar sólidos suspendidos y mejorar las remociones de color y DQO. El agua de prueba se ajustó a pH 3. Las características iniciales se presentan en la ¡Error! No se encuentra el origen de la referencia. 7.26 y las finales del agua de prueba se presentan de la ¡Error! No se encuentra el origen de la referencia. 7.27 y en la ¡Error! No se encuentra el origen de la referencia.7.28. Tabla 7.26. Características del agua de la prueba No. 6 H2O2 mg/L 450 650 1150 1600 2150 FeSO4 mg/L 45 70 130 200 280 Fe mg/L 9.00 14.10 26.18 40.28 56.40 Color (UPtCo) 1050 1933 4166 6491 8116 3000 380 66.54 10491 Solución inicial DQO Conductividad (mg/L) (µS/cm) 19.5 290 52 280 76.4 310 112.16 370 148.7 420 6.73 7.03 7.23 7.30 7.36 190.1 7.25 480 pH Tabla 7.27. Características finales del agua de la prueba No. 6 (2h sedimentación) Fe Conductividad pH Color 111 DQO Remoción Remoción (mg/L) (µS/cm) (UPtCo) (mg/L) Color (%) DQO (%) 4.20 6.20 440 510 3.07 2.97 52 38 15.3 15.3 93.22 97.95 63.22 74.67 11.60 19.00 560 820 2.85 2.77 57 109 15.3 15.3 98.68 98.24 84.76 87.66 24.4 930 2.72 218 15.3 97.40 90.58 35.8 1090 2.67 320 15.3 96.74 92.35 Al analizar el agua con dos horas de sedimentación los resultados muestran que las remociones de unidades de color están entre un 93 y un 98.6% y para DQO entre el 63 y 92%, sin embargo, es necesario aclarar que estos valores están por debajo del límite de detección de 15.3 mg/L, por lo que la remoción puede estar cercana al 100%. La conductividad se incrementa alrededor del 200%. La relación de sulfato y peróxido se mantiene en una relación de 1:10. Bajo estas condiciones de prueba se observa que conforme el color del agua de prueba va en aumento la remoción también hasta cierto punto y después disminuye. Pero para la DQO, la remoción aumenta. También se observa que los sólidos suspendidos aumentan. Tabla 7.28. Características finales del agua de la prueba No. 6(Filtrado) Fe (mg/L) 2.6 4.8 Conductividad pH (µS/cm) 430 2.95 510 2.86 Color (UPtCo) 13 18 DQO (mg/L) 15.3 21.9 Remoción Color (%) 98.31 99.03 Remoción DQO (%) 63.22 63.74 11.8 17.2 22.0 670 810 940 2.74 2.68 2.64 26 48 68 15.3 15.3 19.5 99.40 99.22 99.19 84.76 87.66 87.99 31.6 1080 2.59 86 15.3 99.12 92.35 Si la muestra es filtrada, el clarificado presenta remoción de color superior al 99%, esto hace suponer que el color que queda en la solución después de sedimentar se debe a sólidos suspendidos, además, los valores de la DQO se mantienen. En resumen las condiciones de operación en las pruebas con reactivo Fenton son: Mezcla rápida a 200 rpm por 10 min. Mezcla lenta 20 rpm por 50 min. Sedimentación por 120 min. Filtración En la 7.29 se muestra el agua antes de ser sometida al tratamiento con reactivo de Fenton y en la 112 7.30 unas muestras de agua una vez concluida la prueba. Figura 7.29 Muestra de agua residual inicial Figura 7.30 muestra de agua residual final 7.2.3.1 Pruebas con agua residual industrial Para esta parte del estudio se empleó agua residual proveniente de la Empresa Gütterman que fabrica hilos y está establecida en el parque industrial CIVAC en el municipio de Jiutepec del Estado de Morelos. Se tomaron muestras semanales de agua residual final, a las cuales se les dio el mismo tratamiento y sólo se varió las dosis de sulfato ferroso y de peróxido de hidrógeno, de tal manera que se puedan obtener las mejores remociones de color y de DQO. Todas las pruebas se realizaron en un equipo de jarras con vasos de precipitado de un litro, con: Mezcla rápida a 200 rpm por 10 min. Mezcla lenta s 20 rpm por 50 min. Sedimentación por 120 min. A continuación se muestran las características iniciales de las aguas residuales en estudio, así como los resultados obtenidos en cada prueba. Las celdas marcadas con amarillo indican las 113 mejores dosis de sulfato ferroso y de peróxido de hidrógeno para la remoción de color, y en azul para la remoción de DQO. a) Muestra de agua residual No. 1 Tabla 7.29. Características iniciales muestra No.1 Parámetro Color (UPtCo) Conductividad (µS/cm) pH DQO (mg/L) Valor 1548 750 6.26 1395 Tabla 7.30. Características finales de la muestra 1 FeSO4 (mg/L) H2O2 (mg/L) pH Conductividad Color (µS/cm) (Pt Co) DQO (mg/L) Fe libre (mg/L) Remoción Color (%) Remoción DQO (%) 60 70 80 100 150 200 180 210 240 300 450 600 2.92 2.83 3.19 2.72 2.81 2.8 1180 1240 1010 1370 1230 1230 1038.3 1005.9 1001.9 843.7 839.6 620.6 5.2 3.8 5.4 13.2 2.4 73.9 84.8 72.9 87.0 93.2 90.7 25.6 27.9 28.2 39.5 39.8 55.5 404 235 419 201 106 144 b) Muestra de agua residual No. 2 Tabla 7.31. Características iniciales muestra No. 2 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 4.79 1140 1917 1890 Tabla 7.32. Características finales de la muestra No.2 FeSO4 (mg/L) H2O2 (mg/L) pH Conductividad Color (µS/cm) (Pt Co) 114 DQO (mg/L) Fe libre (mg/L) Remoción Color (%) Remoción DQO (%) FeSO4 (mg/L) 200 250 300 350 400 450 H2O2 (mg/L) 600 750 900 1050 1200 1350 pH 2.69 2.66 2.67 2.66 2.67 2.63 Conductividad (µS/cm) 1590 1600 1590 1600 1590 1630 Color (Pt Co) 250 231 252 257 261 362 DQO (mg/L) 1014 1050.5 973.4 981.5 969.4 1009.9 Fe libre (mg/L) 13.8 6.6 20.6 26.2 27 38.2 Remoción Color (%) 17.1 16.5 17.1 16.5 17.1 15.0 Remoción DQO (%) 46.4 44.4 48.5 48.1 48.7 46.6 c) Muestra de agua residual No. 3 Tabla 7.33. Características iniciales muestra 3 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 5.46 1970 2108 2896 Tabla 7.34. Características finales de la muestra No.3 FeSO4 (mg/L) 260 270 280 290 300 310 320 330 H2O2 (mg/L) 850 860 900 920 940 960 980 1000 pH 2.61 2.6 3.0 2.3 2.5 2.4 2.5 3.4 Conductividad (µS/cm) 2510 2510 2570 2640 2620 2620 2880 2580 Color (Pt Co) 1515 1090 699 768 471 458 418 401 Figura 7. 31 Prueba No 4 Muestra de agua DQO (mg/L) 1910.4 1719.7 1492.6 1468.3 1415.5 1399.5 1415.5 1415.5 Fe libre (mg/L) 14.6 10.6 6.8 6.8 6 6 9.4 6.6 Remoción Color (%) 28.1 48.3 66.8 63.6 77.7 78.3 80.2 81.0 Remoción DQO (%) 34.0 40.6 48.5 49.3 51.1 51.7 51.1 51.1 Figura 7. 32 Vista de prueba 3 en jarras 115 residual. Tabla 7.35. Características iniciales muestra 4 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 6.2 1670 1605 2296 Tabla 7.36. Características finales de la muestra 4 FeSO4 (mg/L) 250 260 270 280 300 320 340 360 400 H2O2 (mg/L) 500 520 540 560 600 960 1020 1080 1200 pH 2.57 2.56 2.54 2.54 2.57 2.62 2.64 2.63 2.65 Conductividad (µS/cm) 2330 2340 2310 2330 2320 2280 2240 2290 2290 Color (Pt Co) 352 338 328 298 283 267 265 265 256 DQO (mg/L) 1220.9 1211.1 1233.1 1211.1 1208.7 1228.9 1289.8 1257.4 1184.4 Fe libre (mg/L) 5.2 5.8 6.2 7.8 9.2 10.6 12.2 14.2 21.6 Remoción Color (%) 78.1 78.9 79.6 81.4 82.4 83.4 83.5 83.5 84.0 Remoción DQO (%) 46.8 47.2 46.3 47.2 47.3 46.5 43.8 45.2 48.4 d) Muestra de agua residual No.5 Tabla 7.37. Características iniciales muestra No.5 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 6.77 1100 1472 2263 Tabla 7.38. Características finales de la muestra No.5 FeSO4 (mg/L) 190 200 220 240 260 280 H2O2 (mg/L) 380 400 440 480 520 560 pH 2.37 2.38 2.3 2.33 2.36 2.38 Conductividad (µS/cm) 2460 2470 2770 2820 2780 2800 Color (Pt Co) 1013 751 708 706 568 585 116 DQO (mg/L) 1533.2 1387.2 1228.9 1338.4 1285.8 1204.6 Fe libre (mg/L) 11 10.4 9.6 11.2 12.8 17 Remoción Color (%) 31.2 49.0 51.9 52.0 61.4 60.3 Remoción DQO (%) 32.3 38.7 45.7 40.9 43.2 46.8 FeSO4 (mg/L) 300 320 340 360 380 400 420 440 H2O2 (mg/L) 600 640 680 720 760 800 840 880 pH 2.39 2.4 2.56 2.57 2.65 2.66 2.67 2.69 Conductividad (µS/cm) 2790 2810 2720 2810 2760 2750 2780 2840 Color (Pt Co) 588 611 692 698 765 686 773 793 DQO (mg/L) 1204.6 1176.2 1168.1 1184.4 1168.1 1200.6 1237.1 1241.1 Fe libre (mg/L) 20 23 23.6 31 31.8 37.8 38 43.8 Remoción Color (%) 60.1 58.5 63.9 63.6 60.1 64.2 59.7 58.7 Remoción DQO (%) 46.8 48.0 46.7 45.9 46.7 45.2 43.5 43.3 e) Muestra de agua residual No.6 Tabla 7.39. Características iniciales muestra No.6 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 5.94 1630 5883 3472 Tabla 7.40. Características finales de la muestra No.6 FeSO4 (mg/L) 260 270 280 290 300 310 H2O2 (mg/L) 780 810 840 870 900 930 pH 2.65 2.74 2.73 2.72 2.78 2.77 Conductividad (µS/cm) 2430 2380 2420 2430 2360 2400 Color (Pt Co) 2236 3676 1443 1426 1370 1133 DQO (mg/L) 2247 2749.9 2084.8 1938.8 2019.8 1946.9 Fe libre (mg/L) 14 23.2 11 12.2 10.6 11.2 Remoción Color (%) 62.0 37.5 75.5 75.8 76.7 80.7 f) Muestra de agua residual 7 Tabla 7.41. Características iniciales muestra No.7 Parámetro pH Conductividad (µS/cm) 117 Valor 6.7 2660 Remoción DQO (%) 35.3 20.8 40.0 44.2 41.8 43.9 Color (UPtCo) DQO (mg/L) 3400 2654 Tabla 7.42. Características finales de la muestra No.7 FeSO4 (mg/L) 200 210 220 230 240 250 H2O2 (mg/L) 400 420 440 460 480 500 pH 2.58 2.58 2.61 2.69 2.68 2.69 Cond. (µS/cm) 3230 3330 3330 3290 3350 3380 Color (Pt Co) 693 792 733 685 658 640 Figura 7.33. Apariencia del agua inicial de prueba No. 7 DQO (mg/L) 1521.3 1513 1497 1492.9 1464.7 1594.1 Fe libre (mg/L) 5.2 7.2 7.8 8.4 10.4 11.6 % Rem Color 79.6 76.7 78.4 79.9 80.6 81.2 % Rem DQO 42.7 43.0 43.6 43.8 44.8 39.9 Figura 7.34. Prueba No. 7 en curso g) Muestra de agua residual 8 Tabla 7.43. Características iniciales muestra 8 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 7.19 2350 3173 2013 Tabla 7.44. Características finales de la muestra No.8 FeSO4 (mg/L) 500 520 H2O2 (mg/L) 500 520 pH 2.24 2.32 Conductividad (µS/cm) 3300 3180 Color (Pt Co) 2913 2178 118 DQO (mg/L) 1047 932.9 Fe libre (mg/L) 81.5 85 Remoción Color (%) 8.2 31.4 Remoción DQO (%) 48.0 53.6 540 560 580 600 540 560 580 600 2.41 2.44 2.47 2.56 3060 3040 2990 3850 1740 1548 1320 1157 855.5 831.1 790.9 749.6 79 88 8.5 84.5 45.2 51.2 58.4 63.5 57.5 58.7 60.7 62.8 h) Muestra de agua residual No.9 Tabla 7.45. Características iniciales muestra No.9 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 4.38 1680 8415 4408 Tabla 7.46. Características finales de la muestra No.9 FeSO4 (mg/L) 500 520 540 560 580 600 500 520 540 560 580 H2O2 (mg/L) 500 520 540 560 580 600 1000 1040 1080 1120 1160 pH 2.8 2.79 2.81 2.82 2.82 2.85 2.7 2.73 2.72 2.73 2.75 Conductividad (µS/cm) 2330 2400 2400 2400 2410 2410 2440 2430 2440 2460 2460 Color (Pt Co) 5525 4758 4483 4133 4042 4450 2943 2760 2540 2340 2143 DQO (mg/L) 2297.7 2126.6 2134.8 2142.9 1963.7 1833.3 1914.8 1898.5 1825.2 1784.4 1727.4 Fe libre (mg/L) 54.5 52 54 56 59.5 59.5 43.5 39 44.5 42 47 Remoción Color (%) 34.3 43.5 46.7 50.9 52.0 47.1 65.0 67.2 69.8 72.2 74.5 Remoción DQO (%) 47.9 51.8 51.6 51.4 55.5 58.4 56.6 56.9 58.6 59.5 60.8 i) Muestra de agua residual No.10 Tabla 7.47. Características iniciales muestra No.10 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 5.84 1610 5358 2999 Tabla 7.48. Características finales de la muestra No.10 FeSO4 (mg/L) 500 H2O2 (mg/L) 1000 pH 2.68 Conductividad Color (µS/cm) (Pt Co) 2280 1112 119 DQO (mg/L) 1197.8 Fe libre (mg/L) 22.8 Remoción Color (%) 79.2 Remoción DQO (%) 60.1 520 540 560 580 600 620 640 660 680 700 1040 1080 1120 1160 1200 1240 1280 1320 1360 1400 2.69 2.73 2.73 2.75 2.58 2.6 2.64 2.66 2.67 2.66 2290 2240 2260 2250 2320 2340 2330 2310 2300 2340 1087 1050 1033 985 992 1052 1060 1042 1023 1013 Figura 7. 35 Agua inicial de prueba 10 1193.7 1157 1181.5 1169.2 1115.2 1131.5 1139.6 1131.5 1115.2 1090.8 25.2 26.8 29.8 33.2 38.2 41 46.8 48.2 51 55.4 79.7 80.4 80.7 81.6 81.5 80.4 80.2 80.6 80.9 81.1 60.2 61.4 60.6 61.0 62.8 62.3 62.0 62.3 62.8 63.6 Figura 7.36 Condiciones finales de prueba 10 j) Muestra de agua residual No.11 Tabla 7.49. Características iniciales muestra No.11 Parámetro Valor pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) 5.7 1400 2123 2653 Tabla 7.50. Características finales de la muestra 11 FeSO4 H2O2 pH Cond. Color DQO 120 Fe libre % Rem % Rem (mg/L) (mg/L) 200 220 240 260 280 300 320 340 360 380 400 200 220 240 260 280 300 320 340 360 380 400 2.78 2.73 2.76 2.73 2.72 2.89 2.85 2.9 2.85 2.88 2.85 (µS/cm) (Pt Co) (mg/L) (mg/L) Color DQO 2030 2010 2010 2040 2060 1860 1920 1880 1940 1900 1990 408 299 255 224 207 197 199 196 204 194 197 1522.2 1461.1 1432.6 1387.9 1345.1 1298.3 1290.2 1233.2 1233.2 1188.4 1237.3 5 4.2 5 4.8 8.4 6.2 9 15.8 14 17 19.6 80.8 85.9 88.0 89.4 90.2 90.7 90.6 90.8 90.4 90.9 90.7 42.6 44.9 46.0 47.7 49.3 51.1 51.4 53.5 53.5 55.2 53.4 Figura 7. 37 Agua inicial de prueba No.11 Figura 7. 38 Agua final de prueba No.11 k) Muestra de agua residual 12 Tabla 7.51. Características iniciales muestra No.12 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 4.02 2020 3767 2434 Tabla 7.52. Características finales de la muestra 12 FeSO4 H2O2 pH Conductividad Color 121 DQO Fe libre Remoción Remoción (mg/L) (mg/L) 200 220 240 260 280 300 320 340 360 380 400 400 440 480 520 560 600 640 680 720 760 800 2.72 2.66 2.79 2.58 2.61 2.53 2.96 2.88 2.94 3.28 3.04 (µS/cm) (Pt Co) (mg/L) (mg/L) Color (%) DQO (%) 2340 2330 2190 2320 2300 2350 2140 2180 2130 2050 2120 2168 1542 1430 782 473 465 680 783 513 464 418 1583.2 1412.3 1383.8 1306.5 1241.4 1225.1 1166.1 1135.5 1200.7 1125.4 1096.9 19.6 13.4 11.8 13 13.4 19 16.6 22.2 16 20.4 28.2 42.4 59.1 62.0 79.2 87.4 87.7 81.9 79.2 86.4 87.7 88.9 35.0 42.0 43.1 46.3 49.0 49.7 52.1 53.3 50.7 53.8 54.9 Figura 7. 39 Agua de inicio prueba No.12 Figura 7. 40 Agua final de prueba No.12 l) Muestra de agua residual No.13 Tabla 7.53. Características iniciales muestra No.13 Parámetro Valor pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) 6.26 1400 4358 2808 Tabla 7.54. Características finales de la muestra No.13 122 FeSO4 (mg/L) 400 420 440 460 480 500 550 600 650 H2O2 (mg/L) 800 840 880 920 960 1000 1100 1200 1300 pH 2.71 2.67 2.7 2.67 2.71 2.7 2.63 2.64 2.65 Conductividad (µS/cm) 2130 2130 2120 2150 2090 2120 2110 2140 2160 Color (Pt Co) 1811.7 1558 1443 1436 1466 1371 720 810 833 DQO (mg/L) 1135.5 1086.7 1033.8 1025.6 1050.1 1102.9 960.5 877.3 879.1 Fe libre (mg/L) 28.6 31.4 34 38.6 44.8 46.2 45.6 57.4 70.5 Remoción Color (%) 58.4 64.2 66.9 67.0 66.4 68.5 83.5 81.4 80.9 Remoción DQO (%) 59.6 61.3 63.2 63.5 62.6 60.7 65.8 68.8 68.7 m) Muestra de agua residual No.14 Tabla 7.55. Características iniciales muestra No.14 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 5.28 1070 3247 3852 Tabla 7.56. Características finales de la muestra No.14 FeSO4 (mg/L) H2O2 (mg/L) pH Conductividad Color (µS/cm) (Pt Co) DQO (mg/L) Fe libre (mg/L) Rem Color (%) Rem DQO (%) 300 320 340 360 380 400 420 440 460 480 500 600 640 680 720 760 800 840 880 920 960 1000 2.68 2.73 2.75 2.73 2.77 2.79 2.7 2.69 2.74 2.76 2.76 1600 1590 1580 1640 1600 1590 1660 1680 1630 1610 1600 1704.8 1626.9 1594.1 1573.6 1512.2 1495.8 1401.5 1381 1360.5 1335.9 1315.5 32.4 31.2 33.2 39.2 40.2 43 46.4 56.6 56.6 58.4 62 20.9 36.9 50.7 49.4 47.0 62.4 68.5 63.7 64.5 64.2 66.2 55.7 57.8 58.6 59.1 60.7 61.2 63.6 64.1 64.7 65.3 65.8 2570 2050 1602 1643 1720 1220 1023 1178 1152 1163 1098 n) Muestra de agua residual No.15 123 Tabla 7.57. Características iniciales muestra No.15 Parámetro pH Conductividad (µS/cm) Color (UPtCo) DQO (mg/L) Valor 7.15 1300 5416 2967 Tabla 7.58. Características finales de la muestra No.15 FeSO4 (mg/L) 400 420 440 460 480 500 H2O2 (mg/L) 800 840 880 920 960 1000 7.2.3.2 pH 2.63 2.64 2.66 2.68 2.7 2.66 Conductividad (µS/cm) 1880 1880 1870 1820 1800 1850 Color (Pt Co) 447 447 457 451 462 479 DQO (mg/L) 1294.9 1208.9 1237.6 1225.3 1163.8 1163.8 Fe libre (mg/L) 34.2 38.8 51 40.6 45.6 52.4 Remoción Color (%) 91.7 91.7 91.6 91.7 91.5 91.2 Remoción DQO (%) 56.4 59.3 58.3 58.7 60.8 60.8 Análisis de resultados de pruebas de agua residual industrial A continuación se presenta un resumen de la calidad del agua residual antes y después del tratamiento, así como de las dosis de sulfato ferroso y peróxido de hidrógeno con las cuales se obtuvieron los % más elevados de remoción de color y de DQO (¡Error! No se encuentra el origen de la referencia.7.59 y ¡Error! No se encuentra el origen de la referencia.7.60). Tabla 7.59. Calidad de agua en remoción de color Prueba pH 1 2 3 4 5 6 7 8 9 10 6.26 4.79 5.46 6.20 6.77 5.94 6.70 7.19 4.38 5.84 Color Conductividad inicial (µS/cm) (Pt Co) 750 1548 1140 1917 1970 2108 1670 1605 1100 1472 1630 5882 2660 3400 2350 3173 1680 8415 1610 5358 124 FeSO4 (mg/L) H2O2 (mg/L) 150 200 330 400 340 310 250 600 1160 1160 450 600 1000 1200 680 930 500 600 2143 985 Color Final (Pt Co) 106 250 401 256 392 1133 640 1157 75 82 Remoción Color (%) 93.15 86.96 80.98 84.05 73.37 80.74 81.18 63.54 99.11 98.47 11 12 13 14 15 Prom 5.70 4.02 6.26 5.28 7.15 5.86 1400 2020 1400 1070 1300 1517 2123 3767 4358 3247 5416 3586 380 400 550 420 400 470 380 800 1100 840 800 867 194 418 720 1023 1295 543 90.86 88.90 83.48 68.49 76.09 83.29 En promedio se tiene que el agua residual es ligeramente ácida, con una conductividad que está entre 750 y 2660, con un promedio de 1500 µS/cm, unos valores de color inicial con un intervalo de 1400 a 8400, con un promedio de 3550 UPtCo. Así, en promedio se emplean 470 mg/L de sulfato ferroso y 867 mg/L de peróxido de hidrógeno para obtener un color residual en el agua tratada de 543 UPtCo en promedio, lo cual corresponde a un 83 % de remoción. En la se aprecia que de la prueba 1 a la seis cuando el pH aumenta o sube su valor la conductividad es inversa y posterior a esta su relación es casi directa. 3000 8 MS/cm 2500 6 2000 1500 4 1000 2 Conductividad pH 500 0 0 1 2 3 4 5 6 7 8 Prueba 9 10 11 12 13 14 15 Figura 7.41 Relación pH vs Conductividad En la figura 7.42 se aprecia claramente una relación inversa entre el color inicial del agua y el pH hasta la prueba 12 y después de ésta es directa. 125 9000 8000 7000 6000 5000 4000 3000 2000 1000 0 8 7 6 UPtCo 5 4 3 Color 2 pH 1 0 1 2 3 4 5 6 7 8 9 Prueba 10 11 12 13 14 15 Figura 7.42 Relación color inicial vs pH MS/cm / UPtCo En la figura 7.43 se puede apreciar que existe una relación directa entre el color y la conductividad, esto puede ser debido a que los colores que se empleen en la industria pueden contener sales, así entre más color se utilice más se incrementará la conductividad del agua residual. 9000 8000 7000 6000 5000 4000 3000 2000 1000 0 Conductividad Color 1 2 3 4 5 6 7 8 Prueba 9 10 11 12 13 14 15 Figura 7.43 Relación color inicial vs conductividad En relación a las dosis empleadas de sulfato ferroso se observa que después de la prueba 7 si el color de agua residual aumenta la dosis de este reactivo también. Para las dosis del peróxido de hidrógeno en todas las pruebas se tiene una relación directa con el color. Esto puede resumirse que si el color aumenta las dosis a emplear de los reactivos también (figura 7.44). 126 Color (UPtCo) 9000 2500 8000 Color 7000 FeSO4 6000 H2O2 2000 1500 5000 4000 1000 3000 2000 500 1000 0 0 1 2 3 4 5 6 7 Prueba 8 9 10 11 12 13 14 15 Figura 7.44 Color Vs dosis empleadas Con respecto al porcentaje de remoción de color no se observó una relación al compararse con el inicial, ni tampoco se observó una mejora si se incrementan las dosis de reactivos a emplear ( 7.45). 9000 120 8000 100 7000 80 Color (UPtCo) 6000 5000 60 4000 3000 40 2000 Color % Rem Color 1000 20 0 0 1 2 3 4 5 6 7 8 9 Prueba 10 11 12 13 Figura 7.45 Porcentaje de remoción de color vs color inicial 127 14 15 Tabla 7.60. Calidad de agua en remoción de DQO. Prueba pH 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Prom 6.26 4.79 5.46 6.20 6.77 5.94 6.70 7.19 4.38 5.84 5.70 4.02 6.26 5.28 7.15 5.86 DQO Conductividad inicial (µS/cm) (mg/L) 750 1395 1140 1890 1970 2896 1670 2295 1100 2263 1630 3972 2660 2654 2350 2013 1680 4405 1610 2999 1400 2653 2020 2434 1400 2808 1070 3852 1300 2967 1583 2766 FeSO4 (mg/L) H2O2 (mg/L) DQO Final Remoción (mg/L) DQO (%) 200 400 310 400 320 290 240 600 580 700 380 400 600 500 480 427 600 1200 960 1200 640 870 480 600 1160 1400 380 800 1200 1000 960 897 620 969 1399 1184 611 1938 1465 749 1727 1090 1188 1096 877 1315 1164 1159 55.56 48.73 51.69 48.41 73.00 51.21 44.80 62.79 60.79 63.65 55.22 54.97 68.77 65.86 60.77 57.75 La ¡Error! No se encuentra el origen de la referencia.7.60 muestra que se tiene una DQO inicial con un intervalo de 1400 a 4400, con un promedio de 2766 mg/L. Así, en promedio se emplean 430 mg/L de sulfato ferroso y 900 mg/L de peróxido de hidrógeno para obtener una DQO residual en el agua tratada de 1160 mg/L en promedio, lo cual corresponde a un 58 % de remoción. Tomando como referencia los datos de la ¡Error! No se encuentra el origen de la referencia.7.60 se presentan las siguientes gráficas. 128 DQO (mg/L) / Conductividad (MS/cm) 5 000 4 500 4 000 3 500 3 000 2 500 2 000 1 500 1 000 500 0 8 7 6 5 4 3 2 Conductividad 1 DQO 0 1 2 3 4 5 6 7 8 9 Prueba 10 11 12 13 14 15 Figura 7.46 Relación DQO inicial vs pH y conductividad En la figura 7.46 se presentan las tendencias de la DQO inicial en relación al pH y la conductividad, así se puede apreciar que de la prueba uno a la seis si aumenta la conductividad también aumenta la DQO del agua residual, sin embargo, después de la siete el comportamiento es inverso, caso similar es para el pH en todas las pruebas. En relación a las dosis empleadas de sulfato y peróxido se puede observar en la figura 7.47, que sus tendencias siguen ligeramente la de la DQO inicial del agua residual, esto es, si la DQO disminuye, también disminuyen las dosis a emplear para su remoción y a la inversa. Respecto a la remoción de DQO se obtuvo que entre menor sea la DQO menor será el residual en el agua tratada, que en promedio es de alrededor de 1150 mg/L, sin embargo, cuando se presentan concentraciones por arriba de los 3500 mg/L, la residual estará alrededor de los 1500 mg/L. 129 mg/L 5000 4500 4000 3500 3000 2500 2000 1500 1000 500 0 DQO FeSO4 H2O2 1 2 3 4 5 6 7 8 9 Prueba 10 11 12 13 14 15 DQO (mg/L) Figura 7.47. Relación DQO inicial vs peróxido de hidrógeno y sulfato ferroso. 5000 4500 4000 3500 3000 2500 2000 1500 1000 500 0 80 DQO 70 DQO final 60 % Rem DQO 50 40 30 20 10 0 1 2 3 4 5 6 7 8 9 Prueba 10 11 12 13 14 15 Figura 7. 48 Remoción de DQO 7.2.3.3 Diseño de prototipo Tomando como referencia lo expuesto en los puntos anteriores, se diseñó un prototipo de prueba para realizar pruebas a nivel piloto, así en la se muestra su configuración. 130 Figura 7.49. Prototipo de prueba. Conclusiones a) Las condiciones de operación para trabajar con reactivo Fenton son: Mezcla rápida a 200 rpm por 10 min. Mezcla lenta s 20 rpm por 50 min. Sedimentación por 120 min. b) El agua residual industrial de la empresa Gutterman en promedio tiene las siguientes condiciones: pH de 5.86 Conductividad de 1538 µS/cm Color de 3586 UPtCo DQO de 2766 mg/L c) Existe una relación inversa entre el pH y el color del agua residual de Guterman. 131 d) Existe una relación directa entre la conductividad y el color del agua residual de Gutterman. e) En promedio se emplean 470 mg/L de sulfato ferroso y 867 mg/L de peróxido de hidrógeno para obtener un color residual en el agua tratada de 543 UPtCo en promedio. f) La remoción de color lograda está en un rango de 63.5 a 99.1%. g) Existe una relación inversa de la DQO con el pH y la conductividad del agua residual de Gutterman. h) Así, en promedio se emplean 430 mg/L de sulfato ferroso y 900 mg/L de peróxido de hidrógeno para obtener una DQO residual e n el agua tratada de 1160 mg/L en promedio. i) La remoción de la DQO lograda está en un rango de 48 a 68 %. j) EN términos generales el reactivo Fenton es útil alcanzar remociones de color del 83% y de DQO de 57%. en promedio. k) Se diseñó y construyó un prototipo de prueba. l) El obtener una remoción de alrededor del 60% en DQO indica que el reactivo Fenton rompe las estructuras de los colorantes y las oxida parcialmente. m) Para obtener una remoción u oxidación total de los compuestos que generan color es necesario un segundo tratamiento. 132 CONCLUSIONES GENERALES Se evaluaron a nivel laboratorio varios métodos de tratamiento que la literatura refiere como posibles para el tratamiento de las aguas residuales de la industria textil, con énfasis en la remoción de los colorantes que contienen. Los métodos convencionales probados fueron el fisicoquímico mediante oxidación avanzada utilizando el método de Fenton y el biológico acoplado anaerobio – aerobio. Como métodos no convencionales se iniciaron las investigaciones probando la efectividad de la biofiltración con el medio de empaque inoculado con hongos conteniendo enzimas del tipo de las peroxidasas.(Biológico fúngico). La matriz o medio de empaque utilizado fue la turba, que fue inoculada con una cepa del hongo Pleurotus ostreatus. El segundo método no convencional que abarcó este estudio fue el biológico enzimático utilizando enzimas también del tipo de las peroxidasas. Se desarrolló un método para la obtención de las peroxidasas provenientes del frijol de soya a partir de un desecho generado durante la fabricación de la leche de soya. Las aguas residuales probadas se obtuvieron de diferentes fuentes: lavadoras de mezclilla, fabricación de playeras y producción de hilos. a) Con respecto a la caracterización de las aguas resid uales: El efluente que se genera en la producción de textiles que utilizan colorantes son en general aguas con características de alta carga orgánica, alta variabilidad en sus características, baja biodegradabilidad y altamente coloridas. Estas características las hace difíciles de tratar. Las características de las aguas residuales seleccionadas para la realización de las pruebas de tratabilidad fue la de la industria productora de hilos. El promedio del efluente general fue: pH ácido de 5.86, conductividad de 1538 µS/cm, alta coloración (Color de 3586 UPtCo) , DQO de 2766 mg/L. (mezcla de procesos de producción)y las de una de las tinas de teñido fue de 7,739±3,180 mg/L de DQO. Asimismo, se hicieron varias caracterizaciones de colorantes tipo azo en donde se observí que muy bajas concentraciones de colorante generar solucione altamente coloridas b) En relación con los procesos biológicos convencionales utilizados: Se utilizó un sistema acoplado anaerobio - aerobio.(UASB-Lodos activados). El reactor anaerobio fue del se utilizó como la primera etapa del tratamiento biológico del efluente general de la industria textil que con una DQO promedio de 2,446±592 mg/L. La carga orgánica aplicada de 5.3 kg DQO.m -3.d-1 y con un TRH de 11.1 h en el reactor UASB. permitió alcanzar una remoción de 67% después de 46 días de operación. Las concentraciones de SST y SSV en el efluente general de la industria son bajas, con promedios de 60±16 mg/L y 46±11 mg/L respectivamente. Las remociones de estos sólidos en el reactor anaerobio UASB son de 21±12% y 30±26% respectivamente. El l agua residual descargada directamente de la tina de teñido en la industria con una DQO promedio de 7,739±3,180 mg/L, casi tres veces mayor que la DQO del efluente general de la industria textil. Esta agua residual es fuertemente inhibitoria para la biomasa granular del reactor UASB. Operando el reactor con una carga orgánica de 8.3 ±1.8 kg DQO m-3 d-1 y con un TRH de 18.2 h durante más de un mes se obtuvo una remoción promedio de DQO de tan solo 16±5% con tendencia de incremento. Las concentraciones de SST y SSV en el efluente de la tina son de 365±87 y 178±62 mg/L respectivamente. Los SSV 131 representan un 49% de los SST, es decir hay muchas partículas finas inorgánicas en los sólidos suspendidos. Las remociones de SST y SSV logradas en el UASB son de 84±9% y 75±11% respectivamente. Los sólidos removidos quedan retenidos en el lecho y la fracción orgánica se puede degradar lentamente, la otra fracción, la inorgánica queda en el lecho. Con respecto al tratamiento aerobio utilizado, el reactor de lodos activados usado como segunda etapa del tratamiento biológico del agua residual de la tina de teñido de la industria textil, operado con una carga orgánica volumétrica de 6.51±1.27 kgDQO.m-3.d-1y un TRH de 14.0 h, permitió obtener una remoción promedio de 14.9±7.7%. La aclimatación de la biomasa al sustrato presente en el agua residual efluente del UASB es difícil, con problemas de intoxicación de la biomasa e inhibición de la degradación de la materia orgánica y del crecimiento de la biomasa, sin embargo, fue posible superar la intoxicación en unos 10 días, pero la remoción aumenta muy lentamente. El promedio de la remoción global de la DQO (en los dos reactores) durante los últimos 30 días de operación fue de 28.7±7.3% con una tendencia de incremento. Se necesita seguir el proceso de aclimatación y estabilización del proceso en ambos reactores. Las remociones de SST y SSV en el reactor lodos activados son de 20±20% y 36±27% respectivamente, obteniéndose en el efluente concentraciones de SST y SSV de 41±2 mg/L y 24±5 mg/L respectivamente. c) Referido a los procesos biológicos no convencionales: Es importante el considerar que la extracción de la enzima peroxidasa se realizó a partir del residuo de la obtención de la leche de soya, ADES (Okara), lo cual se considera como algo no realizado con anterioridad. Se utilizaron para estos experimentos no el agua residual del efluente general o de la tina, sino sólo el colorante azul negro directo , AND., esto para tener un mayor control del proceso. La oxidación enzimática del colorante AND mediante la enzima Peroxidasa constituye un método muy efectivo para su degradación. Las condiciones en las cuales la oxidación es más rápida y la actividad enzimática se ve menos afe ctada. El crudo enzimático es el factor más costoso del proceso. Por ello, para determinar el valor de actividad enzimática más adecuado se consideraron parámetros económicos. Por encima de 150 -200 U/L de Peroxidasa no se apreciaron grandes cambios en cuan to a la cinética del proceso. Por ello, se consideró ese rango como el más adecuado para los procesos de degradación. Aun cuando la investigación es incipiente y no está concluida, se han obtenido remociones hasta del 50 % del color con la ventaja de que l a enzima puede ser recuperada. d) Con respecto al tratamiento mediante biofiltración con turba inoculada con Pleutorus ostreatus (fúngico), se probaron cuatro variantes de biofiltros para poder evaluar el efecto de la turba, del hongo y de su combinación. Un bifiltro fue sólo empacado con turba sin esterilizar, otro fue empacado con turba inoculada sin esterilización y dos mas con las misma condiciones descritas sólo que esterilizados. se observa que de los cuatro reactores utilizados en el experimento el que mejor desempeño tuvo fue el reactor inoculado con el hongo Pleurotus ostreatus y sin esterilizar , mostrando que el procedimiento de esterilización del material de empaque si tuvo un efecto negativo; además de mostrar hasta el momento que la materia or gánica fue removida y disminuida por el proceso de adsorción, absorción de la turba y degradación debida a microorganismos adheridos al mismo material de empaque de los biofiltros. e)Para los procesos fisicoquímicos de oxidación avanzada las mejores condiciones fueron: 132 Mezcla rápida a 200 rpm por 10 min; mezcla lenta a 20 rpm por 50 min, seguida de una sedimentación por 120 min. En promedio se emplean 470 mg/L de sulfato ferroso y 867 mg/L de peróxido de hidrógeno para obtener un color residual en el agua tratada de 543 UPtCo La remoción de color lograda en las diferentes pruebas está en un rango de 63.5 a 99.1%. Así, en promedio se emplean 430 mg/L de sulfato ferroso y 900 mg/L de peróxido de hidrógeno para obtener una DQO residual en el agua tratada de 1 160 mg/L en promedio. La remoción de la DQO lograda está en un rango de 48 a 68 %. El obtener una remoción de alrededor del 60% en DQO indica que el reactivo Fenton rompe las estructuras de los colorantes y las oxida parcialmente. Para obtener una remoción u oxidación total de los compuestos que generan color. Es necesario un segundo tratamiento por lo que se probará en la continuación de este estudio el proceso acoplado fisicoquímico (Fenton) y biológico aerobio.(Lodos activados para permitir que el efluente obtenido mediante este tren cumpla con las regulaciones vigentes y que su descarga no afecte el sitio donde se descargue o eventualmente pueda ser reutilizado. Para esta segunda fase del proyecto se diseñó y construyó un prototipo de prueba que se probará con el tratamiento acoplado FQ -Biológico 133 REFERENCIAS 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. Adriana Aristizábal Castrillón, María Catalina Bermúdez Agudelo. (2007). Estudio de la factibilidad de un sistema de electrocoagulación para tratamiento de aguas procedentes de lavanderías industriales con fines de reuso. Aitken, M. D. (1993). Waste treatment applications of enzymes: Opportunities and obstacles. The Chemical Engineering Journal and the Biochemical Engineering Journal. 52: B49–B58. Akhtar, S., Khan, A.A. and Husain, Q. (2005a). Partially purified bitter gourd (Momordica charantia) peroxidase catalyzed decolorization of textile and other industrially important dyes. Bioresource Technology 96: 1804–1811. Alatorre, F. A. (2007). Diseño de reactores empacados p ara la remoción de color en aguas residuales industriales. Tesis de Maestría en Ingeniería, Facultad de Ingeniería, UNAM, México. DF, México, 137pp. Aleboyeh, A., Ilya, M., Aleboyeh, H. (2009). Oxidative treatment of azo dyes in aqueous solution by potassium permanganate. Journal Hazardous Materials; 162, 1530-1535. Allegre, C., Maisseu, M., Charbit, F., Moulin, P., (2004). Coagulation–flocculation–decantation of dye house effluents. Journal Hazardous Materials; B116, 57–64. Amjad .A. K. y Qayyum H. (2007). Decolorization and removal of textile and non-textile dyes from polluted wastewater and dyeing effluent by using patato (Solanum tuberosum) soluble and immobilized polyphenol oxidase. Bioresource Technology, 98: 1012-1019. Anliker, R. (1977). Ecotoxicology of dyestuff a Joint efforts by industry. 3, 59 -74. Arroyave, J., Giraldo, L., Mejía, J. (2008). Empleo del reactivo de Fenton para la degradación del colorante Tartrazina. Revista Lasallista de investigación Vol. 6 No. 1. Azzi, M. et al. (abr. 2006) Contribution to the study of electrocoagulation mechanism in basic textile effluent. En: Journal of Hazardous Materials. Vol. 131, No.1-3; p.73-78 Baborova, P., Moder, M., Baldrian, P., Cajthamlova, K. and Cajthaml, T. (2006). Purification of a new manganese peroxidase of the white-rot fungus Irpex lacteus, and degradation of polycyclic aromatic hydrocarbons by the enzyme. Resourse Microbiology, 157: 248–253. Barbusiński, K. (2004). The Modified Fenton Process for Decolorization of Dye Wastewater. Institute of Water and Wastewater Engineering, Silesian University of Technology, Konarskiego 18, 44-101 Gliwice, Poland. Basheer, S., Kut, O.M., Prenosil, J.E., and Bourne, J.I. (1992). Kinetics of enzymatic degradation of cyanide. Biotechnology. Bioengineering. 39; 629–634, 1992. Beltran de Heredia, Jesús y Gonzáles, María Concepción. (dic. 1991) Tratamiento de las aguas residuales en la industria textil. En: Ingeniería Química. Vol. 23, No.273 p. 131-134. Bhunia, A., Durani, S., & Wangikar, P. P. (2002). Horseradish peroxidase catalyzed degradation of industrially important dyes. Biotechnology and Bioengineering, 72: 562–567. Bishop, P. and Jiang, H. (1994). Aerobic biodegradation of azo dyes in biofilms. Water Science and Technology. 29, 525 -530. 134 17. Blánquez, P., Casas, N., Font, X., Gabarrell, X., Sarrà, M., Caminal, G. and Vicent, T. (2004). Mechanism of textile metal dye biotransformation by Trametes versicolor . Water Research, 38: 2166-2172. 18. Bradford, M. M. (1976). A rapid and sensitive method for the quantification of micrograms quantities of proteins utilizing the principle of protein-dye binding. Analytical Biochemistry, 72: 248-254. 19. Buelna, G. (1994). La biofiltración en lecho orgánico: una novedosa alternativa para el tratamiento de efluentes industriales y de pequeños municipios”. II Congreso y exposición internacional de la industria del medio ambiente. 20. Buitron, G. (1996). Biodegradación aerobia de compuestos xenobióticos. En: Kuppusamy, I. Y Briones, R. (Eds) Biodegradación de Compuestos Orgánicos Industriales. UNAM, Instituto de Ingeniería, DF, México. 1, 1 -10. 21. Buitrón, G., Melgoza, R.M., Jiménez, L. (2003). Pharmaceutical wastewater treatment using an anaerobic/aerobic sequencing batch biofilter. Journal of Environmental Science and Health. Part a- Toxic/Hazardous Substances & Environmental Engineering. 38(10): 2077-2088. 22. Buitrón, G., Quezada, M., Moreno, J., (2004). Aerobic degradation of the azo dye acid red 151 in a sequencing batch biofilter. Bioresource Technology, 92: 143-149. 23. Calderón Alonso A. I. A., Romero G. (2003). Degradación de colorantes textiles utilizando a la peroxidasa de chayote. Tesis en curso. BUAP, Puebla. 24. CAM (1998). Manual de minimización, tratamiento y disposición. Concepto de manejo de residuos peligrosos e industriales para el giro textil. Comisión Ambiental Metropolitana. México. 25. Campos, R.; Kandekbaeur, A.,Robra, K.; Cavaco, P.; GÜbitz, G. (2001). Indigo degradation with purified laccases from Trametes hirsuta and Sclerotium rolfsii. Journal Biotechnoly, 89: 131–139. 26. Chattopadhyay, S.N.; Day, A. and Pan, N.C. (ene. 2006). Reuse of reactive dyes for dyeing of jute fabric. En: Bioresource Technology. Vol. 97, No.1 p.77-83. 27. Cheng, M.M., Ma, W.H., Li, J., Huang, Y.P., Zhao, J.C., (2004). Visible-light-assisted degradation of dye pollutants over Fe (III)-loaded resin in the presence of H2O2 at neutral pH values. Environmental Science Technology, 38: 1569–1575. 28. Christian, V., Shrivastava, R., Shukla, D., Modi, H.A., y Vyas, B.R. (2005). Degradation of xenobiotic compounds by lignin-degrading white-rot fungi: Enzymology and mechanisms involved. Indian Journal. Exp. Biol, 43: 301–312. 29. Christie, R. M. (2003). La química del color. Zaragoza (España), Editorial Acribia, S.A. 30. Claus, H., Faber, G., and Konig, H. (2002). Redox-mediated decolorization of synthetic dyes by fungal laccases. Applied Microbiol. Biotechnology. 59: 672–678. 31. Cohen, R., Persky, L., Hadar, Y. (2002). Biotechnological applications and potential of wood-degrading mushrooms of the genus Pleurotus. Appl. Microbia l. Biotechnology. 58, 582-594. 32. CrespiI, M y Huertas, J. A. (jul.–dic. 1987) ¿Industria textil: Depuración biológica o fisicoquímica? En: Boletín Intextar del Instituto de Investigación Textil y de Cooperación Industrial Terrasa. Vol. 2, No. 92 p.75-90 33. Cruz, A., Buitrón, G., llangovan, K. (1996). Desarrollo de tecnología para el tratamiento de aguas residuales de la industria textil. En X Congreso Nacional de Ingeniería Sanitaria y Ambiental. Febrero. Toluca, México 135 34. Dávila, G., Vázquez, R. (2006). Enzimas l igninolítica fúngicas para fines ambientales: Mensaje bioquímico. 30, 29-55. 35. Dávila, S. V. (2005). Degradación Fúngica del Colorante Naranja ácido 24. Tesis de Maestría en Ingeniería, Facultad de Ingeniería, UNAM, México, DF, México, 114pp. 36. Dávila, S. V., Moeller, Ch. G., Garzón, Z. M. A. y Farfán, G. (2003). Fungal colour reduction of azo dyes in wastewater. Memorias de la IWA Conference on Enviromental Biotechnology. Kuala Lumpur, Malasia. 37. Dellamatrice, P. M., Monteiro, R.T.R., Kamida, H. M., Nogueira , N. L., Rossi, M. L., Blaise, C. (2005). Decolourization of municipal effluent and sludge by Pleurotus sajor-caja and Pleurotus ostreatus. World journal of microbiology and Biotechnology. 21,1363-1369. 38. Delee, W., O’Neill, C., Hawkes, F.R., Pinheiro, H.M., (1998). Anaerobic treatment of textile effluents: a review. Journal Chemistry Technol. Biotechnology. 73: 323–335. 39. Domenech.Xavier., Litter.Marta.I. y Jardim.Wilson. F., (2001), “Procesos Avanzados de oxidación para la eliminación de contaminantes”, Red Cyted VIII-G, Comisión Nacional de energía atómica, Buenos Aires, 1, 3 -26. 40. Duran, N., and Esposito, E. (2000). Potential applications of oxidative enzymes and phenoloxidase-like compounds in wastewater and soil treatment: A review. Applied Catalisis. B: Environmental. 28: 83–99. 41. Duran, N., Rosa, M. A., D’ Annibale, A., and Gianfreda, L. (2002) Applications of laccases and tyrosinases (phenoloxidases) immobilized on different supports: A review. Enzyme Microbiology. Technology 31: 907–931, 2002. 42. Eibes, G., Lu-Chau, T., Feijoo, G., Moreira, M.T. y Lema, J.M. (2005). Complete degradation of anthracene by manganese peroxidase in organic solvent mixtures. Enzyme Microbiology. Technology 37: 365–372. 43. EPA (1996). Best Management Practices for pollution prevention in the textile Industry. U.S. Environmental Protection Agency, Cincinnati, USA. 44. EPA (1997). Profile of Textile Industry; Environmental Protection Agency; EUU. 45. Estadisticas del Agua en México, (2011). CONAGUA 46. Faroco V., Pezzella C., Miedele A., Giardina , P., Sannia, G. (2009). Bio-remediation of colored industrial wastewaters by the white -rot fungi Phanerochaete chrysosporium and Pleurotus ostreatus and their enzymes. Biodegradation. 20, 209-220. 47. Feijoo C. G., Lema R., J. M. y Moreira V. M. (2003). Proc edimiento de degradación de compuestos orgánicos presentes en efluentes industriales mediante reactores enzimáticos y su aplicación en la decoloración de tintes industriales. Universidad de Santiago de Compostela. Solicitud de patente 48. Filiz A., Catalkaya, E., Kargi, F. (2008). Advanced Oxidation of Direct Red (DR 28) by Fenton Treatment. Enviromental Engineering Science Volume 25, Number 10. 49. Forgacs, E., Cserhati, T., Oros, G., (2004). Removal of synthetic dyes from wastewaters: a review. Environmental. Int. 30: 953–971. 50. Gomes, A., Gonclaves, I., de Pinho, M., (2005). The role of adsorption on nanofiltration of azo dyes. Journal of Membrane Science. 255, 157-165. 51. Guaratini, C. C. I. y Zanoni, M. V. B. (2000). Textile dyes. Química Nova 23(1), 71-78. 136 52. Gudelj, M., Fruhwirth, G.O., Paar, A., Lottspeich, F., Robra, K.H., Cavaco- Paulo, A. and Guebitz, G.M. (2002). A catalase-peroxidase from a newly isolated thermoalkaliphilic Bacillus sp. with potential for the treatment of textile bleaching effluents. Extremophiles. 5: 423–429. 53. Gungor, I. (2008). The effect of Heavy metals on peroxidasa from Jerusalem artichoke (Helianthus tuberosus L.) tubers. African Journal of Biotechnology, 7(13):2248-2253. 54. Gulnaz, O., Kaya, A., Dincer, S., (2006). The reuse of dried activated sludge for adsorption of reactive dye. Journal Hazardous Materials, B134, 190-196. 55. Gupta V. K. y Suhas (2009). Application of low-cost adsorbents for dye removal. A review. Journal of environmental Management. 90: 2313-2342. 56. Gomes, M.K.M., y Matheus, D.R. (2006). Biodegradation of remazol brillant blue R by ligninolytic enzymatic complex produced by Pleurotus ostreatus. Brazilian Journal of Microbiology. 37, 468-473. 57. Guía de Mejores Técnicas Disponibles en España del Sector de Química Fina Orgánica, 2006). 58. Guo, M., Lu F., Liu, M., Li T., Pu, J., Wan N., Liang P. Zhang C. (2008). Purification of recombinant laccase from Tremetes versicolor in Pichia mehanolica and its use for the decolorization of anthraquinone dye. Biotechnol Lett. DOI 10. 1007/s 10 529008-9817-z. 59. Hai, F.I., Yamamoto, K., Fukushi, K., (2007). Hybrid treatment systems for dye wastewater. Environmental. Science Technology. 37, 315–377. 60. Haug W. Schmidt, A., Nortermann, B., Hempel, D., Stolz, A. y Knackmuss H. (1991). Mineralization of sulfonated azo dye Mordant Yellow 3 by a 6 aminonaphthalene -2sulfonate-degrading bacterial consortium Appl. Environ. Microbiol. 57, 3144 -3149. 61. Hessel C., Allegre C., Maisseu M., Charbit F., Moulin P. (2007). Guidelines and legislation for dye house effluents. Journal Environmental Management, 83: 171-180. 62. Herbst W. y Hunger K. (1997). Industrial Organic Pigments: Production, Properties, Applications, John Wiley & Sons, Inc., 2a edition. 63. Hunger, K., (2003). Industrial dyes: Chemistry, Properties, Aplications. Wiley-VCH Weinheim; Cambriege. 64. Husain, Qayyum (2006). Potential Applications of the oxidoreductive enzymes in the decoloration and detoxification of textile and other synthetic dyes from polluted water. Critical reviews in Biotechnology. 26: 201-221. 65. Instituto Nacional de Estadística y Geografía (2011). La Industria textil y del vestido en México; Instituto Nacional de Estadística Geográfica e Informática, México. 66. Instituto Nacional de Estadística y Geografía (2011). La industria textil y del vestid o en México 2011. Serie estadísticas sectoriales. 67. IPPC. (2003). Integrated Pollution Prevention and control. Reference document on best available techniques for the textiles industry. European Commession. 68. Jakoby, W.B. (1971). Enzyme purification and related techniques. Methods in Enzymology. 22: 273-315. 69. J. Patlan, D. Delgado (2010). La industria textil en México; diagnostico, prospectiva y estrategia. Centro de estudios de competitividad del Instituto tecnológico autónomo de México. 1-69. 137 70. Kabdaslı, I., Arslan-Alaton, I., Vardar B., Tünay, O. (2007). Comparison of electrocoagulation, coagulation and the Fenton process for the treatment of reactive dyebath effluent. Water Science & Technology Vol55 No10 pp 125 –13 4. 71. Kalme, S.D., Parshetti, G.K., Jadhav, S.U. and Govindwar, S.P. (2007). Biodegradation of benzidine based dye Direct Blue 6 by Pseudomonas desmolyticum NCIM 2112. Bioresource Technolology 98: 1405–1410. 72. Kaushik, P., Malik, A., (2009). Fungal dye decolorization: Recent advances and future potential. Environmental. Internacional, 35: 127-141. 73. Kim, S. J., y Shoda, M. (1999). Purification and characterization of a novel peroxidase from Geotrichium candidum Dec I involved in decolorization of dyes. Applied Environmental Microbiology, 65: 1029–1035. 74. Kulshrestha, Y., y Husain, Q. (2007). Decolorization and degradation of acid dyes mediated by partially purified turnip (Brassica rapa) peroxidases. Toxicology. Environmental Chemistry, 89(2): 255–267. 75. Kulla H. G, (1981). Aerobic Bacterial De gradation of Azo Dyes. Microbial Degradation of Xenobiotics and recalcitrant compounds. FEMS Symp. No 12. Academic Press, Ed. By Leisinger R. Hutter, A. M. Cook and J. Nuesch, London. 387 399. 76. Kuo, W.G. (2000). Decolorizing dye wastewater with Fenton’s Rea gent. Water Res. 26, 881–886. 77. Landolo, D., Amore, A., Birolo, L., Leo, G., Olivieri, G., Farazo V. (2011). Fungal solid state fermentation on agro-industrial wastes for acid wastewater decolorization in a continuous flor packed-bed bioreactor. Bioresourse Technology. 102, 7603-7607. 78. La industria del vestido en México: diagnóstico, prospectiva y estrategia, (2008). ITAM 79. Lee, C. Y. y Pennesi, A. P. (1984). Isolation and fhurter characterization of a heat resistant peroxidasa isoenzymes from cauliflower. Journal Food Science, 4 (6).1616-1617. 80. Lee, J. W., Choi, S.-P., Thiruvenkatachari, R., Shim, W.-G., Moon, H., (2006). Evaluation of the performance of adsorption and coagulation processes for the maximum removal of reactive dyes. Dyes Pigments 69: 196–203. 81. Leist, K. H. (1982). Subacute toxicity studies of selected organic colorants. Ecotoxicol Environmental. 6(5): 45-63. 82. Lemley, Ann T. and McCLUNG, Suzanne. (aug. 1994). Electrochemical treatment and HPLC analysis of wastewater containing acid dyes. En: Textil e Chemist and Colorist. Vol.26, No. 8 p. 17-22 83. Li, G., Wang, N., Liu, B., Zhang, X. (2009). Decolorization of azo bye Orange II by ferrate (IV) hypochlorite liquid mixture, potassium ferrate (VI) and potassium permanganate. Desalination, 249, 936-941. 84. Libra, J., Borchert, M., Vigelanhn, L., Storm, T., (2004) Two stage biological treatment of a diazo reactive textile dye and the fate of the dye metabolites. Chemosphere, 56; 167-180 85. López-Ayala, S. (2004). Degradación de un colorante diazo mediante procesos de oxidación química y biológica. Tesis de Maestría en Ingeniería Ambiental. Programa de Maestría y Doctorado Ambiental. Universidad Nacional Autónoma de México: 91. México, D.F. 138 86. Luna, Jiménez. (2007). Composición y procesamiento de la soya para consumo humano. Investigación y ciencia. Universidad Autónoma de Aguascalientes. 15 (037): 35-44. 87. Maddhinni V. L., Hima B.V., y Anjaneyulu Y. (2006). Degradation of azo dye with horse radish peroxidase (HRP). Journal Indian Inst. Science. 86: 507–514 88. Mejia, Claudia y Osorio, Víctor. Decoloración de las aguas residuales con alto contenido de índigo por el método de electrocoagulación. En: Revista Facultad de Ingeniería de la Universidad de Antioquia. Vol. 1, No. 29 (jun. 2003) 89. Matto, M., and Husain, Q. (2007). Decolorization of direct dyes by salt fractionated turnip proteins in the presence of hydrogen peroxide and redox mediators. Chemosphere 69(2): 338– 345. 90. McMullan, G., Meehan, C., Conneely, A., Kirby, N., Robinson, T., Nigam, P., Banat, I. M., Marchant, R. and Smyth, W. F. (2001) Microbial decolorization and degradation of textile dyes. Applied Microbiology and Biotechnology 56: 81-87. 91. Melgoza R. Ma., Cruz A. y Buitrón G. (2004). Anaerobic/aerobic treatment of colorants present in textile effluents. Water Science and Technology. 50(2): 149-155. 92. Meric, S., Kaptan, D., Tunay, C., (2003). Removal of color and COD from a mixture of four reactive azo dyes using Fenton oxidation process. Journal Environmental Science Health Part AToxic/Hazard. Subst. Environ. Engineering 38: 2241–2250. 93. Metcalf y Eddy. (2003). ”Wastewater Engineering. Treatment, Disposal, Reuse”. Ed. Mc Graw Hill, 4a. Ed. EEUU. 94. Mielgo, I., Lopéz, C., Moreira, M. T. Feijoo, G. y Lema, J. M. (2003). Oxidation degradation of azo dyes by manganese peroxidase under optimized conditions. Biotechnology. 19: 325-331. 95. Mishra, A., Bajpai, M., Pandey, S., (2006). Removal of dyes by biodegradable flocculants: a lab scale investigation. Sep. Science Technology. 41: 583–593. 96. Moeller, Ch. G. y Garzón, Z. M. A. (2003). Desarrollo de tecnologías no convencionales para el tratamiento de efluentes de la fabricación de colorantes tipo azo. Proyecto Interno IMTA. 97. Moeller G. y Garzón M. (2006).Decoloración y reducción de toxicidad de efluentes de la industria química de colorantes y pigmentos. Informe, primera etapa; Instituto Mexicano de Tecnología del Agua, Jiutepec, México. 98. Mohan, S.V., Prasad, K.K., Rao, N.C. and Sarma, P.N. (2005). Acid azo dye degradation by free and immobilized horseradish peroxidase (HRP) catalyzed process. Chemosphere. 58: 1097– 1105. 99. Mohsina H. y Khalil R. (2009). Potential applications of peroxidases. Food Chemistry, 115: 11771186 100.Nawar S.S. y Doma H. S. (1989). Removal of dyes from effluents using low cost agricultural byproducts, Science total Environ., 79(1):271-279. 101.Neamtu, M., Yediler, A., Siminiceanu, L., Macoveanu, M. &Kettrup, A. (2004). Decolorization of disperse red 354 azo dye in water by several oxidation processes-a comparative study. Dyes Pigm. 60(1), 61–68. 102.Neyens, E. & Baeyens, J. (2003). A review of classic Fenton’s peroxidation as an advanced oxidation technique. J. Hazard. Mater. 98(1–3), 33–50. 103.Nitheranont, T., Watanabe, A., Suzuki, T., Katayama, T., Asada, Y. (2011). Decolorization of synthetic dyes and biodegradation of bisphenol A by laccase from the edible mushroom, Grifola frondosa. Biosci. Biotechnol. Biochem. 75 (9), 1845-1847. 139 104.NOM-001-SEMARNAT-1996. Establece los límites máximos permisibles de contaminantes en las descargas residuales en aguas y bienes nacionales. Diario Oficial de la Federación. 105.López, C., Moreira V. M. T., Feijoo, G., Lema, J.M. (2007). Tecnologías para el tratamiento de efluentes industriales textiles. Revista de Química Teórica y Aplicada. 64, 561-573. 106.Ollikka, P., Alhomaki, K., Lepparen, V.M., Glumoff, T., Raijola, T. y Suominen, Y. (1993). Decolorization of azo, triphenyl methane, heterocyclic and polymeric dyes by lignin peroxidase isoenzymes from Phanerochaete chrysosporium. Applied Environmental Microbiology. 59: 4010–4016. 107.O´Neill C., Hawkes F. R., Hawkes D. L., Lourenço N. D., Pinheiro H. M y Delée, W. (1999). Colour in textile effluents-sources, measurement, discharge contents, and simulation: A review. Journal of Chemical Technology and Biotechnology, 74: 1009-1018 108.Pandey, A., Singh, P., Iyengar, L., (2007). Bacterial decolorization and degradation of azo dyes. International Biodect y Biodegradation, 59: 73-84. 109.Papadopoulos, A., Fatta, D., Loizidou, M. (2007). Development and optimization of dark fenton oxidation for the treatment of textile wastewater with high organic load. Journal Hazardous Materials; 146: 558-563. 110.Papinutti, L. and Forchiassin, F. (2010). Adsorption and decolorization of dyes using solid residues from Pleurotus ostreatus mushroom production. Biotechnology and Bioprocess Engineering. 15,102-1109. 111.Park, H., and Choi, W. (2003). Visible light and Fe (III)-mediated degradation of Acid Orange in the absence of H2O2. J. Photochem. Photobiol. A: Chemistry 159, 241–247. 112.Park, C., Lee, B., Han, E.J., Lee, J. and Kim, S. (2006). Decolorization of Acid Black 52 by fungal immobilization. Enzyme Microbiology Technology 39: 371–374. 113.Park, C., Lee, M., Lee, B., Kim, S.W., Chase, H.A., Lee, J. and Kim, S. (2007). Biodegradation and biosorption for decolorization of synthetic dyes by Funalia trogii. Biochemical Engeenerinh Journal. 36: 59–65. 114.Pasti-Grigsby M.B., Paszczynski A., Goszczynski, S., Crawford, D.L. and Crawford R.L. (1992). Influence of aromatic substitution patterns on azo dye degradability by Streptomyces spp. and Phanerochaete Chrysosporium. Applied and Enviromental Microbiology. 3605-3613. 115.Pignatello, J. J., Oliveros, E., MacKay, A. (2006). Advanced oxidation process for organic contaminant destruction based on the Fenton reaction and related chemistry. Environmental Science Technology; 31: 2399-2406. 116.Pütter J. (1974). Peroxidases. En Methods of enzymatic analysis. (H.U. Bergmeyer. Ed. Academic Pres, New York, 2da. Ed.301-315) 117.Quezada, M. y Buitrón, G. (1996). Biodegradación aerobia de colorantes tipo azo (rojo acido 151). XXV Congreso Interamericano de Ingeniería Sanitaria y Ambiental. Tratamiento de aguas residuales. Memoria; México, 2. 118. QUIMINET, 2012 119.Rai, H.S., Bhattacharyya, M.S., Singh, J., Bansal, T.K., Vats, P., Banerjee, U.C., (2005). Removal of dyes from the effluent of textile and dyestuff manufacturing industry: a review of emerging techniques with reference to biological treatment. Crit. Rev. Environmental Science Technology, 35: 219–238. 120.Razo-Flores, E., Donlon, B., Field, j., Lettinga, G., (1996). The effect of granular sludge on the strategies to obviate the problem of biological persistence. Journal Biotechnology, 94:101-123 140 121.Renhammar, B. y Malstrom, B. (1981). “Blue” copper-containing oxidases. In copper proteins. Edited by spiro, T. y Wiley, J. New York, N.Y. Metal ions in biology. 3, 109-149. 122.Robison, T. Mcmullan, G. Marchan R., Nigman, P. (2001). Remediation of dyes in textile effluent: A critical review on concurrent treatment technologies with a proposed alternative. Bioresourse technology. 77,247-255. 123.Rodríguez, E., Pickard, M. y Vázquez-Duhalt, R. (1999). Industrial dye decolorization by laccases from ligninolytic fungi. Current Microbiology. 38,27-32. 124.Rodríguez, P.S., Rosa C., Bermúdez, S., Serrat, D. M. y Kouroma, A. (2006). Selección de cepas de Pleurotus ostreatus para la decoloración de efluentes industriales. Revista Mexicana de Micología, 23. 9-15. 125.Rodríguez, Oscar y Roldan, Jhon Jairo. (1997) Alternativas para el tratamiento de aguas residuales en tintorerías textiles : Caso PANTEX S.A.Medellín, 126.Rodríguez C., S., Domínguez, A. y Sanroman, A. (2002). Production of manganese-dependent peroxidase in a new solid-state bioreactor by Phanerochaete chrysosporium grown on wood shavings: application to the decolorization of synthetic dyes. Folia Microbiology. 47: 417–421. 127.Rodríguez, L., Tudela, S., J., B. y García C., F. (2002). Extracto de alcachofa (Cynara scolymus, L.) y su empleo en la descontaminación de medios contaminados con fenoles, aminas aromáticas, haluros orgánicos y/o metales pesados. Patente 2 167 277. España. 128.SAGARPA, (2009). Secretaria de Agricultura, Ganadería, Desarrollo Rural Pesca y Alimentación. Boletín de Agricultura. México D. F. 129. Salas Colotta G. 2003 Tratamiento físico -químico de aguas residuales de la industria textil 130.Saldaña, F.P., Sandoval, M.J.C., López, L.R. y Salcedo, S.E., (2001). Utilización de un índice de diversidad para determinar la calidad del agua en sistemas loticos. Ingeniería Hidráulica de México, 16(2): 57-66. 131. Secretaria de Economía, 2012 132.Schönberger, H., Schäfer, T., (2002) Best Available techniques in textile industry, Research Report 200 94 329 UBA-FB 000325/e, Federal Environmental Agency, Berlin Germany 133.Shaffiqu, T.S., Roy, J.J., Nair, R.A. and Abraham, T.E. (2002). Degradation of textile dyes mediated by plant peroxidases. Applied Biochemical Biotechnoly. 102–103: 315–326. 134.Shi, B.Y., Li, G.H., Wang, D.S., Feng, C.H., Tang, H.X., (2007). Removal of direct dyes by coagulation: the performance of preformed polymeric aluminum species. Journal Hazardous. Material. 143: 567–574. 135.Singh-Rai, H., Shankar, M., Singh, J., Bansal, T., Vats, P., Benerjee, U. (2005). Removal of dyes from the effluent of textile and dyestuff manufacturing industry: a review of emerging techniques with reference to biological treatment. Critical reviews in environmental science and technology. 35:219-238 136.Siddique, M. H., St. Pierre, C. C., Biswas, N., Bewtra, J. K., & Taylor, K. E. (1993). Immobilized enzyme catalyzed removal of 4-chlorophenol from aqueous solutions. Water Research. 27: 883– 890. 137.Soares, O.S.G.P.,O´ rfa˜o, J.J.M., Portela, D., Vieira, A., Pereira, M.F.R., (2006). Ozonation of textile effluents and dye solutions under continuous operation: Influence of operating parameters. Journal. Hazardous. Material. 137: 1664–1673. 141 138.Sponza, D., Isik, M., (2005). Reactor performances and fatenof aromatics amines through decolorization of Direct Black 38 dye under anaerobic/aerobic sequential. Process Biochemical, 40; 35-44 139.Stolz, A. (2001). Basic and applied aspects in the microbial degradation of azo dyes. Applied Microbiology and Biotechnology. 56: 69-80. 140.Sundrarajan, M., Vishnu, G., Joseph, K., (2007). Ozonation of light-shaded exhausted reactive dye bath for reuse. Dyes Pigments 75: 273–278. 141.Sun, J. H., Sun, S. P., Fan, M. H., Guo, H. Q., Qiao, L. P. & Sun, R. X. (2007a) A kinetic study on the degradation of p-nitroaniline by Fenton oxidation process. J. Hazard. Mater. 148 (1–2), 172–177. 142.Sun, J. H., Sun, S. P., Wang, G. L. & Qiao, L. P. (2007b) Degradation of azo dye Amido black 10B in aqueous solution by Fenton oxidation process. Dyes Pigm. 74(3), 647–652. 143.Sun, S. P., Li, C. J., Sun, J. H., Shi, S. H., Fan, M. H. & Zhou, Q. (2009). Decolorization of an azo dye Orange G in aqueous solution by Fenton oxidation process: effect of system parameters and kinetic study. J. Hazard. Mater. 161(2–3), 1052–1057. 144.Supaka, N., Juntongjin, K., Damronglerd, S., Delia, M. L., Strehaiano, P. (2004). Microbial decolorization of reactive azo dyes in a sequential anaerobic-aerobic system. Chemical Engineering Journal. 99(2): 169-176. 145.Tan, N., (2001) Integrated and sequential anaerobic/aerobic biodegradation of azo dyes. PhD thesis, Wageningen University, Wageningen, The Netherlands. 146.Texteira, S.S. R., Pereira, P., y Ferreira-Leitao, V. (2010). Extraction and application of laccases from Shimeji Mushrooms (Pleurotus ostreatus) residues in decolourization of reactive dyes and a comparative study using commercial laccase from Aspergillus oryzae. Enzyme Research. 2010, 1-8. 147.Van der Zee, F.P., Villaverde, S., (2005). Combined anaerobic-aerobic treatment of azo dyes – a short review of bioreactor studies. Water Resource, 39: 1425–1440. 148.Vandevivere P, Veartraete W. (1998). Treatment and reuse of wastewater from the textile industry: review of emerging technologies. Journal of chemical technology and biotechnology. 72, 289-302. 149.Verma, P. and Madamwar, D. (2002). Decolorization of synthetic textile dyes by lignin peroxidase of Phanerochaete chrysosporium. Folia Microbiology. 47: 283–286. 150.Villalobos D. A. y Buchanan I. D. (2002). Removal and aqueous phenol by Arthromyces ramosus peroxidase. Environmental Engineer Science. 1: 65-73. 151.Villegas R. O., Geissler G., Silva H. A., Vergara G. E. (2003). Inmovilización de una peroxidasa de chayote y su potencial aplicación en la remoción de sustancias fenólicas en aguas contaminadas. Revista Internacional de Contaminación Ambiental. 19 (2): 73-81. 152.Wagner y Nicell J. A. (2002). Detoxification of phenolic solutions with horseradish peroxidase and hydrogen peroxide. Water Resource.36:4041-4052 153.Wang, M., Li, H., Wu, J., Huo, Y., Guo, G., Cao, F., (2006a). Flocculant for purification of printing and dyeing wastewater. Univ Shanghai Normal. 154.Wang, S. B. (2008) A comparative study of Fenton and Fenton-like reaction kinetics in decolourisation of wastewater. Dyes Pigm. 76(3), 714–720. 155.Weisburger, J. H. (2002) Comments on the history and importance of aromatic and heterocyclic amines in publichealth. Mutation Research, 506-507: 9-20. 156.Welinder, K. (1992). Haem peroxidases. Extraído 20 Agosto, 2012. De http://metallo.scripps. 142 157.World Bank Group, (2011). Pollution Prevention and Abatement: Textiles Industry. Draft Technical Back-ground Document. Environment Department, Washington, D. C. 158.Wu, J., Doan, H., Upreti, S., (2008b). Decolorization of aqueous textile reactive dye by ozone. Chemicals Engineering. 142, 156–160. 159.Wu, H., Fan M., Li, C., Peng, M., Sheng, L., Pan, Q., Song, G. (2010). Kinetic studies on the degradation of crystal violet by the Fenton oxidation process. Water Science & Technology-62.1. 160.Yesilada O, Asma D, Cing S. (2003). Decolorization of textile dyes by fungal pellets. Process Biochemical. 38: 933-938. 161.Yu, G., Wen, X., Li, R. and Qian, Y. (2006). In vitro degradation of a reactive azo dye by crude ligninolytic enzymes from nonimmersed liquid culture of Phanerochaete chrysosporium. Process Biochemistry 41: 1987–1993. 162.Yue, Q.Y., Gao, B.Y.,Wang, Y., Zhang, H., Sun, X., Wang, S.G., Gu, R.R., (2008). Synthesis of polyamine flocculants and their potential use in treating dye wastewater. Journal Hazardous. Material. 152: 221–227. 163.Zeybek Z., Yuce Cetinkaya S., Alioglu F., Alpbaz M. (2007). Determination of optimum operating conditions for industrial dye wastewater treatment using adaptive heuristic criticism pH control. Journal of Environmental Management. 85: 404-414. 164.Zhang, Y., Ma, C., Ye, F., Kong, Y., Li, H. (2009). Treatment of wastewater of paper mill with integrated membrane process. Desalination, 236,349-356. 165.Zhao, X., Lu, Phillips, D., Hwang, H. y Hardin, I. (2006). Study of biodegradation products from azo dyes in fungal degradation by capillary electrophoresis/electrospray mass spectrometry. Journal of Chromatography. 1159: 217-224. 166.Zia, MA. (2002). Standardization of conditions for glucose estimation using indigenously purified enzymes. Thesis de Maestria. Department of Agriculture (Biochemistry). University of Agriculture, Faisalabad 167.Zhou, Y., Liang, Z., Wang, Y., (2008). Decolorization and COD removal of secondary yeast wastewater effluents by coagulation using aluminum sulfate. Desalination, 225: 301–311. 168.Zoollinger H. (2001). Color Chemistry: Syntheses, Properties and Applications of Organic Dyes and Pigments. John Wiley & Sons, 3a edición. 169.Greenpeace (2012). Ríos Mexicanos Ríos Tóxicos. 170.Greenpeace (2012). Estudio de la Contaminación en la cuenca del Río Santiago y la salud pública en la región. 143




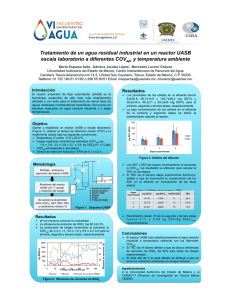


![A↔ B (-rA) = 0.04CA-0.01CR, [=] mol*L](http://s2.studylib.es/store/data/005357341_1-6e8dd554fb791e1c2c9f555a9c29f5b3-300x300.png)