Microsoft PowerPoint - Materiales cer\341micos.ppt
Anuncio

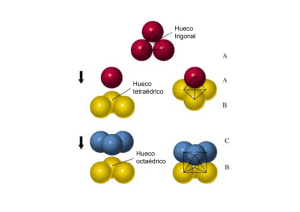
Materiales cerámicos Ciencia de Materiales Otoño 2009 Lilia Meza Montes Características generales Inorgánicos, no metálicos Formados por elementos metálicos y no metálicos, enlaces iónicos y/o covalentes Compuestos simples hasta mezclas de fases Duros y frágiles, tenacidad y ductilidad bajas Buenos aislantes eléctricos y térmicos Temperaturas de fusión altas y gran estabilidadi química (estabilidad de enlaces) á Tipos de cerámicos Tradicionales - Hechos de tres componentes básicos: arcilla, sílice (silex) y feldespato - Ejemplos: vidrios, ladrillos, azulejos, porcelana eléctrica de Ingeniería - Compuestos puros o casi puros - Ejemplos: óxido de aluminio (Al2O3), carburo de silicio (SiC) y nitruro de Si (Si3N4). Configuraciones de coordinación Factores que determinan empaquetamiento 1. Tamaño relativo de iones 2. Equilibrio de cargas para neutralidad. Sólidos iónicos tienden a ser densos para disminuir energía total. Cationes: más pequeños que aniones Si los aniones no tocan el catión central, se vuelve inestable (puede vibrar) Razones de radios Razón del radio del catión central al de aniones circundantes rcatión/ranión razón de radios crítica (mínima): Cuando iones se tocan Estructura de CsCl Iónica NC=8 (8cl -1Cs) CsBr, TlCl, TlBr AgMg, LiMg, AlNI No es de importancia para cerámicos Razones de radio elevadasNC más altos Celda unitaria de NaCl NC=6 Otros cerámicos MgO, CaO,NiO, FeO Espacios intersticiales Espacios entre los átomos o iones octaédrico tetraédrico Huecos intersticiales de fcc y hcp Huecos intersticiales fcc 12 aristas1/4 hueco en cada arista4 huecos octaédricos en cada celda unitaria Blenda de Zinc 4 Zn, 4 S Dos redes intercaladas 87% covalente tetraédrica con enlace covalente NC=4 Cloruro de Ca Ca2+ sitios de fcc F- 8 huecos tetraédricos, otros huecos vacantes UO2, BaF2, AuAl2, PBMg2 ZrO2: deformado (monoclínico) Corindón: Al2O3 Iones O2- ocupan los sitios de celda unitaria hcp Iones Al3+ ocupan solo dos tercios de los sitios intersticiales del octaedro para conservar la neutralidad eléctrica Perovsquita CaTiO3 Estructuras de silicatos Si, O (más abundantes de la naturaleza) Arcillas, feldespatos y micas Bajo costo, disponibilidad y propiedades Vidrios, cemento portland y ladrillos Aislantes Ión tetraédrico SiO44- 50%covalente Razon de radios 0.29 Fuerzas de enlace grandes Enlaces: esquina-esquina Estructura de cadena de silicato Cada O tiene un electrón disponible variedad de estructuras Cadena o anillo : dos esquinas unidas (MgSiO3, Berilo) Laminar: tres (talco mineral) Moldeo de vaciado de suspensión Drenado en un molde poroso de yeso de París Moldeo sólido Conductividad térmica de materiales cerámicos Aplicaciones Temperatura de fusión Transición vítrea Solidificación de materiales cristalinos y amorfos Cristobalita (silice cristalina ideal), Tetraedro Si-O sílice cristalina. Notar la falta de orden a largo alcance Vidrio de soda-cal Vidrio de alúmina-sílice Recubrimientos Por aspersión térmica con WC/1-Co4Cr Microestructura Aplicaciones en medicina: prótesis Cadera fractura y prótesis Componentes de prótesis: cabeza de alúmina, cavidad de alúmina y base. Bibliografía Fundamentos de la ingeniería y ciencia de materiales, W.F. Smith y J. Hashemi, McGraw Hill Interamericana, 4a. Ed., India 2006.