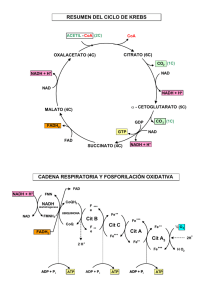
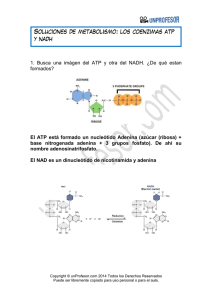
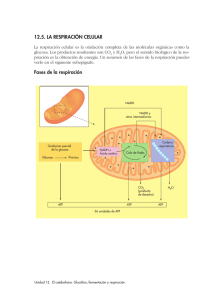
Tema 12.- Introducción al metabolismo Ciclo de materia y flujo de energía en la biosfera Visión general del metabolismo: Catabolismo y anabolismo Variación de energía libre. Compuestos ricos en energía: ATP Oxidorreducción biológica. Sistemas de transporte electrónico. Fosforilación oxidativa: Estudio de la ATPasa mitocondrial. Fotofosforilación Objetivos; Conceptos sobre vías metabólicas: Catabolismo y anabolismo Significado del acoplamiento energético de reacciones enzimáticas: “una R endergónica se produce si se acopla con otra R exergónica ∆GT < 0. Comprender qué son los compuestos ricos en energía y calcular el potencial de transferencia de grupos fosfato. Función del ATP. Entender la función del NADH en la oxidación de nutrientes y como se efectúa el transporte de e- en los complejos de proteínas transmembrana con grupos red-ox activos. La Coenzima Q y el citocromo c son transportadores móviles de e- en la membrana. Los H+ son traslocados a través de la membrana interna por los complejos I, III y IV. La energía libre de la oxidación del NADH se conserva como un gradiente electroquímico de H+(fuerza protomotriz), que activa a la ATP-asa. 2NADH + 2H+ + O2 transporte de 4e- 4 H2O Se traslocan 20 H+ 2,5 ATP Introducción al metabolismo Metabolismo: Conjunto ordenado de reacciones enzimáticas que se producen en las células. Conjunto de reacciones que transforman la materia con intercambio de energía. Las reacciones bioquímicas organizadas en vías metabólicas. están Las vías metabólicas son interdependientes y su actividad está regulada y coordinada Funciones del metabolismo: Degradar las moléculas de los nutrientes para obtener energía química (ATP) Sintetizar las biomoléculas componentes de las células, consumiendo energía (ATP). ESQUEMA DEL METABOLISMO Bioenergética: Bases termodinámicas de las reacciones bioquímicas: Variación de energía libre ∆Gº Las células y los organismos vivos son sistemas abiertos que intercambian materia y energía con su entorno. 1- Aprovechan la energía: A partir de la energía solar (org. autótrofos) A partir de componentes químicos (nutrientes) de su entorno (org. heterotótrofos) 2 - Utilizan la energía para la producción de un trabajo biológico. Biosíntesis (anabolismo) Trabajo mecánico (contracción muscular) Gradientes osmóticos (transporte contra gradiente) Trabajo eléctrico (transmisión del impulso nervioso) Bioenergética: estudio cuantitativo de la transferencia y utilización de la energía en los sistemas biológicos. La única energía que pueden utilizar las células vivas (P y T = ctes) es la energía libre Energía libre de Gibbs (G) Bioenergética Las reacciones metabólicas se rigen por las leyes de la termodinámica Principio de conservación de la energía Aumento natural del desorden, al realizarse un trabajo, una parte de la energía se disipa en forma de calor. ∆G = ∆H - T ∆S Energía libre de Gibbs (G): Cantidad de energía capaz de realizar trabajo durante una reacción a temperatura y presión constantes Entalpía (H): contenido calórico del sistema ∆H > 0 Reacción endotérmica (absorbe calor) ∆H < 0 Reacción exotérmica (libera calor) Entropía (S): aleatoriedad o desorden del sistema ∆S > 0 Aumenta entropía en el sistema ∆S < 0 Disminuye entropía en el sistema Energía libre de Gibbs Cantidad de energía capaz de realizar trabajo durante una reacción a Tª y presión constantes Proporciona información sobre: La dirección de la reacción química Composición en el equilibrio La cantidad de trabajo desarrollado Variación de energía libre (∆G) Predice si una reacción es factible o no Reactivos GR Productos GP ∆ G = GP - GR ∆G = 0 Proceso en equilibrio ∆G > 0 Reacción endergónica, consume energía ∆G < 0 Reacción exergónica, genera energía (espontánea) Relación entre ∆G, ∆Gº y Keq ∆Go = variación de E libre en condiciones estándar. Valor fijo para cada reacción ∆G = variación de E libre real. Es variable, depende [R] y [P] y de la Tª ∆G = ∆Go + RT ln Si la reacción está en el equilibrio ∆G 0 = ∆Go + RT ln [C] [D] [A] [B] =0 [C]eq [D]eq [A]eq [B]eq Si la reacción es en condiciones fisiológicas (pH = 7) ∆Go = - RT ln Keq ∆Go’ = - RT ln K’eq Compuestos ricos en energía y Potencial de transferencia de ̴ P El acoplamiento de las reacciones endergónicas y exergónicas está mediado por intermediarios de alta energía Los compuestos ricos en energía: Liberan la energía mediante la hidrólisis de un enlace y transferencia de grupo (rotura de un enlace rico en energía ~) Transfieren la energía en una sola reacción Son aquellos que ceden una energía > 25 kJ/mol (potencial de transferencia de grupo) Potencial de transferencia de grupo: Capacidad de un compuesto para de ceder “el grupo” a otra sustancia. Se mide por la energía libre desprendida en la hidrólisis del enlace del grupo a transferir (alta energía). Grupos transferidos en reacciones bioquímicas: Fosfato, Acilo, metilo, etc. ATP: 5’-Adenosina trifosfato: estructura y función Adenina Enlace fosfoéster Enlace fosfoanhidro 5´-Adenosina trifosfato Ribosa ATP = Nexo entre los procesos dadores de energía y los procesos biológicos consumidores de energía. Desarrolla: - trabajo químico y - trabajo biológico Compuestos fosfato ricos en energía Fosfoenolpiruvato piruvato + Pi ∆G´o = -63 kJ/mol 1,3-Bisfosfoglicerato 3-Fosfoglicerato + Pi ∆G´o = -49,3 kJ/mol Fosfocreatina Creatina + Pi ∆G´o = -43 kJ/mol Fosfoenolpiruvato ∆G´o de hidrólisis (kJ/mol) 1,3-Bisfosfoglicerato Fosfocreatina Compuestos Fosfato de alta energía ATP Compuestos Fosfato de baja energía Glucosa-6-fosfato Glicerol-3-fosfato Flujo de grupos P Dadores de P de alta energía ATP Aceptores de P de baja energía Metabolismo = catabolismo + anabolismo Catabolismo Anabolismo Ejemplo de acoplamiento energético: papel del ATP ATP ∆G´o2 ∆G´oTOTAL = ∆G´o1 + ∆G´o2 = 13,8 + (-30,5) = = -16, 7 kJ/mol ADP = -30,5 kJ/mol ∆G´o1 = 13,8 kJ/mol Glucosa Glucosa + Pi ATP + H2O Glucosa + ATP Glucosa 6-P + H2O ADP + Pi Glucosa 6-P + ADP Reacción global exergónica Glucosa 6-P El ATP es un índice de la carga energética celular La [ATP] + [ADP] + [AMP] en el interior celular es constante [ATP] + ½ [ADP] Carga energética celular = [ATP] + [ADP] + [AMP] Velocidad relativa Vía generadora de ATP Vía utilizadora de ATP Carga energética T 12B.- Oxido-reducción biológica Las células oxidan los nutrientes orgánicos para generar ATP, necesario para su trabajo útil. Perdida de electrones = Oxidación A A+ + eoxidado Ganancia de electrones = Reducción reducido El flujo de electrones en el metabolismo se canaliza a través de intermediarios metabólicos y de transportadores (COENZIMAS REDOX) que convierten la energía del flujo de e- (∆ Eo) en energía química (∆ Go): ATP. Ejemplo: La glucosa es un nutriente reducido, una fuente de electrones. Su degradación producirá la coenzima reducida NADH CO2 NAD+ FAD NADH FADH2 ∆ Eo ∆ Go ∆ Go H2O ATP Potencial de reducción: Eo Fe2+ (donador) / Fe3+ (aceptor): par redox conjugado NADH (donador) / NAD+ (aceptor): par redox conjugado Potencial de reducción ( E ): tendencia de un reductor a ceder e En condiciones estándar ( Eo ): 25º C, 1 atm presión, [oxidante] y [reductor] = 1 M H + + e- Eo = 0 V ½ H2 En condiciones fisiológicas pH = 7 ( Eo´ ) Patrón o par estandar Eo(H+/1/2H2) = 0,42 V •Tendencia a adquirir e- > par estándar Eo´ + Mucha afinidad por e- ->OXIDANTE •Tendencia a adquirir e- < par estándar Eo´ - Poca afinidad por e- ->REDUCTOR Los e- fluyen desde las especies reductoras, con un Eo´ más electronegativo (- Eº’) a las especies oxidantes, con un Eo´ más electropositivo (+ Eº’). Potencial de reducción e ∆Gº (ejemplo) Los potenciales de reducción estándar de los compuestos permiten calcular la ∆Gº de la reacción redox Piruvato + NADH + H+ Lactato + NAD+ Semirreacciones: Piruvato + 2H+ + 2e- Lactato NADH - 2H+ - 2e- NAD+ Eo´ = -0,19 V Eo´ = -0,32 V ∆Go´ = - n F ∆E ∆ o´ n = nº de e- cedidos = 2, F = 96,48 kJ/mol V ∆Eo´ = Eo´ (aceptor e-) – Eo´ (donador e-) ∆Eo´ = Eo´ (oxidante) – Eo´ (reductor) ∆Eo´ = -0,19 – (-0,32) = 0,13 V Piruvato acepta e- del NADH ∆Go´´ = -2 (96,5 kJ/mol V) (0,13 V) = -25,09 kJ/mol La reacción es espontánea en condiciones estándar: [ ]= 1M, 25ºC y pH 7 Respiración mitocondrial • Las células aeróbicas consumen O2 y lo reducen a H2O con los e- procedentes de la oxidación de nutrientes (NADH, FADH2). TRANSPORTE ELECTRÓNICO MITOCONDRIAL: Se da en la membrana interna mitocondrial a través de una serie de transportadores de e- (componentes de la cadena respiratoria) que llevan los e- desde las coenzimas reducidas (NADH, FADH2) hasta el O2. Membrana interna Es impermeable a casi todos los iones,Se pliega en crestas Contiene los componentes de la cadena de transporte de e-, desde el NADH hasta el O2. y la ATP sintasa Durante la transferencia de e- desde el NADH, o el FADH2 , hasta el O2 se genera un bombeo de H+ hacia el espacio intermembranoso, originando una fuerza protomotriz (H+-motriz) que activa a la ATP-sintasa. • La fosforilación oxidativa consiste en la fosforilación del ADP hasta ATP por la ATP-sintasa, activada por los H+ (fuerza proton-motriz). • constituye la fuente más importante de ATP en los organismos aerobios La oxidación del NADH se produce en la cadena respiratoria mitocondrial Formada por complejos proteicos y otros transportadores 1.- Transporte de electrones desde el NADH • Complejo I: NADH CoQ oxidorreductasa • Complejo III: Ubiquinol citocromo c oxidorreductasa • Complejo IV: Citocromo c oxidasa 2.- Transporte de electrones desde el FADH2 • Complejo II: Succinato CoQ reductasa • Otras proteínas similares: - glicerol-P-deshidrogenasa - acil-CoA-deshidrogenasa Compuestos redox Otros componentes de la cadena respiratoria Transportadores de electrones Coenzimas: NAD+ NADP+ Coenzimas SOLUBLES de enzimas deshidrogenasas FMN FAD UNIDAS covalentemente a flavoproteínas (grupo prostético) Quinonas: Transportadores en medio lipídico (membranas) Ubiquinona = Co Q = Q Citocromos: Proteínas con grupo prostético hemo Centros ferro-sulfurados Proteínas con Fe asociado a átomos de S algunos transportadores de e- están asociados a proteínas y forman lo que llamamos Complejos: I, II, III y IV Coenzimas transportadoras de e- : DINUCLEOTIDOS DE ADENINA y NICOTINAMIDA NADH (coenzima soluble) o NADH (reducido) NAD+ (oxidado) Adenina NAD+ + 2H+ + 2e- AH2 + NAD+ Coenzima de oxidorreductasas o deshidrogenasas Responsable entrada e- por el complejo I NADH + H+ A + NADH + H+ MONONUCLEOTIDOS DE FLAVINA y DINUCLEOTIDOS DE FLAVINA y ADENINA FMN FAD FMN y FAD (coenzimas NO solubles, ligadas a proteínas) Anillo de isoaloxazina FMN . . FADH (FMNH ) (semiquinona) FADH2 (FMNH2) (totalmente reducido) FAD FMN presente en complejo I FADH2 entrada de e- por el complejo II FAD + 2H+ + 2e- FADH2 FMN + 2H+ + 2e- FMNH2 COENZIMA transportadora de e- : Ubiquinona, Coenzima Q, CoQ Unidades de ISOPRENO Ubiquinoa (Q) Totalmente oxidada Lípido isoprenoide Radical Semiquinona Parcialmente oxidado QHo Difunde libremente por la membrana No está ligado a ninguna proteína Ubiquinol Totalmente reducido QH2 Puede transferir 1 e- o 2 e- Método: Extraible con isooctano Proteínas con transportadores de e- : Citocromos (HEMO) Proteínas con un grupo hemo Transfieren 1 e- mediante la oxidorreducción del Fe (2+, 3+) Clasificación según su espectro de absorción: a, b, c Citocromos a y b están en LOS complejos III y IV Citocromo c es una proteína soluble, se asocia con la membrana interna Proteínas con centros ferro-sulfurados Proteínas con Fe en forma NO HEMO sino asociado a átomos de S de los residuos de cisteína en las proteínas Transfieren 1 e- mediante la oxidorreducción del Fe Fe-S 2Fe-2S 4Fe–4S NADH CoQ reductasa Transfieren 2 e- desde diversos sustratos (succinato, glicerol-3-P, Acil-CoA) que son oxidados por estas enzimas, y los e- van a través de FAD y por grupos ferrosulfurados hasta la CoQ Transfiere 2 e- desde el NADH hasta la CO Q, pasando por FMN y por grupos ferosulfurados (Fe-S) en el complejo proteico Enzimas tipo complejo II • succinato CoQ reductasa • Glicerol-3-P desHasa • Acil-CoA desHasa CoQ cit c reductasa Cit c oxidasa Transfiere 2 e- desde la CO Q hasta el cit c, pasando por los cit b y c1 y por grupos ferosulfurados Los e- se transfieren aquí de 1 en 1 Transfiere e- desde el citocromo c (4 viajes) hasta el O2, pasando por dos grupos de Cu y por los citocromos a y a3. A) 2NADH 4e- O2 2H2O Bombean 20 H+ 5 ATP B) 2FADH2 4 e- O2 2H2O Bombean 12 H+ 3 ATP Potenciales de reducción de los pares red-ox transportadores de e- en la cadena respiratoria REACCIÓN E0‘ •NAD+ / NADH + H+ -0.32 •Flavoproteina-FMN (ox) / Flavoproteina-FMNH2 (red) -0.30 Piruvato / Lactato –0.18 Acetaldehido / Etanol -0.16 Oxalacetato / L - malato -0.166 •Coenzima Q (ox) / Coenzima Q (red) +0.04 •Citocromo C (ox) / Citocromo C (red) +0.25 •Citocromo a3 (ox) / citocromo a3 (red) +0.55 •½ O2 / H2O +0.82 [ H+] FADH2 [ H+] [ H+] Determinación de la secuencia con Inhibidores del transporte electrónico Impiden el paso de e- a través de los transportadores de la cadena respiratoria, interrumpiendo en consecuencia la forforilación oxidativa. NADH → FMN CoQ → cit b → cit c1 → cit c → cit a → cit a3 → O2 FADH2 Transportadores reducidos y transportadores oxidados Rotenona barbitúricos Amital Azida Teoría quimiosmótica de Mitchel: Los Complejo I, III, y IV generan un gradiente de H+ (fuerza protón-motriz) que que activa la ATP sintasa La FUERZA PROTÓNMOTRIZ, en el espacio intermembranoso, tiene dos componentes El gradiente de carga potencial eléctrico = ∆Ψ El gradiente de [ H+ ] potencial químico = f(pH) BALANCE: A) 2NADH 4e- O2 Bombean 20 H+ 5 ATP B) 2FADH2 4 e- O2 Bombean 12 H+ 3 ATP Agentes desacoplantes DISIPAN LA FUERZA PROTÓN-MOTRIZ y p-DNF p-dinitrofenol desacoplan la fosforilación oxidativa del TEM, por tanto bajan el rendimiento de la síntesis de ATP Los agentes desacoplantes son sustancias que introducen H+ desde el espacio intermembranoso hacia el interior mitocondrial. El p-DNF entra en las células en estado molecular y en el interior se disocia. En el espacio intermembranoso (pH inferior) se protona y entra a la mitocondria, en el interior hay un pH superior y se disocia. La gramicidina A es un ionóforo ATP sintasa: la subunidad F0 la ancla a la membrana y la F1 en la matriz mitocondrial El anillo c gira con el paso de H+ El giro de “γε γε” γε provoca cambios conformacionales en las subunidades αβ F1= α3 β3 γ δ ε F0= a b2 c12 Las 3 unidades β de la ATP sintasa no son equivalentes, la rotación de “γγ−ε” las cambia la conformación. Según va girando el complejo por el paso de H+ las unidades β cambian de conformación: L: une ADP y Pi; T: sintetiza ATP; O: libera ATP Transportadores de iones a través de la membrana interna mitocondrial El ATP sintetizado en el interior Espacio intermembranoso mitocondrial debe de exportarse al citoplasma para cumplir allí con las necesidades propias -Esto se hace con un sistema antiporte: 1 ATP sale y 1ADP entra a refosforilarse - Hay otro sistema simporte que importa Pi y H+ Traslocasa de nucleotidos de adenina (antiporte) ATP sintasa Traslocasa de fosfato (simporte) DENTRO de la Matriz La síntesis de materia orgánica en la biosfera (glúcidos: Gal-3-P; F-6-P) se efectúa en base a la energía hν ν en los organismos fotosintéticos. FOTOSÍNTESIS: se produce en los cloroplastos que poseen un sistema de membranas altamente organizado, los tilacoides, dentro del estroma. En la FOTOSÍNTESIS se pueden diferenciar dos tipos de procesos: 1- FOTOFOSFORILACIÓN: conversión de la energía lumínica en energía química: ATP Y NADPH. 2- SÍntesis de glúcidos. Ciclo de Calvin. 1.En las membranas tilacoides de los cloroplastos hay pigmentos que absorben la luz y toman e- del H2O, los activan y los transportan hasta generar NADPH. Además, el paso de e- por algunos complejos transportadores procura un gradiente de H+ entre el interior tilacoidal y el estroma. La fuerza protón-motriz activa a la ATP-asa y se obtiene ATP. LOCALIZACIÓN DE LA FOTOFOSFORILACIÓN La fotofosforilación se produce en los fotosistemas y los complejos proteicos situados en las membranas tilacoides. Las reacciones del ciclo de Calvin o fase oscura se producen en el estroma. ESTRUCTURA y MICROGRAFÍA DE UN CLOROPLASTO Localización de los componentes que realizan la fotofosforilación. Se distribuyen en las regiones apiladas de las membranas tilacoides 1) FOTOFOSFORILACIÓN = Generación de energía química: ATP y de NADPH En los cloroplastos existen 2 fotosistemas (I y II) compuestos por pigmentos: clorofilas y otros. Iluminados los dos funcionan de forma concertada, así que: ESQUEMA EN Z.- los fotosistemas absorben los fotones y se activan - en los sistemas activados, la energía se utiliza para extraer los edel H2O - los e- se transportan hasta generar NADPH - con el transporte de ese impulsan los H+ a través de la membrana tilacoide. - el gradiente de H+ generado activa a la ATPasa para producir ATP. Los pigmentos fotosintéticos (clorofilas, carotenoides, etc.) absorben fotones debido al sistema de dobles enlaces conjugados Esquema de los fotosistemas en los fotosistemas ESPECTROS DE ABSORCIÓN de las CLOROFILAS a y b Los e- fluyen desde el FS II al FS I y atraviesan el complejo citocromo bf, que es una bomba de H+. TRANSPORTADORES: Ph: feofitina; Qa y Qb: plastoquininas y PC: plastocianina En el FS I, la absorción de luz induce la transferencia de e- desde el H2O a través del P700 a la ferredoxina-reductasa por una C.T.E. TRANS.: clorofila, una quinona y complejos 4Fe-4S. Los dos fotosistemas tienen que funcionar, absorbiendo fotones, para que se produzca un flujo ininterrumpido de edesde el H2O hasta el NADP+. Estroma SE GENERA NADPH Y ATP en el estroma FOTOFOSFORILACIÓN cíclica y no cíclica (generación de ATP) Fotofosforilación cíclica: Absorbe fotones sólo el FS I y la Ferredoxina reducida puede pasar los e- a la cadena PQ, cyt bf, PC y de nuevo caer los e- al propio FS I, cerrando el ciclo. Al pasar los e- por el complejo cyt bf se produce el bomneo de H+, que permite activas a la ATP-asa Se genera ATP Fotofosforilación no cíclica, cuando los dos fotosistemas absorben luz simultáneamente Se genera ATP y NADPH
 0
0
Anuncio
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados