La regulación orgánica de la ingesta energética constituye un papel
Anuncio

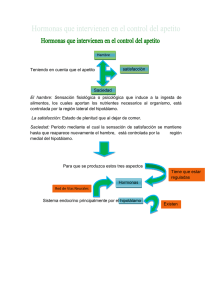
RESEÑA CLUB DE REVISTA POSGRADO DE MEDICINA DE LA ACTIVIDAD FÍSICA Y EL DEPORTE - FUCS TÍTULO DEL ARTÍCULO Regulación de la ingesta alimentaria y del balance energético; factores y mecanismos implicados. AUTOR E. González-Jiménez y J. Schmidt Río-Valle BIBLIOGRAFÍA (Nutr Hosp. 2012;27:1850-1859) pag 117 a 126 La regulación orgánica de la ingesta energética constituye un papel importante en la función celular, el cual implica un equilibrio entre la cantidad de energía almacenada en forma de grasa corporal y el catabolismo de esta. La suma de varios factores que van desde estructuras nerviosas centrales hasta la última unidad funcional del tejido adiposo son las encargadas de mantener este equilibrio. Este proceso que describimos, es regulado en su totalidad por el hipotálamo, pero es llevado a cabo por numerosos péptidos que tiene acción sinérgica o antagónica, los cuales interactúan entre si y son activados por diferentes señales, luego ésta información es llevada a los diferentes núcleos los cuales se encargan de emitir respuestas en términos de comienzo o finalización de la ingesta y por ende de aumento o inhibición del gasto calórico. La alteración de este equilibrio puede desencadenar obesidad y otras enfermedades crónicas. Materiales y métodos: La revisión de la literatura se realizó en Medline y Ebsco de artículos publicados en inglés o español entre enero de 2009 y enero de 2012. Los resultados de búsqueda fueron 198 estudios de los cuales 70 cumplían requisitos y fueron analizados. Homeostasis nutricional: Conjunto de procesos fisiológicos implicados en los mecanismos de digestión, absorción de los nutrientes, almacenamiento de estos y finalmente su uso y gasto; con el único objetivo de lograr una buena talla y peso en la adolescencia, mientras que en la edad adulta su objetivo es adquirir y mantener un peso adecuado. Aunque este proceso parce complejo en realidad está limitado a una ingestión de los alimentos con su posterior digestión y absorción en donde participan enzimas y hormonas gastrointestinales. De manera secuencial los depósitos de glucógeno hepático y muscular son abastecidos, de la misma forma pasa con los triglicéridos en los adipocitos en la fase postprandial. En la fase de ayuno, la obtención de nutrientes se logra mediante diferentes procesos metabólicos como la lipólisis, la glucogenólisis y la neoglucogénesis, de la misma forma debemos establecer una diferencia entre el gasto de procesos de mantenimiento y el gasto derivado de actividad física, crecimiento, acción dinámico específica de los alimentos y la que se pierde mediante fluidos corporales. Todos estos procesos están controlados por un amplio número de señales nerviosas periféricas, moléculas y mediadores de acción neuroendocrina, todo integrado al sistema nervioso central. A nivel del hipotálamo encontramos además estructuras responsables del hambre (núcleo lateral) y la saciedad (núcleo ventromedial), una vez llegan estos estímulos la respuesta nerviosa eferente que controlará el volumen de energía almacenado y consumido a corto, mediano o largo plazo. Señales de regulación energética: Mecanismo de la regulación de la ingesta a corto plazo: En este artículo la idea es cambiar la idea que se tiene de que el hambre es producida por la baja en los niveles plasmáticos de glicemia y de lípidos, pero como veremos a continuación este proceso es un poco más complejo pero será detallado a continuación; éste proceso tiene un inicio que está limitado por una serie de señales (olor, sabor, textura, temperatura, presentación) activadas desde la percepción de los alimentos, estas señales son llevadas a través de los pares craneales hasta el SNC. Por otra parte el inicio de la producción insulínica parece ser otro factor que desencadena la ingesta de alimentos; a estos procesos se conoce en la actualidad como fase cefálica de la alimentación y el mecanismo compensatorio a esta fase es la disminución del apetito en el sujeto, dicho mecanismo se sustenta en la existencia de receptores en la orofaringe, los cuales controlan el volumen calórico total ingerido en cada ingesta, en teoría genera señales para inhibir el deseo de comer. Ante la demora de la ingesta de alimentos, si se produce una disminución de glicemia plasmática, esto genera una sensación de hambre mucho mayor con el objetivo de recobrar la reserva energética consumida durante el ayuno (Teoría glucostática). La reserva de lípidos por otra parte proporciona también información para controlar la ingesta de nutrientes, para este fin encontramos lo receptores en el SNC encargados de regular niveles de ácidos grasos, glicerol o 3 hidroxibutirato (Teoría lipostática). Por ultimo existe una teoría relacionada con la oxidación de nutrientes en la cual una disminución implica sensación de hambre y un aumento con la sensación de saciedad (Teoría energostática). Además de las teorías expuestas encontramos moléculas a nivel gastrointestinal las cuales se encargan de producir señales ya sea a nivel local o a nivel del torrente sanguíneo, en donde trasportadas hasta el SNC al núcleo del tracto solitario, de ahí hasta el hipotálamo en donde se producirá la sensación de saciedad. Dentro de las moléculas y péptidos señalados unas de las más importantes son la colecistokinina (CCK), bombesina, glucagón, enterostatina, el polipéptico pancreático y la amilina entre otros. En 1973 se describió el efecto de saciedad de la CCK por Gibs y cols, los cuales encontraron su efecto al introducirlo por vía peritoneal, este generaba saciedad en ratas y posteriormente en humanos. Su liberación tiene lugar en las células enteroendocrinas a nivel de la mucosa del duodeno y yeyuno, como respuesta a la ingesta de grasas (ácidos grasos no saturados y de cadena larga principalmente) y proteínas. Los receptores que se encargaran de mediar este proceso como tal son de dos tipos; los CCK-1 están localizados en el tracto alimentario, como páncreas, vesícula biliar, píloro y en múltiples localizaciones del SNC y los receptores CCK-2, sobre estos actúa la colecistoquinina la cual crea un efecto anorexígeno. Estos receptores están localizados en el nervio vago y en el SNC. La bombesina es la encargada de disminuir la cantidad de alimento ingerido en cada comida. El glucagón se encarga de disminuir la ingesta en especial de proteína. La enterostatina se origina de la fragmentación de la lipasa a nivel intestinal y provoca disminución en la fragmentación en la duración de las comidas y el polipéptido pancréatico y la amilina inducen la reducción en la ingesta de alimentos. Mecanismo de la regulación de la ingesta a mediano plazo: Regulada por el péptido YY, una hormona compuesta por 36 aminoácidos, es sintetizado en las células L del intestino, se encuentran en dos tipos de origen endógeno, el subtipo 1-36 y el 3-36; el primero es más activo metabólicamente, mientras que el subtipo 3-36 tiene la capacidad de disminuir un 36% un volumen de alimento ingerido en forma inmediata y en un 33% el volumen total de 24 horas. Mecanismos de la regulación de la ingesta a largo plazo: Estas son llevadas por las señales periféricas de adiposidad y neurotransmisores centrales. Señales periféricas de adiposidad con efecto anorexígeno: Estas están integradas en dos señales de origen hormonal, la leptina y la insulina. La secreción de ambas está regulada en función del volumen graso orgánico total, pero las dos actúan inhibiendo procesos anabólicos y estimulando los catabólicos. Leptina: Constituye el resultado o la síntesis final del gen-ob, este es un péptido compuesto por 167a.a. la leptina del ratón es 84% similar a la del humano, produce una reducción de la adiposidad por medio de una inhibición del apetito, estimulando las reservas de energía logrando así la lipolisis del tejido adiposo. La síntesis de esta es llevada a cabo por los adipocitos, hipófisis, hipotálamo, músculo esquelético, placenta, mucosa gástrica y epitelio mamario. Su liberación se lleva a cabo con el ritmo circadiano, mediante pulsos con intervalos de 45 minutos, por lo cual aumenta a lo largo del día logrando su pico máximo a media moche, en cuanto a género, se encontró que los niveles plasmáticos son mayores en mujeres, al parecer por los andrógenos que hacen que estas concentraciones sean menores en los hombres. Los efectos anorexígenos se dan principalmente por dos vías; la primera es una periférica en la que juegan un papel importante los receptores específicos. Y la segunda acción, es a nivel central, debe atravesar la barrera hematoencefálica, en donde se une a receptores específicos en hipotálamo tales como núcleo arcuato, paraventricular y ventromedial. La carencia de leptina en sujetos sea por la vía que sea hace que aparezcan complicaciones precoces entre las que se encuentran obesidad, hiperfagia, diabetes e infertilidad. De modo paradójico, en sujetos con obesidad extrema se han encontrado niveles elevados de leptina, este caso en especial hace sospechar de resistencia a esta hormona, al igual que lo que pasa con la insulina. Las vías por las cuales se crea esta resistencia son múltiples pero los más estudiados son las alteraciones en cuanto a trasporte o por alteración en sistemas neuronales que respondan a señalización. Insulina: Al igual que la leptina, esta también es directamente proporcional al volumen graso corporal del sujeto. Esta también puede acceder a nivel del SNC mediante el mismo sistema de transporte que la leptina y la distribución de los receptores es la misma. A pesar de la similitud de las dos moléculas la diferencia radica en que la liberación de la insulina se hace en respuesta a una única comida. Se ha comprobado que la aplicación de insulina provoca un efecto anorexígeno y una pérdida de peso corporal. Señales periféricas y centrales de adiposidad con efecto orexígeno (anabólico) y anorexígeno (catabólico): Estas moléculas que se describirán a continuación mostraran su acción en la producción de un efecto anabólico respecto a la energía que se obtiene de la dieta; se han clasificado en centrales y periféricas. Señales orexígenas periféricas: Ghrelina: Aislada en 1999 de estómago de rata, es un ligando endógeno que al ser activado induce una potente liberación de hormona de crecimiento. Esta pertenece a la familia de los secretagogos de hormona de crecimiento, consta de 28 a.a y posee una estructura capaz de atravesar barrera hematoencefálica, lo cual le permite actuar sobre el hipotálamo, en cuanto a conducta alimentaria se refiere, su origen y producción está fuera del SNC. Ésta hormona es la única que se produce a nivel gastrointestinal con efecto orexígeno, además de esta cualidad ésta también es producida en menor proporción a nivel hipotalámico, en hipófisis, páncreas, riñón, intestino, linfocitos y corazón, así como también ha sido aislada en placenta y testículos. Los niveles más elevados se han encontrado en pacientes con caquexia y ayuno además que se ha encontrado disminuida en obesos y en pacientes sanos tras ingerir nutrientes. La regulación de la ingesta por esta molécula está determinada por varios mecanismos, uno de los cuales se encuentra en su nivel competitivo con la leptina y otro con su interacción con el nervio vago, desde donde puede inducir una activación neuronal en el núcleo del tracto solitario y dorsomotor lo cual causa motilidad, secreción gástrica, inducción del apetito y consumo de alimentos. La principal vía de actuación y ejercicio orexígeno, tiene que ver con su efecto sobre el núcleo arcuato, lugar en donde actúan otros neuropéptidos, y ejerciendo un estímulo para la síntesis de estos. Señales orexígenas centrales: Neuropéptido Y (NPY): Es sintetizado en el hipotálamo a nivel del núcleo arcuato, su acción es central en el núcleo paraventricular en donde estimula y potencia la ingesta de alimentos generando ganancia de peso, sus niveles se elevan ante la depleción de depósitos de grasa corporal, especialmente en ayuno y en diabetes no controlada. La síntesis de este péptido es inhibido por la leptina, lo más importante es que disminuye el efecto ejercido por el sistema nervioso simpático al tejido adiposo pardo. Todo lo anterior lleva a una disminución del gasto energético y un aumento y desarrollo del tejido adiposo blanco. En ratones la falta de este péptido ha mostrado el desarrollo de una obesidad moderada más que un fenotipo delgado. Proteína relacionada con agoutí (AGRP): Su origen es peptídico, su hallazgo fue fortuito, se sintetiza en el hipotálamo, es un agente inductor del apetito y por ende del aumento del peso corporal. Su mecanismo de acción es principalmente su efecto antagonizante respecto a los receptores MC3 y MC4 de la α-MSH. Hormona con centradora de melanina (MCH): Es un Neuropéptido de 19 a.a, se sintetiza en el hipotálamo lateral durante periodos de ayuno y en respuesta a déficit de niveles de leptina. Tiene un efecto inhibidor sobre el eje hipotálamo - hipófisis - tiroides controlando el grado de apetito y también puede reducir el gasto energético. Estudios en ratones ha logrado demostrar que la inactivación del gen que produce esta hormona va a generar cuadros de hipofagia y delgadez extrema en estos animales. Señales anorexígenas centrales: Hormona α-melanocito estimulante (α-MSH): Péptido derivado de la proteólisis de una prohormona denominada propiomelanocortina (POMC), su acción anorexígena está dado por la unión a los receptores MC4-R, en estudios realizados en ratones se ha demostrado que su inactividad genera cuadros de obesidad. En pacientes obesos estudiados se ha demostrado una mutación en su receptor MC4. Esta mutación genera un mal funcionamiento de esta hormona y su subsiguiente disbalance energético. De esta alteración genética derivan numerosas complicaciones entre las que se encuentran la obesidad temprana acompañada de hiperfagia, hiperinsulinemia e hiperglucémia. Hormona liberadora de corticotropina (CRH) y hormona liberadora de tirotropina: Su efecto es la inhibición del apetito, son sintetizadas por neuronas del núcleo paraventricular, la corticotropina aumenta el gasto energético a expensas de la activación del SNC simpático y ejerce un efecto regulador del eje hipotálamo pituitaria - tiroides. La hormona liberadora de tirotropina ayuda en la regulación de dicho eje, a la síntesis a nivel de hipotálamo y al aumento en la respuesta a la leptina. Elaborado por CAMILO ALBERTO CAMARGO PUERTO RESIDENTE SEGUNDO AÑO MEDICINA DE LA ACTIVIDAD FÍSICA Y EL DEPORTE FUCS FECHA 14 – Abril – 2015 Bogotá - Colombia