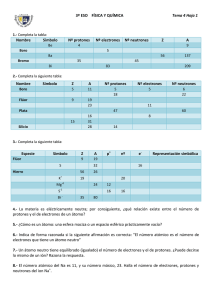
número atómico (Z)
Anuncio

1.2 LA MATERIA Y LOS CAMBIOS Por equipo definir que es átomo, molécula y de que están formados Equipo 1 2 3 4 5 6 7 8 Átomo Molécula ÁTOMO 1. 2. 3. 4. Un átomo es eléctricamente neutro. tiene el mismo número de protones que de electrones. Todos los protones y neutrones se encuentran en el centro del átomo. La carga del núcleo es positiva e igual a la cantidad de protones. El número atómico (Z) es igual a la cantidad de protones que posee el átomo. La cantidad de protones más la cantidad de neutrones es igual al número de masa (A) del átomo. La masa de los electrones se considera insignificante. En general A E Z 13 Ejercicios protones, electrones y neutrones número atómico (Z) = número de protones (información en tabla periódica) número de masa (A) = protones + neutrones (información en tabla periódica, masa atómica redondeada) átomo es eléctricamente neutro número de protones = número de electrones Ejercicios protones, electrones y neutrones Completa el nombre o símbolo químico que falta y escribe el número atómico (Z), el número de protones (p+) y la masa atómica para los siguientes átomos: Nombre Símbolo Sodio Aluminio Cobre Ag Au Xenón (Z) Masa atómica Número de Protones Características Sólido Líquido Gas Forma Tiene forma definida Adopta la forma del recipiente que lo contiene Adopta la forma del recipiente que lo contiene Volumen Tiene volumen definido Tiene volumen definido Llena todo el volumen del recipiente que lo contiene Ordenamiento de las partículas Movimiento Atracción entre partículas Cercanía de las partículas Definido Aleatorio Aleatorio Lento Moderado Muy rápido Fuerte Moderado No hay Muy cercanas Cercanas Muy distantes 16 1.2.2 Clasificación de la materia COMPUESTOS + ELEMENTOS MEZCLAS ELEMENTOS + ELEMENTOS (homogéneas o heterogéneas) COMPUESTOS + COMPUESTOS MATERIA ÁTOMOS MOLÉCULAS ELEMENTOS ÁTOMOS SUSTANCIAS PURAS MOLÉCULAS COMPUESTOS ÁTOMOS REDES 17 MATERIA SUSTANCIAS PURAS COMPUESTOS MEZCLAS (homogéneas o heterogéneas) ELEMENTOS 18 MATERIA SUSTANCIAS PURAS MEZCLAS (homogéneas o heterogéneas) COMPUESTOS + COMPUESTOS ELEMENTOS + ELEMENTOS COMPUESTOS + ELEMENTOS 19 PROPIEDADES GENERALES Son aquellas características que posee la materia sin importar su estado de agregación. • Volumen: la materia ocupa un lugar en el espacio. • Peso: fuerza con que la tierra atrae a los cuerpos. • Inercia: oposición a cambiar la posición de reposo o movimiento rectilíneo. • Impenetrabilidad: dos cuerpos no pueden ocupar el mismo espacio al mismo tiempo. • Porosidad: espacios entre las partículas. • Divisibilidad: posibilidad de fragmentación. • Elasticidad: deformación por fuerzas externas que al dejar de actuar la materia vuelve a la normalidad. 20 PROPIEDADES PARTICULARES Son específicas de una sustancia y sirve para identificarla. Propiedades físicas. Pueden ser observadas sin que la sustancia se transforme en otras, ejemplos: olor, color, sabor, punto de fusión, punto de ebullición, solubilidad, densidad, conductividad eléctrica, calor específico, etc. Propiedades químicas. Indican de que forma reacciona una sustancia, ejemplos: carácter ácido o básico, carácter reductor u oxidante, si es combustible o comburente, corrosivo, estabilidad, reactividad, etc. 21 CAMBIO FÍSICO Cambio en el que no se altera la naturaleza de la sustancia. Ejemplos: fusión, evaporación, sublimación, condensación, cristalización, licuefacción, etc. Muchas de estas propiedades se utilizan para la separación de mezclas. 22 CAMBIOS DE ESTADO LÍQUIDO GAS SÓLIDO SUBLIMACIÓN 23 CAMBIO QUÍMICO Cambio que al realizarse produce una nueva clase de materia con propiedades diferentes (reacción química). Ejemplos: Reacción del hidrógeno con oxígeno para producir agua y energía energía H2 + O2 2 H2O + energía Combustión del gas doméstico con el oxígeno para producir dióxido de carbono, agua y energía. energía 2CH4 + 4O2 2 CO2 + 4H2O energía Reacción de un ácido con una base para formar una sal y agua. HCl + NaOH NaCl + H2O 24