18 interpretacion caracteriticas apl m.martinez v
Anuncio

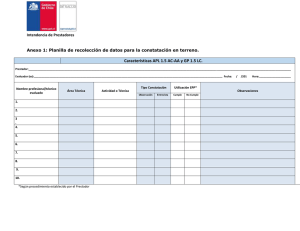
Interpretaciones de Características del Estándar de Acreditación para Prestadores Institucionales correspondientes a Laboratorio clínico TM Marisol Martínez Vilugrón Jefa Unidad de Fiscalización de Laboratorios Características que son objeto de observaciones e incumplimientos en la acreditación. 1.- Autorización Sanitaria APL 1.1 2.- Caso Hospitales con instalación antes del 08/02/2006. 3.- Caso Instituto de Salud Pública 4.- Caso derivación al extranjero. 2 APL 1.1 1.- Respecto a la Autorización Sanitaria : a) Copia autorizada ante Notario de la resolución de la Autoridad Sanitaria que originalmente autorizó la instalación y el funcionamiento de dicho prestador institucional; b) Copia autorizada ante Notario de todas las demás resoluciones de la Autoridad Sanitaria mediante las cuales ésta haya autorizado la ampliación, modificación o traslado del establecimiento de que se trate o de sus dependencias; y c) Copia autorizada ante Notario de las demás autorizaciones sanitarias relativas a dependencias, áreas o instalaciones que se ubiquen dentro de dicho establecimiento y en los que se desarrollen funciones asistenciales o actividades que, de conformidad con la reglamentación vigente, requieran de una autorización sanitaria específica, tales como las salas de toma de muestras, los laboratorios clínicos, los centro de diálisis, las instalaciones radiactivas o los equipos generadores de radiaciones ionizantes.. Numeral 1.1. Circular IP N° 8, de 19 de agosto de 2010 2.- Respecto de aquellos establecimientos que se encontraban en funcionamiento al día 8 de febrero de 2006, fecha de publicación de los D.S. N° 152/05 y N° 141/05, ambos del Ministerio de Salud, se aplican las siguientes normas: Hospitales dependientes de los Servicios de Salud: De conformidad a lo dispuesto en el N° 2 del citado D.S. N° 152/05, “los hospitales dependientes de los Servicios de Salud actualmente en funcionamiento, no requerirán de nueva autorización en conformidad con el presente decreto, sin perjuicio de lo cual, para los efectos de someterse al procedimiento de acreditación deberán demostrar previamente ante la Secretaría Regional Ministerial de Salud competente su cumplimiento de los requisitos que establece el Reglamento de Hospitales y Clínicas.”. 3.- En el caso de la Autorización Sanitaria del Instituto de Salud Pública: 4.- En el caso de muestras enviadas al extranjero: De acuerdo a las actuales exigencias del Sistema de Acreditación sólo deberá asegurarse que el tercero que le provee el servicio cuente con la autorización sanitaria que corresponda. Ahora bien, atendido que, en este caso las muestras son enviadas a Laboratorios Extranjeros, deberá entenderse que dicha prestación, se encuentra regulada en virtud de lo dispuesto en el D.S. N° 20, de 2011, MINSAL, que Aprueba el Reglamento de Laboratorios Clínicos, publicado en el Diario Oficial de 28 de Abril de 2012, en el Artículo N°5, cuyo texto exige, el listado de exámenes que realizará el Laboratorio Clínico según área especialidad y los que realizará a través de convenio. Tal exigencia es igualmente aplicable a los prestadores autorizados, en su momento, por el anterior Reglamento de Laboratorios Clínicos (D.S. N°433, de 1993, MINSAL) Por tanto, será suficiente que el prestador exhiba la Resolución de Autorización Sanitaría que lo autorizó para su instalación y funcionamiento de conformidad al Reglamento de Laboratorios Clínicos (D.S. N°433, de 1993, MINSAL), del Subdepartamento de Profesiones Médicas y Farmacia, de la SEREMI correspondiente. Características que son objeto de observaciones e incumplimientos en la acreditación. 1° elemento medible: Puntos de verificación. Gestión documental. 2° elemento medible: Pertinencia del indicador. GP 1.2 LAB/APL 1.2 3° elemento medible: Puntos de verificación. 4° elemento medible: Formularios de plazo de entrega de los exámenes. 6 APL 1.2 Si un prestador : a.- Prestador de atención cerrada, compra servicios a un laboratorio externo pero mantiene salas de tomas de muestras en propiedad y administración o No, le aplica: características APL 1.1, sobre compra de servicios a terceros; la característica APL 1.2 referida a los procesos de la etapa pre analítica y la característica AOC 1.3 AC, sobre notificación oportuna de situaciones de riesgo detectadas a través de exámenes diagnósticos. b.- Prestador de Atención Abierta, que compra servicios a un laboratorio y mantiene salas de tomas de muestras en su interior le son aplicables solamente las características sobre compra de prestaciones a terceros (APL 1.1) y AOC 1.2, sobre notificación oportuna de situaciones de riesgo detectadas a través de exámenes diagnósticos. GP 1.2 Numeral 3.4.1. de la Circular IP N°24, de 16 de mayo de 2013, que sustituyó el numeral 2.1.1. de la Circular IP N° 15, de 30 de septiembre de 2011 12.1.2. APL 1.2 c.- Por el contrario si las salas de tomas de muestras se mantienen en propiedad y administración del Prestador que desea acreditarse, en tales casos son aplicables a dicho prestador las características APL 1.1, sobre compra de servicios a terceros; la característica APL 1.2 referida a los procesos de la etapa pre analítica y AOC 1.2, sobre notificación oportuna de situaciones de riesgo detectadas a través de exámenes diagnósticos. GP 1.2 Numeral 3.4.2. de la Circular IP N°24, de 16 de mayo de 2013, que sustituyó el numeral 2.1.2. de la Circular IP N° 15, de 30 de septiembre de 2011 APL 1.2 GP 1.2 . 1° Elemento medible: Puntos de verificación: es importante considerar que cuando en el primer elemento medible se solicita documentación, ésta debe encontrarse replicada en todos los puntos verificadores correspondientes. Es el laboratorio el responsable de controlar que eso ocurra. Gestión documental: Los documentos deben ser de carácter institucional, vigentes. Además es necesario que el laboratorio mantenga el debido control de los documentos. Punto de verificación ¡OJO! Verificar que la información se encuentre en todos los puntos de verificación Puntos de verificación Elaboración de documentos “documento de carácter institucional”. Los documentos firmados por el director nacional o regional de una red de prestadores, pública o privada, que carecen de la firma o suscripción del director o gerente del prestador local en evaluación, no son aptos para los efectos de cumplir la exigencia relativa a que este último pruebe la existencia de un “documento de carácter institucional” propio. Sobre los requisitos formales que deben cumplir en los prestadores públicos los documentos para ser estimados como “documento de carácter institucional”, según las exigencias del Manual de Acreditación, se aclara: a.- En los organismos públicos el carácter institucional de un documento se adquiere a través de un acto administrativo que lo aprueba y oficializa como tal. Dicho acto administrativo estará, normalmente, constituido por una resolución, debidamente fechada y firmada por el director del establecimiento que aprobó tal documento. Numeral 2.1. de la Circular IP N° 23, de 26 de octubre de 2012 Elaboración de documentos Numeral 2.1. de la Circular IP N° 23, de 26 de octubre de 2012 Dicho acto administrativo puede también adoptar la forma de un oficio, ordinario o memorándum, debidamente fechados y firmados, todos los cuales pueden ser incluidos o adjuntados al mismo documento. Respecto de los prestadores institucionales públicos que utilizan sistemas informáticos para mantener sus documentos institucionales, se requiere de una resolución u otra clase de acto administrativo, dictado por el director del establecimiento, que ordene tal forma de mantención de los documentos institucionales, así como la forma en que tales documentos se ingresan a dicho sistema informático y cómo se resguarda su integridad, de modo que ellos no sean vulnerables a modificaciones por parte de personas no autorizadas. Gestión documental: Elaboración de documentos b.- En el caso de Prestadores de la red privada, no se cuenta con la figura legal de este acto administrativo (contemplado en la ley 19.880 de 2003 de Procedimientos administrativos que rigen los actos de los órganos de la administración del Estado), entonces al documento se le confiere el carácter de institucional con la debida firma del Director o Gerente a través del acto administrativo que el propio Prestador haya definido e implementado. Vigencia de la documentación: Es importante recordar, que tal cómo se señala en las Pautas de Cotejo de los diferentes Manuales de Acreditación, el período de vigencia de los documentos es de hasta 5 años de antigüedad desde la fecha del proceso de Acreditación o lo que determine cada Prestador. Numeral 2.2.9.2 de la Circular IP N° 17, de 30 de diciembre de 2011 1.- Diagnóstico de la situación actual de la documentación Llevar a cabo de manera eficiente los procesos y actividades. Cumplir con la normativa legal y reglamentaria, tanto de la Institución como externa. Obtener información para las evaluaciones de las actividades. Es recomendable que el sistema de gestión se encuentre centralizado aunque la elaboración de documentos pueda ser descentralizada. 2.- Atributos un de un Sistema de Gestión documental Los atributos de un sistema de gestión documental son: ingreso al sistema, registro, clasificación, conservación/almacenamiento, acceso, trazabilidad y disposición. 3. Diseño sistema de gestión de los documentos 1. 2. 3. 4. 5. 6. 7. 8. Las características de los documentos. La designación de responsabilidades. Los formatos utilizados (electrónico, papel o ambos) Calendario de conservación distintos tipos de documentos. Los responsables de supervisar la actualización de los documentos disponibles. Acceso y medidas de seguridad para documentos. El mecanismo de evaluación(indicador y período de evaluación). Clasificación, Tipo Documento, Contenido , Responsable , Disposición , Fecha Elab., Fecha Rev., Codificación y Carácter documento. 4. Identificación de los requisitos documentales Para un Prestador Institucional que desee acreditarse es fundamental considerar entre estos requisitos las exigencias en relación a la documentación del Estándar General aplicable. a.- Estandarizar adecuadamente los procedimientos críticos. b.- Cumplimiento con la normativa legal vigente. Es importante identificar los documentos y contenidos que serán exigibles según el Estándar de Acreditación aplicable e interiorizarse de los Elementos Medibles que menciona la Pauta de Cotejo correspondiente en relación a cada documento, ya que en algunas características se solicitan contenidos específicos en relación directa a los procedimientos o complementando la información de su desarrollo. En general cuando en el contexto de un proceso de Acreditación se habla de documentos “institucionales” la intención es evidenciar el adecuado conocimiento por parte de la Dirección o Gerencia del Prestador para así asegurar la difusión de dicha información al interior de la Organización por los conductos regulares establecidos, y que esta sea avalada explícitamente por la jefatura. 5. Elaboración de los documentos La elaboración de los documentos requeridos para un proceso de Acreditación no es una tarea que pueda realizarse a puerta cerrada a cargo del equipo de Calidad. Es una actividad en la cual debe involucrarse profesionales de todas los Servicios implicados, ya que la difusión y cumplimiento de lo establecido en los documentos depende en importante medida en que estos sean elaborados en base al consenso y considerando el contexto local. Se facilita la tarea de elaboración y a su vez su gestión posterior si desde la Unidad de Calidad se distribuye el formato estándar que utilizará toda la Institución, el cual incluye los contenidos específicos para cada tipo de documento. 6.-Control de documentos Numeral 2.1. de la Circular IP N° 23, de 26 de octubre de 2012 Permite asegurar el adecuado manejo y disponibilidad de los documentos requeridos por el Sistema de Gestión de la Calidad (SGC), a través de una metodología para la generación, actualización, revisión, aprobación, distribución y control de los documentos, tanto internos y/o externos. Cada institución los debe elaborar de acuerdo a su realidad, infraestructura y recursos humanos. 2° Elemento medible: Indicador APL 1.2 El indicador debe ser pertinente y bien formulado GP 1.2 PROCESOS MONITOREADOS EN EL LABORATORIO 2. Analítica GP 1.3- AOC 1.3 APL 1.3 1. Pre-analítica GP 1.2- GP1.6 APL 1.2 CICLO EXAMEN 3. Post-analítica GP 1.3-AOC 1.3 APL 1.3 Características Atención Abierta y Cerrada APL 1.2 : Procesos relacionados con la etapa pre analítica. APL 1.3: Procedimientos escritos y evaluaciones de los procesos analítico y post analítico. Características para Laboratorios clínicos GP 1.2: Procesos relacionados con la etapa pre analítica. GP 1.3: Procedimientos escritos y evaluaciones de los procesos analítico y post analítico. GP 1.6: Precauciones estándar y uso de antisépticos. AOC 1.3: Sistema de notificación oportuna de situaciones de riesgo detectadas a través de exámenes diagnósticos. Indicador y fórmula matemática El indicador debe ser pertinente y bien formulado Ejemplo Nombre del Indicador Construcción de fórmula del indicador Eventos que queremos medir, en el numerador. Definir la población expuesta, en el denominador. Constante para expresar porcentajes o tasas. Los indicadores de calidad son instrumentos para evaluar la calidad y pueden aplicarse a tres elementos básicos del sistema: la estructura, el proceso y los resultados. Fórmula matemática Umbral de cumplimiento ¿Cuáles deben ser los criterios para la fijación de los umbrales? Punto de corte, con miras a que una próxima medición se supere el umbral. Tener implícito un objetivo o meta a cumplir para posteriormente contrastar el desempeño observado con el que se ha fijado. No son exigibles umbrales específicos. No es exigible que las mediciones superen el umbral. Valor de referencia para gatillar análisis y/o intervención ¿Cuáles deben ser los criterios para la fijación de los umbrales? Los umbrales referidos a prácticas para la prevención de eventos graves que poseen evidencia concluyente de efectividad debieran ser 100%. Los umbrales referidos a la prevención de eventos calificados como “Eventos adversos” debieran aproximarse al 100%. Periodicidad: Considerar relación con tamaño muestral, precisión de las mediciones. Se pueden agregar mediciones mensuales, trimestrales, semestrales, anuales. ¿Qué tipo de umbrales existen? Valor de referencia para gatillar análisis y/o intervención. Considerar estrategias de cumplimiento progresivo: Óptimo: a lo que debe aspirar la institución en condiciones de excelencia técnica. Aceptable: reflejan un grado de cumplimiento o seguridad razonable, que debe mejorarse. Crítico: a lo que no se debe llegar. Umbral de cumplimiento y periodicidad Evaluación periódica/Fuente de datos Confiables Veracidad Validez Primaria Información ORIGINAL Y DIRECTA Registros originales Entrevistas, encuestas. Secundaria Fuente de datos Recopilaciones a partir de la fuente primaria. Informes, estadísticas, datos. Fuentes de datos 4° elemento medible: Formularios de plazo de entrega de los exámenes. APL 1.2 Se debe entregar en forma escrita cuándo el paciente debe retirar sus exámenes GP 1.2 Características obligatorias que son objeto de observaciones e incumplimientos en la acreditación. GP 1.3 LAB/APL 1.3 1.- Tiempo de respuesta de los exámenes urgentes: Punto verificador Microbiología. 2.- Control de calidad interno técnicas manuales y periodicidad. 39 Segundo elemento medible: Tiempo de respuesta de los exámenes urgentes: a.- Es importante tener claro que las áreas técnicas no son lo mismo que los puntos verificadores. b.- Es necesario conocer cómo se clasifican los exámenes dentro de los puntos verificadores y áreas técnicas. (Normas técnicas básicas). Tiempo de respuesta Cuarto elemento medible: Control de calidad interno para todas las prestaciones que realiza el laboratorio. a.- Se evidencia ausencia de control de calidad interno sobre todo para técnicas manuales o semi automatizadas. b.- No se especifica la periodicidad de evaluación del control de calidad. c.- No se detalla cuando existen equipos y técnicas que se evalúan con una periodicidad dependiente del equipo, área técnica y servicio que prestan (urgencia, rutina, ambulatorio). Características obligatorias que son objeto de observaciones e incumplimientos en la acreditación. 1.-No se ha realizado una de las evaluaciones correspondiente al subprograma. GP 1.4 LAB/APL 1.4 2.- Registro de participación. 3.- Prestador no presenta un subprograma por cada Programa del PEEC. 45 Sobre si, para cumplir con el requisito de control de calidad externo, se debe estar necesariamente adscrito al Programa de Evaluación Externa de la Calidad del Instituto de Salud Pública y, si respecto de las determinaciones no consideradas en dicho programa es obligatorio para las instituciones comprar dichos servicios a empresas extranjeras, se aclara: El programa de control externo de la calidad a que hace referencia esta característica del sistema de acreditación no se refiere exclusivamente al que realiza el Instituto de Salud Pública, sino a cualquier programa de control de calidad equivalente a éste ejecutado por empresas que pueden ser nacionales o extranjeras. Numeral 3.4.3. de la Circular IP N°24, de 16 de mayo de 2013, que sustituyó el numeral 2.1.3. de la Circular IP N° 15, de 30 de septiembre de 2011 72 Salud Pública de Chile En ese sentido, para dar por establecido razonablemente que el laboratorio participa en un programa de control de calidad externo se debe probar que la globalidad de los procesos que en él se ejecutan se encuentran sometidos a alguno de dichos programas, lo que significa que ellos se aplican, al menos, a un subprograma de cada área técnica de la que dispone el laboratorio. A modo de ejemplo, si el laboratorio realiza exámenes de química clínica, debiera estar adscrito, al menos, al subprograma de química sanguínea, al de química de orina cuantitativa, o a cualquier otro subprograma de esa área. Para estos efectos, y en tanto no se demuestre mejor evidencia en contrario o se dicten normativas al efecto, las Entidades Acreditadoras entenderán que los subprogramas y sus respectivas áreas técnicas son las que determine el Programa Anual de Control de Calidad Externa establecido por el Instituto de Salud Pública de Chile. Numeral 3.4.3. de la Circular IP N°24, de 16 de mayo de 2013, que sustituyó el numeral 2.1.3. de la Circular IP N° 15, de 30 de septiembre de 2011 72 Salud Pública de Chile Primer elemento medible: Participación en un Programa Externo de la Calidad. a.- Es importante recordar que cuando se trata del PEEC ISP, este no entrega el certificado de participación si el prestador no ha completado todas las evaluaciones anuales que comprende el programa. b.- El PEEC ISP permite dentro de un rango de tiempo poder justificar la no participación en una evaluación para lo cual entrega un Certificado de Justificación correspondiente. Numeral 3.4.3. de la Circular IP N°24, de 16 de mayo de 2013, que sustituyó el numeral 2.1.3. de la Circular IP N° 15, de 30 de septiembre de 2011 72 Salud Pública de Chile APL 1,4 GP 1.4 Segundo elemento medible: Análisis y acciones de mejora en caso de incumplimientos. a.- Es importante realizar análisis y acciones de mejora para cada incumplimiento dentro del PEEC. b.- Se debe disponer un subprograma para cada programa. Características obligatorias que son objeto de observaciones e incumplimientos en la acreditación. GP 1.5/APL 1.5 1.- Cumplimiento de lo comprometido en el Manual de Bioseguridad. (EPP) 50 APL 1.5 GP 1.5 Primer elemento medible: Elaborar un procedimiento que refleje la realidad del laboratorio. Segundo elemento medible: Que se de cumplimiento al uso de EPP, según lo indicado por el propio prestador en el documento del primer elemento medible. APL 1.5 GP 1.5 La constatación debe realizarse en base a la observación directa del personal clínico que se encuentre en sus labores al momento de la visita. Si no se pudiese constatar al personal clínico, porque no se encuentran realizando ninguna técnica, se realizarán entrevistas que incluyan la simulación de procedimientos o técnicas específicas con el fin de valorar la utilización de los EPP acorde a lo establecido por el propio prestador. “Orientaciones Técnicas para la Constatación en terreno del cumplimiento del uso de elementos de protección personal en la manipulación de muestras clínicas, en el Laboratorio Clínico”.- APL 1.5 GP 1.5 El tamaño muestral es el equivalente a 30 personas. Por tanto si al momento de la visita en un Laboratorio se encuentran 30 o menos personas ejerciendo sus labores, se deberá constatar a todas ellas, independiente si en dicho Laboratorio clínico trabajen más de 30 personas. En consecuencia, es fundamental al iniciar la evaluación al Laboratorio requerir el número de profesionales y técnicos que se encuentran en ese momento, para así determinar cuántas personas deberán ser constatadas. “Orientaciones Técnicas para la Constatación en terreno del cumplimiento del uso de elementos de protección personal en la manipulación de muestras clínicas, en el Laboratorio Clínico”.- APL 1.5 GP 1.5 Umbral de cumplimiento Del total de observaciones y/o entrevistas al menos el 80% debe cumplir con la utilización de EPP en la manipulación de muestras clínicas establecido en el procedimiento local del prestador. Si en el Laboratorio se desempeñan más de 30 personas (entre profesionales y técnicos) al momento de la visita, tal como se mencionó previamente se evaluarán 30, de las cuales 24 deben cumplir con lo descrito en el procedimiento del propio prestador en cuanto a la utilización de EPP. En el caso de contar con menos de 30 profesionales y técnicos para observación u entrevista al momento de la visita, se evaluará a todo el personal presente, considerando el mismo umbral de cumplimiento de 80%, por lo que se deberá observar y/o entrevistar el número de personas indicadas en la tabla siguiente. “Orientaciones Técnicas para la Constatación en terreno del cumplimiento del uso de elementos de protección personal en la manipulación de muestras clínicas, en el Laboratorio Clínico”.- Características obligatorias que son objeto de observaciones e incumplimientos en la acreditación. 1.-Responsabilidad de notificación (Prestadores Externos). AOC 1.3 AC/LAB 2.-Elaboración de documentos. 3.- No hay respaldo realizadas. 55 de las notificaciones AOC 1.2 AA AOC 1.3 AC-LC Sobre la aplicabilidad de esta característica en una evaluación, cuando en el prestador institucional se han externalizado los servicios relativos a exámenes diagnósticos, se aclara: Las Entidades Acreditadoras no podrán declarar inaplicable esta característica en la evaluación de un prestador, cuando en ese prestador se hayan externalizado los servicios relativos a exámenes diagnósticos. La responsabilidad de notificar las situaciones de riesgo detectadas a través de exámenes diagnósticos en las áreas de anatomía patológica, laboratorio e imagenología cuya ejecución fue ordenada por sus profesionales, es del prestador institucional que está siendo acreditado, independientemente de dónde se hayan procesado los exámenes. Numeral 2.3.1. de la Circular IP N° 8, de 19 de agosto de 2010 AOC 1.2 AA AOC 1.3 AC-LC ¿Qué se entiende por valores o resultados críticos en el Laboratorio Clínico? Son aquellos valores que indican que el paciente tiene un elevado riesgo de morbimortalidad y consecuencias adversas, de no instaurarse un tratamiento oportuno en el tiempo. Este resultado puede provenir de una prueba solicitada de manera urgente o de rutina. AOC 1.3 Sobre si esta característica es aplicable a las Unidades de Centros de Sangre, se aclara: Si el prestador ha definido que la notificación de resultados de exámenes de laboratorio, que se realizan en el Centro de Sangre, se efectúen en él, la constatación se realizará en dicho centro y los resultados de tales constataciones deben consignarse, junto con los propios del Laboratorio Clínico, en la columna APL de la Pauta de Cotejo. Numeral 3.3.2. de la Circular IP N° 23, de 26 de octubre de 2012 AOC 1.3 Primer elemento medible: Es recomendable que el documento que contenga el procedimiento de notificación incluya: El Listado de resultados críticos que el Prestador Institucional de Salud defina, acorde a su organización local y cartera de Servicios. El listado debe ser idealmente el producto de un trabajo colaborativo entre las especialidades involucradas. Estratificación de la urgencia de notificación y el tiempo de notificación asociado a cada resultado crítico (oportunidad de respuesta). Las definiciones de las características del procedimiento en caso de pacientes hospitalizados o ambulatorios. Las especificaciones en relación a qué sucederá en los días inhábiles o en jornadas particulares para asegurar el flujo continuo de información. La delimitación clara de las responsabilidades en el procedimiento de notificación: persona que notifica y a cuál miembro del equipo responsable del cuidado del paciente se le notificará, cómo proceder en caso de no contactar a la persona a quien debe notificarse, médico o profesional responsable del seguimiento de la notificación ¿será el médico tratante? ¿el médico que solicitó el examen?, persona responsable de la notificación al paciente (esto es particularmente importante en aquellas notificaciones que deban realizarse en un intervalo de días en la atención ambulatoria), responsable de la actualización de los datos de contacto de los equipos de salud y de los pacientes. AOC 1.3 Modo de comunicación: definir claramente que los resultados que involucren riesgo inminente al paciente serán comunicados personalmente o vía telefónica, considerando que el medio empleado permita a quien comunica verificar de manera efectiva que la notificación fue exitosa. No se recomienda la notificación vía correo electrónico. Definición de los registros y sus contenidos en cada una de las etapas del procedimiento Definición de la metodología e indicadores que se utilizarán para evaluar el cumplimiento del procedimiento y enfocar las mejoras necesarias. Los indicadores incorporados en los procedimientos de Notificación pueden evaluar la implementación de dicho procedimiento o directamente la ejecución de éste. AOC 1.3 Segundo elemento medible: Se pueden implementar dos tipos de indicador: a.- Indicadores de implementación/aplicación del procedimiento. b.- Indicadores de cumplimiento de tiempo de notificación. AOC 1.3 Cuarto elemento medible: Qué registrar en la notificación de un resultado crítico La comunicación realizada, debe quedar registrada en un sistema documental, que permita mantener la evaluación periódica de la ejecución de este sistema con fines de mejora. Este registro escrito, es adaptable a los recursos de cada Prestador Institucional de Salud (informático, manual) y debe contener información como: Datos de identificación del paciente Prueba diagnóstica/procedimiento diagnóstico realizado. Determinación realizada (Laboratorio Clínico) Resultado Fecha y hora de detección Fecha y hora de Notificación Identificación de persona que comunica resultado Identificación de persona que recibe la comunicación Medio por el cual se realiza comunicación Confirmación a través de Read-back. Motivo por el cual no se puede efectuar comunicación. Gracias Total de Laboratorios clínicos REGION FFAA Arica y Parinacota Tarapacá Antofagasta Atacama Coquimbo Valparaíso Metropolitana O'Higgins Maule Biobío Araucanía Los Ríos Los Lagos Aysén Magallanes Total general 1 1 3 2 11 2 2 2 24 PRIVADOS PÚBLICOS Total general 11 4 16 13 5 19 32 13 48 17 10 27 22 15 37 76 30 108 175 65 251 30 27 57 31 27 58 55 47 104 18 43 61 19 11 30 25 32 59 2 6 8 5 6 13 531 341 896