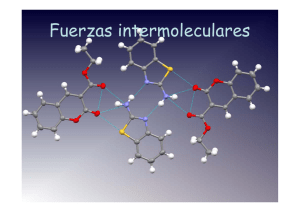
Fuerzas intermoleculares
Anuncio

Polaridad del enlace
ESTRUCTURA DE LA
MATERIA
FUERZAS
INTERMOLECULARES
•
•
•
Introducción
Introducción
Semestre 2009-1
•
Pareciera claro, que cuando dos átomos de un
mismo elemento comparten un par de
electrones, los comparten igualmente
Sin embargo, cuando los átomos son de
diferentes elementos, esto no tiene por que
ocurrir
Es decir hay unos átomos que atraen más a los
electrones que otros
En particular es claro, que los metales atraen
menos a los electrones que los no-metales
Rafael Moreno Esparza
26/11/08
FUERZAS INTERMOLECULARES
0
26/11/08
Polaridad del enlace
Para mostrar esto, vale la pena presentar dos
casos extremos:
– En el Cl2 tenemos dos átomos iguales y
entonces el par electrónico está
compartido en ambos átomos por igual
– Por otro lado en el NaCl el electrón 3s del
Na se incorpora en la estructura electrónica
del átomo de Cl quedando el sodio
despojado de su electrón formando el
catión Na+ y por su parte el cloro genera al
anión Cl-, dando a lugar a una malla iónica
• La mayoría de las sustancias tienen un
carácter del enlace que forman que está
entre estos dos extremos
FUERZAS INTERMOLECULARES
1
Polaridad del enlace
•
26/11/08
FUERZAS INTERMOLECULARES
•
Un concepto muy útil para describir como
comparten sus electrones un par de átomos es
el de polaridad del enlace
• Podemos definir los enlaces así:
– Un enlace covalente no-polar es aquel en el
cual los electrones están compartidos
igualmente por los dos átomos
– Un enlace covalente polar es aquel donde
uno de los átomos tiene mayor atracción
por los electrones que el otro
– Si esta atracción relativa es suficientemente
grande, el enlace es un enlace iónico
2
26/11/08
FUERZAS INTERMOLECULARES
3
1
Electronegatividad
•
•
•
Electronegatividad
La electronegatividad se define como la
capacidad que tiene un elemento en una
molécula específica para atraer electrones
hacia sí
Entre mayor sea esta capacidad de atraer
electrones mayor será el valor de la
electronegatividad
Esta cantidad se usa para determinar si un
enlace es covalente no-polar, covalente polar
o iónico
26/11/08
FUERZAS INTERMOLECULARES
•
La electronegatividad es una cantidad que está
en función o que depende de:
–
La energía de ionización del átomo
Es decir, que tan fuertemente retiene un
átomo a sus propios electrones
–
La afinidad electrónica del átomo
Es decir, que tan fuertemente atrae un
átomo a otros electrones
Nótese que estas dos últimas propiedades son
de los átomos aislados
4
26/11/08
Electronegatividad
FUERZAS INTERMOLECULARES
5
Electronegatividad
•
Así por ejemplo un átomo que tiene:
– Una afinidad electrónica grande
– Un potencial de ionización grande
• Será capaz de:
– Atraer electrones de otros átomos
– Resistirá que sus propios electrones sean
atraídos por el otro elemento
• Un átomo como este, será muy
electronegativo
• Un átomo con propiedades opuestas será
muy poco electronegativo
•
•
Según Pauling (1932), es la medida de la
tendencia que tiene un átomo en una molécula
de atraer a los electrones hacia sí
Y la estima a partir de las energías de enlace o
energías de disociación de diversas sustancias,
empleando esta expresión:
D ( A ! B) =
•
1
D ( A ! A ) + D (B ! B) + ∆ AB
2
Donde ΔAB es la diferencia de
electronegatividad entre los dos átomos
χA −χB = 0.208 ∆ AB
26/11/08
FUERZAS INTERMOLECULARES
6
26/11/08
FUERZAS INTERMOLECULARES
7
2
Electronegatividad
•
Electronegatividad
La electronegatividad se designa con la letra
griega χ
•
– El Flúor es el elemento más electronegativo:
electronegatividad = 4.0
– El Cesio por su parte es el menos
electronegativo
electronegatividad = 0.6
Nótese que estos dos elementos están en las
esquinas y diagonales en la tabla periódica
26/11/08
FUERZAS INTERMOLECULARES
8
26/11/08
Electronegatividad
•
•
1 v
I + A1v
2 1
(
)
χP =
•
•
•
•
La electronegatividad de Mulliken se puede
ajustar a la escala de Pauling así:
26/11/08
FUERZAS INTERMOLECULARES
9
Electronegatividad
Usando argumentos teóricos, Mulliken muestra
que la tendencia de un átomo en una molécula a
competir por los electrones de otro átomo al que
esté unido, debe ser proporcional al promedio de
la energía de ionización y la afinidad electrónica
de dicho átomo en su estado de valencia
χM =
Principio de igualación de la electronegatividad
– Toda especie química que tiende a asociarse
con otra, lo hace de manera que después de
hacerlo, ambas promedian su
electronegatividad
El concepto de electronegatividad de AlredRochow se basa en la fuerza electrostática de
atracción que existe entre un electrón en un
átomo y su propio núcleo.
e 2Zeff
La atracción entre el electrón
f =
y un núcleo está gobernada
r2
por la ley de Coulomb:
Donde e es la carga del electrón, Z eff es la carga
nuclear efectiva y r es el radio del átomo
Al graficar las fuerzas contra la χP podemos
ajustarlas a los valores de Pauling
χM
χP = 0.359
2.8
FUERZAS INTERMOLECULARES
10
26/11/08
Zeff
r2
+ 0.744
FUERZAS INTERMOLECULARES
11
3
•
•
•
S
•
•
Di
Donde D se refiere a la densidad electrónica del
átomo:
3 Ze
D=
•
Electronegatividad
Otro concepto más de electronegatividad es el
formulado por Sanderson
Este concepto considera la electronegatividad
como una función de la densidad electrónica
del átomo
D
Y se define así: χ =
⋅
4π r
3
y Di es la densidad electrónica ideal y se
determina extrapolando la densidad de los
gases ideales anterior y posterior al átomo en
cuestión
26/11/08
FUERZAS INTERMOLECULARES
dE
χM = −
dN
26/11/08
•
FUERZAS INTERMOLECULARES
10
8
6
4
2
-2
-1
0
1
2
3
Estado de oxidación
oxidación
FUERZAS INTERMOLECULARES
4
13
Tendencias generales de la χ
La electronegatividad crece de izquierda a
derecha a lo largo de un periodo
Para los elementos representativos (bloques s y
p) crece al subir en una familia
26/11/08
12
0
N =0
12
Tendencias generales de la χ
•
Finalmente, el concepto más moderno lo
sugieren Jaffe y colaboradores
Que puntualizan que la electronegatividad
de Mulliken es igual a la pendiente que pasa a
través del origen,
Ne
de la curva de
O
energía contra
F
carga para
Cl
cualquier
átomo, es decir:
Energía total MJ mol-1
Electronegatividad
•
•
14
El grupo de los elementos de transición tiene un
comportamiento un poco más complicado que el
de los representativos
26/11/08
FUERZAS INTERMOLECULARES
15
4
Electronegatividad
Electronegatividad y polarización
En los elementos representativos
– Al avanzar en un período aumenta y al
bajar en una familia disminuye
• En los elementos de transición
– Al bajar en una familia aumenta
• En iones
– Al cambiar el estado de oxidación de un
átomo cambia su electronegatividad
– A mayor estado de oxidación mayor su
atracción por los electrones y por ello
mayor será su electronegatividad
• En grupos de átomos
– Al combinarse dos átomos, la
electronegatividad resultante es un
promedio de la χde los átomos originales
•
26/11/08
FUERZAS INTERMOLECULARES
•
16
Electronegatividad y polarización
•
•
•
•
26/11/08
Compuesto
F2
Δχ = (χΑ−χΒ)
4.0- 4.0=0
Tipo
Covalente nopolar
26/11/08
HF
LiF
4.0-2.1=1.9 4.0-1.0=3.0
Covalente
polar
Iónico
FUERZAS INTERMOLECULARES
17
Electronegatividad y polarización
En el F2 los electrones están compartidos
igualmente entre los dos átomos
El enlace es covalente no-polar
En el HF el átomo de F tiene mayor
electronegatividad que el átomo de H
Los electrones no se comparten igualmente,
el átomo de F atrae más densidad electrónica
que el átomo de H
El enlace es covalente polar.
En el LiF, la electronegatividad del átomo de
F es suficientemente grande como para
despojar completamente de su electrón al Li y
el resultado es
Un enlace iónico
FUERZAS INTERMOLECULARES
Podemos usar la diferencia en la
electronegatividad Δχ entre dos átomos para
conocer la polaridad de su enlace:
•
El enlace en H-F puede representarse así:
•
Los símbolos δ+ y δ- indican las cargas
parciales positiva y negativa
respectivamente.
•
La flecha indica hacia donde jalan los
electrones
18
26/11/08
FUERZAS INTERMOLECULARES
19
5
Redistribución de carga
Electronegatividad y polarización
•
•
•
•
La regla general para predecir el tipo de enlace se
basa en las diferencias de electronegatividades de
los átomos que constituyen el enlace:
Si las electronegatividades son iguales, la
diferencia de electronegatividad es 0, y el enlace
es covalente no-polar
Si la diferencia de electronegatividades es mayor
que 0 pero menor que 2.0, el enlace es covalente
polar
Si la diferencia entre las electronegatividades de
los dos átomos es de 2.0, o mayor, el enlace es
iónico
26/11/08
FUERZAS INTERMOLECULARES
20
•
•
•
•
26/11/08
Momento dipolo
•
•
•
Es un vector y se define como:
•
El momento dipolo se determina
experimentalmente midiendo el cambio respecto a
la temperatura en la capacitancia de dos placas
cargadas entre las cuales se pone una sustancia
cualquiera.
•
•
•
µ = q ! re
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
21
Momento dipolo
Es la interacción resultante entre dos cargas
puntuales +q y -q, separadas a una distancia re
Se representa así:
26/11/08
Parece entonces evidente que cuando dos
átomos se encuentran juntos, la carga
electrónica se redistribuye
Dependiendo de la electronegatividad de cada
átomo, ello da como resultado la formación de
un dipolo
Entre mayor sea la diferencia de sus
electronegatividades, mayor será el dipolo que
se genere
Así por ejemplo en el caso del HCl, el átomo de
Cl al ser más electronegativo, controla
parcialmente al electrón del H
22
•
•
Así en el caso del HCl, el valor obtenido
experimentalmente, es:
3.45x10-30 C m
Como es un número muy pequeño, conviene crear
una unidad apropiada.
La unidad de momento dipolo se llama Debye (D) y
vale:
3.33x10-30C m
De manera que en estas unidades el momento
dipolo del HCl es de:
1.035 D
El momento dipolo de dos cargas unitarias
contrarias a una distancia de 100 pm vale:
4.89 D
26/11/08
FUERZAS INTERMOLECULARES
23
6
Cálculo del momento dipolo
•
Porcentaje de carácter iónico
•
Para calcular aproximadamente el valor del
dipolo de una molécula se resuelve la siguiente
ecuación:
Para calcular que tan polarizada está la carga
en esta molécula, dividimos el momento dipolo
obtenido entre la distancia de enlace:
3.45×10 -30 C m
µAB ≈ χA − χB = ∆ χ
•
•
−12
De manera que para el HCl se tiene que:
µHCl ≈ χCl − χH = (3.0 − 2.1) D = 0.9D
•
A las moléculas con momento dipolo = 0 se les
conoce como moléculas no polares,
A las que tienen momento dipolo ≠ 0 se conocen
como moléculas polares
El caso extremo de una molécula polar es el CsF
(Δχ=3.2)
•
•
26/11/08
FUERZAS INTERMOLECULARES
24
1.602×10−19
26/11/08
r(pm)
δcalc (D)
δobs (D)
% CI=(δ obs / δ cal)
HF
92
4.41
1.90
43
HCl
127
6.06
1.03
17
HBr
143
6.81
0.79
11
HI
162
7.74
0.41
6
FUERZAS INTERMOLECULARES
= 0.168
FUERZAS INTERMOLECULARES
25
Porcentaje de carácter iónico y χ
Esto mismo puede hacerse para todos los ácidos
de los halogenuros
26/11/08
m
En el caso del HCl nos encontramos que esto
representa aproximadamente un sexto de la
carga del electrón (1.602x10-19C) o lo que es lo
mismo 17% del total de la carga total en cada
átomo:
−20
2.7 ×10
Porcentaje de carácter iónico
•
127.5×10
= 2.7 ×10−20C
•
Se han sugerido varias ecuaciones empíricas
para determinar el carácter iónico de un enlace
en función de la electronegatividad de sus
constituyentes, una de ellas (Hannay & Smyth):
%CI = 16 (∆χ ) + 3.5 (∆χ )
2
•
•
26
Para HBr,
χBr=2.74, y χ H=2.20
de manera que:
26/11/08
% CI = 16 (.54 ) + 3.5 (.54 ) = 9.7
FUERZAS INTERMOLECULARES
2
27
7
Porcentaje de carácter iónico y χ
•
Polaridad de las moléculas
Pauling mismo, deriva una relación entre el
carácter iónico y la electronegatividad
• Las moléculas polares se alinean cuando:
– aplicamos un campo eléctrico
– están cerca unas de otras
– al estar en presencia de iones
Campo eléctrico
− 1 (χ −χ )
B
4 A
%CI AB =
1
−e
⋅100
26/11/08
FUERZAS INTERMOLECULARES
28
Polaridad de las moléculas
H-F
FUERZAS INTERMOLECULARES
Iones
• Lo cual les concede propiedades muy
importantes.
26/11/08
FUERZAS INTERMOLECULARES
29
Polaridad de las moléculas
• Si hay diferencia en la electronegatividad (χ) de
los átomos de una molécula, tendremos un
sistema donde uno de los átomos jala más a los
electrones que el otro
• Ello conduce a que la carga de la molécula se
polarice
• Cuando la carga esta polarizada, se formará un
dipolo
• Cualquier molécula diatómica con un enlace polar
es una molécula polar, es decir forma un dipolo
26/11/08
Cercanía
Cercanía
• Cada vez que hayan dos átomos con diferente
electronegatividad en la misma molécula se
formará un dipolo
• Además, los átomos en la molécula pueden
orientarse de tal manera que uno de los lados de
la molécula tenga una carga neta negativa y el
otro una carga neta positiva
• Por ello es evidente que la distribución de carga
de una molécula se determina por
– La polaridad de sus enlaces
– La forma de la molécula
30
26/11/08
FUERZAS INTERMOLECULARES
31
8
Polaridad de las moléculas
Polaridad de las moléculas
• Una molécula polar tiene:
• Una molécula no-polar:
– Un centro de la carga negativa total en una zona
– No tiene cargas en lados opuestos de la
molécula
de la molécula
– Un centro de la carga positiva total en otra zona
– O, tiene cargas iguales en lados opuestos de la
molécula
de la molécula
– Al tener la misma carga en lados opuestos, no
se presenta el dipolo
• La molécula no tiene polos, es decir no tiene
dipolo
– Pero no coinciden uno con el otro
– Ni con el centro de masa de la molécula
• Es decir, tiene dos polos
26/11/08
FUERZAS INTERMOLECULARES
32
Polaridad de las moléculas
33
• Para determinar el dipolo total en una molécula
se debe considerar lo siguiente
– La forma de la molécula
– La dirección del dipolo para cada par de
átomos
– La suma vectorial de cada contribución
• Las moléculas con µ = 0 se conocen como
moléculas no polares
• A las que tienen µ ≠ 0, como moléculas polares
• La polaridad de las moléculas poliatómicas
– Cada enlace polar en una molécula
poliatómica tendrá asociado un dipolo
– El dipolo total de la molécula será la suma de
los dipolos individuales
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
Polaridad de las moléculas
• El momento dipolo de una molécula se definirá
entonces por:
– La diferencia de electronegatividad entre dos
de sus átomos, que es lo que define la carga
en los extremos del dipolo
– La disposición de los dipolos formados
26/11/08
26/11/08
34
26/11/08
FUERZAS INTERMOLECULARES
35
9
Polaridad de las moléculas
Polaridad de las moléculas
• El monóxido de carbono (CO) tiene dipolo y se
orientará en un campo eléctrico
• Por otro lado, la molécula de Dióxido de carbono
(CO2) no tiene dipolo, es decir no se orienta en
un campo eléctrico
– A pesar de que en el dióxido de carbono los
oxígenos tienen carga parcial negativa, y el
carbono tiene carga parcial positiva
Dipolo total
cero
FUERZAS INTERMOLECULARES
36
Polaridad de las moléculas
FUERZAS INTERMOLECULARES
26/11/08
FUERZAS INTERMOLECULARES
37
Polaridad de las moléculas
• Aunque un enlace polar es un prerrequisito para que
una molécula
tenga dipolo, no todas
las moléculas con enlaces
polares tienen dipolo total
• Para las moléculas ABn
donde el átomo central
está rodeado por átomos
idénticos de B
• Hay ciertas geometrías
que no presentan momento
dipolo efectivo a pesar
que los enlaces individuales presenten dipolo
26/11/08
Dipolos de enlace
Dipolo total
• A pesar de que una molécula sea muy grande, las
reglas concernientes a la geometría y al dipolo se
mantienen
Dipolos de enlace
26/11/08
• El agua por otra parte también tiene tres átomos
pero contrariamente al caso del CO2 si tiene
momento dipolo
38
• Para que una molécula sea polar debe tener:
– Enlaces polares
– Forma adecuada
H
CH4 = H
H
Cl
CCl4 = Cl
C
Cl
26/11/08
H
C H=
µ=0
H C H =
H
Cl
Cl =
Cl
C
Cl
Cl
FUERZAS INTERMOLECULARES
µ=0
39
10
Momento dipolo
Polaridad de las moléculas
H
CH3Cl = H
C
Cl =
H
H
C
C
Cl
26/11/08
C
µ=1.90
•
Cl =
µ=1.60
•
Es un vector y se define como:
•
El momento dipolo se determina
experimentalmente midiendo el cambio respecto
a la temperatura en la capacitancia de dos placas
cargadas entre las cuales se pone una sustancia
cualquiera.
Cl
Cl =
H
Cl
CHCl3 = H
Cl =
Es la interacción resultante entre dos cargas
puntuales +q y -q, separadas a una distancia re
Se representa así:
H
Cl
CH2Cl2 = H
•
H
H
C
H
Cl
Cl =
H
C
Cl
µ=1.04
Cl
FUERZAS INTERMOLECULARES
40
26/11/08
Momento dipolo
•
•
•
•
•
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
41
Cálculo del momento dipolo
Así en el caso del HCl, el valor obtenido
experimentalmente, es:
3.59x10-30 C m
Como es un número muy pequeño, conviene
crear una unidad apropiada.
La unidad de momento dipolo se llama Debye
(D) y vale:
3.33x10-30C m
De manera que en estas unidades el momento
dipolo del HCl es de:
1.08 D
El momento dipolo de dos cargas unitarias
contrarias a una distancia de 100 pm vale:
4.89 D (16.28x10-30 C m)
26/11/08
µ = q ⋅ re
•
Para calcular aproximadamente el valor del
dipolo de una molécula se resuelve la siguiente
ecuación:
•
De manera que para el HCl se tiene que:
µAB ≈ χA − χB = ∆ χ
•
•
•
42
µHCl ≈ χCl − χH = (3.0 − 2.1) D = 0.9D
A las moléculas con momento dipolo = 0 se les
conoce como moléculas no polares,
A las que tienen momento dipolo ≠ 0 se conocen
como moléculas polares
El caso extremo de una molécula polar es el CsF
(Δχ=3.2)
26/11/08
FUERZAS INTERMOLECULARES
43
11
Porcentaje de carácter iónico
•
Para calcular que tan polarizada está la carga
en esta molécula, dividimos el momento dipolo
obtenido entre la distancia de enlace:
3.45×10 -30 C m
127.5×10−12 m
•
Porcentaje de carácter iónico
•
r(pm) δcalc (D)
= 2.7 ×10−20C
En el caso del HCl nos encontramos que esto
representa aproximadamente un sexto de la
carga del electrón (1.602x10-19C) o lo que es lo
mismo 17% del total de la carga total en cada
átomo:
2.7 ×10−20
= 0.168
−19
1.602×10
26/11/08
FUERZAS INTERMOLECULARES
44
δobs (D)
% CI=(δobs / δcal)
HF
92
4.41
1.90
43
HCl
127
6.06
1.03
17
HBr
143
6.81
0.79
11
HI
162
7.74
0.41
6
26/11/08
Porcentaje de carácter iónico y χ
•
Esto mismo puede hacerse para todos los
halogenuros
FUERZAS INTERMOLECULARES
45
Porcentaje de carácter iónico y χ
Se han sugerido varias ecuaciones empíricas
para determinar el carácter iónico de un enlace
en función de la electronegatividad de sus
constituyentes, una de ellas (Hannay & Smyth):
•
Pauling mismo, deriva una relación entre el
carácter iónico y la electronegatividad
%CI = 16 (∆χ ) + 3.5 (∆χ )
2
•
•
Para HBr,
χBr=2.74, y χ H=2.20
de manera que:
% CI = 16 (0.54 ) + 3.5 (0.54 ) = 9.7
2
26/11/08
FUERZAS INTERMOLECULARES
%CI AB
46
26/11/08
1
− (χ −χ )
B
4 A
= 1 −e
⋅100
FUERZAS INTERMOLECULARES
47
12
Polaridad de las moléculas
Interacciones Ión-Dipolo
Ión-Dipolo
Se trata de una interacción entre un ion cargado
y una molécula polar (es decir un dipolo)
• Los cationes se verán atraídos por el lado
negativo de un dipolo
• Los aniones se verán atraídos por el lado positivo
de un dipolo
• La magnitud de la energía de esta interacción
depende
– de la carga del ion (Q),
– el momento dipolo de la molécula (µ) y
– la distancia del centro del ion al punto medio
del dipolo (r)
•
• Las moléculas polares se alinean cuando:
– aplicamos un campo eléctrico
– están cerca unas de otras
– al estar en presencia de iones
Campo eléctrico
Cercanía
Cercanía
Iones
• Lo cual les concede propiedades muy
importantes.
26/11/08
FUERZAS INTERMOLECULARES
48
26/11/08
Interacciones Ión-Dipolo
Ión-Dipolo
•
•
Y así pictóricamente:
•
Z± ⋅µ
r2
•
•
•
26/11/08
FUERZAS INTERMOLECULARES
49
Interacciones Dipolo-Dipolo
Dipolo-Dipolo
Se puede describir matemáticamente así:
FI −D = −
FUERZAS INTERMOLECULARES
50
Ocurre cuando los átomos de una molécula
tienen diferencias de χ , se polarizan y producen
un dipolo
Cuando dos dipolos se avecindan, se atraen,
dando como resultado un enlace
Se describen matemáticamente así:
−2µ1µ2
E D−D =
r3
Y pictóricamente así:
26/11/08
FUERZAS INTERMOLECULARES
51
13
Interacciones Dipolo-Dipolo
Dipolo-Dipolo
Interacciones Dipolo-Dipolo
Dipolo-Dipolo
• Si los átomos muy electronegativos se encuentran
unidos directamente a un H, también se formará
un dipolo.
• Estas interacciones se presentan entre las
moléculas neutras polares
• Las moléculas polares se atraen entre sí cuando la
carga parcial positiva de una molécula está cerca
de la carga parcial negativa de otra
• Las moléculas polares deben de estar cerca unas de
otras para que la fuerza atractiva de la interacción
sea significativa
26/11/08
FUERZAS INTERMOLECULARES
52
•
•
•
26/11/08
Puente de hidrógeno
hidrógeno
•
•
•
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
53
Puente de hidrógeno
hidrógeno
•
El puente de hidrógeno, es la atracción
intermolecular resultante de la interacción de
dipolos donde participa el H
Esta atracción es responsable de muchas de las
propiedades características del H2O y de otras
muchas moléculas entre las que se encuentran
las proteínas y el ADN
Un átomo de hidrógeno en un enlace polar (por
ejemplo H-F, H-O o H-N) puede experimentar
una fuerza atractiva hacia una molécula polar o
un ión vecino que cuenta con pares electrónicos
sin compartir, usualmente átomos de F, O o N
26/11/08
Las interacciones dipolo-dipolo son menores que
las interacciones ion-dipolo
Las fuerzas dipolo-dipolo crecen al incrementarse
la polaridad de una molécula
Otra forma de presentarlo es esta:
•
•
54
A este tipo de interacción se le conoce con el
nombre de enlace de hidrógeno y en última
instancia no es más que una interacción del tipo
dipolo-dipolo
Un enlace entre un hidrógeno y un átomo
electronegativo como el F, O o N es muy polar
Tomando en consideración que el átomo de H no
tiene electrones de core, entonces el lado del
átomo que está hacia afuera del dipolo es
virtualmente un núcleo desnudo
26/11/08
FUERZAS INTERMOLECULARES
55
14
Puente de hidrógeno
hidrógeno
•
•
•
Puente de hidrógeno
hidrógeno
La carga parcial positiva se verá atraída a la carga
parcial negativa de un átomo electronegativo de
una molécula cercana
Debido a que el átomo de hidrógeno en un
enlace polar tiene deficiencia de electrones
(particularmente en un lado, es decir, el lado
opuesto al enlace covalente polar)
Entonces, puede acercarse mucho al átomo
electronegativo de la molécula vecina (el cual
tiene carga parcial negativa) de manera que
puede interactuar fuertemente con él.
26/11/08
FUERZAS INTERMOLECULARES
56
•
•
•
•
26/11/08
Puente de hidrógeno
hidrógeno
•
•
•
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
57
Puente de hidrógeno
hidrógeno
El agua tiene una capacidad poco común para
formar una red de enlaces de hidrógeno muy
extensa
Como líquido, la energía cinética de las moléculas
previene que un arreglo ordenado extenso de los
átomos de hidrógeno
Al enfriarse, las moléculas van perdiendo energía
cinética y esto permite que las moléculas se
vayan ordenando en un arreglo que maximiza las
interacciones atractivas de los enlaces de H
26/11/08
Recuérdese que entre más cerca pueda estar
mayor será la atracción electrostática
La energía de los enlaces de hidrógeno va de
alrededor de 4 kJ/mol a 25 kJ/mol, es decir, son
más débiles que los enlaces covalentes
Pero son mayores que las interacciones dipolodipolo o las fuerzas de dispersión
Este tipo de interacción tiene gran importancia
en la organización de las moléculas biológicas y
su influencia es notable en la estructura de las
proteínas y los ácidos nucleicos
58
•
•
•
Este arreglo de las moléculas tiene un volumen
mayor (es decir, es menos denso) que el agua
líquida, de manera que el agua se expande al
congelarse
El arreglo de moléculas de agua en el hielo normal
tiene geometría hexagonal (es decir que está
compuesto de anillos con seis moléculas de agua),
lo cual es la base estructural de la forma hexagonal
de los copos de nieve.
Esto se debe a que cada molécula de agua puede
participar en cuatro enlaces de H
26/11/08
FUERZAS INTERMOLECULARES
59
15
Puente de hidrógeno
hidrógeno
•
•
Interacciones de dispersión
dispersión
•
Es decir uno con cada par de no enlace del
oxígeno
Y uno con cada átomo de hidrógeno
•
•
•
26/11/08
FUERZAS INTERMOLECULARES
60
Interacciones de dispersión
dispersión
¿Cómo actúan las fuerzas de dispersión de
London?
– El helio tiene 2 electrones si consideramos que
estos electrones son partículas la distribución
promedio de los electrones alrededor del
núcleo es esféricamente simétrica
– Los átomos no tienen dipolo y por tanto su
momento dipolo es cero
– Sin embargo, puede ocurrir que la distribución
de los electrones alrededor del núcleo de cada
átomo en un instante dado, no sea
completamente simétrica.
• Así puede pasar que:
– Ambos electrones queden en el mismo lado del
núcleo
•
26/11/08
FUERZAS INTERMOLECULARES
62
No pareciera que las moléculas no-polares
tengan ninguna base física para tener
interacciones atractivas.
Sin embargo, los gases de las moléculas nopolares pueden licuarse, y esto indica que si la
energía cinética se reduce, existe algún tipo de
interacciones atractivas que predominan.
Fritz London (1930) sugiere que el
movimiento de los electrones en un átomo o una
molécula no polar puede dar como resultado un
dipolo transiente
(transiente quiere decir que tiene tiempos de
vida muy cortos)
26/11/08
•
•
•
•
FUERZAS INTERMOLECULARES
61
Interacciones de dispersión
dispersión
Esto, dará como resultado que en ese instante el
átomo tenga un dipolo aparente y por tanto un el
momento dipolo sea diferente de cero, es decir que
haya un dipolo transiente
Un átomo vecino que se encuentre cerca de este
átomo, se verá influido por este dipolo, los
electrones de este átomo se alejarán de la región
negativa del dipolo.
Es decir, debido a la repulsión electrónica, un
dipolo temporal puede inducir un dipolo similar en
un átomo o molécula vecino, si este está lo
suficientemente cerca.
Causando que los átomos o moléculas vecinos se
sientan atraídos unos a los otros
26/11/08
FUERZAS INTERMOLECULARES
63
16
Interacciones de dispersión
dispersión
•
•
Interacciones de dispersión
dispersión
A este fenómeno se le conoce con el nombre de
interacciones de dispersión de London (o
simplemente fuerzas de dispersión)
•
Estas interacciones son significativas únicamente
cuando los átomos o moléculas que lo presentan
están muy cerca unas de otras
La expresión matemática que describe este
fenómeno es esta:
Edispersión =
•
−2µ1α
r6
Pictóricamente esto se puede mostrar así:
Dipolo inducido Dipolo instantaneo
Atracción
26/11/08
FUERZAS INTERMOLECULARES
64
Interacciones de dispersión
dispersión
•
•
•
FUERZAS INTERMOLECULARES
FUERZAS INTERMOLECULARES
65
Interacciones de dispersión
dispersión
La facilidad con la que un campo eléctrico
externo (por ejemplo el de otra molécula) puede
inducir un dipolo (es decir, alterar la distribución
electrónica) en una molécula se le conoce como
polarizabilidad de esa molécula
Entre mayor sea la polarizabilidad de una
molécula será más fácil inducir un momento
dipolo momentáneo y serán más fuertes las
interacciones de dispersión
Entre mayor sea la molécula, mayor será su
polarizabilidad, esto ocurre pues:
26/11/08
26/11/08
66
–
Sus electrones están más lejos del núcleo, dado que a
mayor separación entre las cargas mayor es el dipolo
producido
– El número de electrones es mayor y por tanto hay
mayor probabilidad de que se genere una distribución
asimétrica
• Entonces, las interacciones de dispersión tienden a
incrementarse al incrementar la masa de la molécula
• Las interacciones de dispersión también estarán
presentes en todas las moléculas, sean o no polares
26/11/08
FUERZAS INTERMOLECULARES
67
17
Interacciones moleculares
I nterac ción
Covalente
M o d elo
Cuántica
Z +Z −
Iónica
E=
r
− Z± µ
Ion # dipolo E =
r2
−2µ1µ2
Dipolo#dipolo E =
r3
−Z 2α
Ion#dipolo
E=
inducido
2r 4
µ12α
Dipolo#dipolo
E= 6
inducido
r
−2µ1α
Dispersión de
E
=
London
r6
26/11/08
Fue rza
muy fuerte
F unción de r
muy fuerte
" /r! {r} largo
fuerte
" /r2! {r} corto
moderado
" /r 3! {r} corto
débil
" /r 4! {r} muy corto
muy débil
" /r 6! {r} cortísimo
muy débil
" /r 6! {r} cortísimo
e-r! {r} corto
FUERZAS INTERMOLECULARES
68
18