II. ESTRUCTURA Y FUNCIÓN DE MEMBRANAS
Anuncio
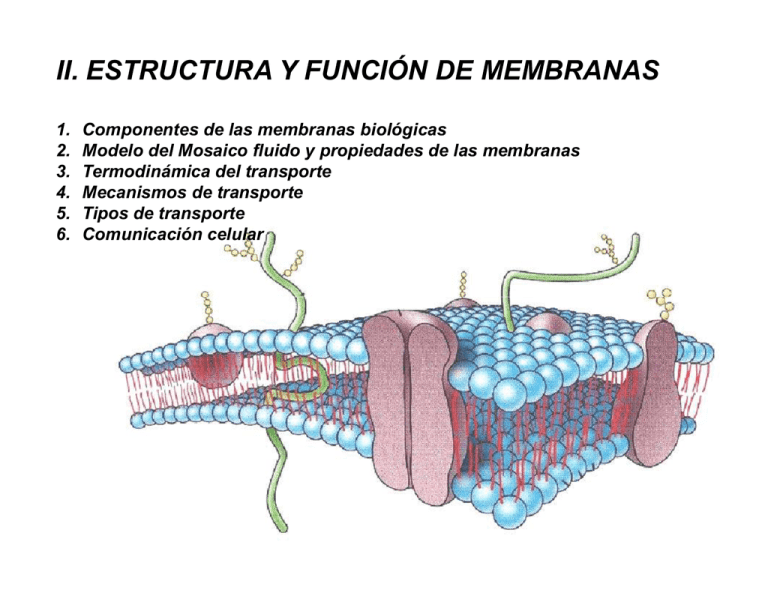
II. ESTRUCTURA Y FUNCIÓN DE MEMBRANAS 1. 2. 3. 4. 5. 6. Componentes de las membranas biológicas Modelo del Mosaico fluido y propiedades de las membranas Termodinámica del transporte Mecanismos de transporte Tipos de transporte Comunicación celular MODELO DEL MOSAICO FLUIDO propuesto por Jonathan Singer y Garth Nicolson en 1972 Grupos polares de lípidos Interacciones hidrofóbicas Proteínas globulares LAS MEMBRANAS SON DISOLUCIONES BIDIMENSIONALES DE PROTEÍNAS GLOBULARES Y LÍPIDOS ORIENTADOS. LA BICAPA ES DISOLVENTE Y BARRERA DE PERMEABILIDAD LAS PROTEÍNAS DE MEMBRANA DIFUNDEN LIBREMENTE LA BICAPA LIPÍDICA PUEDE PRESENTAR DOS ESTADOS FÍSICOS: ESTADO PARACRISTALINO O FASE DE GEL (los lípidos están ordenados, casi no se mueven) FLUIDEZ ESTADO LÍQUIDO DESORDENADO O FLUIDO (las cadenas acilo tienen mucho movimiento y no hay una organización regular) LA FLUIDEZ MEMBRANAL DEPENDE DE: LA LONGITUD DE LAS CADENAS HIDROCARBONADAS EL GRADO DE INSATURACIÓN LA CANTIDAD DE ESTEROLES MENOR FLUIDEZ LA ESTRUCTURA DE LOS LÍPIDOS DETERMINA SU ORDEN DENTRO DE LA MEMBRANA GLICEROLÍPIDO Fosfatidilcolina ESFINGOLÍPIDO Esfingomielina LA ESTRUCTURA DE LOS LÍPIDOS DETERMINA SU EMPAQUETAMIENTO Fase líquida desordenada (ld) Fluidez Movilidad lateral Fosfatidilserina Fosfatidilglicerol Fosfatidilinositol Fosfatidiletanolamina Fase líquida ordenada (lo) Fluidez Movilidad lateral Esfingomielina Cerebrósidos Globósidos Gangliósidos Esteroles PRESENCIA DE MICRODOMINIOS O BALSAS (RAFTS) LIPÍDICAS EN LAS MEMBRANAS CELULARES AGP Esfingolípidos Fosfatidilcolina Inositolfosforilceramida VENTAJAS DE LOS RAFTS propiciar interacciones efectivas entre componentes membranales específicos CARA EXTERNA Fosfatidilinositol Fosfatidiletanolamina Fosfatidilserina CARA INTERNA ESTRUCTURA DE LA MEMBRANA PLASMÁTICA Edidin, 2003 LAS MEMBRANAS BIOLÓGICAS SON SEMIPERMEABLES NO PERMITEN EL PASO LIBRE DE COMPUESTOS POLARES O CARGADOS O IONES EL MOVIMIENTOS DE COMPUESTOS POLARES O CARGADOS O IONES A TRAVÉS DE LAS MEMBRANAS BIOLÓGICAS REQUIERE DE TRANSPORTADORES DE NATURALEZA PROTEICA TERMODINÁMICA DEL TRANSPORTE La difusión de una molécula entre los dos lados de una membrana se parece a un equilibrio químico: A (fuera) A (dentro) Una diferencia en las concentraciones de la molécula entre los dos lados de la membrana genera una diferencia de potencial químico: ∆G A= GA (dentro) – GA (fuera) = RT ln A A dentro fuera A fuera > > > A dentro ∆G negativo A dentro > > > A fuera ∆G positivo Requiere ser acoplado a un proceso exergónico DEPENDIENDO DE LA NATURALEZA DEL SOLUTO PUEDE HABER DOS TIPOS DE DESPLAZAMIENTO CON CARGA SIN CARGA EL MOVIMIENTO DEPENDE: DEL GRADIENTE DE CONCENTRACIÓN (QUÍMICO) Y DEL GRADIENTE ELÉCTRICO (POTENCIAL DE MEMBRANA, Vm) GRADIENTE ELECTROQUÍMICO O POTENCIAL ELECTROQUÍMICO DOS TIPOS CLASIFICACIÓN DE LOS TRANSPORTADORES PORTADORES O ACARREADORES PASIVO O TRANSPORTADORES ACTIVO CANALES EL TRANSPORTE MEDIADO SE CLASIFICA DE ACUERDO CON LA ESTEQUIOMETRÍA DEL PROCESO DE TRANSPORTE UNIPORTADORA SIMPORTADORA ANTIPORTADORA DIFUSIÓN SIMPLE (Compuesto NO POLAR, a favor de su gradiente de concentración) DIFUSIÓN FACILITADA (A favor de su gradiente electroquímico) TRANSPORTE ACTIVO PRIMARIO (Contra gradiente electroquímico) TRANSPORTE IÓNICO FACILITADO POR IONÓFORO (A favor de gradiente electroquímico) CANAL (A favor de gradiente electroquímico, puede presentar entrada regulada por un ligando o ion) TRANSPORTE ACTIVO SECUNDARIO (Contra gradiente electroquímico, impulsado por el movimiento iónico a favor de gradiente) BOMBAS ACARREADORES CANALES TRANSPORTE PASIVO SON DE DOS TIPOS: EL SIMPLE Y EL FACILITADO A FAVOR DE SU GRADIENTE EN AMBOS TIPOS EL MOVIMIENTO ES A FAVOR DE SU GRADIENTE DE CONCENTRACIÓN Y NO HAY REQUERIMIENTOS DE ENERGÍA DIFUSIÓN FACILITADA CARACTERÍSTICAS: LA UNIÓN ES ESPECÍFICA LA ESTABILIDAD ESTA DETERMINADA POR INTERACCIONES DÉBILES NO-COVALENTES FACILITA LA ENERGÍA DE ACTIVACIÓN DEL PROCESO DE TRANSPORTE EL SUSTRATO NO ES MODIFICADO QUÍMICAMENTE TRANSPORTE DE GLUCOSA HACIA EL INTERIOR DE LOS ERITROCITOS DIFUSIÓN FACILITADA ESPACIO EXTRACELULAR MP CITOSOL Transportador de glucosa Unión de glucosa El transportador bajo un cambio conformacional Difusión de la Glucosa hacia el citosol Transportador retorna a su estado original EL TRANSPORTE SE PUEDE DESCRIBIR POR ANALOGÍA CON UNA REACCIÓN ENZIMÁTICA TRANSPORTE ACTIVO PERMITE EL MOVIMIENTO DE UN SOLUTO CONTRA UN GRADIENTE DE CONCENTRACIÓN O ELECTROQUÍMICO ES UN TRANSPORTE DESFAVORECIDO TERMODINÁMICAMENTE (ES ENDERGÓNICO) REQUIERE DE UN APORTE DE ENERGÍA PUEDE HABER TRASPORTE PRIMARIO Y SECUNDARIO LAS BOMBAS TIPO P (ATPasas TIPO P) SE CARACTERIZAN POR TENER UN TRANSPORTE DE IONES ACOPLADO A LA HIDRÓLISIS DE ATP TRANSPORTE ACTIVO PRIMARIO EL MOVIMIENTO DE UN SOLUTO EN CONTRA DE SU GRADIENTE ELECTROQUÍMICO ESTÁ ACOPLADO A UNA REACCIÓN QUÍMICA EXERGÓNICA LA BOMBA Na+-K+ O Na+-K+-ATPasa TRANSPORTE ACTIVO PRIMARIO ANTIPORTADORA LA BOMBA Na+-K+ O Na+-K+-ATPasa ATPasa de H+ 2+ + Ca H Dominio de unión del ATP ATPasa de Na+-K+ K+ Na+ ATPasa de Ca2+ Gadsby 2007 Nature news 450:957 Ejemplos de Transporte Primario: H+-ATPasa (UNIPORTADORA) Ca+-ATPasa (UNIPORTADORA) H+-K+-ATPasa (ANTIPORTADORA) H+ CAMBIOS GENERALES EN LA FORMA Y ORIENTACIÓN DE LA ATPasa DE H+-K+ TRANSPORTE ACTIVO SECUNDARIO La energía libre almacenada en un gradiente de potencial electroquímico puede aprovecharse para impulsar varios procesos fisiológicos endergónicos EL MOVIMIENTO DE UN SOLUTO EN CONTRA DE SU GRADIENTE ELECTROQUÍMICO ESTÁ ACOPLADO A UN TRANSPORTE ACTIVO PRIMARIO TRANSPORTE SECUNDARIO TRANSPORTE PRIMARIO Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ Na+ + Na+ Na Mecanismo de co-transporte Na+/glucosa en epitelio intestinal SIMPORTADOR CANALES •Son proteínas transmembranales que forman un poro en su interior por donde atraviesan los solutos •El tamaño de poro es particular, pero alcanzan a pasar aquellas moléculas o iones de tamaño parecido (son ligeramente inespecíficos) •Varias subunidades polipeptídicas pueden formar el poro •La dirección del transporte depende del gradiente de concentración del soluto transportado (va del lado de mayor concentración al de menor concentración) •A diferencia de los transportadores pueden no ser saturables •Permiten el desplazamiento transmembrana a velocidades superiores a las típicas de los transportadores Transportador (Bomba) = 100 – 103 iones/seg Canal iónico = 107 – 108 iones/seg TRANSPORTE MEDIADO POR UN CANAL (PROTEICO) Los canales pueden tener “puertas” que se abren con una señal que puede ser: 1. la unión de un ligando o 2. un cambio de voltaje en la membrana Los canales también pueden tener un “filtro de selectividad” CANALES CANAL DE AGUA (PORINA) Los canales pueden ser proteínas con estructura cuaternaria Gavilanes, 2008