: LANASEVE CRITERIOS DE ACEPTACIÓN DE LA
Anuncio
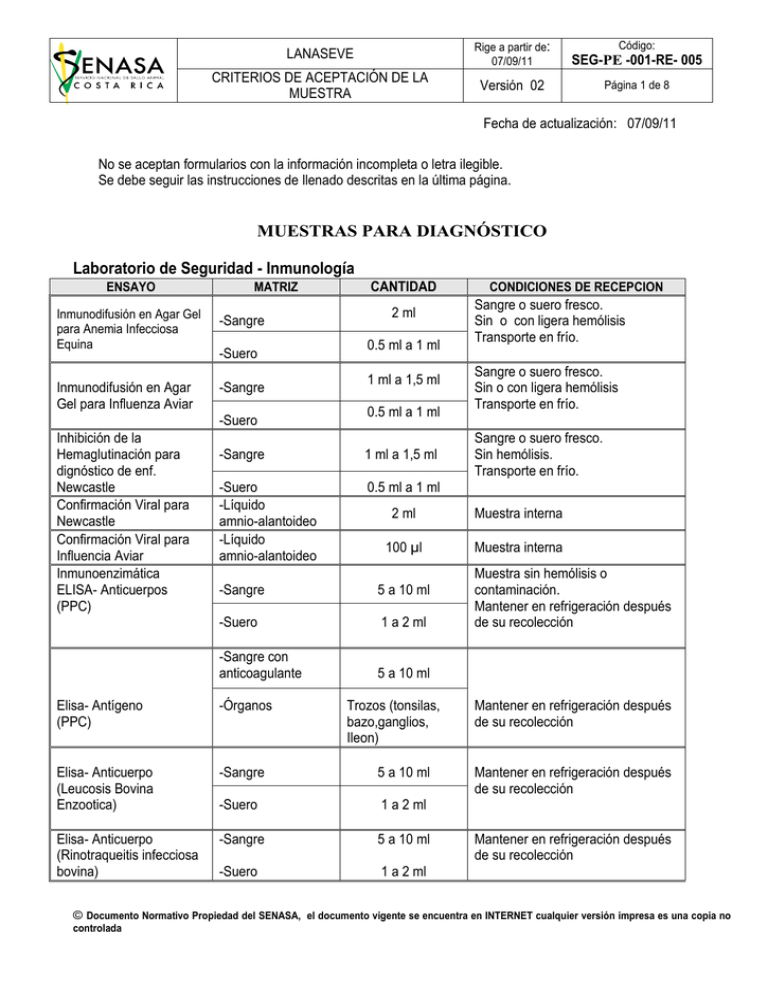
LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 1 de 8 Código: Fecha de actualización: 07/09/11 No se aceptan formularios con la información incompleta o letra ilegible. Se debe seguir las instrucciones de llenado descritas en la última página. MUESTRAS PARA DIAGNÓSTICO Laboratorio de Seguridad - Inmunología ENSAYO Inmunodifusión en Agar Gel para Anemia Infecciosa Equina Inmunodifusión en Agar Gel para Influenza Aviar MATRIZ -Sangre -Suero -Sangre -Suero Inhibición de la Hemaglutinación para dignóstico de enf. Newcastle Confirmación Viral para Newcastle Confirmación Viral para Influencia Aviar Inmunoenzimática ELISA- Anticuerpos (PPC) CANTIDAD 2 ml 0.5 ml a 1 ml 1 ml a 1,5 ml 0.5 ml a 1 ml -Sangre 1 ml a 1,5 ml -Suero -Líquido amnio-alantoideo -Líquido amnio-alantoideo 0.5 ml a 1 ml CONDICIONES DE RECEPCION Sangre o suero fresco. Sin o con ligera hemólisis Transporte en frío. Sangre o suero fresco. Sin o con ligera hemólisis Transporte en frío. Sangre o suero fresco. Sin hemólisis. Transporte en frío. 2 ml Muestra interna 100 µl Muestra interna -Sangre 5 a 10 ml -Suero 1 a 2 ml -Sangre con anticoagulante 5 a 10 ml Elisa- Antígeno (PPC) -Órganos Trozos (tonsilas, bazo,ganglios, Ileon) Elisa- Anticuerpo (Leucosis Bovina Enzootica) -Sangre 5 a 10 ml -Suero 1 a 2 ml Elisa- Anticuerpo (Rinotraqueitis infecciosa bovina) -Sangre 5 a 10 ml -Suero 1 a 2 ml Muestra sin hemólisis o contaminación. Mantener en refrigeración después de su recolección Mantener en refrigeración después de su recolección Mantener en refrigeración después de su recolección Mantener en refrigeración después de su recolección © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 2 de 8 Código: Laboratorio de Seguridad LSE-DV Aislamiento viral ENSAYO Aislamiento Viral y Prueba de Hemaglutinación Hemaglutinación MATRIZ -Hisopado cloacal, traqueal -Órganos -Heces -Huevo embrionado ( Líquido amnio-alantoideo ) -Huevo Embrionado CANTIDAD 2 ml Tejido individual 5 por pool CONDICIONES DE RECEPCION De 1 a 5 aves por tubo, Tomar con aplicador estéril. Transporte en CICC. Transporte en frío. congelado Huevo sano, sin daños en su cáscara. En refrigeración ( recomendación 13 ºC ) Patología ENSAYO MATRIZ Detección de BSE Cerebro que incluya el obex Inmunofluorescencia para Rabia 1 Hemisferio Cerebral que incluya talamos, hipocampo y corteza Estudios Histopatológicos Histopatología de camarones Tejidos (que incluyan la lesión observada en la necropsia) Camarón completo CANTIDAD Individuales individual Varios por animal varios CONDICIONES DE RECEPCION Fijados en formalina bufferada 10% en un recipiente diseñado para transporte de muestras biológicas antiderrames de plástico y de boca ancha, capacidad 4 litros Fresco a 4 ºC recipiente diseñado para transporte de muestras biológicas antiderrames de plástico. fijados en formalina bufferada 10% en un recipiente diseñado para transporte de muestras biológicas antiderrames de plástico y de boca ancha, capacidad 10 veces mayor al volumen del tejido enviado Si el envió es dentro de 24 horas debe venir fijado en Davison, posterior a 24 horas deben pasarse del Fijador (Davison) a Etanol al 70%. Volumen 10 veces mayor al volumen del tejido enviado. El Fijador Davison debe inyectarse en el Hepatopáncreas mientras los animales están vivos, © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada ENSAYO LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 3 de 8 MATRIZ CANTIDAD Código: CONDICIONES DE RECEPCION posteriormente se realizan dos cortes paralelos a ambos lados del cefalotórax y sumergir el animal en un volumen del fijador 10 veces mayor. En un recipiente diseñado para transporte de muestras biológicas antiderrames de plástico y de boca ancha. Laboratorio de Seguridad- Biología Molecular ENSAYO MATRIZ CANTIDAD Reacción en Cadena de la Polimerasa (PCR) para Virus de la enfermedad de la Mancha Blanca -Camarones (deben ser animales enfermos o moribundos no muertos) 10 camarones adultos o 50 gr de larvas Confirmación presencia de Ácido nucleico de los virus de la infección hipodermal y necrosis hematopoyética (IHHNV), Hepatopancreatitis necrotizante HNP y por hepatopancreatitis por parvovirus (HPV) Confirmación presencia de Ácido nucleico de los virus de la cabeza amarilla (YHV) y Taura Muestras de camarones adultos PCR para la detección de ácido nucleico de Laringotraqueitis infecciosa PCR para la detección de ácido nucleico del virus de Newcastle 6 Individuales CONDICIONES DE RECEPCION -Etanol al 95%, -Tejido fresco transportar refrigerado -Tejido congelado evitar el descongelamiento Tejido en congelación Pleopodos de camarones adultos Muestra compuesta Etanol 75% de 6 individuos Nauplios o larvas Muestra compuesta Etanol 75% de 150 a 200 Muestras de camarones adultos 6 Individuales Tejido en congelación Pleopodos de camarones adultos Muestra compuesta Etanol 75% de 6 individuos Nauplios o larvas Muestra compuesta Etanol 75% de 150 a 200 Individuales Congeladas Tráqueas Hisopados Muestra compuesta refrigeración traqueales de 5 aves Hisopado traqueal o Muestra compuesta Refrigeración cloacal de 5 aves solo tráqueas traqueales o solo Tejido en congelación cloacales © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada ENSAYO PCR para la detección de ácido nucleico de Micoplama gallisepticum PCR para la detección de ácido nucleico de Bronquitis infecciosa PCR para la detección de ácido nucleico de Influenza tipo A, H5, H7, H9 PCR para la detección de ácido nucleico del virus de Influenza Porcino H1N1 PCR para la detección de ácido nucleico de Pestivirus LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 4 de 8 MATRIZ CANTIDAD Código: CONDICIONES DE RECEPCION Tráqueas, pulmón Hisopados traqueales Tráqueas Individuales Congeladas Muestra compuesta refrigeración de 5 aves Individuales Congeladas Hisopados traqueales Muestra compuesta refrigeración de 5 aves Hisopado traqueal o Muestra compuesta Refrigeración cloacal de 5 aves solo traqueales o solo Tráqueas cloacales Tejido en congelación individuales Hisopados nasales Sangre entera con Heparina, Tejido (tonsilas), linfonodos Individuales refrigeración refrigeración Individuales Congeladas Laboratorio de Seguridad- Diagnóstico Apícola ENSAYO Estudio de panales de abejas meliferas. (Loque americana y Loque europea) Parásitos externos en Abejas Melíferas Ácaros ( Varroa spp) Parásitos internos en Abejas Melíferas Nosema. MATRIZ -Panal con cría de abejas. -Abejas adultas recolectadas en cámara cría con obreras jóvenes -Abejas adultas pecoreadoras recolectadas de la piquera CANTIDAD Trozo de 5 x 20 cm o panal entero De 300 a 500 abejas 60 a 100 abejas CONDICIONES DE RECEPCION Enviar un trozo de panal envuelto en papel toalla o periódico, mantener en refrigeración. Enviar en frasco plástico o vidrio con alcohol 70 %, bien cerrado. Enviar en frasco plástico con alcohol 70 %, bien cerrado. © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada ENSAYO Parásitos traqueales en Abejas Melíferas Ácaros (Acariosis). LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 5 de 8 CANTIDAD MATRIZ -Abejas adultas. 50 a 60 abejas Código: CONDICIONES DE RECEPCION Enviar en frasco plástico con alcohol 70 %, bien cerrado. Laboratorio de Seguridad- Parasitología ENSAYO MATRIZ -Sangre con anticoagulante Hemoparásitos Parásitos Externos Parásitos Internos -Frotis de sangre capilar. -Raspado de piel -Heces CANTIDAD 5 ml a 10 ml 1 o 2 frotis, en papel toalla o caja de transporte. 0.5 g a 1 g 100 g a 200 g CONDICIONES DE RECEPCION Mantener en refrigeración después de su recolección y transportar refrigerado. Remitir las muestras dentro de las 24 horas de tomadas. Frotis a temperatura ambiente. Enviar en recipiente bien cerrado a temperatura ambiente En bolsas plásticas o frascos plásticos y transportar refrigerado Microbiología Medico Veterinaria –Brucelosis ENSAYO Rosa de Bengala y Elisa competitivo MATRIZ CANTIDAD -Sangre 5 ml a 10 ml -Suero 1 ml a 2 ml Técnica de Anillo en Leche -Leche 50 ml CONDICIONES DE RECEPCION Muestra sin hemólisis o contaminación. Mantener en refrigeración después de su recolección Muestra en buen estado de conservación sin contaminación. Mantener en refrigeración después de su recolección, remitir dentro de las 24 horas de tomadas. © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 6 de 8 Código: Microbiología Medico Veterinaria - Leptospirosis ENSAYO MATRIZ -Sangre Cultivo de Leptospira CANTIDAD 5 ml a 10 ml -Suero 1 ml a 2 ml -Orina 2 ml a 10 ml -Aguas 10 ml -Tejido CONDICIONES DE RECEPCION Trozos (riñon, liq. Raquídeo, ojos, contenido estomacal feto abortado) -Sangre 5 ml a 10 ml -Suero 1 ml a 2 ml Microaglutinación (MAT) Muestra sin hemólisis o contaminación. Mantener en refrigeración después de su recolección. Remitir dentro de las 24 horas de tomadas. Muestra sin hemólisis o contaminación. Mantener en refrigeración después de su recolección Microbiología Medico Veterinaria - Bacteriología ENSAYO Ántrax Brucella spp. MATRIZ -Sangre sin anticoagulante. Vaca Viva: Hisopado del exudado vaginal tras el parto o aborto Leche (De los 4 cuartos) Placentomas o Cotiledones CANTIDAD CONDICIONES DE RECEPCION 5 ml a 10 ml Muestra sin contaminación, mantener en refrigeración después de su recolección .Y transportar refrigerado. Remitir dentro de las 24 horas de tomadas. Remitir dentro de las 24 horas de tomadas. Mantener en refrigeración. Si no es posible entregar la muestra dentro de las primeras 24 horas, las 10 ml de cada muestras se pueden congelar por 3 cuarto días y deben ser entregadas congeladas al laboratorio. Deben ser recolectadas en bolsas nuevas sin 3 a 5 placentomas contaminación por ejemplo bolsas o cotiledones ZIPLOC® 3 a 5 hisopados © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 7 de 8 ENSAYO MATRIZ Necropsia Vaca: Linfonodos supramamarios Linfonodos cefálicos (submaxilar, retrofaríngeo y parotídeo) Linfonodos iliacos,escapulares,c rurales Bazo Feto : Abomaso de feto (liquido) Pulmones, bazo, hígado de feto Clostridium sp Trichomonas y Campylobacter Listeria spp. Cabeza (cerebro feto) -Sangre sin anticoagulante -Tejido -Lavado prepucial -Hisopado vaginal. -Sangre sin anticoagulante -Tejido. -Heces CANTIDAD Código: CONDICIONES DE RECEPCION 2 linfonodos 2 linfonodos 2 linfonodos Trozo de 10 x 10 cms 2-3 mililitros Órganos completos Cabeza completa 10 ml Trozos pequeños (10 x 10 cms) Hisopo + 50 ml de medio Locke o solución salina al 0.85 % 10 ml Trozos pequeños (10 x 10 cm) 25 gramos Hisopados 12 pooles de 5 hisopos (en total 60 hisopos) Huevos 5 huevos por pool Tejidos Órganos completos Salmonella sp Las muestras deben ser recolectadas en bolsas nuevas (estilo Ziploc) y deben ser transportadas SIN refrigeración a temperatura ambiente. Mantener en refrigeración después de su recolección y transportar refrigerado. Traer al laboratorio el mismo día que las recolectan Mantener en refrigeración después de su recolección y transportar refrigerado. Remitir dentro de las 24 horas de tomadas. Enviar la muestra en bolsa plástica o recipiente bien cerrado , transportar refrigerado Mantener en refrigeración después de su recolección y transportar refrigerado Temperatura ambiente, frescos y sin quebrar. En bolsas nuevas (idealmente estilo Ziploc), rotulados y en refrigeración. Remitir dentro de las 24 horas de tomadas. © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada LANASEVE Rige a partir de: 07/09/11 SEG-PE -001-RE- 005 CRITERIOS DE ACEPTACIÓN DE LA MUESTRA Versión 02 Página 8 de 8 ENSAYO MATRIZ Gazas Tuberculosis Mastitis Paratuberculosis Prueba resistencia antimicrobiana (ANTIBIOGRAMA) Cultivo Bacteriológico -Tejido (Lifonodos o tejido sospechoso) -Leche Raspado de mucosa intestinal /Heces Cepa remitida de otro laboratorio o aislamiento en el laboratorio de Bacteriología en LANASEVE Tejidos Hisopados Exudados Contenido estomacal fetal. CANTIDAD Código: CONDICIONES DE RECEPCION Previo a la recolección de la muestra las 5 gasas debe empaparse en el buffer de leche descremada. Cada 2 pooles de 5 pool de 5 gasas debe transportarse gasas (en total 10 en bolsa plástica nuevas en gazas) refrigeración con 50 ml de agua peptonada. Remitir dentro de las 24 horas de tomadas. 2 a 3 trozos de Mantener en refrigeración después de 100 g (10 x 10 su recolección y transportar cms) refrigerado. Mantener en refrigeración después de su recolección y transportar 25 ml refrigerado. Remitir dentro de las 24 horas de tomadas. Mantener en refrigeración después de 25 gramos su recolección y transportar refrigerado, en bolsas plásticas bien cerradas. Remitir dentro de las 24 horas de tomadas. Mantener en refrigeración y transportar en bolsas plásticas bien cerradas. Cepa aislada Trozos de 10 x 10 cms, 3 -5 hisopados 3 a 5 ml exudado 2-5 ml contenido fetal Mantener en refrigeración después de su recolección y transportar refrigerado en las primeras 24 horas de recolectado © Documento Normativo Propiedad del SENASA, el documento vigente se encuentra en INTERNET cualquier versión impresa es una copia no controlada
