Ejemplo Reporte Cualitativo (cualidades)
Anuncio

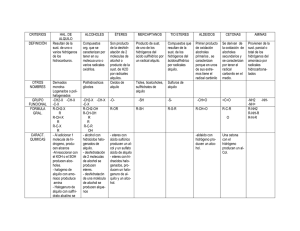
1 A. RESUMEN El objetivo de la presente práctica fue preparar un halogenuro de alquilo a partir de un alcohol primario en este caso alcohol n-propílico (CH3CH2CH2OH) y conocer el tipo de reacción que se lleva a cabo. Se realizó la práctica protonando el alcohol n-propílico (CH3CH2CH2OH) con pequeñas cantidades de ácido sulfúrico (H2SO4), se añadió bromuro de sodio (NaBr), se dio una sustitución nucleofílica formando un halogenuro de alquilo. Se realizaron pruebas de combustión, bromo en tetracloruro de carbono, Baeyer, nitrato de plata alcohólico y yoduro en acetona. Todas las pruebas fueron positivas a excepción de la de Baeyer y de bromo en tetracloruro de carbono. La práctica se realizó a temperatura ambiente de 25°C y a una presión barométrica local de 640mmHg. 2 B. RESULTADOS Tabla 1 Pruebas efectuadas al nitrobenceno preparado Prueba Resultado Combustión Positivo Br2 en CCl4 Negativo Baeyer Negativo Nitrato de plata alcohólico Positivo Yoduro en acetona Positivo Fuente: Hoja de datos originales y pruebas de identificación 3 C. PRUEBAS DE IDENTIFICACIÓN Prueba # 1: Nombre: Combustión Criterio de la prueba: Se produce una llama amarilla, ya que es un hidrocarburo monosustituido. Reacción: 2CH3CH2CH2Br+19/2O2→6CO2+7H2O+Br2 Observación: Se produjo una llama color amarilla. Conclusión: La prueba fue positiva. Prueba # 2: Nombre: Br2 en CCl4 Criterio de la prueba: se da un mecanismo en cadena, el proceso termina sólo por la combinación al azar de dos radicales. La reacción es catalizada por la luz solar. Reacción: CH3CH2CH2Br + Br2→ CH3BrCH2BrCH2Br Observación: se observó color café rojizo del bromo en una fase y amarillo casi incoloro del producto en otra fase. Conclusión: La prueba fue negativa Prueba # 3: Nombre: Baeyer Criterio de la prueba: Es una prueba de saturación, la cual depende de la habilidad del permanganato de potasio para oxidar dobles enlaces carbonocarbono y triples enlaces. Reacción: No hay reacción. Observación: Se mantuvo el color púrpura del permanganato de potasio. Conclusión: La prueba fue negativa. 4 Prueba # 4: Nombre: Nitrato de plata alcohólico Criterio de la prueba: Forma un precipitado del halogenuro de plata, la reacción se da por SN1. Reacción: RX+AgNO3→AgX+RONO2 Observación: Se formó un precipitado de color amarillo oscuro o café claro. Conclusión: La prueba fue positiva Prueba # 5: Nombre: Yoduro en acetona Criterio de la prueba: El bromuro de alquilo no es soluble en acetona, la sustitución del bromo por el yodo, se verifica, a medida que se solubilizan las dos fases. Reacción: RBr+NaI→RI+NaBr Observación: Se formaron dos fases distintas e incoloras. Conclusión: La prueba fue positiva 5 D. INTERPRETACIÓN DE RESULTADOS Los halogenuros de alquilo se preparan mediante reacciones en el que se substituye el grupo oxidrilo (OH) por un halógeno. Se da por el mecanismo de reacción de sustitución nucleofílica, por la siguiente reacción: R-OH + M-X → R-X + H2O La característica fundamental de los halogenuros de alquilo es la polaridad de sus enlaces C-X. Esta polaridad de enlace tiene dos implicaciones importantes, el carbono que se halla ligado al halógeno de la molécula sostiene una carga parcial positiva y el enlace C-X es muy fácil de romper heterolíticamente. (Ref. 3) Se añade ácido sulfúrico (H2SO4) para protonar al alcohol, logrando que el grupo OH se vuelvan un buen grupo saliente, con lo que por el mecanismo de reacción de sustitución nucleofílica al agregar una sal de bromo, en este caso NaBr, se facilita la reacción para formar el halogenuro de alquilo. Debido a un accidente en el laboratorio, no se pudo realizar la practica ya que se utilizó un equipo de destilación convencional, cuando lo ideal habría sido reflujar los líquidos, de modo que la cinética de la reacción aumentara por el aumento en la temperatura global del sistema. Al utilizar el equipo a reflujo, se disminuye la presión global del sistema, minimizando los riesgos de fugas indeseables. Es necesario instalar una trampa de agua en la parte superior del equipo de destilación, para evitar la liberación en forma de gas de ácido bromhídrico (HBr). La prueba de combustión fue positiva, ya que se produjo un llama, que se logro dar ya que el halógeno le quita a la parte alifática muy poco de su habilidad combustiva. En la prueba de bromo en tetracloruro (Br2/CCl4) se dio un mecanismo de reacción en cadena, pues una vez que se inicia el proceso prosigue por sí mismo. El proceso termina sólo por la combinación al azar de dos radicales. La reacción es catalizada por la luz solar. Ya que no se observó un cambio visible de la solución, la prueba fue negativa. 6 La prueba de Baeyer fue negativa ya que el permanganato de potasio busca centros de instauración, en el caso del halogenuro de alquilo no existen instauraciones. Para la prueba de nitrato de plata, se formó un precipitado del halogenuro de plata, por lo que la prueba es positiva. La prueba de yoduro en acetona produce bromuro de alquilo, produciendo dos fases que se solubilizan, al pasar el tiempo, por lo que de a cuerdo a lo esperado, ya que se formaron dos fases, la prueba se considero positiva. 7 E. CONCLUSIONES 1. Los halogenuros de alquilo se forman por sustituciones nucleofílicas. 2. El ácido utilizado protona al alcohol, volviéndolo un buen grupo saliente. 3. Se necesita un equipo de reflujo para la obtención del halogenuro de alquilo. 8 F. PROCEDIMIENTO 1. En un balón se colocaron 30 ml de alcohol n-propílico (CH3CH2CH2OH) al que se agregaron cuidadosamente, agitando y enfriando 33 ml de ácido sulfúrico concentrado. Cuando la mezcla estuvo fría, se agregaron 35 ml de agua enfriada con hielo y 30 gr de bromuro de sodio en polvo; se agitó constantemente. 2. Se armó el equipo de acuerdo a la figura. 3. En el balón se agregaron perlas de ebullición, se calentó manteniendo una temperatura constante durante 45 minutos; luego se elevó la temperatura hasta que dejó de formarse el producto aceitoso blanco, se cuidó que no se formara espuma en exceso. 4. Se eliminó del earlenmeyer recolector, la mayor cantidad de agua que sea posible. 5. Se enfrió rápidamente con hielo y agua. 6. Se le añadieron 4 ml de ácido sulfúrico al producto obtenido contenido en una ampolla, se agitó y luego se separó la fase aceitosa. 7. Se lavó con 12 ml de agua, luego con 8 ml de solución de hidróxido de sodio al 10% y por último con 12 ml de agua. 8. Se agregaron 3 g de cloruro de calcio anhidro. 9. Se agitó periódicamente y se decantó el liquido en una probeta para medir el volumen obtenido. 9 Equipo y cristalería: Reactivos: tubos de ensayo Alcohol n-propílico Soporte NaBr Beacker 1000ml ácido sulfúrico Mechero agua destilada Tapones de hule Balón 250ml Perlas de ebullición Termómetro 10 11 G. OBSERVACIONES Tabla 2 Observaciones obtenidas de las pruebas aplicadas al halogenuro de alquilo Prueba Observación Combustión Formación de llama amarilla. Br2 en CCl4 Se observó color café rojizo del bromo en una fase y amarillo casi incoloro del producto. Baeyer Nitrato de plata Se mantuvo el color púrpura del permanganato Precipitado de color amarillo oscuro o café claro. alcohólico Yoduro en Formaron dos fases distintas e incoloras. acetona Fuente: Hoja de datos originales 12 H. REFERENCIAS BIBLIOGRÁFICAS 1. SHRINER, RALPH. “IDENTIFICACIÓN FUSON, REYNOL SISTEMÁTICA C. DE CURTIN, DAVID. COMPUESTOS ORGANICOS”.Editorial Limusa. México 1974. 2. MERCK. “MERCK INDEX”. Merck and Company. Novena edición. Rahwy, NJ, USA, 1976. 3. SLOWING, IGOR. “UN TEXTO BASICO DE ORGÁNICA” Departamento de Química Orgánica. Facultada de Ciencias Químicas y Farmacia. Universidad San Carlos de Guatemala. Ediciones de los Geógrafos. 4. WINGROVE, Alan S. “QUÍMICA ORGÁNICA” Traducida por Lic. Mei Mei Alicia Chu Pulido. Editorial Mexicana. Primera edición en Español. Mexico1999. Página 1056.