NOTA: PARA ESTA EVALUACIÓN EL SIGNO COMA (,) SE TOMARÁ... = 1,000.
Anuncio
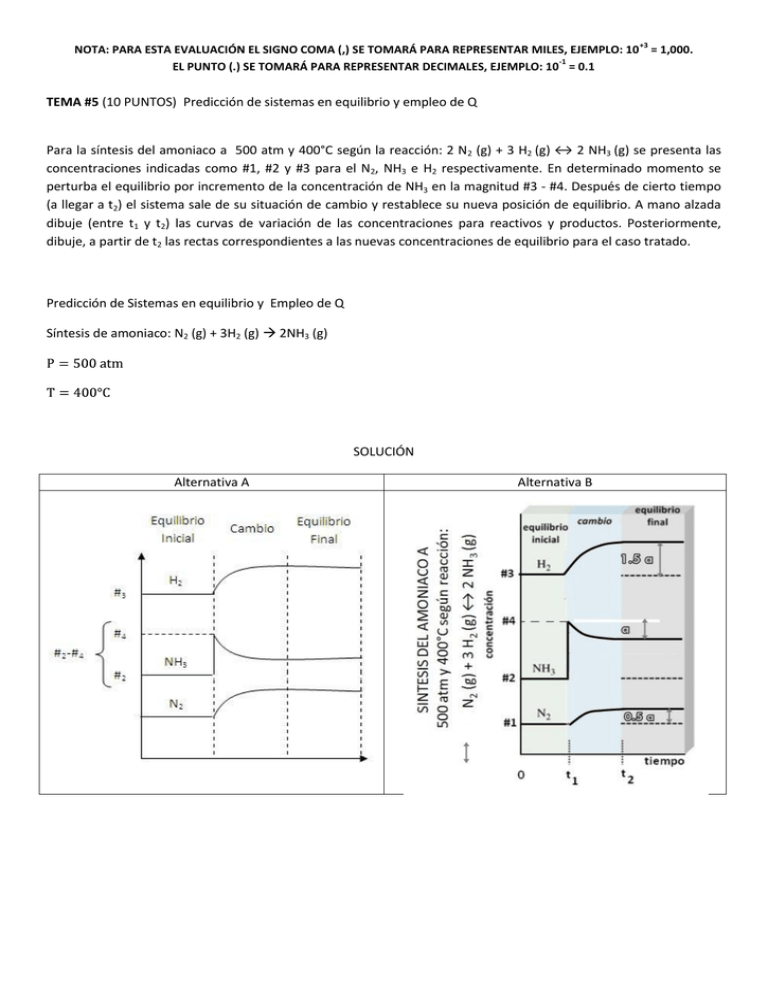
+3 NOTA: PARA ESTA EVALUACIÓN EL SIGNO COMA (,) SE TOMARÁ PARA REPRESENTAR MILES, EJEMPLO: 10 = 1,000. -1 EL PUNTO (.) SE TOMARÁ PARA REPRESENTAR DECIMALES, EJEMPLO: 10 = 0.1 TEMA #5 (10 PUNTOS) Predicción de sistemas en equilibrio y empleo de Q Para la síntesis del amoniaco a 500 atm y 400°C según la reacción: 2 N2 (g) + 3 H2 (g) ↔ 2 NH3 (g) se presenta las concentraciones indicadas como #1, #2 y #3 para el N2, NH3 e H2 respectivamente. En determinado momento se perturba el equilibrio por incremento de la concentración de NH3 en la magnitud #3 - #4. Después de cierto tiempo (a llegar a t2) el sistema sale de su situación de cambio y restablece su nueva posición de equilibrio. A mano alzada dibuje (entre t1 y t2) las curvas de variación de las concentraciones para reactivos y productos. Posteriormente, dibuje, a partir de t2 las rectas correspondientes a las nuevas concentraciones de equilibrio para el caso tratado. Predicción de Sistemas en equilibrio y Empleo de Q Síntesis de amoniaco: N2 (g) + 3H2 (g) 2NH3 (g) SOLUCIÓN Alternativa A Alternativa B




![4. Equilibrio químico [][] [][]](http://s2.studylib.es/store/data/005103464_1-84d96671ea48a848d0a38dd23a30c1e3-300x300.png)








![750 y su constante de formación es K Cu(NH ) [Cu ][NH ] = = × [ ] . 5](http://s2.studylib.es/store/data/008468339_1-7cb62f1a9924a5c19532c033585fed72-300x300.png)






